腹腔镜联合GnRH-a治疗对EMS伴不孕症性激素、CA125水平及妊娠率的影响
2023-02-16崔金秀
崔金秀
滨州医学院附属医院妇产科,山东滨州 256600
子宫内膜异位症(endometriosis,EMS)人群伴有不孕的概率高达50%[1],因此积极治疗EMS对降低不孕率具有重要意义。传统治疗方案是行腹腔镜手术切除子宫内膜异位病灶,但单纯手术治疗难以完全切除微小病灶,残留的病灶可造成术后疾病复发,不利于受孕[2]。雌激素在EMS的发病中具有重要作用,亮丙瑞林是促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonists,GnRH-a),其具有调节垂体卵巢性腺轴功能的作用。腹腔镜术后联合亮丙瑞林,能抑制子宫内膜上的残余病灶生长。上述联合治疗方案用于EMS伴不孕症,或能提高临床效果,降低术后疾病复发,从而改善妊娠率。基于此,本研究探讨腹腔镜联合GnRH-a治疗EMS伴不孕症的效果。现报道如下。
1 资料与方法
1.1 一般资料
本研究经医院医学伦理委员会批准,已获取患者或其家属知情同意。选择滨州医学院附属医院(我院)妇产科2019年1月至2021年1月收治的98例EMS伴不孕症患者,按照随机数表法分为C组和O组,每组各49例。
其中C组年龄25~37岁,平均(29.46±3.16)岁;不孕时间2~8年,平均(4.68±1.20)年;EMS分期:Ⅰ期10例,Ⅱ期16例,Ⅲ期13例,Ⅳ期10例。O组年龄25~35岁,平均(29.80±3.25)岁;不孕时间3~8年,平均(4.75±1.14)年;EMS分期:Ⅰ期8例,Ⅱ期12例,Ⅲ期17例,Ⅳ期12例。两组患者一般资料比较,差异无统计学意义(P> 0.05),具有可比性。
纳入标准:符合EMS的诊断[3];无避孕性生活,但12个月未受孕;配偶无影响妊娠的疾病;无手术禁忌证;对本研究所用药物不过敏。排除标准:其他原因所致的不孕;合并子宫肌瘤等其他生殖系统疾病;伴有免疫系统疾病者。
1.2 方法
C组:采取腹腔镜手术治疗。于患者月经干净后3~5 d行手术治疗。行全身麻醉,建立CO2气腹,行三孔法,在腹腔镜下剥离囊壁,取出异位病灶,分解盆腔粘连,恢复盆腔的正常结构,放置防粘连胶,预防术后粘连。对于重度EMS患者需去除深部病灶,然后封闭直肠陷窝,恢复其正常形态,另外术中需尽量用电凝破坏卵巢、腹膜、子宫表面的微小病灶。术后采用生理盐水冲洗盆腔,灌洗直至冲洗液清亮。
O组:采用腹腔镜联合GnRH-a(注射用醋酸亮丙瑞林缓释微球,北京博恩特药业有限公司,国药准字 H20093809,规格:3.75 mg/支)治疗。患者在术后3~5 d,经皮下注射给药,3.75 mg/次,以后每间隔28 d给药一次,持续用药3个月。
两组治疗结束后随访12个月。
1.3 观察指标及评价标准
性激素水平:于治疗前、治疗后(C组术后3个月,O组持续用药3个月结束后),采集患者的月经期间2~3 d的空腹静脉血,采用生化分析仪(迈瑞BS-830)检测黄体生成素(luteinizing hormone,LH)、卵泡刺激素(follicle stimulating hormone,FSH)、雌二醇(estradiol,E2)水平。
血 清 糖 类 抗 原125(carbohydrate antigen,CA125)、抗米勒管激素(anti-mullerian hormone,AMH)水平:于治疗前、治疗后,采集患者的空腹静脉血,使用ELIAS法检测血清CA125、AMH水平。
术后妊娠率:如患者在孕45 d后经超声检查可见子宫内有妊娠囊,则评价为妊娠成功。分别于术后6、12个月随访,评价两组患者的妊娠率。
术后12个月复发率。复发定义:经规范治疗后,患者的症状体征全部消失,再于几个月后出现内膜异位病灶,且伴有子宫内膜囊肿复发、疼痛、慢性或周期性腹痛等表现。
1.4 统计学方法
应用SPSS 22.0统计学软件进行数据分析。计量资料用均数±标准差()表示,行t检验,计数资料用[n(%)]表示,行χ2检验,P< 0.05为差异有统计学意义。
2 结果
2.1 两组性激素水平比较
治疗前,两组的血清LH、E2、FSH水平比较,差异无统计学意义(P> 0.05);治疗后,O组的血清LH、E2、FSH水平低于C组,差异有统计学意义(P< 0.05),见表1。
表1 两组性激素水平比较(±s)

表1 两组性激素水平比较(±s)
注 LH:黄体生成素;FSH:卵泡刺激素;E2:雌二醇
组别 n LH(U/L) FSH(U/L) E2(pmol/L)治疗前 治疗后 t值 P值 治疗前 治疗后 t值 P值 治疗前 治疗后 t值 P值C组 49 6.50±1.16 2.81±0.43 20.879 <0.00112.35±2.10 8.14±1.40 11.676<0.001 67.50±4.69 52.37±7.20 12.325 <0.001 O组 49 6.34±1.25 2.21±0.45 21.761 <0.00112.81±2.50 6.35±1.16 16.408<0.001 68.11±6.43 46.82±6.55 16.237 <0.001 t值 0.657 6.748 0.986 6.892 0.537 3.991 P值 0.513 <0.001 0.327 <0.001 0.593 <0.001
2.2 两组CA125、AMH水平比较
治疗前,两组的血清CA125、AMH水平比较,差异无统计学意义(P> 0.05);治疗后,O组的血清AMH水平高于C组,CA125水平低于C组,差异有统计学意义(P< 0.05),见表2。
表2 两组CA125、AMH水平比较(±s)
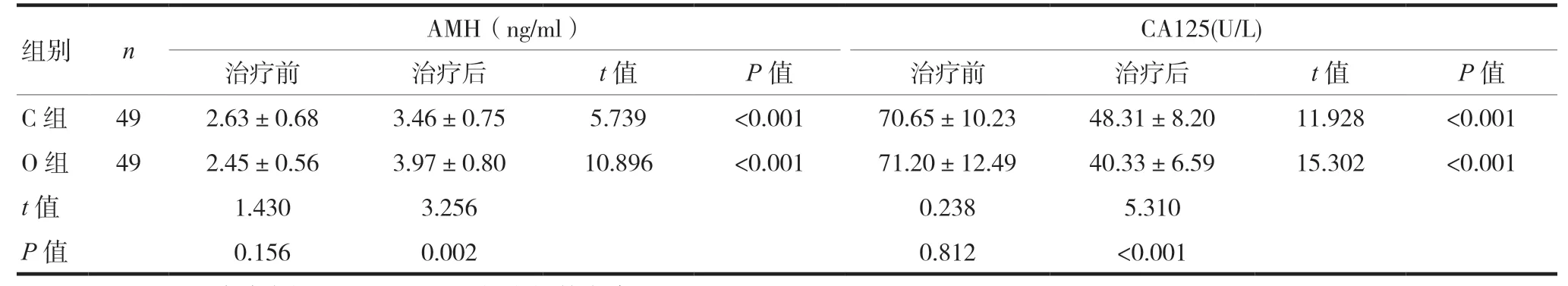
表2 两组CA125、AMH水平比较(±s)
注 CA125:血清糖类抗原125;AMH:抗米勒管激素
组别 n AMH(ng/ml) CA125(U/L)治疗前 治疗后 t值 P值 治疗前 治疗后 t值 P值C组 49 2.63±0.68 3.46±0.75 5.739 <0.001 70.65±10.23 48.31±8.20 11.928 <0.001 O组 49 2.45±0.56 3.97±0.80 10.896 <0.001 71.20±12.49 40.33±6.59 15.302 <0.001 t值 1.430 3.256 0.238 5.310 P值 0.156 0.002 0.812 <0.001
2.3 两组术后妊娠率及复发率比较
两组患者均完成12个月随访。随访6个月,两组的妊娠率比较差异无统计学意义(P> 0.05);随访12个月,O组的妊娠率高于C组,EMS复发率低于C组,差异有统计学意义(P< 0.05),见表3。
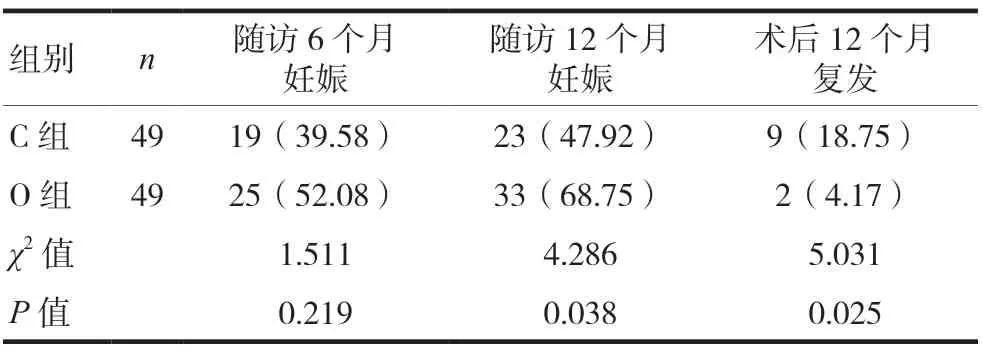
表3 两组术后妊娠率及复发率比较[n(%)]
3 讨论
EMS的发病率在4%~17%,其为引起不孕症的一个重要原因[4]。腹腔镜具有创伤小、出血少、术后恢复快的优势,是临床广泛用于治疗EMS的方法,但由于手术难以切除深部病灶和不典型病灶,单纯手术术后的复发风险高,提高妊娠率的效果有限。调查发现腹腔镜术后的3~6个月内的妊娠率仅为36.25%[5]。GnRH-α类药最常用的是亮丙瑞林,术后给予亮丙瑞林,在手术清除明显的异位内膜病灶的基础上联合GnRH-α药物调节患者的激素水平,旨在改善盆腔微环境,抑制残留病灶的继续生长,以期能提高疗效和妊娠率。
FSH可促进卵泡成熟,也可增加LH、E2的分泌,EMS患者的激素分泌处于紊乱状态[6]。CA125是常见的肿瘤标志物,CA125在EMS患者中也呈现高水平表达,EMS虽为良性,但其异位病灶可向盆腔、腹腔扩展种植,与恶性肿瘤的转移行为相似,EMS患者CA125水平表达随着疾病严重程度增加,Ⅰ、Ⅱ期患者的CA125水平基本正常[7]。AMH仅由女性卵巢分泌,是由窦前卵泡和小窦卵泡产生,其用于评价卵巢的储备功能,即卵巢内存留的卵泡数量和质量,其水平下降是导致女性生育能力及卵巢功能下降的主要因素[8]。研究表明[9-10],EMS患者的血清AMH水平低于正常值,是由于双侧卵巢受异位内膜侵犯后导致卵巢功能减退,腹膜型和深部结节型EMS即使异位内膜未累及卵巢组织,异位病灶激活了的机体免疫系统,以巨噬细胞为主释放炎性细胞因子作用于卵巢,也可一定程度影响卵巢功能。结果发现腹腔镜联合GnRH-a显著调节EMS伴不孕症患者的性激素水平释放,改善病情和卵巢功能。垂体分泌的FSH受GnRH和卵巢E2共同调控。注射给予亮丙瑞林,该药与垂体后叶的受体相结合后双向调节垂体功能,抑制FSH等性腺激素的分泌,并抑制卵巢分泌LH、E2,造成假绝经现象,可抑制盆腔内异位病灶引起的炎症反应、新生血管生成,促进残存内膜病灶的消亡[11]。通过腹腔镜手术清除宫腔内的异位病灶,并在术后联合亮丙瑞林防止病灶继续生长,从而降低异位病灶引起的CA125升高,并减少异位病灶为卵巢功能的不利影响。
秦莉[12]研究表示腹腔镜联合GnRH-a药物亮丙瑞林治疗的EMS伴不孕患者随访12个月的妊娠率可达67.4%,高于对照组的46.50%,本研究结果发现腹腔镜联合GnRH-a可提高EMS伴不孕症患者的妊娠率,减少疾病复发,与既往报道相似。笔者分析,腹腔镜可松解粘连的盆腔组织,清除病灶,并改善盆腔环境。亮丙瑞林为人工合成的GnRH-a同类物质,其活性较天然的GnRH强,可强效抑制垂体性腺功能系统,抑制E2的分泌,调节LH水平。在腹腔镜术后给予亮丙瑞林,强效抑制子宫内膜上残留异位病灶细胞的活性,使得残留病灶组织逐渐萎缩,促进病灶吸收;同时刺激子宫内膜上皮再生,加速腔内裸露区上皮化,防止再次粘连的同时改善盆腔内微环境,为患者受孕提供有利条件,控制病情复发[13-15]。
综上所述,腹腔镜联合GnRH-a显著调节EMS伴不孕症患者的性激素水平,改善病情和卵巢功能,提高其妊娠率和并减少疾病复发。
