垂体后叶素联合去甲肾上腺素在脓毒性休克中的应用
2023-02-13潘麒
潘 麒
北京市仁和医院重症医学科 102600
脓毒性休克(IS)是急性发作的全身性严重疾病,我国脓毒症发病率约为236/10万,其中IS的发病率约为120/10万,死亡人数为70万/年,不仅危及患者的健康,且给其家庭及整个社会带来了巨大的负担[1]。目前,临床针对IS主要采用血管活性药、液体复苏、抗病毒与抗菌药、清除病灶,以及器官支持治疗,早期精准的治疗方案能够显著降低患者的死亡率。去甲肾上腺素(NE)是治疗IS的首选血管活性儿茶酚胺类药物,能够有效促进心脏收缩功能,增加外周血管阻力,继而调节微循环[2]。然而,一些研究发现大剂量使用NE会降低血流量,干扰易损器官的供氧,甚至加重病情[3-4]。因此,亟需采用高效且安全的药物强化整体治疗效果。垂体后叶素(PIT)包含催产素与血管加压素,能改善血流动力学效应,且利于增加尿量,纠正休克症状。2020年1月—2022年5月期间本院对46例IS患者应用了PIT联合NE治疗,收效较为满意,现报道如下。
1 资料与方法
1.1 一般资料 选取2020年1月—2022年5月本院收治的92例IS患者作为观察对象,采用随机数字表法分为研究组(46例)与对照组(46例)。对照组:男25例,女21例;年龄35~79岁,平均年龄(62.65±5.56)岁;急性生理功能和慢性健康状况评分系统Ⅱ(APACHEⅡ)为21~32分,平均APACHEⅡ评分(27.00±1.23)分;序贯性器官功能衰竭评分(SOFA)为6~14分,平均SOFA评分(8.65±1.26)分。研究组:男24例,女22例;年龄35~78岁,平均年龄(62.60±5.50)岁;APACHEⅡ评分21~31分,平均APACHEⅡ评分(27.20±1.35)分; SOFA评分6~14分,平均SOFA评分(8.60±1.30)分。两组上述一般资料比较,差异无统计学意义(P>0.05)。该方案经医院伦理委员会批准。
1.2 入选标准 (1)纳入条件:符合《中国严重脓毒症/脓毒性休克治疗指南(2014)》[5]中对于IS诊断标准;休克时间<6h;研究方案已向患者家属进行充分的告知,并取得了知情同意权。(2)排除条件:其他原因所致的休克;肝肾功能异常;急性冠脉综合征、急性心肌梗死、心脏瓣膜病变、严重心律失常;凝血功能异常;恶性肿瘤;妊娠期。
1.3 治疗方法 两组均采取常规抗菌、抗感染、液体复苏、清除病灶、营养支持等常规治疗措施。对照组应用NE(规格:1ml∶2mg×2支,国药准字H31021177,上海禾丰制药有限公司)治疗,10mg的NE以5%葡萄糖注射液配置溶液50ml,采用深静脉导管持续泵入,用量为0.1~1.5μg/(kg·min),维持平稳动脉压(MAP)在65~90mmHg。在对照组的基础上,研究组联合PIT(规格:1ml∶6单位,国药准字H34022977,安徽宏业药业有限公司)治疗,18U的PIT以5%葡萄糖注射液配置成50ml,深静脉泵入,用量为0.7~2.3U/h。两组持续治疗3d。
1.4 观察指标 (1)实验室指标及氧合指数采集患者晨起空腹状态下静脉血5ml,高速离心(3 000r/min)10min,血清分离,以免疫荧光法检测降钙素原(PCT),酶联免疫吸附法检测C反应蛋白(CRP),比色法检测血乳酸。通过血气分析对动脉氧分压进行检测,计算氧合指数,即动脉氧分压/吸入氧浓度。(2)机械通气时间及ICU入住时间。(3)不良反应情况:低钠血症、心肌缺血、电解质紊乱、心律失常、肢体远端缺血坏死等。(4)跟踪28d,观察并记录患者的死亡率。
2 结果
2.1 两组治疗前后PCT、CRP、血乳酸及氧合指数比较 治疗前两组PCT、CRP、血乳酸及氧合指数比较,差异无统计学意义(P>0.05);治疗后研究组PCT、CRP、血乳酸指标较对照组低(P<0.05),氧合指数较对照组高(P<0.05)。见表1。
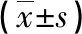
表1 两组治疗前后PCT、CRP、血乳酸及氧合指数比较
2.2 两组机械通气及ICU入住时间比较 研究组机械通气及ICU入住时间比对照组短(P<0.05)。见表2。

表2 两组机械通气时间及ICU入住时间比较
2.3 两组不良反应及28d死亡率情况比较 两组不良反应总发生率比较差异无统计学意义(χ2=5.060,P=0.024<0.05);研究组28d死亡率比对照组低(χ2=0.511,P=0.475<0.05)。见表3。

表3 两组不良反应比较[n(%)]
3 讨论
IS属于临床常见的危重症,极易引起细胞代谢异常与循环衰竭,累及多器官功能,具有较高的死亡率[6]。目前,缩血管药物是IS患者的首选用药,包括NE、多巴胺等,此类药物可以提高血压水平,纠正血流动力学变化。NE作为IS患者常用的缩血管药物,能够刺激α受体与β受体兴奋,广泛收缩全身小静脉、小动脉,促使血管非张力性容量向张力性容量转化,继而改善微循环与组织灌注,促使血流动力学指标恢复[7]。然而,单纯应用NE对于血管的作用较为轻微,且在升高血压的同时易增加血管阻力,减少组织器官血流量,甚至导致组织缺血[8-9]。
有研究发现,早期IS能够释放大量的血管加压素,随着病情的进展,血管加压素相对缺失,而适当补充外源性血管加压素利于改善血流动力学指标及脏器功能[10]。PIT属于一种激素,在体内与肾素—血管加压素系统及交感神经系统共同维持内环境的稳态平衡[11]。外源性PIT是血管加压素与催产素组成的混合剂,能够增强血管平滑肌受体与迷走神经兴奋性,恢复血管张力及收缩功能,且具有一定的免疫调节作用,利于调节机体应激反应,发挥出保护脏器功能的功效[12]。同时,PIT可以与迷走神经释放的乙酰胆碱炎症受体结合,发挥出显著的抗炎功效。一些研究认为,适量补充外源性血管加压素利于减少IS患者儿茶酚胺类药物的用量,但不推荐其作为一线治疗药物使用[13-14]。本文研究组在常规使用NE的基础上对46例IS患者应用了PIT治疗,结果发现其治疗后PCT、CRP、血乳酸指标较对照组低(P<0.05),氧合指数较对照组高(P<0.05)。可见,相较于单纯NE治疗,NE联合PIT能够有效改善机体的氧供,抑制炎症反应。究其原因可能为:二者协同作用有效改善了血流动力学与组织灌注压,保护器官功能,继而促进组织氧供;PIT在催产素与血管加压素的叠加作用下更利于兴奋迷走神经,抑制脂多糖,纠正机体的炎症状态。同时,研究组机械通气时间及ICU入住时间均较对照组短(P<0.05),且28d死亡率较对照组低(P<0.05)。可见PIT联合NE联合应用能够促进血管收缩,并通过改善机体炎症状态与感染程度,快速纠正组织缺氧及休克状态,进一步加快了康复速度,保障预后效果。此外,两组不良反应总发生率比较差异无统计学意义(P>0.05),说明PIT与NE联合应用并不会增加不良反应,安全性较佳。
综上所述,IS患者应用PIT联合NE治疗效果确切,可以加快康复进程,降低死亡率,具有临床推广价值。
