富马酸丙酚替诺福韦治疗特殊慢性乙型肝炎的相关进展
2023-02-08宋玉文沙丽丽陈立震李梦昆王玉荣辛永宁
宋玉文, 沙丽丽, 陈立震, 李梦昆, 王玉荣, 辛永宁
1 青岛大学附属青岛市市立医院 感染性疾病科, 山东 青岛 266011; 2 南京医科大学附属青岛临床医学院, 南京 210000
据世界卫生组织[1]估计,2019年全球慢性乙型肝炎(CHB)感染者达到2.96亿。每年新增HBV感染人数约为150万。2019年因HBV相关疾病死亡人数约为82万,主要死亡原因为肝硬化和原发性肝癌。新生儿乙型肝炎疫苗普种计划以及母婴阻断等措施的实施使新生儿HBV感染率大幅下降,但我国仍为HBV中高感染率(5%~7.99%)地区[2],90%以上的HBV感染者是20岁以上的成年人。近年来,我国CHB发病率有上升趋势[3-4],其中46~60岁人群发病率最高,占34.4%。
为了延缓和减少肝硬化、原发性肝癌及其他并发症的发生,延长CHB患者的生存时间,需要对CHB患者进行长期规范抗病毒治疗。我国《慢性乙型肝炎防治指南(2019年版)》[5]推荐恩替卡韦(ETV)、富马酸替诺福韦酯(TDF)和富马酸丙酚替诺福韦(TAF)3种强效低耐药药物为临床一线抗病毒治疗用药。本文就TAF在低病毒血症(low-level viremia,LLV)、耐药、妊娠期、 HBV相关的慢加急性肝衰竭、CHB相关肝移植患者等特殊类型CHB患者中的作用展开综述。
1 TAF治疗LLV的CHB患者
LLV在此描述为:排除依从性问题及病毒耐药突变后,接受 ETV、TDF、TAF治疗48周及以上的CHB患者采用灵敏qPCR法(最低检测限为20 IU/mL或10 IU/mL)仍可检测到血清HBV DNA,但<2000 IU/mL[6]。LLV的存在被认为是肝纤维化进展的独立危险因素[7],与更高的终末期肝病和原发性肝癌发病风险相关[8-9]。理想目标是LLV患者尽早达到病毒学应答,延缓疾病向终末期肝病和原发性肝癌进展。
Ogawa等[10]的研究中LLV患者换用TAF治疗48周后,有97.1%和77.8%达到病毒学应答,平均估计肾小球滤过率(estimated glomerular filtration rate,eGFR)水平有小幅度增加,特别是对于慢性肾脏病(CKD)(eGFR<60 mL·min-1·1.73 m-2)患者。进一步研究[11]发现,换用TAF 96周后大部分LLV患者达到了病毒学应答[ETV、TDF和核苷(酸)类似物(NUC)联合治疗组病毒学应答率分别为97.1%、71.4%和80%]。与48周试验结论相同,CKD患者拥有更高的eGFR改善率。另外两项研究[12-13]发现换用TAF治疗与继续应用ETV治疗相比,TAF组的患者病毒学应答率和ALT复常率均高于ETV组的患者。
对于LLV患者,由ETV换用TAF后,有较高的病毒学应答率,随着抗病毒时间不断延长,病毒学应答率不断升高。因此,对于ETV治疗48周后仍处于LLV状态的患者,及时换用TAF治疗效果显著。对于应用NUC或者TDF的LLV患者,换用TAF后大部分患者达到病毒学应答,但是当前研究数据较少(表1),今后需要更多的研究来验证这一结论。
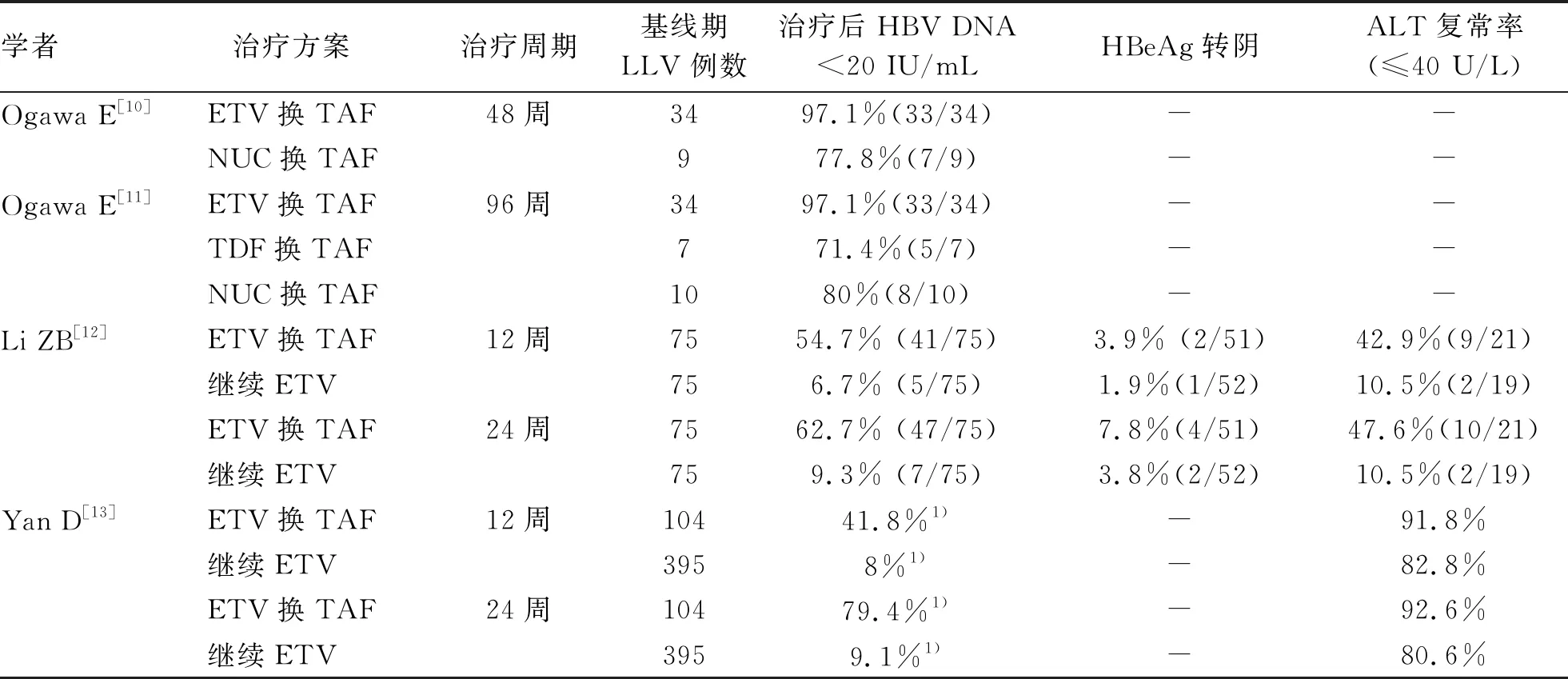
表1 TAF在LLV患者中的疗效
2 TAF治疗对其他药物耐药的CHB患者
随着抗病毒治疗时间的不断延长以及低耐药屏障药物的广泛应用,CHB耐药患者逐年增加。TAF与TDF均具有高耐药屏障,在骨肾安全性方面TAF优于TDF且目前尚没有关于TAF耐药的病例报道。
Byun等[14]对多种药物(拉米夫定、ETV和/或阿德福韦酯)耐药的CHB患者进行了研究,按1∶1随机分配至TAF组和TDF组治疗48周后发现血清HBV DNA检测不到(<15 IU/mL)的患者比例在两组之间没有显著差异(92% vs 88.5%)。TAF组显示脊柱骨密度增加(1.84% vs 0.08%,P=0.01),平均eGFR增加(8.2% vs 4.5%,P=0.06)。在基线指标变化方面,与TDF组相比,TAF组平均体质量(0.71 kg vs-0.37 kg,P=0.01)和总胆固醇、低密度脂蛋白和高密度脂蛋白胆固醇水平增加(P<0.001)。Grossi等[15]报告了1例具有范可尼综合征和多种药物耐药史的慢性CHB患者应用TAF作为抢救治疗方案。在换用TAF治疗9周后患者HBV DNA降至<10 IU/mL。在2年的随访观察中没有发现肾功能的显著变化,也没有出现副作用及不良事件。
TAF与TDF在多重耐药患者中均有较强的抗病毒效果,TAF拥有更好的骨骼肾脏安全性,但在抗病毒过程中需要检测血脂及体质量的变化。
3 TAF治疗妊娠期CHB患者
在我国,母婴垂直传播是HBV主要的传播途径。高病毒载量会导致母婴阻断成功率降低,2020年世界卫生组织“预防母婴HBV传播——妊娠期抗病毒预防组织”指南[16]建议高病毒载量(HBV DNA≥200 000 IU/mL)HBsAg阳性的孕妇从妊娠第28周开始需要抗病毒治疗,推荐强效、低耐药的TDF连续用药至妊娠结束。作为TDF的升级版,越来越多的研究发现TAF应用于妊娠期CHB患者中是安全有效的。
Zeng等[17]的研究中,高病毒载量患者在妊娠28周至分娩期间接受TAF或TDF治疗,所有婴儿进行免疫预防。两组分娩时100%的母亲HBV DNA<200 000 IU/mL。在婴儿7个月随访时,两组中没有婴儿HBsAg阳性,母婴传播率为0。Li等[18]的研究中,TAF组和TDF组治疗前后病毒载量和HBeAg水平显著降低,两组间降低程度无统计学差异。尿视黄醇结合蛋白和β2微球蛋白在TAF治疗后无明显变化(P>0.05),而在TDF治疗后显著升高(P<0.05),同样母婴传播率为0。在抗病毒及母婴阻断方面,其他几项研究[19-22]也得出相同结论(表2)。上述研究中,TAF组所有婴儿出生时未观察到先天性缺陷或畸形(1例胎儿因唇腭裂进行人工流产,该孕妇有被动接触烟雾史及接触农业化学品史,且唇腭裂的发育过程是在胚胎6~10周,而该孕妇从妊娠12周开始应用TAF,所以TAF导致这例胎儿唇腭裂可能性几乎不成立),没有婴儿在出生5 min时的Apgar评分<8,所有婴儿生长发育均在正常范围内。王岩教授[18]的研究还发现,TDF组患者脐带血和母乳中均有药物残留,而TAF组中未检测到药物残留。这为CHB患者在用药的同时进行母乳喂养提供了有力的证据。此外,《乙型肝炎病毒母婴传播预防临床指南(2020)》[23]推荐高病毒载量孕妇从妊娠28~32周开始服用抗病毒药物,大量研究表明在联合新生儿免疫预防的基础上,28~32周开始用药能够保守且有效阻断母婴传播。从经济及安全的角度出发,均不建议从24周开始服药。
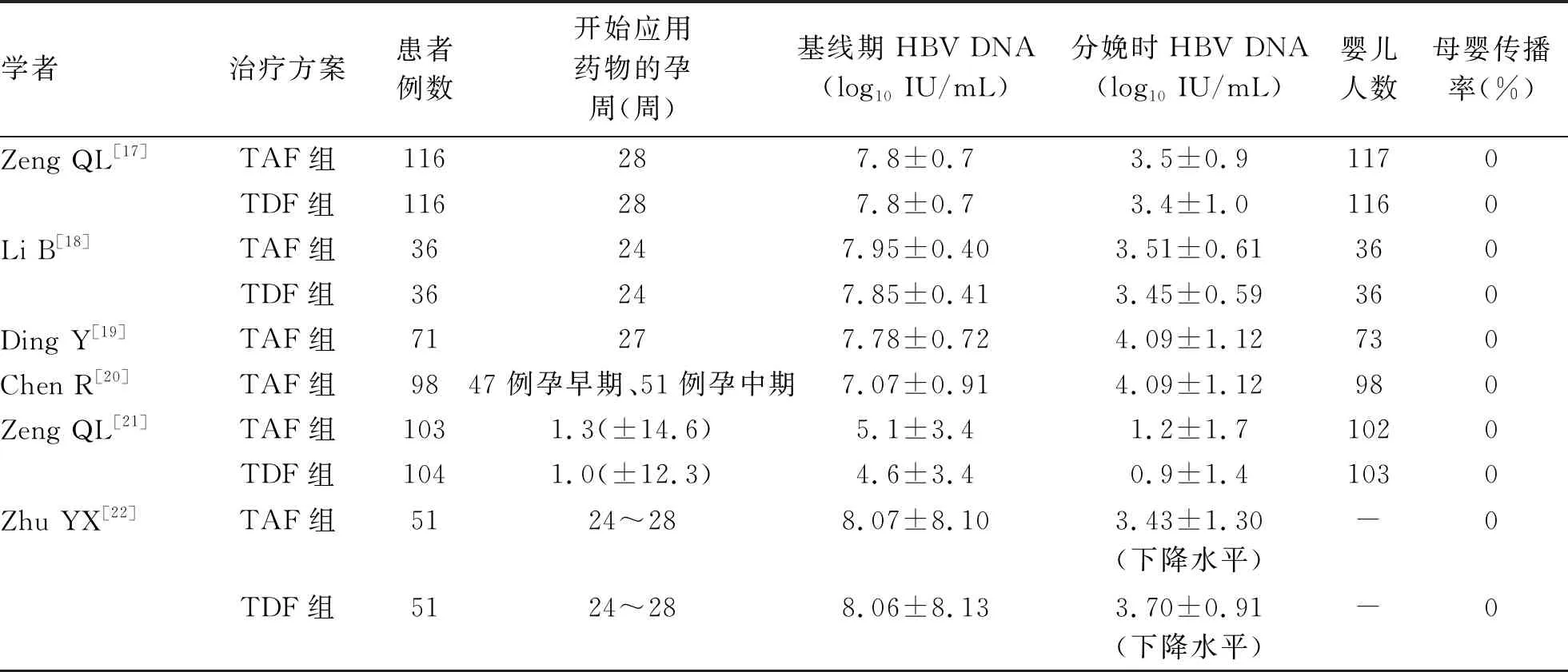
表2 妊娠期CHB患者抗病毒治疗效果汇总
在妊娠期高病毒载量CHB患者中,TAF可以有效降低病毒载量,实现母婴阻断,不会造成婴儿畸形及发育异常。由于妊娠期妇女骨密度下降,应用TAF可以避免更多的钙质流失,起到骨骼保护作用。
4 TAF治疗HBV相关慢加急性肝衰竭(HBV-ACLF)患者
Peng等[24]发现在HBV-ACLF患者中,应用TAF和ETV进行抗病毒治疗,将患者又分为肝衰竭前期、早期、中期和终末期4个阶段。在治疗4周时发现TAF组有较低的肌酐水平(P<0.05)和较高的eGFR水平(P<0.05),治疗12周后数据表明对于肝衰竭前期的患者,TAF组拥有较低的肝移植率和病死率(0 vs 13.89%,P<0.05)。两组对于肝衰竭早期、中期和终末期患者的肝移植率和病死率无明显差异。另一项研究[25]将HBV-ACLF患者分为TAF组、TDF组和ETV组进行抗病毒治疗。第48周时3组的存活率相似(P=0.262),HBV DNA达到病毒学应答的比率相似,肝功能均有改善,这可能与应用保肝药物有关。3组血清肌酐下降和eGFR升高水平没有显著差异,但TAF组的改变幅度更大。
HBV-ACLF合并急性肾损伤会导致病死率升高[26]。在治疗HBV-ACLF过程中,对肾功能的保护十分重要。TAF对于CHB患者肾功能具有保护作用,能够降低肌酐水平,提高eGFR水平,尤其适用于具有潜在肾损伤或者合并肾功能不全的HBV-ACLF患者。在肝衰竭前期患者中,TAF与ETV相比能够降低病死率;在肝衰竭早期、中期和终末期患者中,TAF与ETV作用效果相当。
5 TAF治疗CHB相关肝移植患者
对于终末期肝病患者,肝移植是目前唯一的治疗方法。为了减少肝移植后HBV复发,移植后需要继续应用抗病毒药物和/或免疫球蛋白[27]。目前研究最多的是ETV或TDF联合免疫球蛋白治疗,一项系统综述[28]显示,ETV或TDF联合免疫球蛋白预防肝移植后HBV复发的效果优于LAM联合免疫球蛋白。Saab等[29]研究了肝移植后接受乙型肝炎免疫球蛋白治疗的患者,应用TAF或者其他NUC药物抗病毒治疗。使用TAF的患者肾功能指标随着时间的推移没有显著变化;使用其他NUC药物的患者血清肌酐平均增加0.55 mL/min(P<0.05)。两组患者均未检测到HBV DNA。Rashidi-Alavijeh等[30]的研究中,改为TAF治疗前,全部患者肾功能异常(包括血清肌酐水平升高、eGFR下降等情况),93%的患者同时应用免疫抑制剂,所有患者肝功能稳定。换药1年后TAF对免疫抑制剂没有显著影响,肝肾功能没有显著改变,没有出现HBV DNA再激活。另一项研究[31]中,在转换TAF之前,55%的患者ALT指标异常。换用TAF治疗48周后,ALT复常率达到82%,免疫抑制剂没有显著变化,eGFR有改善但没有统计学意义,转换前后均未检测到HBV DNA。
在肝移植患者中,TAF和其他NUC药物都可以达到预防HBV复发的作用,并不会对免疫抑制药物产生影响。但对于合并肾功能受损的患者,TAF明显优于其他抗病毒药物。
6 TAF治疗其他特殊类型CHB患者
由于肝源有限而且治疗费用高,大部分乙型肝炎相关肝硬化合并严重门静脉高压相关并发症的患者无法接受肝移植治疗,经颈静脉肝内门体分流术(TIPS)是治疗乙型肝炎相关肝硬化并发症的一种治疗手段。Yao等[32]的研究中纳入137例乙型肝炎相关肝硬化门静脉高压症接受TIPS的患者,术后分别给予患者ETV、TAF和TDF治疗24个月,3组的生存率分别是84.3%、89.6%、86.9%;TAF组的Child-Pugh评分和终末期肝病模型评分低于TDF组和ETV组(P<0.05),eGFR高于TDF组和ETV组(P<0.05)。从治疗24个月的结果来看,与TDF和ETV相比,TAF在提高肝功能储备和eGFR方面具有显著优势。
在CKD患者当中,应用TAF可以得到更大的获益。Papatheodoridis等[33]发现大多数患有肾脏和/或骨骼疾病或风险的患者中,TAF治疗12~24个月后eGFR升高,血清磷酸盐、骨密度和ALT也得到改善,TAF还能够维持或诱导病毒学应答。在HIV/HBV合并感染的肾功能不全患者中[34],从TDF换用TAF 1年后eGFR得到改善、尿蛋白下降,ALT异常的患者指标正常化。
7 总结
TAF具有强效抗病毒、高耐药屏障以及保护骨肾的特点,为许多难治性、特殊性、严重性CHB患者提供了新的抗病毒方案。TAF的骨肾保护作用是由于药物靶向性高、用药剂量小,在血液中分解得到的替诺福韦浓度低,使近端肾小管损伤小[35]。目前大部分研究选择肌酐及eGFR来衡量TAF与其他抗病毒药物对肾脏的影响,可能会低估TAF与其他抗病毒药物之间的差异。其对于骨骼具有保护性的特点,更加适用于妊娠期以及老年等具有骨质疏松风险的患者,TAF在老年CHB患者中的骨骼安全性需更多的研究来证明,也缺乏儿童患者中的研究。TAF能够导致血脂及体质量升高,高血脂可以导致心脑血管疾病发生以及脂肪肝的形成,今后需要更多的研究来探索TAF与心脑血管疾病和脂肪肝的关系。由于NUC抗病毒作用机制是竞争性抑制HBV DNA复制、cccDNA无法清除以及患者自身免疫能力等因素影响,单一应用TAF抗病毒可能无法使全部患者达到病毒学应答,加之其在血脂代谢方面的不足,仍需不断探索研究新药以期实现世界卫生组织提出的“2030年消除病毒性肝炎作为重大公共卫生威胁”目标,使更多乙型肝炎患者获益。
利益冲突声明:所有作者均声明不存在利益冲突。
作者贡献声明:宋玉文负责查阅文献,撰写文章;沙丽丽、李梦昆、王玉荣参与论文起草;陈立震参与起草、修改文章关键内容;辛永宁参与指导,修改撰写文章并最后定稿。
