MnOx同步除锰氨氮滤池的快速启动及污染物去除机制
2023-02-04张瑞峰杨世莲郭英明
张瑞峰,杨世莲,杨 靖,郭英明,陈 希
MnO同步除锰氨氮滤池的快速启动及污染物去除机制
张瑞峰*,杨世莲,杨 靖,郭英明,陈 希
(西安工程大学城市规划与市政工程学院,陕西 西安 710600)
通过将MnO负载于石英砂表面形成MnO滤料,并以此构筑滤池,开展动态试验,考察了滤池的启动周期、污染物去除效率及影响因素;同时通过表征MnO结构变化和灭活滤料表面微生物等方法探究了MnO滤池的污染物去除机制.结果表明:运行第1d滤池出水锰即可达标,运行至第9d,滤池启动完成,可实现对水中锰和氨氮的同步有效去除.滤池可稳定同步去除锰和氨氮的最大平均浓度分别为1.4和1.6mg/L,滤速为6m/h,且通过提升水中溶解氧含量可进一步增强滤池对锰和氨氮的去除效果.SEM、EDS和XRD分析结果表明,滤池运行过程中, MnO由相对密实的颗粒堆积形态逐步发展为多孔的一体化海绵状结构,其组成由ramsdellite和birnessite型MnO2,逐步发展为buserite和birnessite型MnO2,但元素组成相对较为稳定.结合滤料表面的微生物灭活实验,认为滤池稳定运行阶段, MnO对锰的去除主要为非生物作用,对氨氮的去除以生物作用为主,化学催化氧化和吸附作用分别占16.9%~23.6%和4.4%~11%.研究结果将为利用MnO促进锰和氨氮高效过滤去除技术的发展提供理论和技术支撑.
MnO;锰;氨氮;快速启动;同步去除
饮用水中锰和氨氮污染是国内外面临的严重问题[1-3].饮用水中氨氮超标不仅会造成管道腐蚀,而且在消毒过程中会大量消耗氯并产生氯胺[4].锰超标时会危害人体的中枢神经系统,可致慢性中毒[5].我国饮用水水质标准规定,饮用水中锰和氨氮的最大限值不超过0.1和0.5mg/L[6].而在饮用水水源中,锰和氨氮污染常常同时存在,这导致其去除难度进一步增大[1].因此,探索高效稳定的锰和氨氮同步去除工艺具有重要意义.
近年来研究发现,当水中同时存在锰和氨氮污染时,水中Mn2+氧化后在滤料表面形成的锰氧化物可以通过化学或者生物作用,促进滤池对锰和氨氮的去除[7-9].已有研究表明,通过向水中投加KMnO4氧化Mn2+,可形成具有催化氧化去除水中锰和氨氮的活性锰氧化物[10].然而采用向水中投加KMnO4氧化Mn2+形成锰氧化物时,药剂投加量不易进行控制,滤池可能出红水,或过量KMnO4进入滤池破坏滤池内的生物作用,同时启动期间生成的活性MnO又大量被反冲洗带走,而通过生物氧化作用形成锰氧化物的周期往往较长[11].因此探索锰氧化物在滤料表面的快速负载方法,以及对滤池启动及运行效率的影响,具有重要意义.
本文通过在实验室条件下利用KMnO4氧化水中Mn2+形成MnO,并将其成功负载于石英砂滤料表面,制备出活性MnO滤料,并以此构筑MnO滤池.考察了MnO滤池的启动过程、运行效率、影响因素和污染物去除机制.研究结果将为利用MnO促进锰和氨氮高效过滤去除技术的发展提供理论和技术支撑.
1 材料与方法
1.1 MnOx滤料制备

图1 MnOx负载前后效果
为保证MnO在滤料表面的负载量,对石英砂滤料进行了3次负载,具体实验过程为:将粒径为1~2mm石英砂,用去离子水洗净,于105℃进行干燥,之后在1mol/L HCl中浸泡24h,并用去离子水洗至中性,再次于105℃干燥后备用.取500g石英砂,加入51mL 6% MnCl2和0.1mol/L CaCl2混合溶液并充分混合,搅拌并缓慢滴加0.3mol/L KMnO4溶液50.4mL,充分反应后于50℃干燥,获得初次负载样品,备用.取初次负载样品,重复上述步骤进行第二次负载,获得二次负载样品.之后取二次负载样品,加入51mL 9% MnCl2和0.1mol/L CaCl2混合溶液并充分混合,搅拌并缓慢滴加0.3mol/L KMnO4溶液75.6mL,反应结束后于50℃干燥,得到MnO滤料,如图1所示.可以看出,石英砂滤料表面被黑色的锰氧化物紧密包裹,MnO滤料制备成功.将其密封保存备用.
1.2 试验装置
试验装置如图2所示.图中滤柱为总高度2430mm,内径50mm的有机玻璃柱.滤柱从下到上依次是配水布气室、承托层、滤层和水头变化区.滤层填充MnO滤料,厚度为1000mm.承托层由粒径4~8mm的卵石构成,厚度为100mm.沿滤层高度分别设置了5个取样口,间距为200mm.
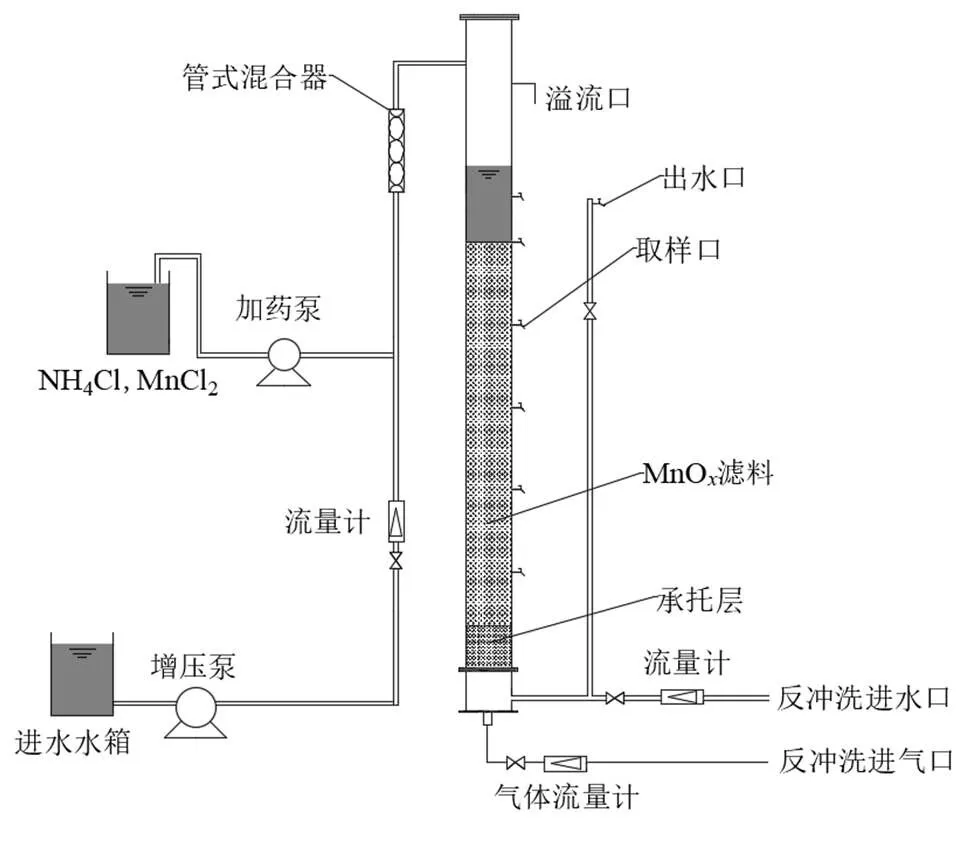
图2 试验装置示意
1.3 MnOx滤池的启动及运行
1.3.1 MnO滤池启动方法 将MnO滤料填入图2所示滤柱中,构筑MnO滤池.以自来水为水源,向其中投加一定量的氯化锰溶液和氯化铵溶液,模拟受锰和氨氮污染水体.试验期间,自来水余氯稳定,通过进水水箱后,余氯浓度为0.1~0.2mg/L.启动过程中滤速为6m/h,滤柱开始溢流时进行反冲洗,启动期间采用单独水洗,反冲洗强度为4~5L/(s∙m2),时间为8min.试验过程中,每24h取样一次,检测样品中锰、氨氮、溶解氧、pH值等水质指标.当出水锰和氨氮浓度同时满足饮用水标准限值,滤池启动完成,继续探究MnO滤池对污染物的去除规律.运行至45d时,为保障反冲洗效果,防止滤池堵塞,将反冲洗强度提升为12L/(s×m2),时间为8min.
1.3.2 溶解氧对去除效果的影响 控制滤池进水锰和氨氮浓度分别约为1.5和2.1mg/L,通过滤池底部的短柄滤头向滤池中通入空气,进行曝气实验.当空气曝气强度为0.8~1.3mL/(cm2∙min)时,可有效保障高浓度锰和氨氮去除过程中的氧需求[12-13],实际采用曝气强度为0.8mL/(cm2∙min).曝气量采用转子气体流量计进行控制(LZM-6T,余姚市宝通仪器仪表有限公司).测定曝气过程中,滤池沿程出水锰、氨氮和溶解氧含量以研究溶解氧对锰和氨氮去除的影响.
1.3.3 滤速对锰和氨氮去除效果的影响 控制进水锰和氨氮浓度分别约为1.3和1.7mg/L,滤速为6, 8和10m/h,测定不同滤速下滤柱沿程出水锰和氨氮含量,探究滤速对氨氮和锰去除效果的影响.
1.3.4 MnO生物作用与非生物作用的区分 高浓度的NaCl溶液可以破坏膜电位,导致细菌的脱水和死亡[14],而H2O2的强氧化性也可破坏细菌的细胞壁或细胞膜,有效杀死滤料表面的细菌[15],且两者对滤料表面特性几乎没有影响[16-17].为区分MnO滤料生物作用和非生物作用,进一步分析MnO对锰和氨氮的去除机理.分别利用NaCl和H2O2溶液对MnO滤料进行微生物灭活.具体方法为:于深度为20cm滤层处取出滤料,将滤料分别放入30% NaCl溶液和3% H2O2溶液中浸泡24h,之后将滤料取出并用去离子水洗净备用.配制Mn2+浓度为1.4mg/L和NH4+浓度为2mg/L的混合溶液,取100mL上述溶液于250mL锥形瓶中,并加入3.0g灭活后滤料,置于恒温水浴摇床上进行反应(水温25℃,转速150r/min),反应时间分别为5, 10, 20, 30, 45和60min.反应结束后,将反应液用0.22μm滤膜过滤,测定滤液中锰、氨氮、NO2--N和NO3--N的含量.滤料生物作用与非生物作用之间的关系按式(1)计算.
=T+T(1)
式中:为灭活前去除量(即总去除量), mg/L;T为生物作用去除量, mg/L;T为灭活后去除量(即非生物作用去除量), mg/L.
1.4 测试方法及表征
锰和氨氮分别采用高碘酸钾氧化和纳氏试剂分光光度法;NO2--N和NO3--N分别采用N-(1-萘基)-乙二胺和紫外分光光度法;DO采用HACH- HQ30D型便携溶解氧仪器测定;pH值采用PHS-3C型精密酸度计(上海雷磁)测定.表征所用滤料样品均取自深度为20cm滤层处.采用X射线衍射分析仪(XRD,MiniFlex600,日本理学)测定样品XRD谱图,Cu Kα射线,管电压40kV,管电流40mA,扫描速率5°/min,步长0.02°;表面形貌和元素组成由场发射扫描电镜搭载能谱仪进行测定(SEM-EDS,QUANTA- 450-FEG,瑞士TEXTEST).
2 结果与讨论
2.1 滤池的启动
如图3所示,阶段Ⅰ为滤池启动阶段,进水锰和氨氮浓度分别为0.4~0.7mg/L和0.9~1.2mg/L.滤池运行第1d实现出水锰浓度达标,但进出水氨氮浓度并无明显变化.运行至第9d,出水锰和氨氮浓度均可降低至水质标准线以下,滤池启动成功.研究表明,生物除锰作用的形成往往需要较长时间[18], MnO滤池运行第1d即可实现对水中Mn2+的有效去除,这说明所制备MnO在初始状态下即具有良好的非生物除锰作用.由图3(b)可知,滤池运行前7d进出水氨氮浓度无明显变化,尽管相关报道指出某些类型的MnO2可通过吸附或化学催化氧化作用去除水中氨氮[19],但本研究所制备的MnO在初始状态下并不具备对氨氮的去除能力.而运行至第9d其氨氮去除能力迅速形成,这可能是由于滤料表面硝化细菌的快速增长,或运行过程中MnO化学结构发生变化,从而形成相应的化学催化能力.这一问题将在2.3.4节继续讨论.相关报道中生物滤池的启动往往需要2~3个月[3,18],而采用KMnO4氧化水中Mn2+启动MnO催化氧化滤池也需要大约26d[10],且受水质条件的限制,滤池可能启动困难[7].这表明本研究所制备的MnO滤料可以显著缩短滤池的启动周期,节约成本.
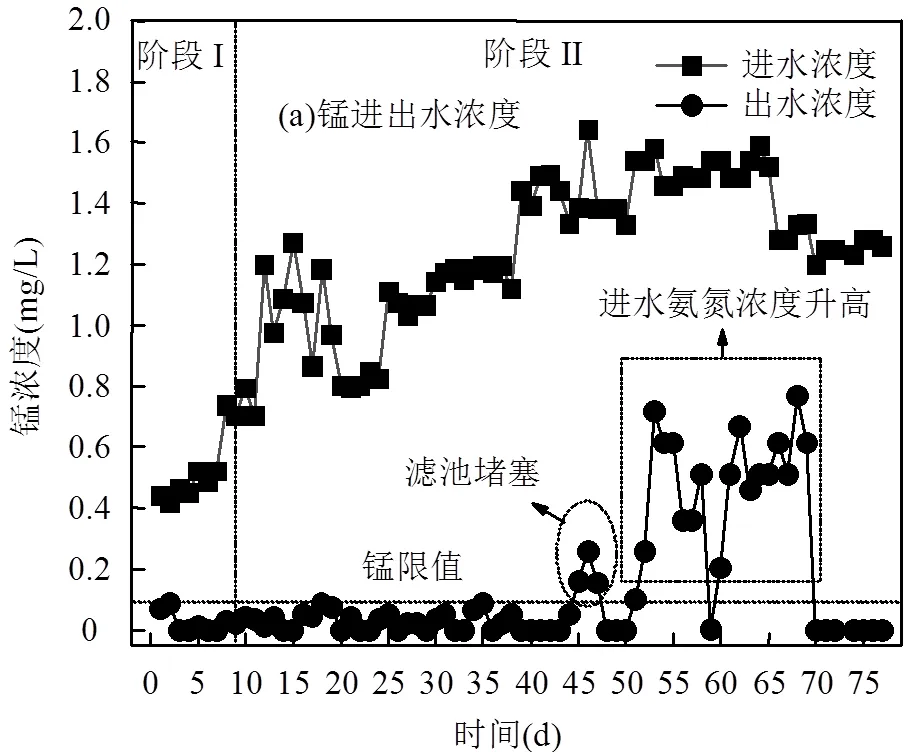
2.2 滤池运行效率的影响因素
2.2.1 进水浓度对锰和氨氮去除的影响 如图3所示,阶段Ⅱ为滤池对不同浓度锰和氨氮的同步去除效果.运行第10~44d滤池进水锰和氨氮浓度分别为0.7~1.5mg/L和0.8~1.7mg/L.运行第39~44d,滤池最大平均进水锰和氨氮浓度约为1.4和1.6mg/L,去除率分别可达99.4%和98.1%.运行至45~47d,滤柱出水锰浓度超标,且出水氨氮浓度有所提升.对滤池进行反冲洗,发现滤柱内滤料出现阻塞.因此,出水锰和氨氮浓度的升高可能是滤柱内发生短流所致.通过将滤池反冲洗强度提升至12L/(s∙m2),堵塞现象消除,此时滤池出水浓度重新达标.运行第52~69d,滤池进水锰和氨氮浓度分别为1.2~1.6mg/L和1.9~ 2.1mg/L,此时滤池出水锰和氨氮浓度超标.对滤池进出水溶解氧浓度的检测发现,进水溶解氧含量在6.5~7.2mg/L,出水则低至2.2~3.1mg/L.因此,可能是因为进水溶解氧不足,导致锰和氨氮不能完全去除.这一原因将在2.2.3节继续讨论.运行至第70~77d滤池进水锰和氨氮平均浓度为1.3和1.7mg/L,滤池出水稳定达标.
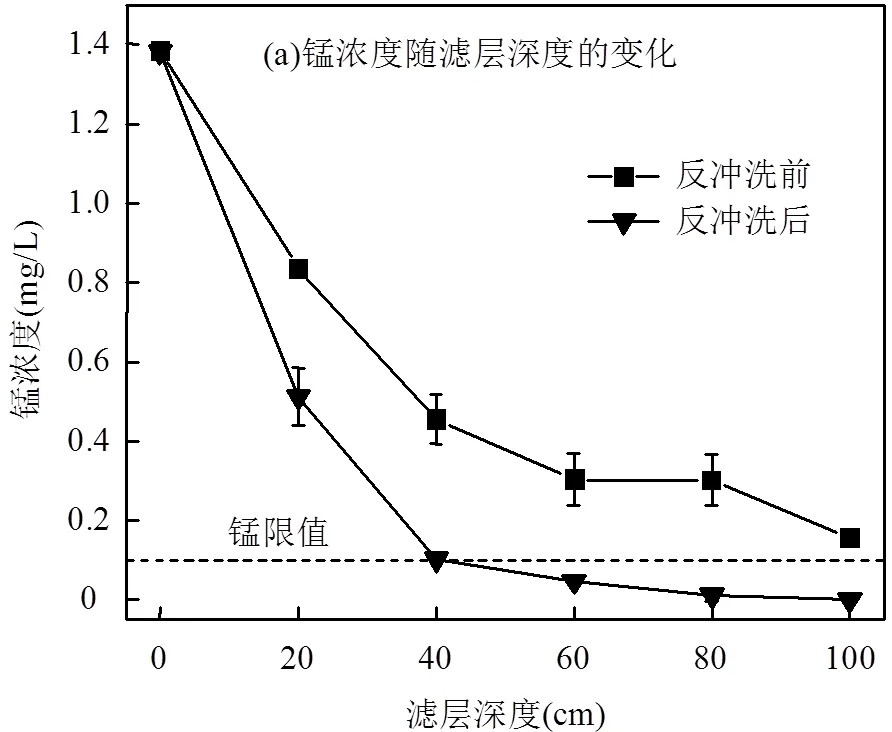
2.2.2 反冲洗的影响 滤池启动后,控制MnO滤池反冲洗周期约为7d,随着运行时间增长,滤池出水水质可能变差.如图4所示,进水锰和氨氮浓度分别约为1.4和1.6mg/L,运行至第7d(反冲洗前),出水锰超过水质标准,出水氨氮浓度升高至0.25mg/L.分析滤池运行过程可知,水中污染物可逐步在滤料表面积聚,从而造成滤料空隙率减小,滤层内实际滤速增大,甚至出现短流,同时污染物也可能会占据滤料表面反应活性位点,并引起锰和氨氮传质阻力增大,进而导致滤池锰和氨氮去除能力下降.由图4(a)、(b)可知,反冲洗后,出水锰和氨氮浓度重新降低至水质标准线以下,这表明反冲洗可有效恢复滤池对锰和氨氮的处理效果.对反冲洗前后滤料表面的元素组成进行了测定,结果如图4(c)所示,反冲洗后,滤料表面Si元素比例从5.5%下降至0.9%,Mn元素比例从19.6%上升至25.8%.这表明反冲洗过程有效去除了滤料表面的Si污染,提高了锰活性位的暴露量,进而提升了滤料活性.
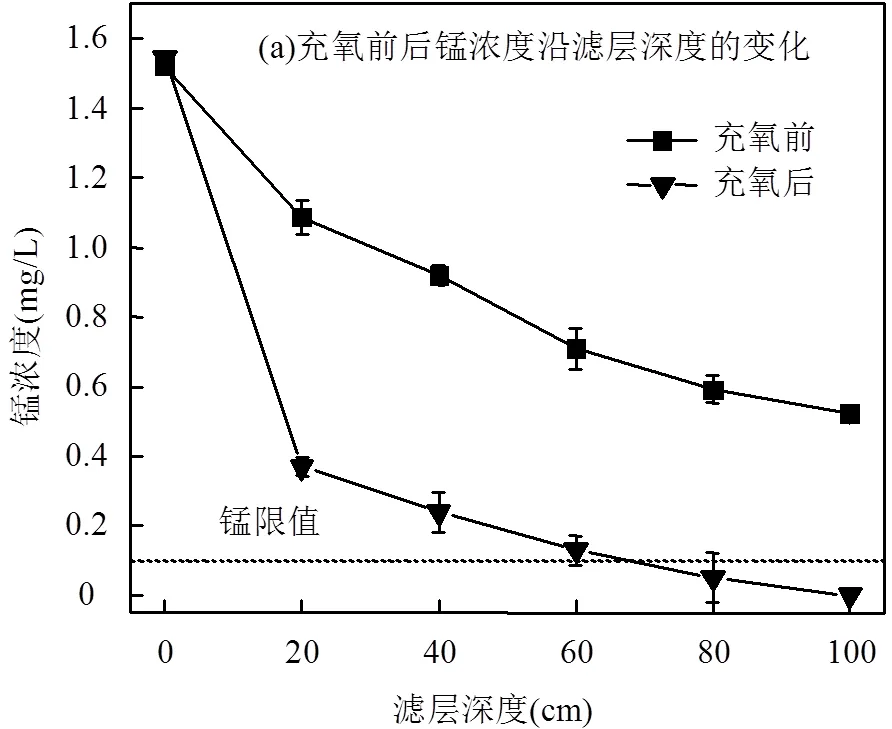
2.2.3 溶解氧对去除效果的影响 如图5(a)、(b)所示,进水锰和氨氮浓度分别约为1.5和 2.1mg/L,出水锰和氨氮浓度分别为0.5和0.6mg/L,均超过水质标准线.此时滤层中的溶解氧浓度变化如图5(c)所示.可以看出,溶解氧含量在深度为40cm滤层处降低至3.76mg/L,滤池出水溶解氧浓度仅为2.53mg/L.理论上,氧化1mg/L NH4+-N需消耗溶解氧4.57mg/L,氧化1mg/L Mn2+需消耗溶解氧0.29mg/L[11],且水中溶解氧含量对滤池氨氮和锰的去除效率有较大影响[19-20].因而可能是水中溶解氧含量降低至一定水平后, MnO对锰和氨氮的去除速率降低,进而导致滤池出水锰和氨氮超标.为进一步验证该结论,通过滤柱底部向滤柱中通入空气,以补充氨氮和锰去除过程中所需溶解氧.由图5可知,充氧后,滤池出水锰和氨氮浓度均降低至水质标准线以下,同时滤柱中溶解氧含量明显上升,滤池出水溶解氧含量达到6.53mg/L.这进一步说明水中溶解氧含量不足是导致高浓度锰和氨氮条件下滤池出水超标的重要原因.
2.2.4 滤速对去除效果的影响 控制滤速为6, 8和10m/h,进水浓度锰和氨氮分别约为1.3和1.7mg/L,考察滤速对出水水质的影响.由图6可知,滤速为6m/h时,锰和氨氮浓度均在40cm滤层处降低至水质标准线以下.而当滤速提高为10m/h,尽管滤池出水氨氮浓度仍低于0.5mg/L,但滤池出水锰浓度超过水质标准线.滤速为10m/h时,滤池出水锰浓度为0.7mg/L,去除率仅为45%.由此可知,锰的去除为该工艺的限制因素,为保证系统对锰和氨氮的同步有效去除,滤速宜控制在6m/h左右.
2.3 MnOx特性变化及污染物去除机理分析
2.3.1 MnO滤料形貌分析 分别对运行初始、运行20d、48d和73d的MnO滤料表面形貌进行表征,结果如图7所示.可以看出,初始MnO表面相对较为密实,且颗粒尺寸较小.运行20d时,氧化物形貌发生变化,表现为尺寸相对较大的、蓬松的球状颗粒堆积.运行48与73d时,滤料表面锰氧化物膜形貌逐步稳定,均表现出一定的整体性,并呈蓬松的类海绵状结构,其形貌具有非生物作用形成的锰氧化物的典型特征[21],该结构有利于Mn2+催化氧化[22].因而随着运行时间的推移,水中Mn2+可持续被氧化并负载于滤料表面,进而导致滤料表面氧化物形貌逐步发生变化,并最终趋于稳定.
2.3.2 MnO元素组成分析 由图8可知,滤料表面MnO主要由C、Ca、Al、Si、Fe、Mn、O等元素组成.其中初始滤料表面MnO中还存在一定比例的Cl和K,这可能来自于样品制备过程中使用的MnCl2∙4H2O和KMnO4药剂.而在滤池运行过程中,Cl元素和K元素最终消失,这表明Cl和K并未结合于氧化物结构之中,而仅是部分残留于氧化物表面,其含量可通过在制备过程中加强清洗而去除.另一方面,MnO滤料投入使用后,氧化物表面C比例显著升高,这可能来自于锰氧化物对水中有机物的吸附.研究表明Mn、O、Al、Ca、Fe等元素含量的变化,对MnO的锰和氨氮去除活性有较大影响[19].由图8可知,这些元素的含量在运行过程中虽有波动,但总体变化不大,这表明尽管实际水体存在较多干扰离子,但对锰氧化物的元素组成影响有限,这有利于锰氧化物在实际水处理过程中保持相对稳定的结构.
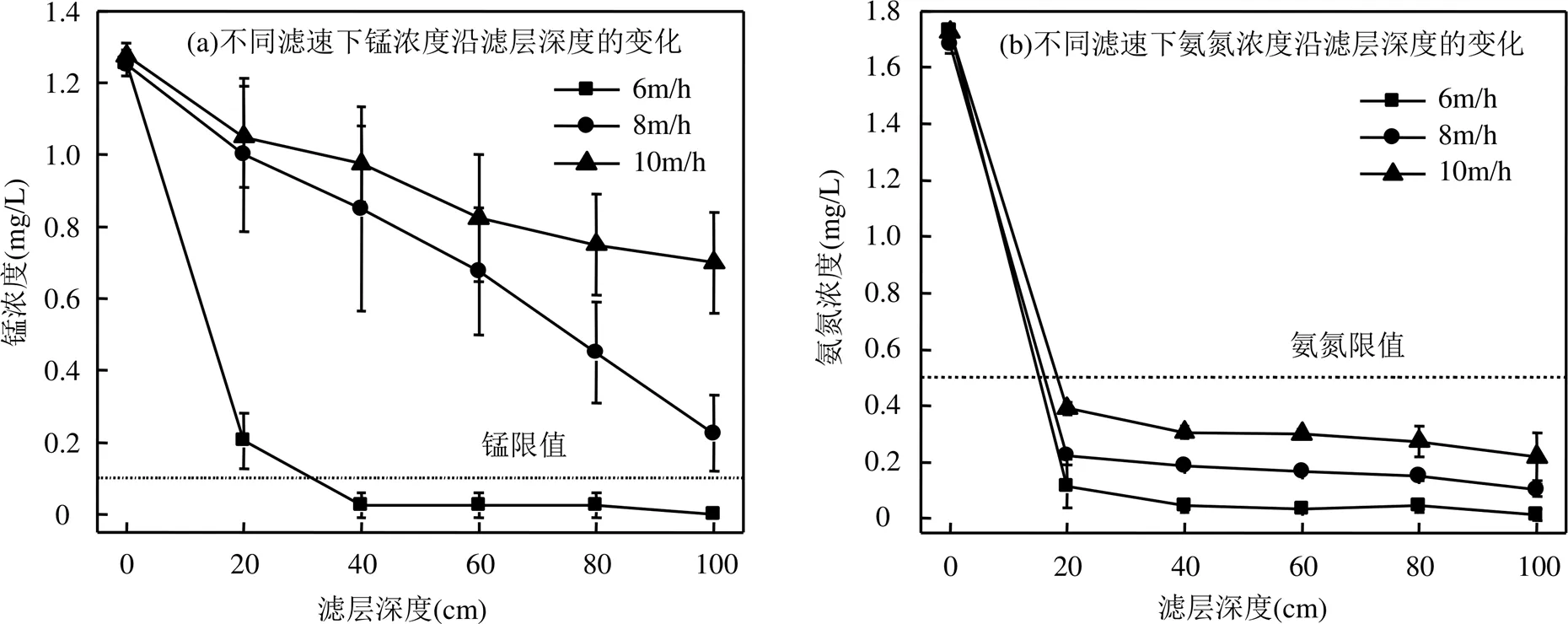
图6 不同滤速条件下锰和氨氮沿滤层深度的变化

图7 MnOx滤料SEM图(10000倍)

图8 运行过程中MnOx元素组成变化
2.3.3 MnOXRD谱图分析 图9为运行过程中MnO的XRD图.结果表明初始MnO主要为birnessite型(PDF#43-1456)和ramsdellite型(PDF#42-1316) MnO2[7],同时,还可看到与SiO2相匹配的衍射峰[23].运行至20~73d,MnO结构逐步发生变化,转变为buserite型和birnessite型MnO2.同时其主要特征峰强度逐步降低,甚至部分消失,这表明该锰氧化物结晶度进一步降低,其结构更趋于无定型态.而运行73d的氧化物谱图与文献报道的具有化学催化氧化氨氮活性的锰氧化物谱图趋于一致[19,24],研究表明,低结晶度的buserite和birnessite复合氧化物具有催化氧化去除水中氨氮的能力[7,19].该锰氧化物主要是通过氧化物中Mn(Ⅳ)、Mn(Ⅲ)和Mn(Ⅱ)之间的价态转化,将水中的NH4+氧化为NO3-[19].因此,运行至73d,该锰氧化物可能具有一定催化氧化氨氮的能力.
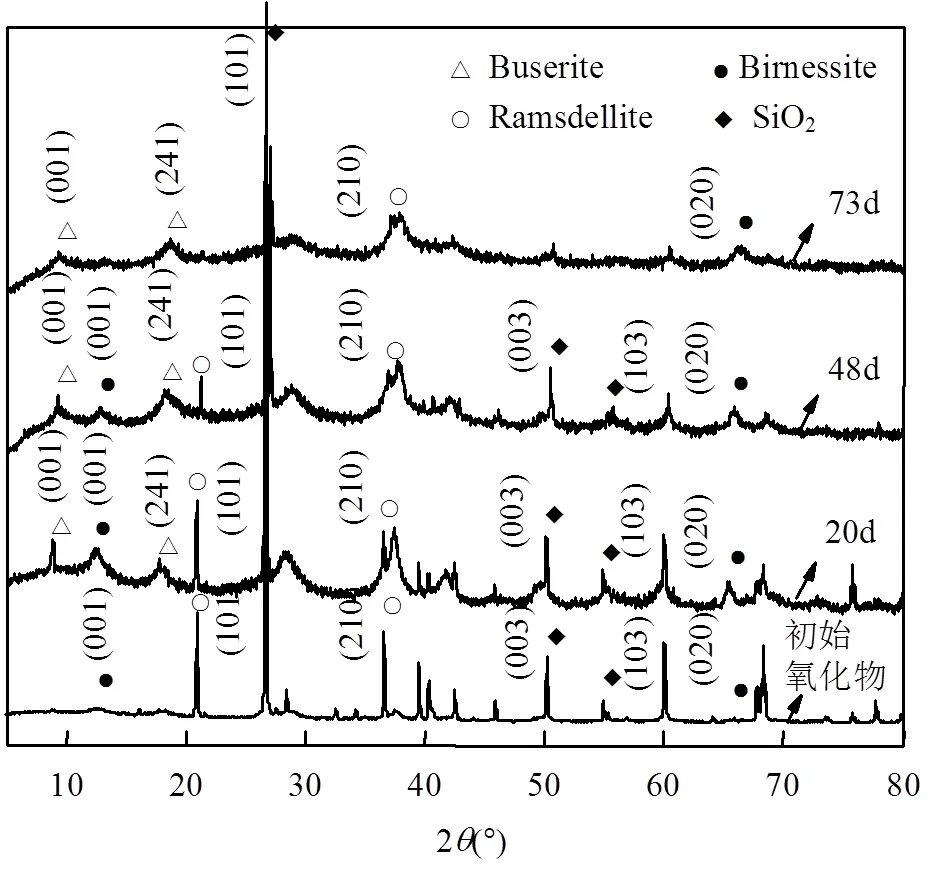
图9 运行过程中滤料XRD图
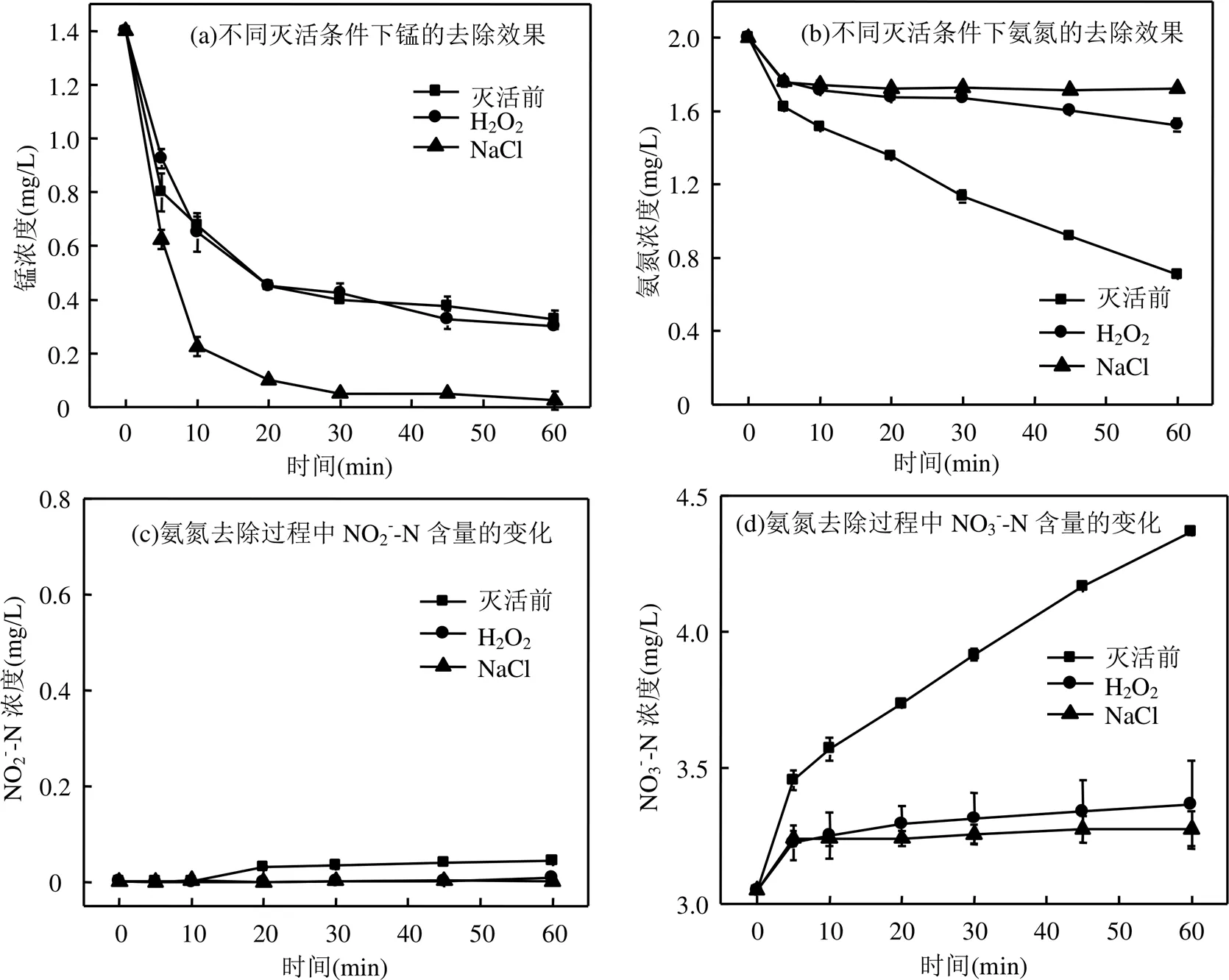
图10 不同灭活条件下MnOx滤料对锰和氨氮的去除效果以及氨氮去除过程中NO2--N和NO3--N含量的变化
2.3.4 MnO污染物去除机理分析 如图10(a)所示,采用3% H2O2灭活后, MnO对Mn2+去除效果与灭活前差异不大.而采用30% NaCl灭活后,反应至20min时水中Mn2+即可降低至0.1mg/L以下,其Mn2+去除效果甚至优于灭活前.这表明,MnO对Mn2+的去除,是以非生物作用为主导.而采用30% NaCl灭活后,MnO对Mn2+去除活性增强,可能是因为高浓度的NaCl溶液对MnO的吸附能力有再生作用[25].由图10(b)可以看出,采用3% H2O2和30% NaCl溶液灭活后, MnO对氨氮去除活性显著下降.这表明,该氧化物对氨氮的去除是以生物作用为主导.灭活前,氨氮总去除量为=1.36mg/L,以30% NaCl溶液进行灭活后,氨氮总去除量为T=0.29mg/L (非生物作用),占总去除量的21.3%.根据公式(1)计算可得,生物作用去除量为T=1.07mg/L,占总去除量的78.7%.滤料非生物作用同时包括吸附作用和化学作用,化学作用可将氨氮氧化为硝酸盐和亚硝酸盐[19].由图10(c)可知,灭活后氨氮去除过程中系统亚硝酸几乎没有增加,硝酸增加量为0.23mg/L(图10(d)).这表明滤料通过化学作用所去除氨氮量为0.23mg/L,吸附作用去除氨氮量为0.06mg/L,两者占比分别为16.9%和4.4%.同理,对3% H2O2溶液灭活后的实验结果进行计算,得到对应的生物作用、化学作用和吸附作用占比分别为65.4%、23.6%和11%.这表明该氧化物可同时通过化学催化氧化去除水中氨氮.这与XRD谱图的分析结果相一致(图9).尽管化学催化氧化和吸附作用占比较小,但生物与非生物的共同作用,可能是滤池具有高效、稳定氨氮去除活性的重要原因.
综合前述试验结果,分析认为所制备的MnO滤料,之所以可以实现滤池的快速启动和高效运行,一方面是因为MnO具有高效的非生物除锰能力,另一方面可以有效促进硝化细菌在滤料表面的生长,同时具有一定的化学催化氧化水中氨氮的能力.
3 结论
3.1 MnO可以实现同步除锰氨氮滤池的快速启动.滤池运行第1d,出水锰浓度即可达到水质标准限值,运行至第9d,滤池启动完成,可同步去除水中锰和氨氮.
3.2 该工艺可同步有效去除的最大锰和氨氮平均浓度分别为1.4和1.6mg/L,去除率分别可达99.4%和98.1%,适宜滤速为6m/h,反冲洗可有效恢复系统运行效果,同时通过提升水中溶解氧含量,可以进一步提升滤池的污染物去除负荷.
3.3 滤池运行过程中,氧化膜表面形态逐步趋于一体化的海绵状结构,氧化物主要组成转变为buserite型和birnessite型MnO2,且元素组成相对稳定.
3.4 MnO滤池对水中锰主要通过非生物作用去除,对氨氮主要通过生物作用去除,同时也具有一定的化学催化氧化水中氨氮的能力.
[1] Hasan H A, Abdullah S R S, Kamarudin S K ,et al. Simultaneous NH4+-N and Mn2+removal from drinking water using a biological aerated filter system: Effects of different aeration rates [J]. Separation and Purification Technology, 2013,118:547-556.
[2] Zhang Q, Zhang S, Lyu C, et al. A cost-effective catalytically adsorbent for in situ remediation of manganese contaminated groundwater [J]. Water Science & Technology: Water Supply, 2018, 18(1/2):504-514.
[3] 王刘煜,李 冬,曾辉平,等.低温高铁锰氨氮地下水两级生物净化快速启动[J]. 中国环境科学, 2019,39(6):2361-2369.
Wang L Y, Li D, Zeng H P, et al. Rapid startup of two-stage bio-purification of low temperature groundwater containing high concentration of iron, manganese and ammonia nitrogen [J]. China Environmental Science, 2019,39(6):2361-2369.
[4] Tekerlekopoulou A G, Papazafiris P G D, Vayenas D V. A full-scale trickling filter for the simultaneous removal of ammonium, iron and manganese from potable water [J]. Journal of Chemical Technology & Biotechnology, 2010,85(7):1023-1026.
[5] 唐朝春,陈惠民,叶 鑫,等.地下水除铁除锰方法的研究进展[J]. 水处理技术, 2016,42(3):7-12.
Tang Z C, Chen H M, Ye X, et al. Advances on the method of removing iron and manganese in groundwater [J]. Technology of Water Treatment, 2016,42(3):7-12.
[6] GB5749-2006 生活饮用水卫生标准[S].
GB5749-2006 Standards for drinking water quality [S].
[7] Yang H, Tang X, Bai L, et al. Synergistic effects of prokaryotes and oxidants in rapid sand filters treatment of groundwater versus surface water: Purification efficacy, stability and associated mechanisms [J]. Chemosphere, 2022,295:133804.
[8] 宫喜君.东北小村镇地区地下水中铁锰氨氮去除实验研究[D]. 长春:吉林大学, 2015.
Gong X J. Removal of iron, manganese and ammonia from groundwater of northest small towns [D]. Changchun: Ji Lin University, 2015.
[9] 李圭白,杨海洋,仲 琳,等.锰质滤膜活性对接触氧化除锰及除氨氮效能的影响[J]. 中国给水排水, 2020,36(21):1-6.
Li G B, Yang H Y, Zhong L, et al. Effect of manganese oxides film activity on removal efficiencies of manganese and ammonia nitrogen by contact oxidation [J]. China Water & Wastewater, 2020,36(21): 1-6.
[10] Guo Y, Huang T, Wen G, et al. The simultaneous removal of ammonium and manganese from groundwater by iron-manganese co-oxide filter film: The role of chemical catalytic oxidation for ammonium removal [J]. Chemical Engineering Journal, 2017,308: 322-329.
[11] Cai Y, Li D, Liang Y, et al. Operational parameters required for the start-up process of a biofilter to remove Fe, Mn, and NH3-N from low-temperature groundwater [J]. Desalination and Water Treatment, 2016,57(8):3588-3596.
[12] 阮昭意.逆流充氧强化铁锰复合氧化膜去除地表水中高浓度氨氮/锰的研究[D]. 西安:西安建筑科技大学, 2020.
Ruan Z Y. Study of Enhancing removal high concentration ammonium and manganese from surface water by oxygenating in reverse flow [D]. Xi’an: Xi’an University of Architecture and Technology, 2020.
[13] Zhang W, Zhang R, Yang Y, et al. Removal of high concentrations of ammonium from groundwater in a pilot-scale system through aeration at the bottom layer of a chemical catalytic oxidation filter [J], Environmental Researchand Public Health, 2019,16(20):3989.
[14] Rivera-Araya J, Schlömann M, Levicán G. Comparative study of NaCl-tolerance mechanisms in acidophilic iron-oxidizing bacteria and archaea [J]. Solid State Phenomena, 2017,262:385-388.
[15] Labas M D, Zalazar C S, Brandi R J, et al. Reaction kinetics of bacteria disinfection employing hydrogen peroxide [J]. Biochemical Engineering Journal, 2008,38(1):78-87.
[16] Yang H, Yan Z, Du X, et al. Removal of manganese from groundwater in the ripened sand filtration: biological oxidation versus chemical auto-catalytic oxidation [J]. Chemical Engineering Journal, 2019, 382(1):123033.
[17] Cheng Y, Xiong W, Huang T. Catalytic oxidation removal of manganese from groundwater by iron–manganese co-oxide filter films under anaerobic conditions [J]. Science of The Total Environment, 2020,737:139525.
[18] Cheng Q, Li N, Bao L, et al. Distribution and genetic diversity of microbial populations in the pilot-scale biofilter for simultaneous removal of ammonia, iron and manganese from real groundwater [J]. Chemosphere, 2017,182:450-457.
[19] Cheng Y, Huang T, Sun Y, et al. Catalytic oxidation removal of ammonium from groundwater by manganese oxides filter: Performance and mechanisms [J]. Chemical Engineering Journal, 2017, 322:82-89.
[20] 张吉库,刘明秀.溶解氧和温度对地下水除铁、锰效果的影响[J]. 安全与环境工程, 2006,13(1):52-54.
Zhang J K, Liu M X. The influence of temperature and dissolved oxygen on removing manganese and iron from groundwater [J]. Safety and Environmental Engineering, 2006,13(1):52-54.
[21] Jiang S, Kim D G, Kim J H, et al. Characterization of the biogenic manganese oxides produced by pseudomonas putida strain MnB1 [J]. Environmental Engineering Research, 2010,15(4):183-190.
[22] Bruins J H, Petrusevski B, Slokar Y M, et al. Biological and physico-chemical formation of Birnessite during the ripening of manganese removal filters [J]. Water Research, 2015,69:154-161.
[23] Duttal S, Bose1S, Ghosh C K, et al. Low temperature synthesis of nickel silica nanocomposites through sol-gel route [J]. Journal of Chemical Engineering and Materials Science, 2013,4(4):50-57.
[24] Cheng Y, Huang T, Chneg L, et al. Structural characteristic and ammonium and manganese catalytic activity of two types of filter media in groundwater treatment [J]. Journal of Environmental Sciences, 2018,72(10):89-97.
[25] Johnson E A, Post J E. Water in the interlayer region of birnessite: Importance in cation exchange and structural stability [J]. American Mineralogist, 2006,91(4):609-618.
Rapid start-up and pollutant removal mechanism of MnOfilter for simultaneous removal of manganese and ammonium.
ZHANG Rui-feng*, YANG Shi-lian, YANG Jing, GUO Ying-ming, CHEN Xi
(School of Urban Planning and Municipal Engineering,Xi’an Polytechnic University, Xi’an 710600, China)., 2023,43(1):197~205
A dynamic experiment was conductedby coating MnOon the surface of quartz sand to form MnOfilter media and constructing a filter with it. The start-up period, pollutant removal efficiency and influencing factors of the filter were investigated and the pollutant removal mechanism of the MnOfilter was explored by characterizing the structural changes of MnOand inactivating the microorganisms on the surface of the filter media. The results showed thatthe manganese in the effluent of the filter can meet the standard in the first day of operation, and it can achieve the simultaneous and effective removal of manganese and ammonium from water when the filter starts to complete in the 9th day of operation. The maximum average concentrations of manganese and ammonium were 1.4 and 1.6 mg/L respectively at the filtration rate of 6 m/h. The efficient removal of manganese and ammonium could be further enhanced by increasing the dissolved oxygen content in the water. The results of SEM, EDS and XRD analysis showed that during the operation of the filter, MnOgradually developed from a relatively dense particle accumulation morphology to a porous integrated sponge-like structure, and its composition gradually developed from ramsdellite and birnessite type MnO2to buserite and birnessite type MnO2, but the elemental composition was relatively stable. Combined with the microbial inactivation experiments on surface of the filter media, it was concluded that the removal of manganese from the filter during the stable operation stage was mainly abiotic, and the removal of ammonium was mainly biological, with chemical catalytic oxidation and adsorption accounting for 16.9%~23.6% and 4.4%~11%, respectively. The results of the study will provide theoretical and technical support for the development of efficient filtration removal technologies for manganese and ammonium using MnO.
MnO;manganese;ammonium;rapid start-up;simultaneous removal
X52
A
1000-6923(2023)01-0197-09
张瑞峰(1989-),男,陕西咸阳人,讲师,博士,研究方向为给水处理理论与技术.发表论文7篇.
2022-06-02
陕西省重点研发计划项目(2022SF-287);陕西省自然科学基础研究计划项目(2021JQ-688, 2021JQ-690);陕西省教育厅专项科研计划项目(20JK0656);西安工程大学研究生创新基金资助项目(chx2022029);西安工程大学博士科研启动项目(107020418)
* 责任作者, 讲师, ruifengzhangtry@xpu.edu.cn
