石草鞋化学成分及对人乳腺癌高转移细胞增殖的影响
2023-01-18唐素勤
唐素勤,罗 顺
(1.河南省中医药研究院,河南 郑州,450004;2.河南中医药大学第三附属医院,河南 郑州,450002)
石草鞋,又称铁足板、铁草鞋、打草鞋,为萝藦科植物球兰属香花球兰Hoya lyi Levl.[H.yuen-nanensis Hand.-Mazz]的全草[1],广泛分布于海拔800~2400 m的丘陵、山地密林间,常附生于岩石和大树上。石草鞋性温,味辛、微酸,具有化瘀活血、祛风除湿、消积化食的功效,用于皮疹、跌打损伤、风湿关节痛、脚强痛、胸前饱胀[2]。石草鞋的主要化学成分为黄酮类、香豆素类、三萜类、有机酸类、甾体类等[3],现代药理作用表明,石草鞋具有抗肿瘤、抗衰老、抗炎、降低血管 通 透 性、抗 病 毒 等 活 性[4]。代 红 梅 等[5]从 石 草 鞋95%乙醇提取物中分离得到11个化合物,除阿魏酸外,均为首次从石草鞋中分离得到。本研究组曾对石草鞋的化学成分进行分离,鉴定出39个单体化合物[6-8]。本研究组通过前期预实验,发现石草鞋对乳腺癌细胞具有一定的抑制作用。为进一步探讨石草鞋对乳腺癌细胞增殖影响的作用基础,笔者对石草鞋乙醇提取物再次进行分离纯化,并研究所得化合物对人乳腺癌高转移(MDA-MB-435)细胞增殖的影响,现报道如下。
1 仪器与材料
核磁共振波谱仪(瑞士Bruker公司,Avance Neo型),质谱仪(美国Thermofisher公司,TSQ Altis型),全自动转子离心机(惠州市华高仪器设备有限公司,Rosh87型),超声波清洗器(济宁隆成仪器设备有限公司,Kldk-1200L型),电子天平(广州晓芬仪器有限公司,Rohs1100型),葡聚糖凝胶LH-20(Sephadex LH-20,瑞士Pharmacia公司,20200911),柱色谱硅胶(青岛海洋化工厂,100~200目、300~400目),薄层硅胶板(青岛海洋化工厂,GF254型),二甲基亚砜(德国Biofroxx公司,批号20200506),噻唑蓝(上海西唐生物科技有限公司,批号20210125),人乳腺癌高转移细胞株(MDA-MB-435,中科院上海生命科学研究院,批号20210219),5-氟尿嘧啶(海南卓泰制药有限公司,国药准字H20051626)。所用试剂均为分析纯。
石草鞋采自河南省郑州市,经河南省中医药研究院王治阳副主任药师鉴定为石草鞋Hoya lyi Levl.的全草,标本收藏于河南省中医药研究院标本室。
2 药材提取
取干燥的石草鞋全草21.4 kg,采用90%乙醇溶液加热回流提取3次,每次2 h。合并提取液,过滤、减压浓缩后,得石草鞋浸膏2.1 kg。浸膏经超声溶解于水中,分别采用等体积的石油醚、二氯甲烷、乙酸乙酯和正丁醇萃取,所得提取液分别减压浓缩,得石油醚部分浸膏273.9 g、二氯甲烷部分浸膏217.4 g、丙酮部分浸膏172.9 g、正丁醇部分浸膏264.7 g。
3 提取物分离
3.1 二氯甲烷部分的分离
取二氯甲烷部分,采用硅胶拌样,经硅胶(100~200目)色谱柱,以石油醚-丙酮(75∶25-50∶50-25∶75)进行梯度洗脱,得到7个流分(Fr.B1~7)。Fr.B2(12.6 g)经硅胶(100~200目)色谱柱,以石油醚-乙酸乙酯(70∶30-50∶50-20∶80)进行梯度洗脱,得到6个组分Fr.B2-1~Fr.B2-6。Fr.B2-3(0.9 g)经硅胶(300~400目)色谱柱,以石油醚-丙酮(40:60)进行洗脱,得化合物2(19 mg)、5(26 mg);Fr.B2-5(0.6 g)经结晶、重结晶,得化合物4(24 mg)。Fr.B4(17.4 g)经硅胶(100~200目)色谱柱,以石油醚-乙酸乙酯(50∶50-20∶80)进行梯度洗脱,得到7个组分Fr.B4-1~Fr.B4-7。Fr.B4-2(0.8 g)经硅胶(300~400目)色谱柱,以石油醚-丙酮(30:70)进行洗脱,得化合物1(28 mg)、8(31 mg);Fr.B4-3(0.4 g)经Sephadex LH-20色谱柱,以甲醇进行洗脱,得化合物7(18 mg)。
3.2 乙酸乙酯部分的分离
取乙酸乙酯部分浸膏,采用硅胶拌样,经硅胶(100~200目)色谱柱,以二氯甲烷-丙酮(90∶10-50∶50-10∶90)进行梯度洗脱,得到7个流分(Fr.C1~7)。Fr.C3(10.3 g)经硅胶(100~200目)色谱柱,以二氯甲烷-丙酮(80∶20-50∶50-20∶80)进行梯度洗脱,得到8个组分Fr.C3-1~Fr.C3-8。Fr.C3-2(0.7 g)经硅胶(100~200目)色谱柱,以二氯甲烷-丙酮(40∶60)进行洗脱,得化合物10(25 mg);Fr.C3-4(0.9 g)经硅胶(300~400目)色谱柱,以二氯甲烷-丙酮(30∶70)进行洗脱,得化合物3(32 mg)、12(17 mg)。Fr.C6(11.2 g)经硅胶(100~200目)色谱柱,以二氯甲烷-丙酮(30∶70-70∶30)进行梯度洗脱,得到5个组分Fr.C6-1~Fr.C6-5。Fr.C6-3(0.6 g)经硅胶(100~200目)色谱柱,以二氯甲烷-丙酮(40∶60)进行洗脱,得化合物6(23 mg)。
3.3 正丁醇部分的分离
取正丁醇部分浸膏,采用硅胶拌样,经硅胶(100~200目)色谱柱,以丙酮-甲醇(80∶20-50∶50-20∶80)进行梯度洗脱,得到8个流分(Fr.D1~8)。Fr.D4(8.1 g)经硅胶(100~200目)色谱柱,以丙酮-甲醇(80∶20-50∶50-20∶80)进行梯度洗脱,得到6个组分Fr.D4-1~Fr.D4-6。Fr.D4-3(0.4 g)经硅胶(300~400目)色谱柱,以丙酮-甲醇(30∶70)进行洗脱,得化合物9(31 mg);Fr.D4-5(0.3 g)经Sephadex LH-20色谱柱,以甲醇进行洗脱,得化合物11(28 mg)。
4 化合物结构鉴定
化合物1:白色粉末(甲醇),分子式:C20H32O2,EIMS m/z:327.4[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:7.81(2H,dd,J=8.2,2.2 Hz,H-2,5),7.49(2H,q,J=8.2,2.2 Hz,H-3,4),3.97(4H,d,J=8.2 Hz,H-1',1″),1.86(2H,m,H-2',2″),1.04(12H,d,J=8.2 Hz,H-3',3″,4',4″)。13C-NMR(DMSO-d6,150MHz)δ:131.9(C-1),127.6(C-2),129.4(C-3),129.4(C-4),127.6(C-5),131.9(C-6),72.3(C-1'),28.1(C-2'),20.6(C-3'),20.6(C-4'),72.3(C-1″),28.1(C-2″),20.6(C-3″),20.6(C-4″),168.2(C=O)。以上数据与参考文献[9]isoagatholal数值基本一致。
化含物2:白色粉末(甲醇),EMS m/z:331.2[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:6.81(1H,s,H-5),5.24(1H,m,H-3),4.63(1H,d,J=8.2 Hz,H-4),4.23~4.08(1H,m,H-10),3.86(3H,s,6-OH3),3.75(3H,5,7-OCH3),2.59~2.51(1H,m,H-9β),1.95(1H,dd,J=12.0,8.2,2.2 Hz,H-9a),1.58(1H,m,H-11β),1.49(1H,m,H-11β),1.29(2H,m,H2-12),1.04(3H,t,J=8.2 Hz,H3-13)。13C-NMR(DMSO-d6,150 MHz)δ:171.2(C-1),159.6(C-2),82.7(C-3),106.2(C-4),107.1(C-5),104.6(C-6),139.1(C-7),161.4(C-8),39.7(C-9),80.3(C-10),40.2(C-11),19.8(C-12),13.7(C-13),76.4(7-OCH3),56.9(C-OCH3)。以上数据与参考文献[10]monoeerin基本一致。
化合物3:黄色粉末(甲醇),ESI-MS m/z:200.7[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:7.57(1H,d,J=8.2 Hz,H-7),7.39(2H,d,J=8.2 Hz,H-2,6),6.68(2H,d,J=8.2 Hz,H-3,5),6.31(1H,d,J=8.2 Hz,H-8),3.84(3H,s,9-OCH3)。13C-NMR(DMSO-d6,150 MHz)δ:129.1(C-1),127.4(C-2),117.5(C-3),163.1(C-4),115.4(C-5),1295(C-6),144.6(C-7),114.8(C-8),167.4(C-9),51.7(9-OCH3)。以上数据与参考文献[11]对羟基肉桂酸甲酯数值基本一致。
化合物4:白色粉末(甲醇),EMS m/z:413.1[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:7.13(1H,t,J=8.2 Hz,H-3),5.61(1H,d,J=8.2 Hz,H-1),5.39(1H,m,H-8),5.14(1H,m,H-10a),5.07(1H,m,H-10β),4.72(1H,d,J=8.2 Hz,H-1'),3.91(1H,m,H-6'a),3.75(1H,m,H-6'β),3.63(2H,m,H-6),3.37~2.94(4H,m,H-2',3',4',5'),2.81(1H,dd,J=8.2,2.2 Hz,H-5),2.25(1H,q,J=8.2 Hz,H-9)。13C-NMR(DMSO-d6,150 MHz)δ:96.5(C-1),91.4(C-2),152.8(C-3),108.4(C-4),27.3(C-5),35.1(C-6),170.8(C-7),133.6(C-8),45.1(C-9),120.7(C-10),175.8(C-11),102.4(C-1'),73.5(C-2'),77.4(C-3'),71.2(C-4'),78.1(C-5'),63.1(C-6')。以上数据与参考文献[12]secologanoside基本一致。
化合物5:白色粉末(甲醇),EMS m/z:301.4[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:7.68(2H,dd,J=8.2Hz,2.2Hz,H-2,5),7.59(2H,dd,J=8.8Hz,2.2Hz,H-3,4),3.52(2H,d,J=8.2 Hz,H-1',1″),1.96(2H,m,H-2',2″),1.03(12H,m,J=8.2,H-3',3″,4',4″)。13CNMR(DMSO-d6,150 MHz)δ:134.2(C-1),130.1(C-2),135.7(C-3),135.7(C-4),130.1(C-5),134.2(C-6),73.2(C-1'),28.3(C-2'),20.1(C-3'),20.1(C-4'),73.2(C-1″),28.3(C-2″),20.1(C-3″),20.1(C-4″),171.5(C-1α,2α)。以上数据与参考文献[13]邻苯二甲酸二正丁酯基本一致。
化合物6:黄色结晶(丙酮),ESI-MS m/z:214.7[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:9.71(1H,brs,4-OH),7.68(2H,d,J=8.2 Hz,H-2,6),6.81(1H,d,J=8.2 Hz,H-7),6.64(2H,d,J=8.2 Hz,H-3,5),5.71(1H,d,J=8.2Hz,H-8),4.05(1H,q,J=8.2Hz,H-1′),1.24(3H,t,J=8.2Hz,H-2′)。13C-NMR(DMSO-d6,150 MHz)δ:125.1(C-1),134.0(C-2),112.1(C-3),132.6(C-4),111.2(C-5),136.1(C-6),143.0(C-7),115.4(C-8),166.2(C-9),60.1(C-1′),112.6(C-2′)。以上数据与参考文献[14]对羟基肉桂酸乙酯数值基本一致。
化合物7:白色粉末(丙酮),ESI-MS m/z:193.1[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:4.29(1H,m,H-7),4.20(1H,m,H-1α),3.71(1H,m,H-1β),2.83(1H,m,H-5),2.69(1H,dd,J=12.0,8.2 Hz,H-4α),2.56(1H,m,H-9),2.51(1H,dd,J=12.0,8.2 Hz,H-4β),2.05(1H,m,H-8),1.87(1H,ddd,J=14.0,12.0,8.2Hz,H-6α),1.68(1H,ddd,J=14.0,12.0,8.2 Hz,H-6β),1.03(3H,d,J=14.0 Hz,H-10)。13C-NMR(DMSO-d6,150 MHz)δ:68.1(C-1),71.9(C-2),176.3(C-3),32.8(C-4),36.1(C-5),39.7(C-6),77.2(C-7),41.5(C-8),46.2(C-9),13.1(C-10)。以上数据与参考文献[15]isobonein数值基本一致。
化合物8:白色粉末(甲醇),ESI-MS m/z:309.7[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:7.71(1H,d,J=12.0 Hz,H-4),7.13(1H,d,J=12.0 Hz,H-5),6.68(1H,d,J=12.0 Hz,H-6),6.18(1H,d,J=12.0 Hz,H-3),5.06(1H,dd,J=8.2,2.2 Hz,H-2'),3.42(1H,dd,J=8.2,2.2 Hz,H-3'),3.28(1H,dd,J=8.2,2.2 Hz,H-3'),2.05(3H,s,H-4″),1.63(3H,s,1″-CH3),1.41(3H,s,1″-CH3)。13C-NMR(DMSO-d6,150 MHz)δ:132.4(C-1),155.8(C-2),116.1(C-3),147.9(C-4),125.4(C-5),107.1(C-6),165.8(C-7),112.1(C-8),149.2(C-9),114.7(C-10),107.3(C-1'),89.7(C-2'),29.8(C-3'),83.6(C-1″),168.5(C-3″),25.1(C-4″),26.4(1″-CH3),21.3(4″-CH3)。以上数据与参考文献[16]columbianetin acetate数值基本一致。
化合物9:白色粉末(甲醇),ESI-MS m/z:427.1[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:5.73(1H,d,J=12.0 Hz,H-6),4.68(1H,d,J=12.0 Hz,H-1’),4.51(1H,d,J=12.0 Hz,H-7),1.27(3H,s,12-OCH3)。13CNMR(DMSO-d6,150 MHz)δ:95.3(C-1),135.2(C-2),155.7(C-3),111.4(C-4),128.3(C-5),142.6(C-6),77.1(C-7),74.0(C-8),52.3(C-9),57.8(C-10),168.3(C-11),100.5(C-1'),72.4(C-2'),76.1(C-3'),70.2(C-4'),77.6(C-5'),59.3(C-6'),50.1(12-OCH3)。以上数据与参考文献[17]gentioside数值基本一致。
化合物10:白色晶体(甲醇),ESI-MS m/z:218.9[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:12.51(1H,s,-OH),6.08(1H,d,J=12.0 Hz,H-4),5.91(1H,d,J=12.0 Hz,H-7),4.03(3H,s,6-OCH3),3.84(3H,s,5-OCH3),2.61(3H,s,2-OCH3)。13C-NMR(DMSO-d6,150 MHz)δ:200.4(C-1),106.1(C-2),171.2(C-3),93.9(C-4),166.2(C-5),161.7(C-6),90.8(C-7),33.1(2-OCH3),55.4(5,6-OCH3)。以上数据与参考文献[18]crototropone数值基本一致。
化合物11:白色粉末(丙酮),ESI-MS m/z:174.8[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:9.62(1H,s,H-7),7.38(2H,dd,J=12.0,8.2 Hz,H-2,6),6.93(1H,d,J=12.0 Hz,H-5),3.85(3H,s,4-OCH3)。13C-NMR(DMSO-d6,150 MHz)δ:129.1(C-1),131.4(C-2),145.7(C-3),161.3(C-4),112.7(C-5),117.4(C-6),56.3(4-OCH3),192.5(7-CHO)。以上数据与参考文献[19]3-羟基对甲氧基苯甲醛数值基本一致。
化合物12:白色粉末(丙酮),分子式:C15H22O3,ESI-MS m/z:272.8[M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:6.41(1H,d,J=12.0 Hz,H-13a),5.64(1H,d,J=12.0 Hz,H-13β),4.27(1H,m,H-8),4.08(1H,t,J=12.0 Hz,H-4),0.93(3H,d,J=12.0 Hz,H-14),0.76(3H,s,H-15)。13C-NMR(DMSO-d6,150 MHz)δ:45.1(C-1),25.3(C-2),30.5(C-3),85.1(C-4),46.3(C-5),38.1(C-6),49.2(C-7),83.5(C-8),46.3(C-9),31.4(C-10),139.7(C-11),171.2(C-12),118.4(C-13),20.6(C-14),19.3(C-15)。以上数据与参考文献[20]2-desoxy-4-epi-pulchellin数值基本一致。
5 抑制细胞增殖活性成分筛选
采用噻唑蓝(MTT)法[21]测试12个化合物的体外抗MDA-MB-435细胞的活性,以5-氟尿嘧啶为阳性对照物。取对数生长期的MDA-MB-435细胞,稀释成密度为每毫升5×104个的单细胞混悬液,每孔取100μL置于96孔板中,在37.0℃恒温条件下培养24 h。然后分别加入5-氟尿嘧啶,5种不同浓度的化合物(0.1、1.0、5.0、10.0、15.0μg/mL),培养24 h后,每孔分别加入10μL MTT溶液染色,继续培养6 h,移弃上清液。每孔分别加入100μL二甲基亚砜溶液,轻摇均匀。采用酶标仪在490 nm波长下测定吸光度,计算MDA-MB-435细胞的抑制率及半数抑制浓度(IC50)值。结果显示化合物2的IC50值为12.35μg/mL,化合物10的IC50值为9.51μg/mL,其他化合物对MDA-MB-435细胞无明显抑制作用。见表1。
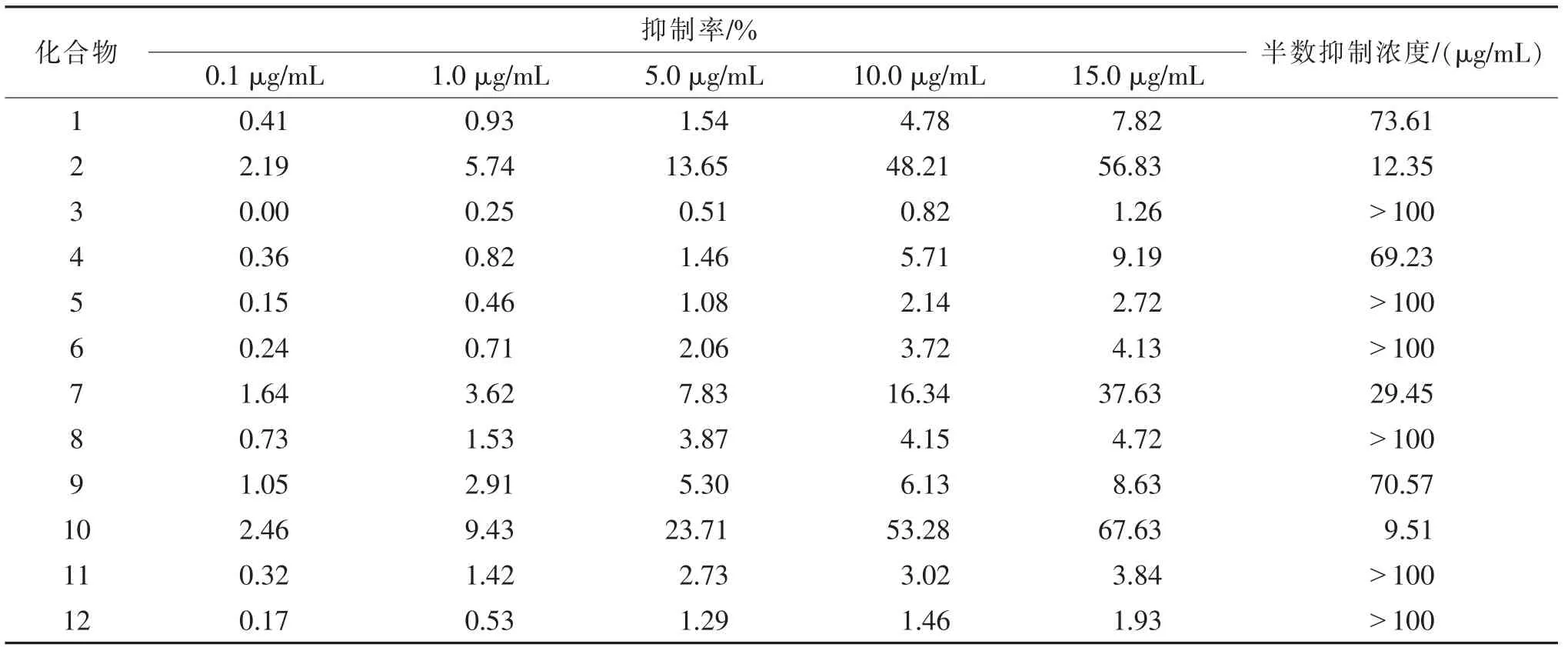
表1 石草鞋中12种化合物对人乳腺癌高转移细胞的体外抑制率及半数抑制浓度
6 结论
本研究从石草鞋90%乙醇提取物中分离得到12个化合物,所有化合物均为首次从石草鞋全草中分离得到,其中化合isoagatholal(1)、monoeerin(2)、isobonein(7)、gentioside(9)、crototropone(10)为首次从该属植物中分离得到。化合物monoeerin(2)、crototropone(10)对MDA-MB-435细胞具有一定的抑制作用。本研究丰富了石草鞋的化学成分资料库,为抑制细胞增殖新药的研发提供了一定依据。
