手术显微镜与手术放大镜下切除周围神经鞘膜瘤的临床效果比较
2023-01-18夏平光张宝成赵东东中部战区总医院骨科湖北武汉430070
夏平光,张宝成,蒋 翔,赵东东 (中部战区总医院骨科,湖北 武汉 430070)
神经鞘膜瘤是起源于神经鞘膜施万细胞的良性肿瘤,其特点是神经穿入瘤外包膜,瘤体紧附在神经纤维上,或包绕在神经纤维周围生长[1]。由于神经鞘膜瘤有完整的包膜,手术切除困难不大,但若处理不当,可造成神经损伤或肿瘤复发。传统的治疗方法是在肉眼下手术切除,但易伤及神经纤维,造成医源性神经损伤;或为了减少神经纤维损伤导致瘤体切除不完全,从而增加了术后复发的风险[2-3]。手术显微镜下切除肿瘤可以更加精准地完成手术操作,降低医源性神经损伤的发生率和肿瘤的复发率[4]。但手术显微镜下操作要求高,学习曲线长,且术中手术显微镜的准备需要时间,手术视野小,操作相对繁琐、不便,从而易延长手术时间。此外,临床还可在手术放大镜下进行肿瘤切除,也取得了不错的效果[5]。目前,手术放大镜与手术显微镜下行周围神经鞘膜瘤切除是否具有相同的疗效尚无定论。基于此,本研究比较了上述两种术式的临床效果,以期为临床提供参考。
1 资料与方法
1.1 临床资料
本研究为前瞻性随机对照研究,纳入2015年1月至2020年6月我院因周围神经鞘膜瘤接受手术切除的28例患者,按照随机数字表法分为显微镜组(n=15,手术显微镜下切除周围神经鞘膜瘤)和放大镜组(n=13,手术放大镜下切除周围神经鞘膜瘤),手术均由同一组医生完成。显微镜组男9例,女6例;年龄(33.2±9.4)岁;病程21.0(8.0,36.0)个月;肿瘤体积14.8(7.7,26.0)cm3;肿瘤累及臂丛神经1例,尺神经1例,正中神经2例,桡神经3例,坐骨神经2例,腓总神经3例,胫神经3例。放大镜组男9例,女4例;年龄(34.7±9.4)岁;病程12.0(5.5,43.0)个月;肿瘤体积9.7(6.7,38.9)cm3;肿瘤累及臂丛神经2例,尺神经2例,正中神经1例,坐骨神经3例,腓总神经3例,胫神经2例。2组患者一般临床资料比较差异无统计学意义(P>0.05),具有可比性。
纳入标准:①肿瘤位于四肢;②沿神经干走行可扪及质硬包块,挤压或叩击可出现沿神经走行的放射性疼痛;③MRI显示病灶呈类圆形或椭圆形,边界清楚,T2WI高信号,T1WI呈薄的低信号边缘;④术后病理检查明确为良性神经鞘膜瘤。排除标准:①术前影像学检查怀疑为恶性神经鞘膜瘤;②术前穿刺活检或术后病理检查诊断为恶性神经鞘膜瘤或其他非周围神经鞘膜瘤;③有精神疾病、无自主行为能力;④合并其他严重内科疾病。
本研究已获得我院伦理委员会批准,患者均签署对手术的知情同意书。
1.2 方法
显微镜组患者使用Moeller Allegra 900手术显微镜(×10)辅助手术,放大镜组应用HBTS FD-501K手术放大镜(×5)辅助手术。手术尽量在止血带下进行,切口应足够大,以完全显露肿物远、近端的神经干为宜。在肿物表面用显微器械仔细分离,在无神经或少量神经纤维走行处纵行切开神经外膜,锐性分离,逐步暴露瘤体,注意将正常的神经束自瘤体包膜外仔细剥离并予以保护,确认外膜从瘤体上完全剥离,将瘤体蒂部从神经束上分离后,完整摘除瘤体。双极电凝彻底止血,生理盐水冲洗创面,切开的神经外膜适当修整后以7-0无损伤线间断缝合,放置胶膜引流条,逐层关闭。
1.3 观察指标
记录2组患者手术时间。随访期间观察患者术后是否出现神经症状或原有神经症状加重的情况;采用B超初步评估肿瘤是否复发,并经MRI确认。通过门诊及电话随访,所有患者均获得随访。
1.4 统计学方法

2 结果
2.1 患者手术时间及随访情况
显微镜组手术时间为(53.1±12.4)min,放大镜组为(41.6±15.7)min,二者比较差异具有统计学意义(t=2.159,P=0.040)。
显微镜组患者术后随访(35.9±19.3)个月,放大镜组随访(41.8±14.5)个月,二者比较差异无统计学意义(t=-0.904,P=0.375)。显微镜组患者术后无肿瘤复发,放大镜组术后有1例(7.7%)复发,2组复发率比较差异无统计学意义(χ2=1.197,P=0.464)。术后有8例患者出现神经症状或原有神经症状加重,其中显微镜组有3例(20.0%),放大镜组有5例(38.5%),二者比较差异无统计学意义(χ2=1.163,P=0.410)。患者术后出现的神经症状或原有神经症状加重均在术后3个月内恢复。
2.2 典型病例
患者,男,43岁,发现右腘窝包块2年入院,右腘窝可触及5.3 cm×4.2 cm圆形质韧包块,肿瘤表面光滑,与周围组织界线清楚,轻压或轻叩包块时足底出现麻木和过电感(Tinel征阳性)。MRI显示右腘窝肿块,病灶与周围组织界线清晰,T1WI呈低信号,T2WI呈高信号。特征性表现:①神经出入征,即肿瘤上、下极与神经干相连;②脂肪包绕征,即肿瘤周围可见薄层脂肪信号。诊断为右腘窝坐骨神经鞘膜瘤。在手术放大镜下行神经鞘膜瘤切除,术中充分显露肿块,在无神经纤维走行处纵行切开神经外膜,锐性分离,完整摘除瘤体,术后病理检查证实为良性神经鞘膜瘤(图1)。术后患者右足底出现轻度灼烧感,3个月后症状消失;术后随访4年,肿瘤无复发。
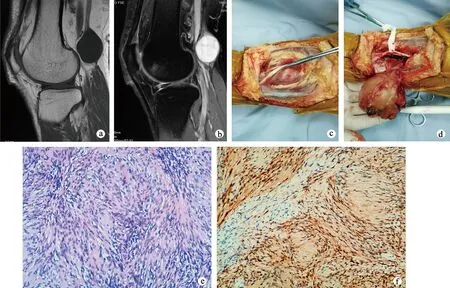
a:MRI矢状位T1WI;b:MRI矢状位T2WI;c:术中完整显露肿瘤;d:完整切除肿瘤;e:术后肿瘤组织HE染色(×100);f:术后肿瘤组织S-100免疫组化染色(×100)图1 典型病例资料
3 讨论
神经鞘膜瘤又名施万细胞瘤,是一种起源于神经鞘膜施万细胞的肿瘤,属于神经外胚层组织肿瘤。其沿神经干附着生长,多为单发,偶有多发,主要为良性。所有年龄均可发病,20~50岁为发病高峰期,发病率无性别倾向[6-7]。
神经鞘膜瘤发病隐匿,生长缓慢,早期多无明显症状,临床中多为偶然发现[8]。肿块较大时可出现疼痛,甚至出现神经压迫症状。局部多可触及肿物,按压时有酸胀和触电感,并向远端放射。该病可为体积较小的肿物,若对其缺乏认识,将肿块连同神经纤维一并切除,或术中粗暴操作,易致永久性神经损伤[9]。影像学检查在诊断周围神经鞘膜瘤中发挥着重要作用,超声检查简便、安全、价廉,可作为临床上的初筛手段,但其敏感性和特异性均不高[10-11]。MRI检查有较高的软组织分辨率,神经鞘膜瘤MRI典型表现为:长轴与神经干走行一致的椭圆形肿块,边界清楚,T1WI呈等或低信号,T2WI呈不均匀高信号;部分呈肿瘤囊性变,表现为瘤内多发T1WI低信号、T2WI高信号囊变区。神经主干的鞘膜瘤常见神经出入征、脂肪包绕征、靶征;而分支神经束的鞘膜瘤常见靶征,受累神经难以显示,脂肪包绕征不常见。少部分神经鞘膜瘤也可能为恶性,其MRI表现为:边界不清晰,T2WI呈混杂信号,T1WI呈低混杂信号,囊变区的T2WI呈高信号,靶征与脂肪分离征少见,而神经束-肿瘤中心性相连征(肿瘤头尾与神经束两极相连,神经束节段性消失)是最常见的征象[12-13]。此外,MRI可以很清楚地显示肿瘤生长的位置、大小及与神经的毗邻关系等,利于更好地制订手术方案。若肿瘤术前影像学检查无法明确其良恶性,可进一步行超声引导下穿刺活检术[14-15]。
神经鞘膜瘤大多为良性肿瘤,但仍有5%出现恶变,确诊后应尽早行手术治疗。充分认识该病的组织来源和生长特点是手术成功的关键[16]。由于神经鞘膜瘤呈膨胀性生长,可推挤周围神经纤维束,肿瘤最膨出的一侧表面神经纤维最稀少,且最浅表,因此手术应于肿瘤包膜最膨出的一面进行,沿神经纤维走行纵向切开至肿瘤表面后开始剥离,可降低神经损伤程度;若未到达肿瘤表面即开始剥离,易损伤残留于肿瘤表面的神经纤维,并造成无神经束进入肿瘤实质的假象而上下切断取出肿瘤。术中应注意减少神经牵拉,精细轻柔地剥离,最大限度地避免伤及神经纤维,减少医源性损伤的发生[17]。包膜外完整切除肿瘤可降低其复发率,但若一味追求低复发率而采用包膜外切除不仅肿瘤切除不彻底,还存在神经损伤的潜在风险;有时要将瘤体完整摘除仍不可避免地会切除、牵拉或侵扰少量神经纤维,术后相应神经支配区域会出现麻木或感觉迟钝,但术后神经功能一般都可以恢复。本研究中共有8例患者术后出现一定的神经症状,但均在3个月内恢复。
神经鞘膜瘤的切除是一个精细的过程,肉眼下手术操作相对粗糙,而手术显微镜具有更好的照明及放大功能,可使手术视野更加清晰,能够准确地显示解剖结构,从而精准地完成手术操作,最大限度避免神经纤维损伤及肿瘤切除不彻底等,具有复发率低、医源性神经损伤小、恢复快等优势。然而,手术显微镜下行神经鞘膜瘤切除手术时间较长、手术视野小,术中需不断调节视野,操作繁琐;同时,手术显微镜下操作要求高、学习曲线长。相比之下,手术放大镜携带方便,不占用手术空间,在手术放大镜辅助下行肿瘤切除更加简便、快捷[18-19],且设备价格低、学习难度小,易于推广。本研究中放大镜组的手术时间明显短于显微镜组,这体现了手术放大镜方便快捷的优势;而2组患者术后神经症状的发生率及肿瘤复发率无统计学差异,提示手术放大镜可在简化手术过程的同时,取得与手术显微镜相同的效果。无论是手术显微镜还是手术放大镜下进行手术,术中最好配合双极电凝。双极电凝是在两个电极之间进行放电,热损伤较轻,范围小,对细小血管的凝闭止血功能较好。因此,术中配合双极电凝止血处理血管,可保证手术视野清晰,方便术者操作,加快手术进度,提高手术效果。
综上所述,手术显微镜与手术放大镜下手术切除周围神经鞘膜瘤都可以取得满意的临床效果,但手术放大镜辅助下手术操作简便、手术时间更短,临床可根据实际情况选择手术方式。
