铁钴镍三元氧化物固相萃取结合气相色谱-质谱法检测环境水样中5种有机磷农药
2023-01-18陈雨莹王泽鹏朱霞萍
陈雨莹, 王泽鹏, 任 维, 王 勇, 朱霞萍*
(1.成都理工大学材料与化学化工学院,四川成都 610059;2.贵州省地质矿产勘查开发局一○五地质大队,贵州贵阳 550018)
固相萃取是有机磷农药常见的前处理方法,应用于有机磷农药固相萃取的常用吸附剂有硅吸附材料[1,2]、碳吸附材料[3 - 5]、分子印迹吸附材料[6,7]、磁性吸附材料[8,9]等。铁、钴、镍的氧化物因其较大的比表面积和优异的结构性能在吸附领域应用广泛。Kang等[10]合成了特定结构的Fe2O3,在最佳实验条件下,对刚果红、甲基橙和亚甲基蓝的最大吸附量分别为723.8、150.7和54.5 mg/g。Saber等[11]采用溶胶-凝胶法制备的NiO纳米颗粒是去除水中Cr(VI)的有效吸附剂。Wu等[12]采用聚乙二醇(PEG)辅助水热法制备了PEG/CoFe2O4纳米复合材料,对有机染料具有吸附选择性,尤其对刚果红有显著的吸附效果。
现有的研究[10 - 12]运用铁、钴、镍的单金属氧化物或双金属氧化物去除水体中的有机物和重金属离子,但将铁、钴、镍的混合氧化物作为固相萃取材料应用于样品前处理鲜有报导。本研究采用共沉淀法制备了铁钴镍三元氧化物(ICNTO),将其应用于分离富集水体中的辛硫磷、敌敌畏、甲基对硫磷、毒死蜱和伏杀硫磷,优化了材料对有机磷农药的固相萃取条件,结合气相色谱-质谱测定了环境水样中5种有机磷农药,为环境水样中有机磷农药的前处理提供了方法选择。
1 实验部分
1.1 仪器、试剂与材料
Crystal 9000气相色谱-质谱联用仪(浙江福立分析仪器有限公司);DF-101S集热式恒温加热磁力搅拌器(巩义市予华仪器有限责任公司);DHG-9030电热鼓风干燥箱(上海一恒科学仪器有限公司);SHB-Ⅲ循环水式多用真空泵(巩义市英峪华科仪器厂);AS150-A SPE筛板和空柱管(美国,安捷伦科技有限公司);YGC-6固相萃取仪(成都雅源科技有限公司);pHS-3C pH计(上海仪电科学仪器有限公司);D8-Advance X射线粉末衍射仪(德国,布鲁克公司);麦克ASAP2460比表面仪(美国,麦克默瑞提克仪器有限公司);Thermo Scientific K-Alpha X射线光电子能谱仪(美国,赛默飞世尔科技有限公司);TA sdt650同步热分析仪(美国,TA仪器公司)。
甲醇、乙酸乙酯、乙酸丁酯、二氯甲烷、正己烷、环己烷、无水乙醇、FeCl3·6H2O、CoCl2·6H2O、NiCl2·6H2O、NaOH(分析纯,成都市科龙化学品有限公司);辛硫磷(Phoxim)、敌敌畏(Dichlorvos)、甲基对硫磷(Methyl parathion)、毒死蜱(Chlorpyrifos)、伏杀硫磷(Phosalone)(纯度>99%,北京百灵威科技有限公司);实验用水为超纯水。
1.2 实验方法
1.2.1 铁钴镍三元氧化物(ICNTO)材料的制备取等物质的量的FeCl3·6H2O、CoCl2·6H2O、NiCl2·6H2O于烧杯中,加入超纯水搅拌至完全溶解。随后,用0.1 mol/L的NaOH溶液调节溶液pH在9.0~10.0。将混合悬浊液在60 ℃下搅拌2 h,在室温下陈化6 h。将沉淀抽滤、洗涤、烘干,研磨过筛,400 ℃马弗炉中焙烧2 h即可得到ICNTO复合材料。
1.2.2 气相色谱-质谱条件色谱条件:DB-5MS石英毛细管柱(30 mm× 0.25 mm× 0.25 μm),进样口温度230 ℃,载气为高纯氦气(>99.999%),载气流量1.0 mL/min;采取不分流进样方式,进样量1.0 μL,溶剂延迟3 min;选择程序升温为:初始温度50 ℃保持2 min,30 ℃/min升温至180 ℃保持5 min,再以30 ℃/min升至300 ℃保持2 min。质谱条件:电子轰击离子源(EI),电子能量70 eV,离子源温度260 ℃,传输线温度280 ℃,通过全扫描模式(SCAN)定性和选择离子模式(SIM)定量。
1.2.3 固相萃取称取2.0 g ICNTO于SPE空柱中。用5 mL无水乙醇活化,5 mL超纯水洗涤2次。控制萃取速率为8 mL/min。以二氯甲烷为洗脱液,洗脱速率为2 mL/min。测定洗脱液中有机磷农药的含量并计算萃取率。
2 结果与讨论
2.1 有机磷农药定性与定量
在选定的气相色谱-质谱实验条件下,确定各目标组分的定性和定量离子,用选择离子扫描模式对100 μg/L的标准溶液进行测定,5种农药能够较好地分离,分离度均大于1.5。具体结果如表1所示。
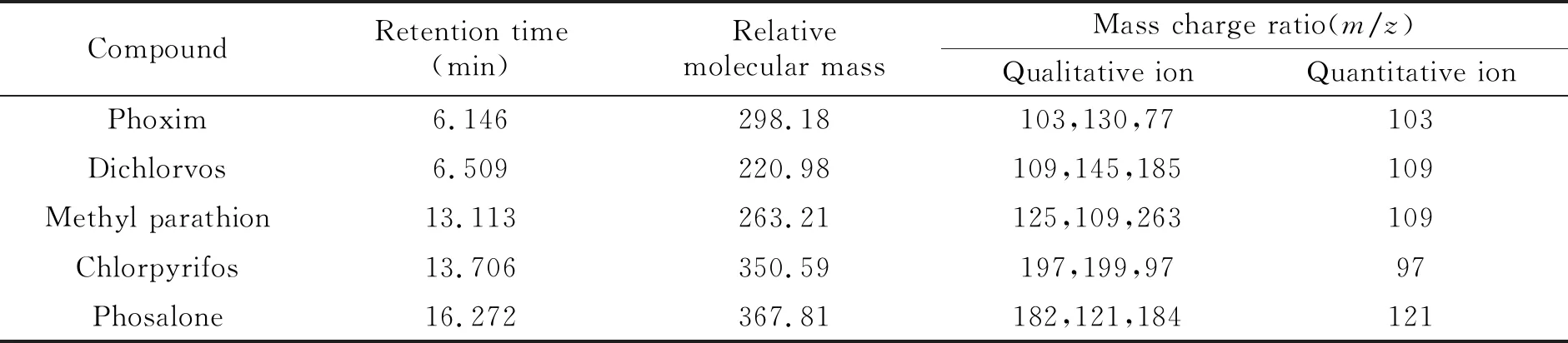
表1 5种有机磷农药的气相色谱-质谱的分离
2.2 复合材料的结构特点
图1A是ICNTO的N2吸附-脱附曲线及孔径分布曲线图。ICNTO属于介孔固体材料。当P/P0<0.74时发生的是单层吸附;当0.74
0.98时,N2吸附量持续上升,但吸附-脱附曲线再一次重合。在低相对压力区(0.05~0.25)取点计算得到ICNTO的比表面积为45.0 m2/g。
ICNTO的X射线衍射(XRD)谱图(见图1B)中出现了Co3O4的(111)、(311)、(511)晶面特征峰,Fe2O3的(206)、(4012)晶面特征峰以及NiO的(200)晶面特征峰,表明了复合材料为Co3O4、Fe2O3与NiO的三元氧化物。
图1C是ICNTO的热重分析(TG-DTG)图谱。ICNTO的热分解过程可分为3个阶段,总失重10.6%。30.0~202.0 ℃为第一阶段,材料失重4.0%,这是由材料表面吸附水脱除所致;202.0~503.0 ℃为第二阶段,此阶段总失重1.7%,此时材料脱除结晶水,材料为Fe2O3、Co3O4、NiO组成的复合物;503.0~830.0 ℃范围内为第三阶段,材料总失重4.9%,当温度超过500 ℃,Fe2O3和NiO形态保持不变,但Co3O4逐渐转化为CoO,并导致在730 ℃左右出现了第三个宽而大的失重峰。因此,材料在500 ℃以下稳定性良好。
图1D是ICNTO的X射线电子能谱(XPS)全谱图。在1350~0 eV范围内出现了材料的O 1s、Fe 2p、Co 2p、Ni 2p的原子轨道峰。在700~740 eV Fe精细谱图出现了Fe3+的2p3/2和2p1/2及Fe2+的2p3/2和2p1/2轨道峰,与文献报道的Fe2O3能谱一致[13,14]。在775~800 eV Co精细谱图出现了Co3+2p3/2和2p1/2的轨道峰及Co2+的2p3/2和2p1/2的轨道峰,与已有Co3O4的能谱研究数据相同[15,16]。850~885 eV Ni精细谱图出现了NiO的2p3/2轨道和2p1/2轨道,与NiO的文献数据吻合[17,18]。元素分析结果显示Fe、Co、Ni 3种元素的含量分别为13.51%、17.36%、16.50%。

图1 复合材料ICNTO的N2吸附/脱附曲线及孔径分布曲线图(A);X射线晶体衍射图(B);热重分析图谱(C)以及X射线光电子能谱图(D)Fig.1 N2 adsorption/desorption curve and pore size distribution curve(A);X-ray crystal diffraction(B);TG-DTG curves(C) and XPS spectrum of ICNTO(D)
2.3 固相萃取条件的优化
2.3.1 萃取材料的用量不同用量的ICNTO对毒死蜱和辛硫磷萃取率的影响如图2A所示。可以看出两种农药的萃取率随ICNTO用量的增加而增大。当萃取材料的用量大于1.5 g时,毒死蜱和辛硫磷的萃取率均达到平稳,最大萃取率分别为72.9%和81.0%。后续ICNTO的用量选择为2 g。
2.3.2 萃取速率萃取率随萃取速率的变化趋势如图2B所示。当萃取速率超过8 mL/min时,萃取效率随着萃取速率增大明显减小。萃取速率过快,目标物与复合材料接触不充分,萃取速率过慢,不仅耗时,而且可能会引入杂质,因此本实验以8 mL/min作为固相萃取速率。
2.3.3 洗脱剂及其用量的选择选用二氯甲烷、乙酸乙酯、环己烷、正己烷、乙酸丁酯作为洗脱剂。由图2C可知,环己烷、正己烷、乙酸丁酯作洗脱剂时萃取效果较差,两种农药萃取率只有50%左右,乙酸乙酯作洗脱剂时,两种农药萃取率分别为67.7%和76.2%,二氯甲烷作洗脱剂萃取效果最好,毒死蜱和辛硫磷的萃取率分别为73.7%和80.7%。因此选择二氯甲烷做洗脱剂。由图2D可知,萃取率随二氯甲烷使用量的增加而增大,当二氯甲烷用量为5 mL时,对两种农药的洗脱效果最好,继续增加洗脱剂用量,萃取率反而减小,因此选择洗脱剂的用量为5 mL。
2.3.4 洗脱速率洗脱速率对萃取率的影响如图2E所示。当洗脱速率为2 mL/min时,毒死蜱和辛硫磷的萃取率最高。当洗脱速率小于2 mL/min时,洗脱速率较慢导致洗脱时间过长,二氯甲烷易挥发带走部分农药;当萃取速率大于2 mL/min时,洗脱速率过快,洗脱不完全。因此,本实验采用洗脱速率为2 mL/min。
2.3.5 复合材料的重复利用实验在最佳实验条件下对毒死蜱和辛硫磷两种农药进行固相萃取。重复进行6次实验的结果如图2F。在前三次实验中两种农药萃取率基本保持不变,到第5次时毒死蜱和辛硫磷的萃取率与第一次相比,分别下降5.3%和6.8%,下降率均在10%以内,因此材料至少可重复利用5次。
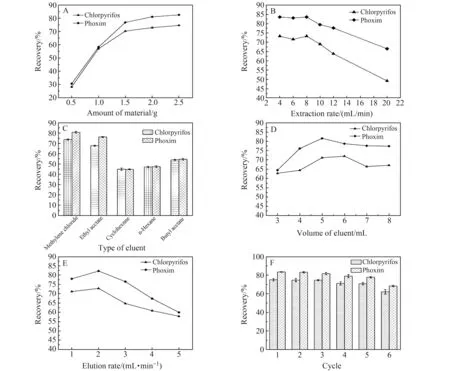
图2 固相萃取条件的优化(n=3)Fig.2 Optimization of solid phase extraction conditions(n=3)(A) amount of material;(B) extraction rate;(C) type of eluent;(D) volume of eluent;(E) elution rate;(F) sorbent reuse times on the extraction efficiencies of chlorpyrifos,phoxim
ICNTO对有机磷农药的吸附是物理吸附和化学吸附两种方式的协同作用,一方面,ICNTO拥有多孔结构和较大的比表面积,能够为有机磷农药的分子提供吸附位点,从而发生物理吸附[19];另一方面,铁、钴、镍金属离子有3d空轨道,而有机磷农药分子中的P、S等原子含有孤对电子,二者在吸附过程能产生配位效应,发生化学吸附。
2.4 GC-MS方法的工作曲线、精密度及检出限
配制0.01、0.05、0.1、0.5、1、5、10、20 μg/L辛硫磷、敌敌畏、甲基对硫磷、毒死蜱和伏杀硫磷的混和标准溶液,取100 mL溶液按“1.2.3”的方法进行固相萃取并按“1.2.2”的GC-MS仪器条件下进行测定。同时在相同实验条件下对11次空白和质量浓度为1 μg/L的农药混合标准溶液进行平行测定,计算出方法的检出限和相对标准偏差,结果如表2所示。5种农药的线性范围在0.01~20 μg/L之间,相关系数(r)均大于0.99,检出限在0.004~0.01 μg/L之间,相对标准偏差为1.6%~5.6%。5种有机磷农药混合标准溶液分离色谱图见图3。
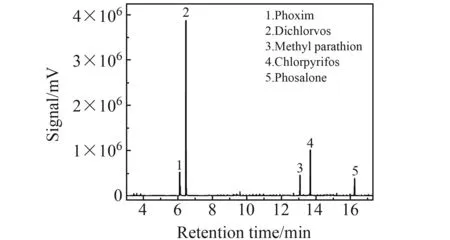
图3 5种有机磷农药的气相色谱-质谱分离图Fig.3 Separation of five organophosphorus pesticides by GC-MS
2.5 实际样品测定结果
分别采集成都市新都区农田灌溉水和青龙湖水作为水样。水样经0.45 μm滤膜过滤直至澄清无悬浮物,按实验方法进行测定,同时做加标回收实验,结果如表3所示。
农田灌溉水中敌敌畏和毒死蜱的残留量分别为0.229 μg/L和1.07 μg/L,辛硫磷、甲基对硫磷和伏杀硫磷未检出;青龙湖水中5种农药均未检出。5种有机磷农药的加标回收率在71.6%~121.7%之间,根据地表水环境质量国家标准[GB 3838-2002]中的限值规定,敌敌畏和甲基对硫磷残留的限值分别为0.05 mg/L、0.02 mg/L,在国标中没有辛硫磷、毒死蜱和伏杀硫磷残留限值的规定,参照国标中对敌敌畏和甲基对硫磷的残留量限值,两个水样中5种有机磷农药的残留含量均低于限值,符合水质管理要求。

表2 5种有机磷农药的线性范围、线性回归方程、相关系数、检出限和相对标准偏差(n=11)

表3 环境水样中有机磷农药测定结果(n=5)
2.6 不同材料固相萃取有机磷农药比较
表4是文献报道的关于硅吸附材料、碳吸附材料、分子印迹吸附材料、磁性吸附材料、C18柱、HLB柱与活性炭柱串联、镁铝铁层状金属氢氧化物等应用有机磷农药测定的方法参数。与现有文献比较,本实验建立的方法线性范围较宽,检出限与其它方法相当或是更低,而且测定了基体更为复杂的农田灌溉水中目标物。萃取材料也具有制备工艺简单、经济环保的优点。
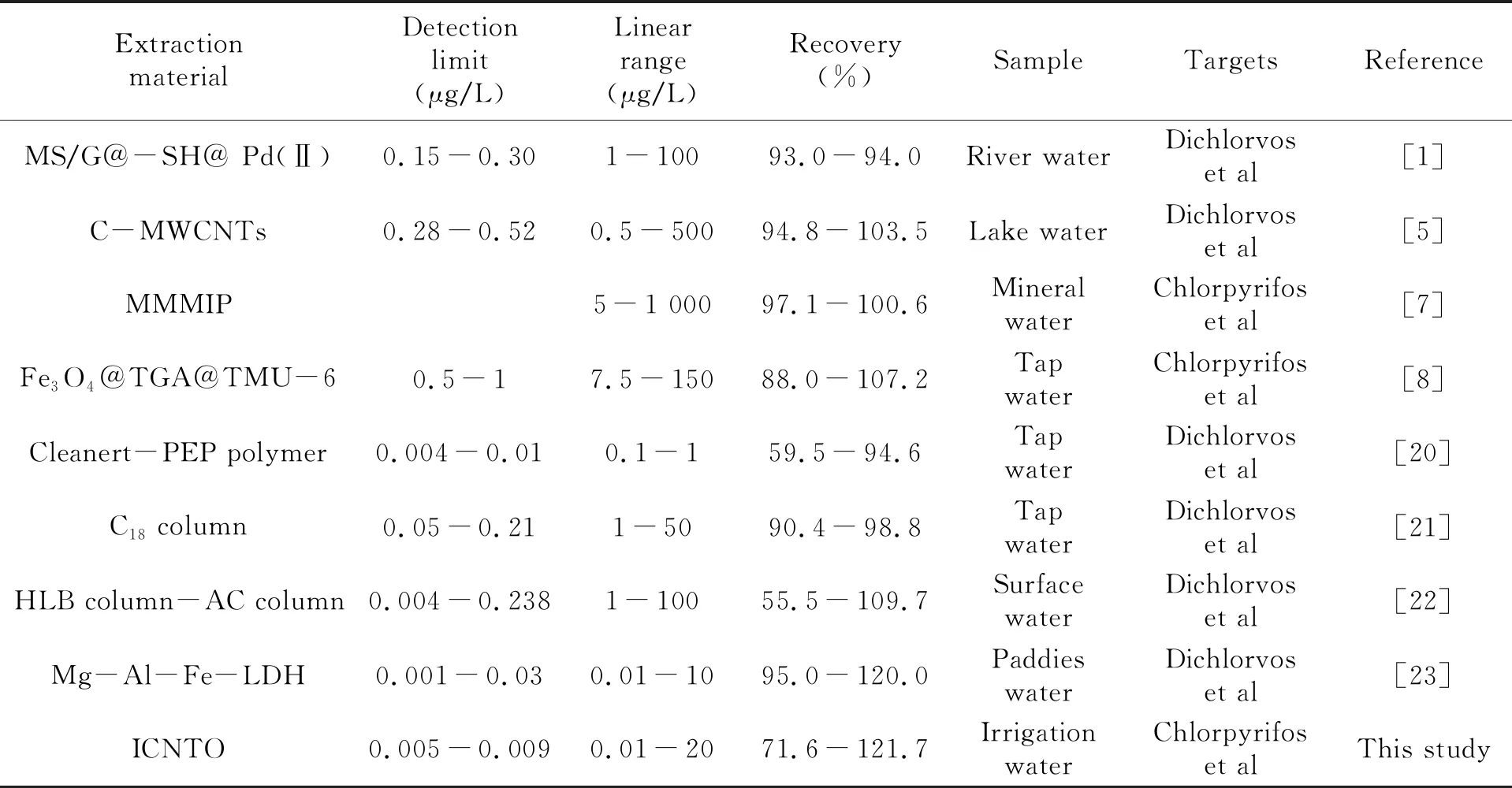
表4 复合材料与其他固相萃取材料对有机磷农药分析性能的比较
3 结论
复合材料ICNTO是由Fe2O3、Co3O4、NiO组成的三元氧化物,是一种介孔固体材料,依靠多孔结构吸附有机磷农药,同时也通过化学配位作用增强对有机磷农药的吸附。优化条件下,材料至少能重复利用5次,且能应用于基体复杂的环境水样中有机磷农药的分离富集。因此ICNTO作为固相萃取材料,为实际环境样品中有机磷农药的测定提供了新选择,有很好的应用前景。
