Mg-2Zn-0.5Ca合金/矿化胶原复合物修复兔下颌骨缺损的实验研究
2023-01-16王树峰陈苗苗王程越
王树峰,陈苗苗,王程越
目前,在临床上广泛应用的医用材料有钛合金、不锈钢及聚乳酸等,这些材料有以下缺点:应力遮挡、机械性能差、生物相容性差、降解性差等。医用镁合金有以下优点:可降解性、弹性模量与人皮质骨接近、较高的机械强度、良好的骨诱导性等,在骨缺损修复材料方面,镁合金有很好的研究价值及应用潜力[1]。本研究用Mg-2Zn-0.5Ca/矿化胶原复合物修复下颌骨缺损,对其在颌骨内的特性进行初步研究。
1 材料与方法
1.1 材料
40只日本大耳兔(徐州医科大学动物实验室),雌雄不限,体重2 kg左右。Mg-2Zn-0.5Ca合金块(北京联合大学):长10 mm、宽7 mm、厚2 mm,羟基磷灰石粉末(北京联合大学,规格20 nm),Ⅰ型胶原蛋白(北京奥精医学,规格100 μL)。电钻、常规手术器械等。本实验中的动物手术过程严格按照徐州医科大学实验动物伦理(批准号202109A024)委员会的规章(2021-017)要求进行。
1.2 方法
1.2.1 Mg-2Zn-0.5Ca合金/矿化胶原制备 羟基磷灰石粉(材料质量占比45%)与Ⅰ型胶原蛋白(0.001 g/mL)加入在0.4 mol/L的盐酸中并搅拌均匀,然后与去离子水按照1.5 g/mL的比例搅拌均匀2 h,加入氯化钠(浓度0.9 mol/L)和氢氧化钾(浓度0.45 mol/L)调节pH值至8,最后离心溶液,将Mg-2Zn-0.5Ca合金放入溶液中,冷冻干燥,高温高压灭菌,密封常温保存。
1.2.2 手术操作 称重后进行全身麻醉,经兔耳缘静脉注射20%乌拉坦(1 000 mg/kg)。在手术区剔除兔下颌区的体毛,碘伏(浓度1%)消毒,无菌条件下局部注射2%利多卡因浸润麻醉,沿下颌骨下缘行25 mm切口,注意保护兔颌下区动静脉。剥离分开下颌骨外侧壁、口底肌肉及骨,定位置用钻滴水降温下切割成10 mm×7 mm×2 mm颌骨缺损,A组植入Mg-2Zn-0.5Ca合金/矿化胶原复合物;B组植入矿化胶原;C组植入Mg-2Zn-0.5Ca合金材料;D组不植入材料。进行常规颗粒饲料喂养,肌注庆大霉素4×104U/只,连续3 d[2]。镁合金植入的位置见手术照片及CT图的箭头所指的位置(图1)。
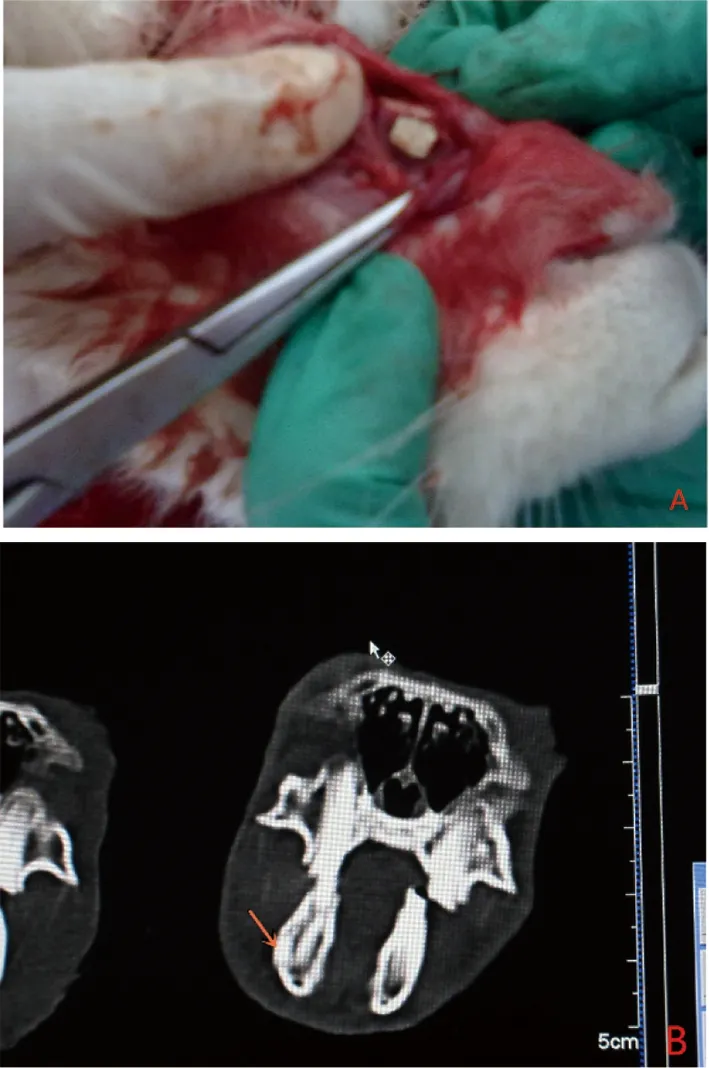
A:植入Mg-2Zn-0.5Ca合金/矿化胶原复合物的手术过程;B:植入Mg-2Zn-0.5Ca合金/矿化胶原复合物术后的CT,箭头所指的方向就是材料植入的位置
1.2.3 大体观察 在术后观察动物的进食状况、活动状况、体重有无改变,创口有无红肿、溢脓出现等。
1.2.4 血清学观察 在术前3 d和术后第1、4、8、12周A、B、C、D组抽取5 mL兔耳动脉血和尿液,检测血液和尿液的镁离子浓度。
1.2.5 放射学检查 在术后12周对植入材料的位置进行X线片拍摄,观察镁合金材料与周围骨组织的状况。
1.2.6 扫描电镜观察 在术后12周取出A组和C组动物体内植入物,用PBS冲洗,2%戊二醛固定,进行乙醇溶液梯度脱水,真空干燥6 h,喷金后进行扫描电镜观察。
1.2.7 组织学观察 在术后12周,取材料周围5 mm范围内的骨组织,进行4%甲醛固定,15%EDTA脱钙处理,每隔4 d换1次脱钙液,共3周。对标本流水冲洗过夜,梯度乙醇脱水,二甲苯透明,石蜡包埋,切片,HE染色,进行光镜观察。
1.3 统计学方法
计量数据用均数±标准差表示,应用SPSS 21进行方差分析。P<0.05表示有统计学意义。
2 结 果
2.1 术后大体观察结果
术后30 min,日本大耳兔精神萎靡。术后前3 d的进食较平时缓慢,术后第4天进食基本达到术前水平。在12周内,无动物死亡,生长良好。伤口均为一期愈合。
2.2 血及尿中镁离子浓度的检测结果
术后第1、4、8、12周A、C组兔血清中镁离子浓度均高于术前3 d,P>0.05,差异没有统计学意义;A组与C组进行比较,F=2.04,P>0.05,差异没有统计学意义;A组与B组进行比较,F=1.96,P>0.05,无显著性差异;A组与D组进行比较,F=2.11,P>0.05,无显著性差异(表1)。术后第1、4、8、12周A组动物尿中的镁离子浓度高于术前3 d,F=2.52,P>0.05,差异没有统计学意义;术后第1、4、8、12周C组动物尿中的镁离子浓度高于术前3 d,F=24.36,P<0.01,差异有统计学意义;A组与C组进行比较,F=40.18,P<0.01,差异有统计学意义;B组术前与术后无显著性差异,F=2.38,P>0.05;D组术前与术后无显著性差异,F=2.42,P>0.05;A组与B组进行比较,F=2.01,P>0.05,无显著性差异;A组与D组进行比较,F=2.42,P>0.05,无显著性差异(表2)。

表1 4组血清中镁离子浓度生化检测结果

表2 4组尿中镁离子浓度生化检测结果
2.3 X线片检查结果
A 组和C组材料周边有不同程度的降解,A组镁合金材料周边与骨组织之间无阴影,结合良好。C组比A材料周围降解更明显,材料与骨组织之间有阴影,成骨速度比材料降解速度慢。B组骨组织愈合良好,无明显阴影;D组有低密度影,骨质较疏松,形成的新生的骨组织相对较少(图2)。

箭头所指的方向是材料与骨组织接触位置
2.4 SEM观察
B组和D组因没有植入镁合金材料,本实验结果只是观察金属材料表面的变化,所以只对植入镁合金材料的动物标本做的电镜扫描。A组近骨组织材料表面变粗糙,有较小的裂隙,降解不明显,有骨组织附着;C组表面可见明显的郓裂和崩解现象,表面没有明显的组织附着(图3)。

A组,箭头所指的方向材料表面变粗糙和骨组织附着;C组,箭头所指方向材料表面有明显的皲裂
2.5 组织学观察
术后12周,A组材料周围可见成骨细胞,有明显骨小梁结构;C组可见有软骨样组织,没有发现明显骨小梁结构;B组可见有明显的成骨细胞和骨小梁结构;D组有空白区,见有少量的骨组织及纤维组织,骨组织疏松(图4)。

A、B组箭头所指方向是明显的骨小梁结构;C组箭头所指的方向是软骨样的组织;D组材料所指的方向疏松的骨组织
3 讨 论
镁是人体新陈代谢的必需物质,是人体储量第4的阳离子,在骨组织中质量约占50%,有调节成骨细胞增殖与分化、参与体内多种组织的新陈代谢等作用[3]。镁的密度及弹性模量接近天然骨(1.8~2.1 g/cm3,20~27 GPa),减少了应力屏障,从而降低植入物不稳定的可能性[4]。研究发现,镁基合金材料在降解的过程中最终以镁离子的形式激发相关的成骨通路[5-6]。镁合金在体内会降解产生一定浓度的Mg2+,能促进钙盐的沉积[5]。镁离子及其周围环境可以增加骨形态发生蛋白,进而局部促进新骨的形成[7]。
锌和钙是人体内的微量和富含元素。锌是活泼元素,合金中锌含量增加,在降解过程中可在合金表面形成保护层,提高了力学性能,降低腐蚀速率[8]。锌在许多酶中有着重要作用,参与多种细胞内代谢活动和功能,还可促进成骨细胞增殖和分化[9-10]。钙可促进骨的生长,钙的增加有助于晶界强化,提高了镁基合金的耐腐蚀性,有利于细胞的活力及增殖[11]。
矿化胶原是一种有机-无机复合材料,其主要成分为纳米羟基磷灰石和胶原[12]。有研究发现,具有多孔结构的矿化胶原在组织结构上与天然骨相似,有助于细胞的生长和形成新生骨[13]。但是机械强度较差,在体内与人体组织相结合的过程中难以维持足够的成骨空间,从而不能形成良好的成骨效果[14]。单纯镁合金具有一定的生物相容性、成骨能力及机械性能,但仍存在降解速度过快等缺点,对不同类型镁基材料复合并进行结构和功能修饰研究有很大的潜力,可以作为修复材料的研究方向[15]。本实验通过组织学的结果显示,Mg-2Zn-0.5Ca合金/矿化胶原组降解的材料边缘有成骨细胞和骨小梁结构,在一定程度上可以说明Mg-2Zn-0.5Ca/矿化胶原复合物在降解的过程中有新骨的形成。但是,Mg-2Zn-0.5Ca合金降解的材料边缘有软骨样组织,无明显骨小梁结构形成。X线片显示,Mg-2Zn-0.5Ca合金/矿化胶原与骨组织结合紧密,没有明显的阴影,而单纯的Mg-2Zn-0.5Ca合金与骨组织之间有明显的阴影。单纯的Mg-2Zn-0.5Ca合金降解速率过快,可能阻碍了成骨细胞和骨小梁结构的形成。从本实验的尿中镁离子浓度结果中发现,单纯的Mg-2Zn-0.5Ca合金组的镁离子浓度明显升高,有显著性差异,高于Mg-2Zn-0.5Ca合金/矿化胶原组,说明单纯的Mg-2Zn-0.5Ca合金的降解速度较快。在以前的实验研究中发现单纯的镁合金降解与新骨生成速率不匹配,镁合金的一侧降解速度较快而没有形成足够的新骨[16]。Brown等[17]利用纯镁颗粒和聚乳酸-羟基乙酸共聚物(PLGA)通过制备成多孔镁/PLGA复合物支架,其可降低PLGA导致的炎症,并且增加了新骨的形成。本实验与以前实验证明,Mg-2Zn-0.5Ca合金/矿化胶原具有良好的生物相容性[18]。单纯的Mg-2Zn-0.5Ca合金降解速率及镁钙锌成分对新的骨组织影响多大,有待需要进一步加深研究。
在镁基合金材料降解的过程中产生的Mg2+如果无法正常代谢,血清中镁离子浓度会增大(超过1.05 mmol/L),会导致肌肉瘫痪和呼吸困难等症状[19]。本实验通过对术前及术后1周到12周的兔血清学检查,结果显示A组的血清镁离子浓度均小于0.90 mmol/L。血清学检查结果表明,Mg-2Zn-0.5Ca合金/矿化胶原复合物作为植入材料,兔体内血清镁离子浓度不会升高。尿中生化检测结果中发现镁离子能够通过肾脏途径正常排泄。实验结果说明镁合金降解产生的大部分Mg2+经过肾脏排出体外,在血液中残留很少,从而不会对机体产生副作用。
Mg-2Zn-0.5Ca/矿化胶原复合物既有镁合金的高强度又有降解可控的性能,同时镁合金降解产物呈碱性,能中和局部酸性变化,是理想的植入材料。镁基合金是一种可降解的金属材料,植入体内不会引起急性及明显的炎症反应,并且能满足所需的机械强度[20]。通过本实验的扫描电镜结果显示,Mg-2Zn-0.5Ca合金/矿化胶原复合物表面变粗糙并有骨组织附着,未见明显的层状崩解现象。有文献表明,材料粗糙的表面促进了材料与细胞的相互作用,助于促进成骨细胞的黏附和生长[21]。而单纯Mg-2Zn-0.5Ca出现明显的郓裂和崩解现象且材料表面相对光滑,没有组织附着。从这也可以看出降解的Mg-2Zn-0.5Ca合金/矿化胶原复合物有利于组织的附着,相反降解的Mg-2Zn-0.5Ca合金抑制了组织的附着。作为植入体内的材料不仅要有良好的机械性能和合适的降解速率,还要有促进新骨形成的能力。由于人体内的骨组织是复杂的,因而最有研究价值的植骨材料几乎都是由两种或两种以上成分整合而成,从而弥补单一材料各自的缺点[22]。从国内外学者的研究中发现镁锌钙合金的优点较多,所以实验所用的材料是Mg-2Zn-0.5Ca合金/矿化胶原复合物。在本实验对Mg-2Zn-0.5Ca合金/矿化胶原复合物进行研究发现,在一定程度上减缓了镁合金的降解速度,促进了骨缺损周围新的骨组织形成。
4 结 论
Mg-2Zn-0.5Ca合金/矿化胶原复合物不会造成血清中镁含量增高,在一定程度上可以降低降解速率,并且具有良好的成骨性能。
