耳迷走神经刺激联合温针灸对卒中患者肢体痉挛及睡眠质量的影响
2023-01-12郭伏玲夏文广张阳普郑婵娟华强刘磊
郭伏玲,夏文广,张阳普,郑婵娟,华强,刘磊
(湖北省中西医结合医院,武汉 430000)
卒中又称中风,是大脑细胞坏死的一种疾病,寒冷季节发病率较高,多发于 40岁以上,男性发病率高于女性,肥胖或糖尿病患者属于好发人群[1-2]。中风后遗症多数为上肢肘关节屈曲或下肢膝关节僵硬,有数据统计患者卒中后因脑部病变使额叶底部受到影响,并发不同程度的睡眠障碍[3-4]。目前用运动疗法和安眠药治疗患者卒中后肢体痉挛及睡眠障碍,但是见效较慢,且服用安眠药有较大的不良反应,疗效尚不令人满意[5]。耳迷走神经刺激可以调整人体神经的平衡,激活体内胆碱能神经元,减少炎症介质释放。温针灸能够通过温热效应作用于患处神经血管,增强局部组织代谢,改善血液循环。有研究表明,耳迷走神经刺激联合作业疗法治疗可有效改善患者肢体运动功能[6]。本文主要观察耳迷走神经刺激联合温针灸治疗对卒中患者的临床疗效,同时观察其对肢体痉挛及睡眠质量的影响。
1 临床资料
1.1 一般资料
将2020年7月至2021年7月在湖北省中西医结合医院治疗的 84例卒中患者随机分为对照组和观察组,每组42例。对照组中男25例,女17例;病程25~51 d,平均(38.01±10.39)d;年龄 41~78岁,平均(60±15)岁;高血压 6例,糖尿病 8例。观察组中男23例,女19例;病程24~50 d,平均(36.99±10.41)d;年龄42~79岁,平均(60±15)岁;高血压7例,糖尿病9例。两组一般资料无统计学差异(P>0.05),具有可比性。
1.2 纳入标准
①符合卒中相关诊断标准[7];②年龄 40~80岁;③之前未产生严重神经功能损伤;④患者处于1~2期痉挛性偏瘫;⑤生命体征平稳;⑥未出现心、肝、肾受损;⑦患者家属均签署知情同意书。
1.3 排除标准
①有失语症、意识障碍者;②有严重出血倾向者;③病情较重者;④有精神障碍者;⑤穴位区域皮肤有破损者;⑥有恶性肿瘤或免疫系统疾病者。
2 治疗方法
两组均予营养神经、活血化瘀、抗血小板聚集、控制基础疾病(如高血压、糖尿病等)的药物治疗,并予物理治疗、作业治疗、推拿治疗等常规康复治疗。
2.1 对照组
予温针灸治疗。上肢取尺泽、曲池、合谷、内关和手三里穴,下肢取风市、太冲、血海、丘墟、环跳和阳陵泉穴。常规消毒后,选用长40 mm毫针针刺上述穴位,得气后,在针柄处插上手制艾炷,点燃,灸3~4壮,治疗过程中谨防烫伤。
2.2 观察组
予耳迷走神经刺激联合温针灸治疗。温针灸治疗同对照组。耳迷走神经刺激治疗取双侧耳甲腔区,局部常规消毒后,采用耳迷走神经刺激仪,将触点的电极导线紧密接触耳甲腔内侧,脉冲频率为4~20 Hz,用疏密波,波宽1 ms,电流从1 mA逐渐增加至产生痛觉,一般为4~6 mA,每次刺激30 min。
两组均每日治疗1次,5次为1个疗程,每个疗程结束后休息2 d,共治疗4个疗程。
3 治疗效果
3.1 观察指标
3.1.1 Fugl-Meyer运动功能(Fugl-Meyer assessment, FMA)[8]评分
采用 FMA评分对两组患者肢体运动功能进行评价。下肢包括17项,共计34分;上肢包括33项,共计66分;分值越高,表示肢体运动功能越好。
3.1.2 日常生活活动能力(activities of daily living, ADL)[9]评分
两组患者日常生活能力采用 ADL评分评价。共11项,分值0~100分;分值越高,说明患者生活活动能力越强。
3.1.3 卒中患者运动功能评估量表(motor assessment scale, MAS)[10]评分
采用MAS评价两组患者肌张力。将MAS分为Ⅳ、Ⅲ、Ⅱ、Ⅰ+、Ⅰ和0级,分别计4分、3分、2分、1.5分、1分和0分;得分越高表示张力越高。
3.1.4 匹茨堡睡眠质量指数(Pittsburgh sleep quality index, PSQI)[11]和睡眠状况自评量表(selfrating scale of sleep, SRSS)[12]评分
采用PSQI和SRSS评分评价两组患者睡眠质量。PSQI评分包括7项,得分为0~21分;分值越高,表示睡眠质量越差。SRSS评分包括10项,得分为0~21分;分值越高,表示睡眠状况越差。
3.1.5 血清炎症因子水平
取患者治疗前后空腹静脉血5 mL,分离血清,采用酶联免疫吸附法检测患者血清白介素-7(interleukin-7, IL-7)、肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)和超敏 C 反应蛋白(hypersensitive C-reactive protein, hs-CRP)的水平。
3.2 疗效标准[13]
显效:肌张力降低 2级,痉挛基本消失,睡眠时间增加>3 h。
有效:肌张力降低 1级,痉挛减轻,睡眠时间增加<3 h。
无效:肌张力和痉挛均未改善,睡眠时间未增加。
总有效率=[(显效+有效)例数/总例数]×100%。
3.3 统计学方法
采用SPSS17.0统计软件进行数据处理。符合正态分布的计量资料以均数±标准差表示,比较采用t检验。计数资料比较采用卡方检验。以P<0.05表示差异具有统计学意义。
3.4 治疗结果
3.4.1 两组治疗前后FMA评分比较
由表1可见,两组治疗前患者下肢和上肢FMA评分比较,差异无统计学意义(P>0.05);两组治疗后下肢和上肢FMA评分均高于同组治疗前(P<0.05),且观察组治疗后下肢和上肢 FMA评分均高于对照组(P<0.05)。
表1 两组治疗前后FMA评分比较 (±s,分)
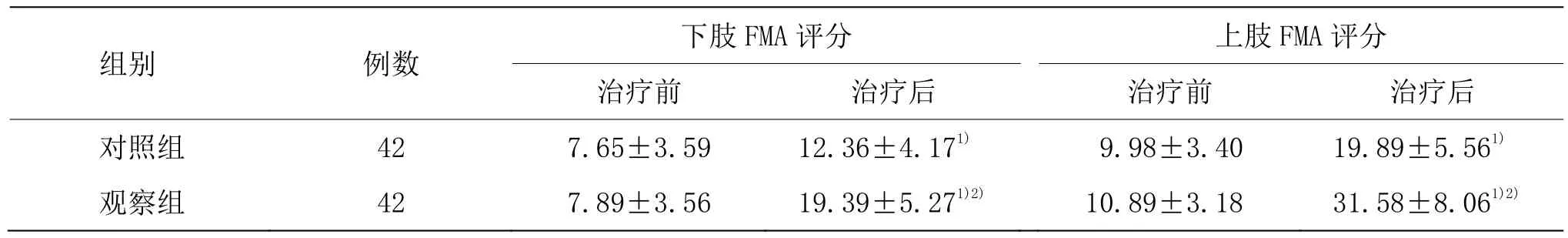
表1 两组治疗前后FMA评分比较 (±s,分)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05。
组别 例数 下肢FMA评分 上肢FMA评分治疗前 治疗后 治疗前 治疗后对照组 42 7.65±3.59 12.36±4.171) 9.98±3.40 19.89±5.561)观察组 42 7.89±3.56 19.39±5.271)2) 10.89±3.18 31.58±8.061)2)
3.4.2 两组治疗前后MAS和ADL评分比较
由表2可见,两组治疗前患者MAS和ADL评分比较,差异无统计学意义(P>0.05);两组治疗后MAS评分均降低(P<0.05),ADL评分均升高(P<0.05);观察组治疗后MAS评分低于对照组(P<0.05),ADL评分高于对照组(P<0.05)。
表2 两组治疗前后MAS和ADL评分比较 (±s,分)

表2 两组治疗前后MAS和ADL评分比较 (±s,分)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05。
组别 例数 MAS评分 ADL评分治疗前 治疗后 治疗前 治疗后对照组 42 2.95±0.63 2.13±0.681) 49.67±4.72 53.67±5.561)观察组 42 2.89±0.60 1.51±0.511)2) 48.01±4.07 64.50±5.961)2)
3.4.3 两组治疗前后PSQI和SRSS评分比较
由表3可见,两组治疗前患者PSQI和SRSS评分比较,差异无统计学意义(P>0.05);两组治疗后PSQI和SRSS评分低于同组治疗前(P<0.05),且观察组治疗后PSQI和SRSS评分均低于对照组(P<0.05)。
表3 两组治疗前后PSQI和SRSS评分比较 (±s,分)

表3 两组治疗前后PSQI和SRSS评分比较 (±s,分)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05。
组别 例数 PSQI评分 SRSS评分治疗前 治疗后 治疗前 治疗后对照组 42 17.21±2.10 12.14±2.361) 39.18±4.25 25.86±3.311)观察组 42 17.32±2.41 7.26±2.431)2) 38.53±5.22 16.28±3.871)2)
3.4.4 两组治疗前后血清炎症因子水平比较
由表4可见,两组治疗前IL-7、TNF-α和 hs-CRP水平比较,差异无统计学意义(P>0.05);两组治疗后IL-7、TNF-α和 hs-CRP水平均低于同组治疗前(P<0.05),且观察组治疗后IL-7、TNF-α和hs-CRP水平均低于对照组(P<0.05)。
表4 两组治疗前后血清炎症因子水平比较 (±s)

表4 两组治疗前后血清炎症因子水平比较 (±s)
注:与同组治疗前比较1)P<0.05;与对照组比较2)P<0.05。
组别 例数 IL-7(pg/mL) TNF-α(pg/mL) hs-CRP(mg/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组 42 67.18±50.22 48.39±38.791) 20.69±3.16 11.38±1.961) 3.97±1.74 2.35±1.351)观察组 42 70.43±52.21 24.98±21.781)2) 21.25±3.03 7.66±1.371)2) 3.89±1.68 1.02±0.981)2)
3.4.5 两组临床疗效比较
由表5可见,观察组总有效率高于对照组,差异具有统计学意义(P<0.05)。

表5 两组临床疗效比较 (例)
4 讨论
卒中主要由脑部血管突然破裂或血管阻塞引起的,有较高的致残率和致死率。临床特点主要为一侧脸部、腿部、手臂突然感到无力,突然发生口眼歪斜、半身不遂,多数卒中患者会有失语或神经功能障碍[14]。卒中是排名第一的国民死亡原因,每年都有超过1 500万人发生卒中,其中500万人死亡,500万人残疾[15]。卒中多发于65岁以上人群,一种是缺血性,另一种是出血性,缺血性占85%,出血性占15%[16]。目前的治疗方法不甚理想,有必要寻找一种安全、有效的治疗手段。本研究旨在观察耳迷走神经刺激联合温针灸治疗对卒中患者肢体痉挛及睡眠质量的影响。FMA评分主要反映患者肢体运动功能,MAS是临床上以功能为向导的评估量表,ADL评分是对患者日常生活活动功能状态进行评估,PSQI及SRSS评分用于评价患者主观睡眠质量及睡眠状况[17-18]。本研究发现采用耳迷走神经刺激联合温针灸治疗可提高患者的下肢和上肢FMA评分以及ADL评分,并降低MAS、PSQI和SRSS评分;说明联合治疗能减轻患者肢体痉挛,提高患者睡眠质量,有助于恢复。可能与耳迷走神经刺激激发脑内多种神经元递质的释放有关。温针灸可促进病变局部的气血运行,以调节气血、平衡阴阳,增强免疫系统和扩张冠状动脉,改善脑血流和微循环。两者联合应用可提高临床疗效。
卒中病情的严重程度及预后与脑组织炎症反应紧密相关[19-20]。IL-7是骨髓基质细胞分泌的糖蛋白,能刺激巨噬细胞和髓样前体细胞产生集落形成血小板。TNF-α主要由巨噬细胞分泌,促进T细胞产生各种炎症因子。hs-CRP是机体受到炎症性刺激合成的急性蛋白。研究[21-22]表明卒中后抑郁病情与炎症因子直接相关。本研究结果发现,耳迷走神经刺激联合温针灸治疗可使患者血清IL-7、TNF-α和hs-CRP水平降低,说明联合治疗能抑制炎症反应,降低患者心理焦虑和抑郁,从而改善患者睡眠质量。炎症减轻能提高患者肢体运动功能,促进肌力恢复。可能与迷走神经刺激可激活胆碱能抗炎通路并有效抑制损伤组织炎症反应有关。温针灸可温通经脉、活血开窍,可缓解肢体痛感,增强关节功能,同时起到宁心安神、平衡阴阳的作用。
综上所述,在常规药物治疗和康复治疗基础上,耳迷走神经刺激联合温针灸可缓解卒中患者四肢痉挛,改善睡眠质量,疗效优于单纯温针灸治疗。但本研究样本量较小,后续还需进一步的研究。
