整体式催化剂分解大气臭氧性能的研究
2023-01-07毛益萍李晶晶王宝珍袁锴彬吴振涛
毛益萍,李晶晶,王宝珍,袁锴彬,吴振涛
(1.浙江工业大学 环境学院,杭州 310014;2.浙江省绍兴市生态环境监测中心,浙江 绍兴 312099;3.长江师范学院 绿色智慧环境学院,重庆 408100)
近年来,由光化学反应引起的区域性大气臭氧(O3)污染已成为我国面临的日益严重的环境问题。室外O3主要由挥发性有机化合物(volatile organic compounds,VOCs)、氮氧化物(nitrogen oxide,NOx)等污染物在光化学反应下产生[1-2],对植物具有毒性,会危害农作物导致其产量显著减少[3-4]。室内O3污染也变得越来越严重,Weschler[5]估计,室外大气中43%~76%的O3会进入室内环境[6-8],也可能有室内O3来源,比如复印机、激光打印机和空气净化设备在操作过程中,由于高压静电和紫外线作用,会产生高浓度O3[9-11]。研究表明,O3浓度达到150 mg/m3以上会引发健康问题,例如,增加呼吸系统疾病的发病率[12],影响心血管系统和肺部功能[13-15]。因此,研究O3去除对人类健康和环境保护具有重要意义。
催化分解法因可在常温下将O3快速转化为O2且不消耗能源而受到越来越多的关注[16]。O3分解催化剂包括贵金属和过渡金属氧化物催化剂[17],其中,贵金属催化剂包括银、铂、钯和钌,对O3分解具有高催化性能,但存在高成本和实用性低的问题[17-18]。在各种催化剂中,锰基氧化物是一种高效、经济的O3分解催化剂。常见的锰基催化剂通常是由非负载型和负载型两大类组成。非负载型锰基氧化物主要通过改变催化剂形貌[19]、晶体结构[20]、表面氧空位[21]和掺杂剂[22-23]来催化分解O3。但非负载型催化剂不能很好地利用活性组分,表现出相对较低的活性,为了提高催化剂的活性,负载型锰基氧化物更为可取。
目前制备的高活性锰氧化物多以颗粒为主,存在成型难和易引起粉尘污染等问题,限制了在实际大气环境中的应用。为了更好地研究二氧化锰(MnO2)的催化效果,本实验通过在不同的载体上负载MnO2得到一系列整体式催化剂,研究了整体式催化剂的载体材料、催化剂负载量对其催化分解O3性能的影响,及其对室内外O3的分解效率。研究结果可为MnO2催化剂分解O3的实际应用提供重要的理论依据。
1 实验部分
1.1 试剂、材料和仪器
催化剂表面的元素及其价态采用X射线光电子能谱仪(K-Alpha型,美国赛默飞世尔公司)测定;催化剂的孔结构比表面积采用全自动比表面积及孔径分析仪(ASAP 2460型,美国Micromeritics公司)测定,形貌特征采用扫描电子显微镜(Sigma 300型,德国Zeiss公司)进行观察和测定;其他仪器包括零气发生器(MODEL 1001,北京雪迪龙公司),动态校准仪(T1700H,北京雪迪龙公司),O3分析仪(T1400H,北京雪迪龙公司),真空干燥箱(DZF6020A,上海坤天实验室仪器公司)等。
1.2 整体式催化剂的制备
利用浸渍法将MnO2催化剂负载在纱布和建筑材料(砖块、瓦片、瓷砖)表面,如图1所示。通过机械搅拌将MnO2催化剂与去离子水的混合液配制成催化剂浸渍液,再将浸渍液均匀涂覆到四种材料表面。当材料表面全部染成棕黑色,将其转移进干燥箱中并在100℃下干燥24 h。制备MnO2负载量分别为0.1 g、0.5 g和1 g的整体式催化剂。

图1 载体负载MnO2制备得到的整体式催化剂Fig.1 Monolithic catalyst prepared by four types of supports loading MnO2
1.3 整体式催化剂的催化活性测试
利用图2所示的装置测试整体式催化剂在实际大气环境中对O3的催化活性。零气发生器中产生的纯净空气通过动态校准仪内置O3发生器,经185 nm的紫外灯照射产生室内O3,其流量通过动态标准仪自带的质量流量控制器来控制调节。动态校准仪气路出口连接12 L密闭反应器的一侧,反应器另一侧连接O3分析仪。实验时将整体式催化剂放入密闭反应器内,剩余O3通过活性炭吸附去除。装置中的气路均由6 mm的聚四氟乙烯管连接而成,记录40 min O3浓度。依次使用了建筑材料(瓦片、瓷砖、砖块)和纱布制备得到的整体式催化剂。
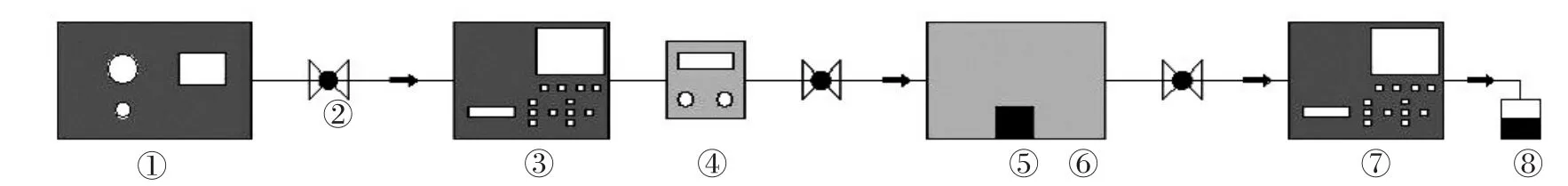
图2 整体式催化剂催化分解O3活性测试装置示意图Fig.2 Schematic diagram of activity test device for catalytic decomposition of O3
气体总流速4000 mL/min,反应温度25℃。通过O3分析仪检测出口的O3浓度。整体式催化剂分解O3的效率采用公式(1)计算。
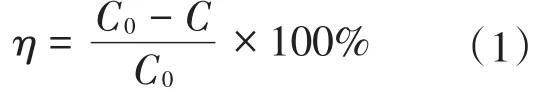
式中:η为O3分解效率;C0为初始O3浓度;C为出口O3浓度。
1.4 整体式催化剂室外O3分解实验
为进一步验证整体式催化剂的实用性,将其与空白组(无催化剂涂层的纱布)在室外天台进行对照实验。实验组和空白组置于天台通风处,为了减少相互干扰,两者相距5 m。实验组和空白组旁边均放置一台O3检测仪,测量12 h室外O3浓度。
2 结果与讨论
2.1 O3稳定性实验
测定整体式催化剂催化分解活性前,先对动态校准仪产生的O3标气进行稳定性实验(以330 μg/m3O3入口浓度为例)。实验结果如图3所示。在200 min内,O3浓度在一定范围内波动。图中央红色实线代表在200 min内O3浓度平均值为330.2 μg/m3。由动态校准仪产生的O3浓度值变化在±0.5%范围内,表明其运行平稳,产生的O3浓度稳定,符合实验要求。
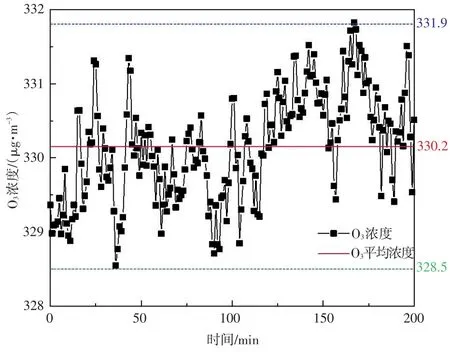
图3 动态校准仪产生的O3标气浓度稳定性Fig.3 Stability of O3standard gas concentration generated by dynamic calibrator
2.2 不同载体对催化分解O3效率的影响
图4(a)分别为建筑材料(瓦片、瓷砖、砖块)和纱布作为载体、MnO2催化剂负载量达到0.5 g时,O3分解效率随时间的变化。由图可知,O3分解效率在开始时均达到100%。随时间增加,分解效率迅速降低,大约10 min后,趋于平稳而缓慢减少。纱布作为载体表现出最佳的O3分解效果(η=74.77%)。纱布表面粗糙,多孔结构,为MnO2催化剂提供了更易于附着的基底。建筑材料中,砖块作为载体表现出最佳的O3分解效果(η=67.56%);而瓷砖(η=46.20%)和瓦片(η=43.77%)作为载体分解O3效果接近,但都比砖块差。这是由于瓷砖和瓦片材料无孔、表面光滑、比表面积小,致使MnO2催化剂附着程度低。由此可知,载体的表面形态决定了其负载MnO2催化分解O3的性能,多孔材料、表面粗糙、比表面积大,更有利于MnO2催化剂的负载,因此,具有较高的催化分解O3的性能。
2.3 MnO2催化剂负载量对催化分解O3效率的影响
图4(b)为纱布负载MnO2整体式催化剂O3分解效率随时间的变化(负载量分别为0.1 g、0.5 g和1 g)。由图可知,整体式催化剂刚使用时均可实现100%的O3分解效率,但随着时间的增加,O3分解效率均有下降。0.1 g负载量的整体式催化剂O3分解效率下降最为明显,经过40 min,O3分解效率从100%下降到49.20%;而1 g负载量的整体式催化剂,仍能保持85.52%的O3分解效率。这主要是由于负载量增加,纱布表面引入的MnO2催化剂也相应增多,从而引入大量的活性位点。MnO2催化剂的活性位点即其表面的氧空位,氧空位浓度逐渐增大,这就为O3的分解提供了充足的活性位点,有利于对O3的吸附和分解[24]。
2.4 O3浓度对整体式催化剂催化分解O3效率的影响
图4(c)为纱布负载MnO2整体式催化剂在不同O3浓度下,O3分解效率随时间的变化。由图可以看出,随着O3浓度的增加,整体式催化剂对O3分解效率逐渐降低。这主要是由于氧空位吸附O3的能力是一定的,即O3会与整体式催化剂上的氧空位发生碰撞,使氧空位达到饱和状态。当O3浓度较低时,整体式催化剂上的活性位点对于O3而言是充足的,O3与活性位点均可发生碰撞。而随着O3浓度的增加,整体式催化剂上的活性位点暂时会被O3全部占据,导致部分O3不能与整体式催化剂上的活性位点碰撞,使得大量O3直接通过没有活性位点的整体式催化剂,以至于影响了整体式催化剂的催化活性。图中还显示O3分解效率随运行时间的延长而降低。在达到稳态后,整体式催化剂的部分活性区域会出现失活,无法分解O3。
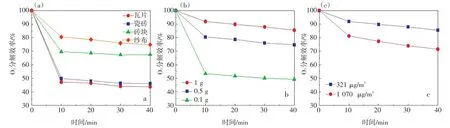
图4 不同条件下整体式催化剂催化分解O3效率Fig.4 Catalytic decomposition efficiency of monolithic catalyst under different conditions
2.5 催化分解室外O3实验
如图5所示,空白组和实验组所测得的O3浓度呈一致趋势。在10:00~16:00时间段,实验组O3浓度远远低于空白组,整体式催化剂表现出较强的催化活性,说明整体式催化剂在室外也对O3具有一定的分解效果。12 h内O3分解效率最高为36.86%,最低为11.03%。
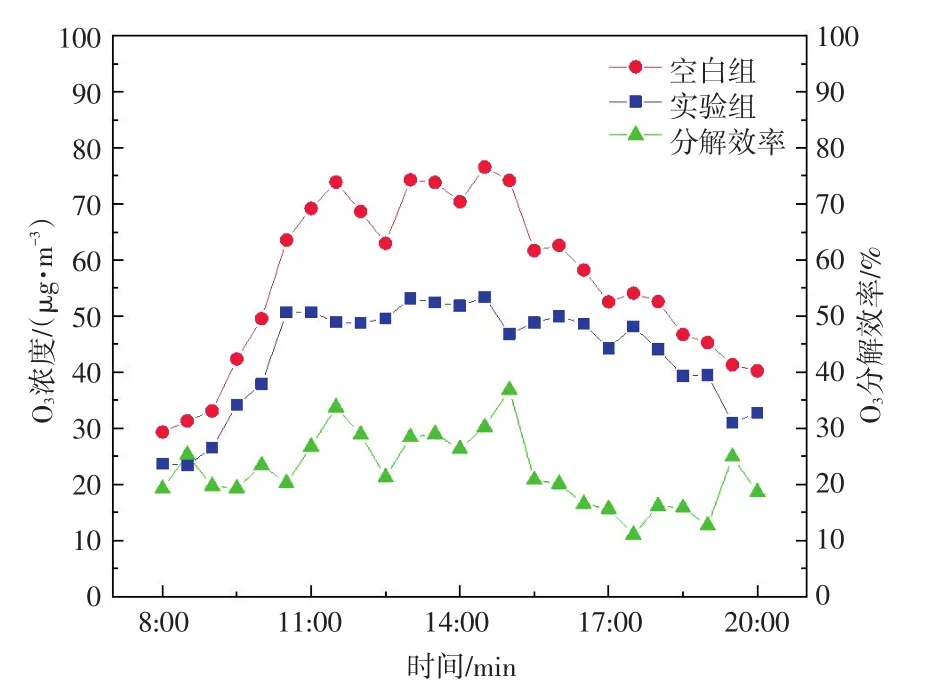
图5 纱布制备的整体式催化剂用于催化分解室外O3的实验结果Fig.5 Experimental results of monolithic catalyst prepared by gauze for outdoor O3decomposition
2.6 分解机理及构效关系
Dhandapani等[17]和 Li等[25]提出的 O3在锰氧化物催化剂上分解的机理现在已被普遍接受。反应步骤包括:O3解离吸附形成O2分子和活性氧物种(O*)[式(2)],O*与O3分子反应形成吸附的过氧化物物种(O2*)[式(3)]和O2分子,以及O2*的分解和O2分子的释放[式(4)]。
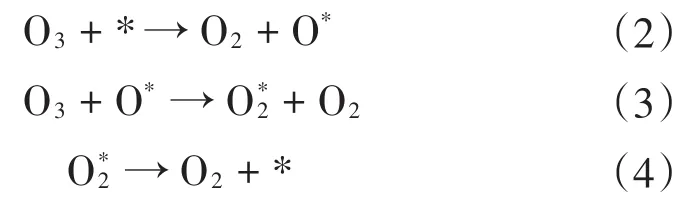
式中:符号*代表表面反应点,O*代表活性氧物种,O2*代表过氧化物物种。MnO2催化剂表面的氧空位强烈影响O3分解行为,预计富含氧空位的锰氧化物对O3分解是有效的。基于氧空位参与和再循环的O3分解机理[26],MnO2催化剂上的氧空位可能是O3分解的反应中心。首先,当氧空位与O3分子接触时,O3分子通过将其中一个O原子插入氧空位而结合到MnO2催化剂表面。氧空位将电子转移到O3分子,从而在氧空位形成活性氧物种(O2-)和O2分子,后者释放到气相中[式(5)]。O2-作为活性位点与另一个O3分子反应,生成过氧化物物种(O22-) 和O2分子[式(6)]。最后,O22-分解成 O2,氧空位被回收,反过来又参与下一个O3分解的循环[式(7)]。如果O22-不能及时分解,氧空位不能被回收,O22-就会转化为晶格氧并释放两个电子,导致催化剂逐渐失活。

为了阐明MnO2催化剂表面O和Mn化学形态与催化活性间的构效关系,对MnO2催化剂进行X射线光电子能谱表征,并对氧的1 s峰和锰的2p3/2谱图进行分峰。图6显示了氧的1 s峰结合能的X射线光电子能谱图。测试谱图能分解为两个独立的峰,提供关于氧物种的信息。结合能为529.80 eV处的峰对应于晶格氧(表示为OI),结合能为531.40 eV处的峰对应于表面吸附氧(表示为OII)。OII/OI摩尔比为0.55。表面吸附氧的含量高,O2*容易脱附,其对应的O3分解速率也就越快[27]。

图6 MnO2催化剂中氧的1 s峰结合能的X射线光电子能谱图Fig.6 X-ray photoelectron spectroscopy of 1 s peak binding energy of oxygen in MnO2catalyst
锰的2p3/2峰结合能的X射线光电子能谱图如图7所示,分别在641.90 eV和643.20 eV处出现峰值,这是MnO2催化剂的特征峰。根据文献[28-29],结合能 (BE) 640.60±0.20 eV、641.70±0.20eV和 643±0.20 eV的锰物种分别被指定为Mn2+、Mn3+和Mn4+物种。因此,MnO2催化剂表面主要存在Mn4+和Mn3+两种价态,Mn3+/Mn4+摩尔比为1.67。表面丰富的Mn3+的含量是影响催化活性的关键因素。MnO2催化剂中只有Mn3+与表面氧空位的数量有关,并且有利于电子转移,这对O3分解至关重要[20,30]。锰氧化物表面的氧空位由于状态不够稳定,常常是化学反应的吸附和活性位点,在O3分解过程中将会发挥显著的促进作用[31]。
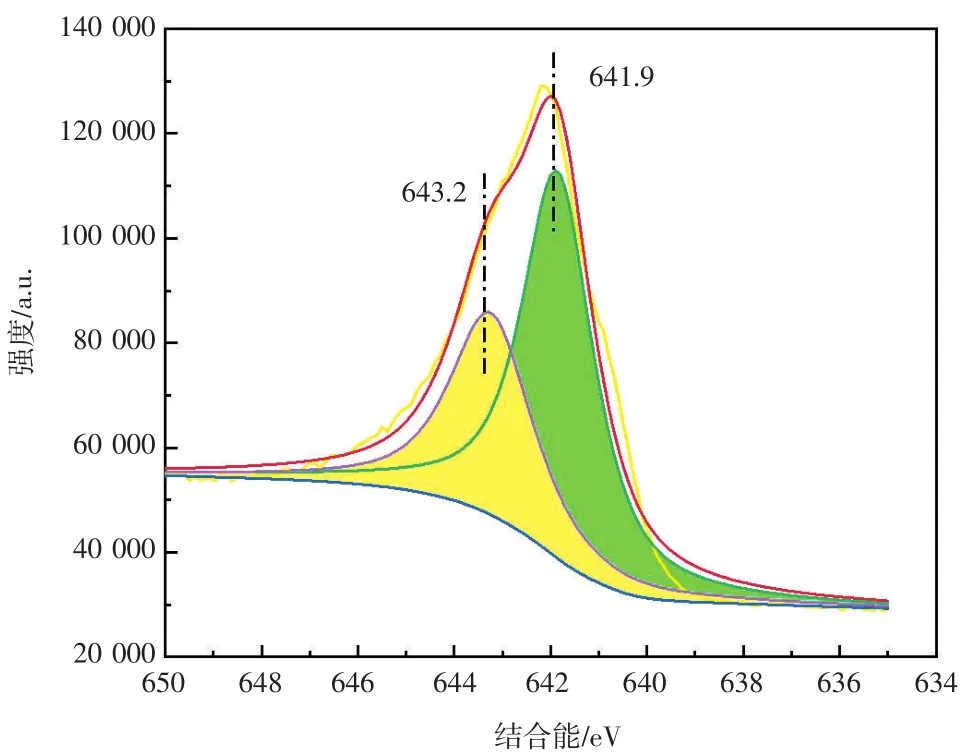
图7 MnO2催化剂中锰的2p3/2峰结合能的X射线光电子能谱图Fig.7 X-ray photoelectron spectroscopy of 2p3/2peak binding energy of manganese in MnO2catalyst
图8显示了MnO2催化剂的N2吸附-脱附等温线及孔径分布图。根据国际纯粹与应用化学联合会(International Union of Pure and Applied Chemistry,IUPAC)分类,MnO2催化剂的吸附脱附等温线属于第IV型曲线,低P/P0时微孔填充,高P/P0时毛细管冷凝。当相对压力达到0.70时,MnO2催化剂出现了H3型滞后环,通常与层状颗粒聚集物吸附有关,形成裂隙状孔隙[32]。
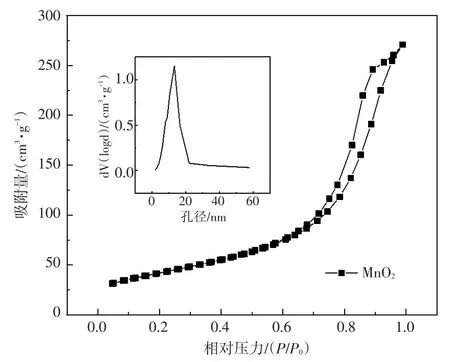
图8 MnO2催化剂的N2吸附-解吸等温线及孔径分布图Fig.8 N2adsorption desorption isotherm and pore size distribution of MnO2catalyst
通过孔结构分析方程计算得出比表面积为151.45 m2/g,孔体积为0.42 cm3/g,孔径为11.06 nm。比表面积是影响MnO2催化剂活性的重要因素之一,当催化剂的比表面积越大,能够暴露出的反应活性位点越多,对提高其去除O3的活性非常有利。
图9显示了MnO2催化剂的扫描电镜图。MnO2催化剂呈不规则球状形貌,颗粒尺寸在几十到几百纳米之间,有团聚现象发生。这种形态可以在材料中形成大量的吸附位点,从而提高O3分解的催化性能。

图9 MnO2催化剂在放大20 000倍和50 000倍下的扫描电镜图Fig.9 SEM of MnO2catalyst at 20 000 and 50 000 magnification
3 结论
(1)在不同条件下MnO2整体式催化剂分解O3催化活性表明:随着催化剂负载量的增加,O3浓度的降低,整体式催化剂分解O3的活性逐渐增强。载体的表面形态(多孔、表面粗糙、比表面积大)决定了其负载MnO2催化剂分解O3的性能,纱布作为载体催化分解O3效果最佳,建筑材料中砖块作为载体,催化分解O3效果次之。
(2)通过研究整体式催化剂分解O3的机理发现:氧空位是吸附和分解O3的活性位点,催化活性会随着MnO2催化剂表面的氧空位的丧失逐渐降低。
(3)通过X射线光电子能谱、扫描电镜和孔结构比表面积表征多种技术,研究了催化剂结构和催化性能的关系:MnO2催化剂表面具有丰富的Mn3+和表面吸附氧,有利于O2*的脱附;较大的比表面积,能够暴露更多的表面活性位,从而促进O3的分解。
