卵泡期高孕激素状态下促排与微刺激方案在卵巢储备功能下降患者中的临床结局比较
2023-01-02杨泽星速存梅王华伟郑宇航和丽梅
杨泽星 ,文 娅 ,速存梅 ,王华伟 ,饶 猛 ,郑宇航 ,和丽梅
(1)昆明医科大学第一附属医院生殖遗传科,云南 昆明 650032;2)云南省生育调节与少数民族优生重点实验室/西部孕前优生重点实验室,云南 昆明 650032;3)温州市疾病预防控制中心,浙江温州 325000;4)昆明医科大学公共卫生学院流行病与卫生统计学系,云南 昆明 650500)
卵巢储备功能下降(diminished ovarian reserver,DOR)是指因年龄、遗传及环境等因素导致卵母细胞数量及质量下降[1]。而DOR 患者在行辅助生育治疗过程中常表现为对促性腺激素低敏,所需剂量大,易出现早发黄体生成素(luteinizing hormone,LH)峰,导致获得的卵子数及胚胎数较少且质量差,不良妊娠结局发生率高[2]。近年来,随着社会的进步,人们生活压力增大、生育观念改变、晚婚,加之我国三胎政策开放等因素影响,DOR人群逐渐增多[3-4],且越来越多的人通过辅助生殖来寻求帮助。据报道,在接受辅助生殖治疗的不孕症女性中,DOR 患者达10%[5]。而在助孕过程中DOR 患者往往需要多次促排卵才能获得妊娠,而促排卵过程不仅会给患者带来巨大的生理和心理压力,也加重了患者的经济负担。因此,选择合理的促排卵方案,减轻DOR 身心痛苦,使患者获得较高的临床妊娠率的同时承担较低的医疗费用具有重要的临床意义,也是临床医生及患者更加关注的问题。微刺激方案较早引进临床,目前已成为DOR 患者较为理想的促排卵方案[6]。近年来,Kuang 等[7]、Wang 等[8]研究结果发现卵泡期高孕激素状态下促排卵(progestin-primed ovarian stimulation,PPOS)方案因为模拟黄体期不排卵的生理现象,几乎没有LH 峰的出现,助孕结局良好。同时,PPOS 方案与微刺激方案由于用药简单,花费较少,并且对卵巢刺激小等优势,目前已成为国内外治疗DOR 的主要方案,但哪种方案效果更佳仍存在争议,且研究报道较少[9]。本文旨在通过比较PPOS 方案与微刺激方案在接受辅助生殖的DOR 患者中的促排卵效果及临床结局,为DOR 患者选择最佳促排卵方案及提高DOR 患者的助孕成功率提供依据。
1 资料与方法
1.1 研究对象
本研究开展于2021 年4 月至2022 年4 月。以昆明医科大学第一附属医院生殖遗传学科行第1 代及第2 代试管婴儿助孕(IVF/ICSI 助孕)的DOR 患者为对象,共纳入294 例周期进行回顾性分析,分为:A 组(PPOS 组,47 个周期)及B 组(微刺激组,247 个周期)。
纳入标准:符合DOR 的诊断患者[10]。满足以下条件:(1)双侧AFC(窦卵泡)总数显著减少(< 6 个);(2)AMH(抗苗勒管激素)显著降低(< 0.5~1.1 ng/mL)。
排除标准:(1)诊断患有影响妊娠结局的疾病,如子宫内膜病变、严重的子宫腺肌症等;(2)合并内分泌、代谢异常患者;(3)因染色体异常等遗传因素需要行第3 代试管婴儿助孕患者;(4)不宜行辅助生殖助孕的患者;(5)不能承受妊娠的患者,如风湿免疫疾病尚未控制、未控制的糖尿病、高血压等。
经正态性检验发现,A 组的年龄、BMI、bLH、bE2、AFC 为正态分布,B 组的一般资料均为偏态分布。经秩和检验,A 组与B 组的一般资料差异均无统计学意义(P> 0.05),表明2 组具有可比性,见表1。
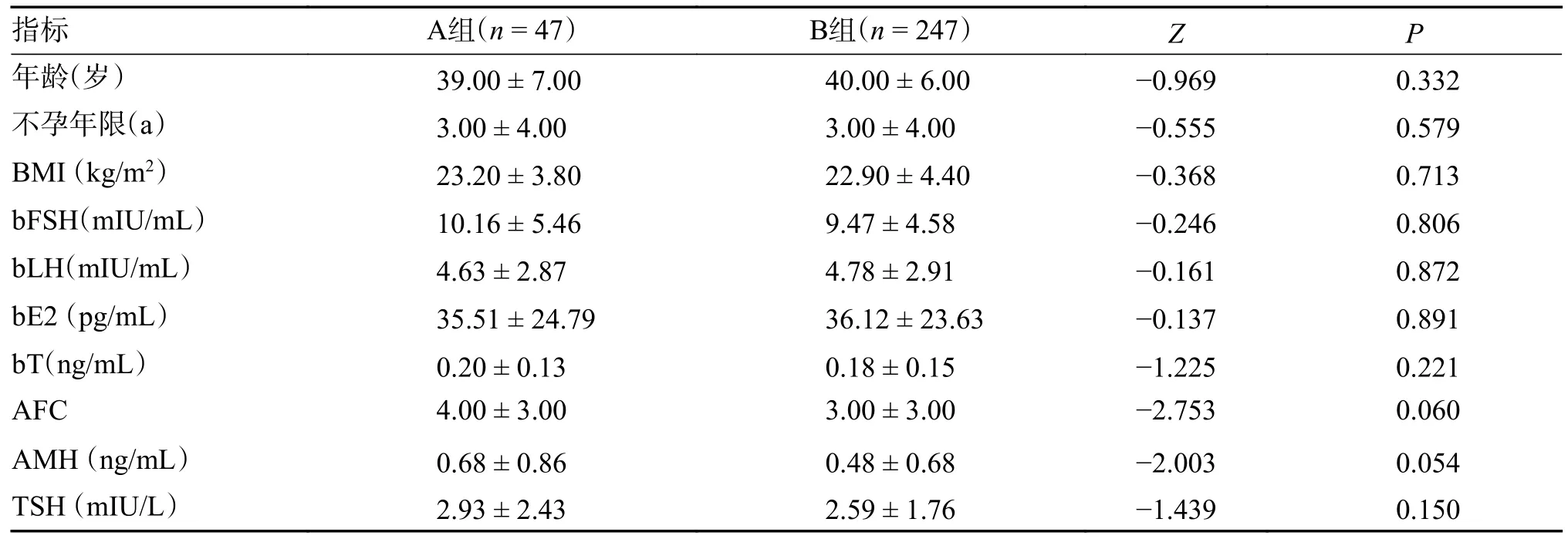
表1 2 组患者临床基线情况比较(M ± Q)Tab.1 Comparison of clinic data between the two groups(M ± Q)
1.2 PPOS 方案
月经周期第2~3 d 检查性激素及B 超窦卵泡情况,确认卵泡处于基始状态,口服安宫黄体酮(浙江仙琚制药,MPA,2 mg/片)8 mg/d,起到模拟黄体期,抑制自发性LH 峰,口服直至板机日。患者使用的促性腺激素(Gn)针为尿促性素针(丽珠制药,HMG,75 U/支),剂量为150~300 U/d,患者一般2~5 d 复诊1 次,Gn 用药剂量根据复诊时B 超下卵泡发育情况,以及激素情况进行调整,当B 超提示达到扳机标准,给予肌肉注射人绒毛膜促性腺激素(HCG)针(5 000 U/支,丽珠制药)5 000~10 000 U 板机,扳机36 h 待卵子完成第2 次减数分裂后,即采用经阴道超声引导下取卵。
1.3 微刺激方案
月经周期第2~3 d 检查性激素及行B 超明确窦卵泡情况,确认卵泡处于基始状态,枸橼酸氯米芬片(高特制药,CC,50 mg/片)100 mg/d,连续服5 d 后改为50 mg/d 直至板机日,患者使用的Gn 剂量根据患者窦卵泡个数、AFC 及体重等情况制定。常选用尿促性素针(丽珠制药,HMG,75 U/支),剂量为150~300 U/d,患者一般2~5 d 复诊1 次,Gn 用药剂量根据复诊时B 超下卵泡生长情况,以及激素情况进行调整,直至板机日,当B 超提示达到扳机标准,给予肌肉注射绒毛膜促性腺激素(HCG)针(丽珠制药,5 000 U/支)5 000~10 000 U 板机,扳机36 h 待卵子完成第2次减数分裂后,即采用经阴道超声引导下取卵。
1.4 胚胎评分
受精后第3 d 胚胎采用Peter 卵裂期胚胎评分系统评估。优质胚胎为Ⅰ级和Ⅱ级卵裂期胚胎。
1.5 观察指标
包括3 个方面:(1)基础资料:主要包括患者一般情况、基础性激素等;(2)临床结局:扳机日性激素情况(LH、E2、P 值)、获卵数、获胚数、优胚数及临床妊娠率;(3)临床妊娠的诊断标准:移植后第28 日行阴道超声提示宫腔可见孕囊,并且有心管搏动。
1.6 统计学处理
采用SPSS 22.0 统计软件进行数据分析。正态分布计量资料用“均数±标准差”()表示,分类资料用例数和百分数[n(%)]表示,偏态分布资料用中位数(M)和四分位数间距(Q)表示。一般资料比较,正态分布用t检验,偏态分布用秩和检验;2 组促排结局的比较用秩和检验。2 组妊娠率的差异分析用χ2检验,P< 0.05 为差异有统计学意义。
2 结果
2.1 2 组方案促排卵结局比较
经正态性检验发现,2 组的促排卵结局指标均为偏态分布。经秩和检验,2 组除HCG 日E2差异无统计学意义(P> 0.05),其余指标差异均有统计学意义(P< 0.05);其中,A 组HCG 日LH、HCG 日P 显著低于B 组(P< 0.05);而A 组获卵数、获胚数、优胚数显著高于B 组(P< 0.05),见表2。

表2 2 组患者临床促排卵过程比较(M ± Q)Tab.2 Comparison of ovulation induction outcomes between the two groups(M ± Q)
2.2 2 组冷冻胚胎移植的临床妊娠率比较
294 周期患者中,共有174 周期患者完成胚胎移植。其中临床妊娠周期为42 个周期,2 组患者总临床妊娠率为24.14%;其中A 组临床妊娠率为25.9%,B 组临床妊娠率为23.8%,2 组临床妊娠率,差异无统计学意义(P> 0.05),见表3。

表3 2 组患者冷冻胚胎移植的临床妊娠率比较[n(%)]Tab.3 Comparison of clinical pregnancy rates between the two groups [n(%)]
3 讨论
卵巢储备下降与高龄(> 35 a)有关,并且还没有药物可以抵抗与年龄相关的生育力衰退。目前,妇女推迟生育的比例大大增加,原因可能与教育和妇女就业增加、职业目标、有效的避孕策略、支持生育的社会激励措施的缺乏有关。年龄增加,导致纺锤体组装检查点(spindle-assembly checkpoint,SAC)的严格性降低,端粒缩短,以及线粒体代谢活性受损,患者将面临卵巢储备的逐渐耗尽,活产能力下降[11]。在当今社会,随着首次生育愿望年龄的增加,这部分患者行辅助生育助孕需要更高的费用,但是妊娠结局差。因此对于高龄合并DOR 患者,选择可以降低患者花费,并且具有较高的获卵数、增加移植机会的促排卵方案,对于患者而言也是一种福音。PPOS 方案可以增加患者获卵机会,并且每周期的持续妊娠率达到20.7%[12]。研究发现PPOS 方案与拮抗剂方案相比,临床结局具有可比性,但PPOS 没有使用价格高昂的拮抗剂,并且促排卵使用的HMG 费用低廉,因此更为经济简便[13]。也有研究分析指出PPOS 在DOR 患者人群使用,同样的避免降调节导致的卵巢抑制,Gn 时间短进而花费少,并且采用的Gn 药物费用低廉,因此疗效好、总花费低,而微刺激方案枸橼酸氯米芬费模拟雌激素负反馈抑制LH,对垂体并没有直接抑制,同样的是较好的选择[14]。本研究在既往研究基础上,进一步分析比较PPOS 方案与微刺激方案的临床效果。
3.1 PPOS 方案的临床结局优于微刺激方案
本研究发现,PPOS 方案的HCG 日LH、HCG 日P 显著低于微刺激方案;而获卵数、获胚数、优胚数显著高于微刺激方案。与既往研究结果一致[10,15-16]。主要原因为,PPOS 方案较微刺激方案存在以下优势:首先,PPOS 中的黄体酮的使用模拟黄体期高雌激素但是却不能诱发LH 峰的特点,模拟该现象避免早发LH 峰的发生,增加获卵数和胚胎数[17]。而微刺激方案促排过程中,卵泡生长后雌激素水平随之升高,造成总的雌激素水平上升,当超过阈值仍然可以引起下丘脑的正反馈,进而使LH 升高,导致部分卵泡提前排卵或卵泡黄素化。其次,由于DOR 患者卵巢储备功能下降,其基础窦卵泡数目大幅下降,加之对促性腺激素不敏感,因此需要更大剂量的促性腺激素才能获得所需卵子数。高促性腺激素意味着高费用,这将增加患者的经济负担和生活压力。PPOS 方案与微刺激方案均有药物费用低廉,总花费低的优点,但曾倩凌等[10]研究表明PPOS 方案的促性腺激素(Gn)用量、Gn 天数及总费用均高于微刺激方案。不过PPOS 方案获卵数及可用胚胎数又高于微刺激方案,所以若平均到单枚胚胎及单枚卵子时,PPOS 方案的费用低于微刺激方案。所以对于DOR 患者,PPOS 方案为更佳的选择。
3.2 2 组冷冻胚胎移植的临床妊娠率无差别
本研究发现,PPOS 方案与微刺激方案的冷冻胚胎移植的临床妊娠率无差别,与刘洋[9]等研究相似,其对153 例高龄 DOR 患者进行分析指出,微刺激方案组的临床妊娠率为23.33%,PPOS 方案组临床妊娠率为25%,且2 组患者临床妊娠率比较,差异无统计学意义(P> 0.05);本研究微刺激方案和PPOS 方案的临床妊娠率分别为23.8%、25%,同样得出无差异的结论。与曾倩凌[10]研究结果的临床妊娠率存在一定的差异,不过同样得出2 组临床妊娠率无差异的结论。其得出的微刺激方案和PPOS 方案的临床妊娠率分别为15%、24.68%,有可能与研究的样本量不同有关,本研究的PPOS 方案组的周期数(47 个周期)显著少于其研究的103 个周期,而微刺激方案组(247 个周期)显著高于其123 个周期,且本研究中2 组方案尚未完成所有患者的胚胎解冻移植。通过本研究及以上学者研究,PPOS 方案组临床妊娠率略微高于微刺激方案组,但是差异无统计学意义(P>0.05),究其原因,考虑胚胎质量是影响冷冻胚胎移植结局的主要因素,子宫内膜厚度、血清维生素D、同型半胱氨酸水平等是影响冷冻胚胎移植后妊娠结局的相关因素[18]。
综上所述,对于DOR 这一特殊人群,选择何种有效的促排卵方案是目前生殖医学领域有争议的热点问题之一。微刺激方案虽然刺激较小、方便经济,但不能有效抑制L H 峰的出现,而PPOS 方案不仅较拮抗剂方案经济廉价,并且可以通过口服孕激素有效抑制LH 的合成和分泌[7],同时孕激素又能促进卵母细胞成熟、胚胎发育等[19]。因此,虽然微刺激方案在促性腺激素用量方面占优势,但不能有效抑制早发 LH 峰的发生。而 PPOS 方案不仅早发 LH 峰率低,且能获得较好的临床结局,比起微刺激方案更值得推荐。但本研究样本量较小,且为回顾性单中心研究,结果有待进一步大样本、多中心、前瞻性的深入研究。
