超高效液相色谱法测定奥沙利铂-PLGA缓释薄膜的含量
2022-12-19冯数橙蔡啟梅王涛申辽高春生
冯数橙, 蔡啟梅, 王涛, 申辽, 高春生
(军事科学院军事医学研究院毒物药物研究所, 北京 100850)
奥沙利铂(化学名为(1R-反式)-(1,2-环己二胺-N,N′)[草酸(2-)-O,O′]合铂,Oxaliplatin)是第三代铂类抗肿瘤药物[1]。奥沙利铂属细胞增殖周期非特异性抑制剂,能够在体内水解产生铂阳离子,铂阳离子与DNA分子交联形成复合物,从而抑制转录及翻译的过程,促进肿瘤细胞的凋亡进而抑制肿瘤增殖[2-4]。相对于顺铂而言,奥沙利铂具有二氨基环己烷(DACH)基团,此基团空间位阻较大,使得奥沙利铂在具有更强抗癌活性的同时和顺铂没有交叉耐药性,并且对机体的毒副作用更低、安全性更高[5-7]。作为一类广谱抗肿瘤药,奥沙利铂对结(直)肠癌、非小细胞癌、卵巢癌、肝癌等均有较显著作用,是临床上用于肿瘤治疗或肿瘤切除术后全身化疗的一线药物[8-10]。目前国内外已上市多款奥沙利铂产品,包括Eloxatin、ELPLAT、佳乐同泰、奥正南、艾克博康等,其主要剂型为注射液。聚乳酸-羟基乙酸共聚物[poly(lactic-co-glycolic acid),PLGA]是由乳酸(Lacticacid,LA)以及羟基乙酸(glycolicacid,GA)两种单体按照一定的比例聚合而成的共聚物,由于其在体内能够被水解,且最终产物为水和二氧化碳,因此PLGA具有良好生物相容性和生物可降解性,是目前应用较为广泛的药用辅料之一[11-13]。由于PLGA具有良好的药物控释性能,被广泛应用于缓释制剂[14-15]。目前以PLGA作为药物载体上市的剂型主要包括微球、微粒以及原位凝胶[16]。同时PLGA在脂质体、纳米粒等剂型上仍有广阔的发展前景[17-19]。
高效液相色谱法(high performance liquid chromatography,HPLC)为经典药物含量分析方法,但在新药研发过程中涉及样本量极大,使用HPLC进行分析时普遍存在分析耗时长、通量低以及资源浪费的问题[20-21]。目前,奥沙利铂制剂中的药物含量测定方法仍以HPLC分析为主。Sun等[22]利用HPLC技术测定聚合物中奥沙利铂的含量,主药出峰时间在6 min左右分析总时长在15 min左右。Cevenini等[23]利用HPLC技术建立了梯度洗脱法测定了奥沙利铂含量,主药出峰时间在6 min左右,分析总时长在16 min左右。因此,开发一种简单、高效、准确的奥沙利铂含量测定方法,能够显著减少新药研发中奥沙利铂的含量分析时间,提高研究、分析效率。
超高效液相色谱(ultra performance liquid chromatography,UPLC)技术是在传统的高效液相色谱基础上,采用了粒径更小的颗粒作为填料,使得柱效有了显著的提升,能够有效降低药物检测时间,减少耗材成本[24-25]。唐莉华等[26]利用HPLC技术测定橙皮苷的含量,其出峰时间在10 min左右。而张丹等[27]利用UPLC技术测定橙皮苷的含量,出峰时间仅需5 min左右,检测时长缩短一倍。刘荷英等[28]利用HPLC技术测定了奥美拉唑钠及其有关物质的含量,其中奥美拉唑钠的出峰时间在30 min左右。而Abdel-Gawad等[29]建立了奥美拉唑钠的UPLC检测方法,其出峰时间在15 min左右。相对于HPLC方法,使用UPLC分析能大大缩短药物检测时间,提高药物检测的效率。作为一种高效的分析手段,UPLC技术目前已广泛应用于药学、农学、生物学等学科的分析[30-32]。然而关于奥沙利铂的UPLC分析方法,各国标准以及文献中报道较少,且HPLC方法无法简单转换以适配UPLC设备,相关研究数据基础仍待补充。
现以自制奥沙利铂-PLGA缓释薄膜为研究对象,旨在建立以UPLC法为基础的奥沙利铂制剂含量测定方法并进行方法学验证,减少药物分析的时间、耗材成本,提升药物研发过程中的检测通量,提高研究效率。
1 仪器与试剂
1.1 仪器
1.2 试剂
自制奥沙利铂-PLGA缓释薄膜;奥沙利铂对照品(上海源叶生物技术有限公司);乙酸乙酯(分析纯,国药集团化学试剂有限公司);甲醇(色谱纯,Fisher);磷酸(分析纯,国药集团化学试剂有限公司);1-庚烷磺酸钠(分析纯,安耐吉化学);娃哈哈纯净水。
2 方法与结果
2.1 色谱条件
色谱柱:Shim-pad GIST-HP-C18 色谱柱(50 mm×2.1 mm,3 μm)、流动相:乙腈∶磷酸水溶液=1∶99,其中磷酸水溶液是在1 000 mL中加入0.6 mL 10%的磷酸溶液,每升流动相加入5 mmol的1-庚烷磺酸钠,并使用磷酸调节pH至3.0;柱温40 ℃,流速0.5 mL/min;进样体积:10 μL,检测波长:254 nm。
2.2 溶液的制备
2.2.1 对照品溶液的配制
精密称定奥沙利铂对照品适量,使用流动相溶解,配制成质量浓度为1 mg/mL的对照品储备液。精密吸取上述对照品储备液1 mL于100 mL容量瓶中,加流动相稀释至刻线,翻转振荡均匀,过滤,得到质量浓度为10 μg/mL的对照品溶液。
2.2.2 供试品溶液的配制
将自制的奥沙利铂-PLGA缓释薄膜溶于1 mL乙酸乙酯中,用流动相定容至100 mL,翻转振荡均匀,14 000 r/min离心过滤后取上清液,得到奥沙利铂供试品溶液。
SSD(Single Shot Multi-Box Detector)[7]算法属于基于回归类的目标检测算法,区别于区域候选类的目标检测算法。SSD算法采用回归思想,利用不同卷积的特征图进行综合,直接预测边界框的类别和位置;该目标检测算法准确率较高,检测速度较快,可满足实时的障碍物检测需求,但在障碍物目标较小时,检测效果较差。
2.2.3 空白辅料溶液的配制
按照奥沙利铂-PLGA缓释薄膜的处方工艺组成,取处方比例的中链甘油三酯(MCT)、甘油、PLGA粉末,制备不含奥沙利铂的缓释薄膜的空白样品,按“2.2.2”节方法制备空白对照溶液。
2.2.4 草酸溶液的配制
精密称定草酸(奥沙利铂已知杂质)对照品适量,使用流动相溶解,配制成质量浓度为100 μg/mL的草酸溶液。使用流动相稀释10倍,翻转振荡均匀,过滤,得到质量浓度为10 μg/mL的草酸溶液。
2.2.5 乙酸乙酯溶液的配制
精密吸取100 μL乙酸乙酯溶液,使用流动相配制,使乙酸乙酯的体积分数为1%,翻转振荡混匀,过滤,得到体积分数为1%的乙酸乙酯溶液。
2.2.6 混合溶液的配制
分别精密称量草酸和奥沙利铂适量,精密吸取乙酸乙酯适量,使用流动相溶解,配制成草酸和奥沙利铂的质量浓度均为10 μg/mL的混合溶液,其中乙酸乙酯的体积分数为1%,翻转振荡均匀,过滤,得到混合溶液。
2.3 系统适用性
将“2.2.2”节供试品溶液,按“2.1”节色谱条件进样分析。结果表明,理论塔板数按奥沙利铂计算为773,拖尾因子为1.267。
2.4 专属性
将“2.2”节溶液,按“2.1”节色谱条件进样分析。结果如图1所示,PLGA不出峰,并且奥沙利铂色谱峰能和乙酸乙酯、草酸色谱峰完全分离,说明溶剂以及辅料对奥沙利铂测定无干扰,并且奥沙利铂在该色谱条件下能与杂质草酸分离开,本方法专属性强。

图1 超高效液相色谱图结果Fig.1 Graphs of UPLC results
2.5 线性关系
精密吸取“2.2.1”节对照品储备液,依次配制质量浓度为1.25、2.5、5、10、50、100 μg/mL的系列对照品溶液,按“2.1”节色谱条件注入液相色谱仪,重复测定3次,记录奥沙利铂色谱峰的峰面积并计算其平均值。以对照品质量浓度对峰面积进行线性回归,结果见图2。结果表明,奥沙利铂质量浓度在1.25~100 μg/mL的范围内线性关系良好。以峰面积(A)为纵坐标,进样浓度(C)为横坐标进行线性回归,A=6 158.7C+2 199.4,R2=0.999 8。
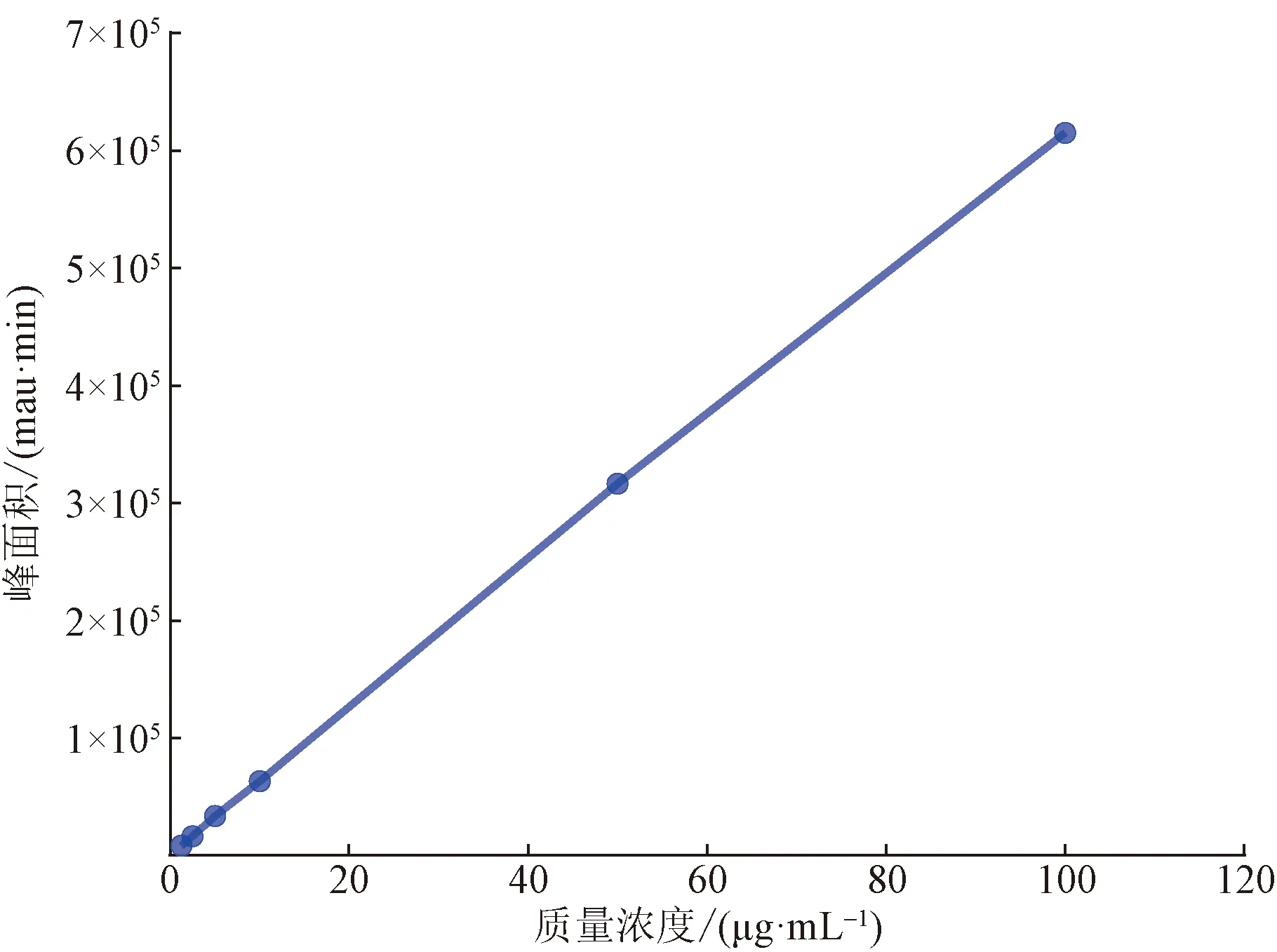
图2 奥沙利铂标准曲线Fig.2 The standard linearity of Oxaliplatin
2.6 重复性试验
取奥沙利铂-PLGA缓释薄膜,按“2.2.2”节方法平行制备供试品溶液6份,按“2.1”节色谱条件进样,记录奥沙利铂的峰面积,使用外标法计算奥沙利铂质量浓度及相对标准偏差(relative standard deviation,RSD)(表1)。结果表明,奥沙利铂的平均含量为1.00 μg/mL,RSD 为0.87%,表明本方法重复性良好,满足测试。

表1 重复性试验结果Table 1 Results of repeatability test
2.7 中间精密度试验
取同一批奥沙利铂-PLGA缓释薄膜,由2名分析人员在不同的日期,按“2.2.2”节方法各平行制备供试品溶液6 份,按“2.1”节色谱条件,分别在安捷伦高效液相色谱仪(型号1200)和岛津高效液相色谱仪(LC20AD)上进样,记录奥沙利铂峰面积,并以外标法计算其质量浓度及其RSD值(表2)。结果显示,奥沙利铂的平均质量浓度为98.96%,RSD 为0.70%,表明本方法中间精密度良好。

表2 中间精密度试验结果Table 2 Results of intermediate precision test
2.8 稳定性试验
取同一批奥沙利铂-PLGA缓释薄膜,按“2.2.2”节下方法制备供试品溶液,室温下存放,分别于0、2、4、6、8、10 h取样,按“2.1”节下色谱条件进样,测定奥沙利铂的峰面积,计算其RSD值(表3)。结果显示,奥沙利铂峰面积的RSD为1.18%,表明供试品溶液中奥沙利铂在室温下10 h内稳定。
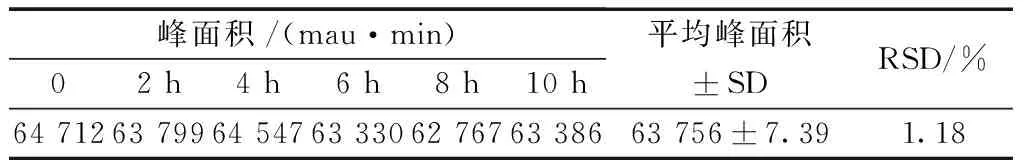
表3 稳定性试验结果Table 3 Results of stability test
2.8.1 回收率试验
按照奥沙利铂-PLGA缓释薄膜处方组成,按配比称取不含奥沙利铂的辅料,以标示量的80%、100% 和120% 水平添加奥沙利铂对照品,每个水平平行添加3 份,按“2.2.2”节下方法制备试验溶液并使用液相色谱仪测定,记录奥沙利铂的峰面积,以外标法计算其质量浓度及回收率,结果见表4。结果显示,奥沙利铂的平均回收率分别为99.93%,RSD为1.29%。

表4 回收率试验结果(n=9)Table 4 Results of recovery test(n=9)
2.8.2 定量下限和检测下限
精密称量奥沙利铂对照品适量,使用流动相逐级稀释,按“2.1”节色谱条件进样测定,以信噪比S/N=3计 确定检测下限为22.5 ng/mL,以信噪比S/N=10计,确定定量下限为112.5 ng/mL。结果表明方法灵敏,满足试验需求。
2.8.3 样品含量测定
选取三批自制奥沙利铂-PLGA缓释薄膜(奥沙利铂标示量1 mg),每批薄膜取3片,每片溶于1 mL乙酸乙酯并以流动相定容至100 mL,振荡均匀,14 000 r/min离心过滤取上清液,按“2.1”节色谱条件进样分析,并以外标法进行定量。测定结果见表5。

3 结论
超高效液相色谱法相比于高效液相色谱法,其所用的色谱柱使用了更小的硅胶颗粒,比表面积更大,分离能力得到增强,分析时间明显缩短,有着更高的分析通量。由于色谱柱填充粒子间隙更为致密,UPLC方法对于仪器设备的压力上限及精密度要求也更高。近年来随着中国研究水平的不断提升,设备条件的不断优化,UPLC分析方法逐渐为科研工作者所熟知并应用,但目前以UPLC为基础的药物分析方法仍然较少,亟待优化补充。本文建立了以PLGA为基质的缓释载药薄膜中奥沙利铂的UPLC含量测定方法。在样品前处理过程中,选择了乙酸乙酯作为溶解剂,其优势是能够快速溶解PLGA并释放奥沙利铂,并且乙酸乙酯的色谱峰与奥沙利铂色谱峰分离良好,不产生干扰。同时,本方法也能够有效分离奥沙利铂以及其主要杂质草酸,为制剂稳定性等相关研究提供依据。以《中国药典》(2020年版)中规定HPLC方法进行分析,单个样品色谱分析时间约为35 min,而本文所述UPLC方法单个样品色谱分析时间仅为5 min,分析时长缩短7倍。综上所述,本文所述UPLC方法简便、灵敏、准确、精密、重复性好,显著提升了分析效率,节约了溶剂和分析时间,符合奥沙利铂-PLGA缓释薄膜的含量测定需求,可以为相关研究提供依据。
