数字化订制钢板及自体髂骨移植修复胸骨缺损的探讨
2022-12-10刘高峰曹军营汤光耀徐彦斌
刘高峰 张 勇 曹军营 周 笠 汤光耀 徐彦斌 刘 艳 张 杰
1.联勤保障部队第988医院心胸外科,河南郑州 450042;2.解放军总医院京北医疗区,北京 100091
随着影像技术的发展,临床上需要胸廓重建的胸部疾患也日渐增多,尤其是累及胸骨的手术,如创伤、胸骨良恶性肿瘤、胸骨骨髓炎、放射性损伤等,常合并胸骨的缺损[1-2]。胸骨重建的质量直接影响了患者的呼吸循环功能,同时使胸廓外形更美观和尽可能减少体内植入物也是胸廓重建的要求。
应用自体髂骨移植到骨缺损处,不受取材的限制,还保证了组织的相容性,有利于缺损处的愈合。其次,自体组织是最符合人体生理的修复材料,拆除内固定后无须长期在体内存留人工材料[3]。临床上常用钢板对植入的髂骨进行内固定,但是胸骨缺损程度的个体化差异较大,且重建过程中需要考虑胸廓的呼吸运动等生理性功能,对重建方式的个性化、精准化要求较高[4]。为此,采用数字化钢板联合自体髂骨移植的方法开展胸廓重建,应用3D技术精准评估胸骨缺损情况及移植髂骨大小,并根据患者胸骨缺损情况订制个性化钢板,将经过塑形后的髂骨块嵌入于胸骨缺损处,以订制的数字化钢板固定胸骨及肋骨,使胸骨与钢板融为一体,形成杠杆并共同运动,取得了良好的效果。
1 病例资料
患者男性,18岁,2017年3月3日因“胸痛10天,活动时明显”入院。查体见胸骨角处隆起、明显压痛,无红肿及波动感。胸部CT提示:“胸骨角骨质破坏并周边软组织增厚,考虑感染性病变”(图1a)。结核抗体三项均为阴性;痰培养未见明显异常,结核杆菌涂片未见抗酸杆菌;肿瘤标志物未见明显异常;血常规、肝肾功能、凝血功能未见明显异常。行胸骨穿刺提示:骨髓液中见异型细胞,不排除恶性。头颅MRI平扫、甲状腺彩超、腹部B超、甲状腺功能等其他检查均未见异常。2017年3月18日行胸骨活检术,术中见胸骨角明显增生,稍有骨质破坏,取部分可疑胸骨送检。病理回报:“胸骨旁软组织送检纤维肌肉组织,其中纤维组织内灶性慢性炎”。活检术后给予头孢呋辛钠1.5 g,q12 h、左氧氟沙星0.2 g,q12 h抗感染治疗7 d。
经血液科、肿瘤科、病理科多科会诊后,考虑胸骨慢性炎,与家属充分沟通后,拟行胸骨部分切除及胸廓成形术。术前根据胸廓三维CT影像数据创立3D模型,确定切除范围及固定部位后订制数字化钢板(图1b,胸骨正中为一纵行钢板,两侧分别连接2个肋骨接骨板固定双侧第2、3肋骨)。2017年3月24日于全身麻醉下取胸部正中切口施术。纵切口沿胸骨正中线自胸骨上窝下1横指到第3肋间水平。切断双侧胸大肌在胸骨、肋骨及肋软骨上的起点,向两侧游离肌皮瓣,充分显露胸骨病变。见病变大小为3.3 cm×3.0 cm×1.6 cm,离断双侧第2肋软骨,分别于距病变上下缘各1 cm处横断胸骨,形成一约4 cm×5 cm的胸壁正中缺损。于右髂骨翼取带髂嵴的全层髂骨块。以订制的数字化钢板固定双侧第2、3肋骨,将修剪成条状的髂骨块前端向上、外面向前嵌入于胸骨缺损处,用剩余的髂骨填塞胸骨缝隙并夯实,继而用螺钉将钢板固定于胸骨上下两端(图2a)。放置纵隔引流管,缝合切口。术后行CT扫描三维重建示数字化钢板与胸廓贴合紧密,胸廓形态正常(图2b),病理检查示:“胸骨角可见骨及软骨组织,伴慢性炎症,局部软骨及血管组织瘤样增生”。术后患者平安返回病房,血常规、肝肾功能、血气分析等检查均未见明显异常。术后第5天复查血常规提示白细胞24.64×109/L,中性粒细胞比率90.41%,遂给予头孢哌酮钠舒巴坦钠1 g,q8 h、左氧氟沙星0.2 g,q12 h治疗6 d,后复查血常规未见明显异常。术后愈合良好,11 d拆除缝线,切口Ⅰ/甲,顺利出院,出院诊断为“胸骨慢性炎”。

图1 术前影像学检查及订制数字化钢板
2017年8月1 日患者再次入院,在全身麻醉下行胸部内固定器取出术。术中取出4枚胸骨处固定螺钉,游离肋骨爪周围组织,将肋骨爪与肋骨完全分离后完整取出数字化钢板。术中见胸骨愈合良好(图2c),术后行CT扫描三维重建见胸廓完整、形态正常(图2d),术后6个月肺功能检查未见明显异常,肺活量3120 ml。随访3年,患者体态及活动正常,每年行1次肺功能及胸部CT检查,均未见明显异常。
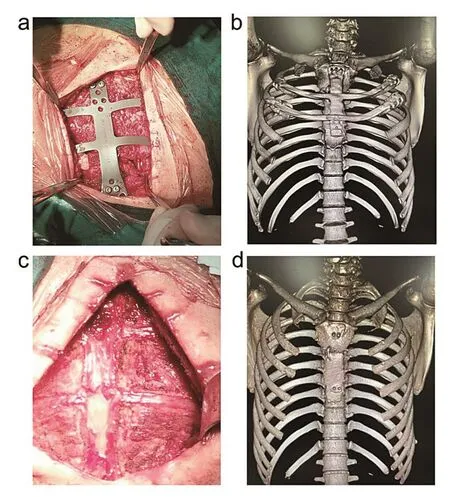
图2 数字化订制钢板联合自体髂骨行胸骨重建
2 讨论
手术切除胸骨后会造成前胸壁存在巨大缺损,不仅使胸骨失去纵向的支撑作用,影响胸廓的稳定性,还会造成胸壁软化、反常呼吸运动等病理生理改变,带来呼吸循环功能的障碍[5]。如何在修复缺损的过程中,维持胸骨及胸廓的结构及功能稳定是胸骨切除重建面临的难点问题要求[6-7]。以本案为例,认为需要从重建材料和重建方式上进行综合考量。
2.1 胸骨重建材料的选择
选择合适的修补重建材料是保证手术成功的关键。目前重建胸壁缺损的材料按来源可分为自体组织、同种异体组织和人工材料三种[8]。按照性状可分为软性材料和硬质材料。对于胸壁缺损,尤其是胸骨缺损,有些专家认为缺损超过1/2,特别是全胸骨切除者应采用硬材料代替胸骨修复骨缺损[9]。
不锈钢丝是胸壁重建中较早应用的材料。因其取材广泛、操作简单,较常用作固定胸骨、肋骨及修补小面积胸壁缺损的材料。但由于其材质软,不仅无法塑性,更容易变形,对于胸骨的缺损并不适合。钛网是在临床上应用较广泛的重建材料之一。其致密的网状结构抗冲击力强,能够为胸腔脏器提供可靠的保护。但钛网作为胸骨重建材料尚有一定的缺点,尤其是随呼吸运动有产生金属疲劳导致钛网局部断裂的风险[10]。对于胸骨中段的缺损,网状的薄层结构很难提供有效的纵向支撑力。
由于单一材料存在一定的局限性,部分学者通过Hybrid技术在重建骨性胸廓后再应用补片类材料封闭胸壁缺损,目前研究较多的是通过构建涤纶布+骨水泥复合体等含骨水泥的“三明治”复合材料行胸廓重塑,取得满意的效果[11]。复合性材料有着明显的优点,如容易操作、方便塑形、重量轻、支撑性好、组织相容度高、骨水泥长期植入对肺功能无影响、长期疗效满意[12]。但复合体置入后有出现植入物松动、植入位置积液、感染等风险,进而造成植入失败。
骨移植是将骨组织移植到患者体内骨骼有缺损、需要固定或加强之处的手术方法。骨移植按移植物来源分为自体骨移植、同种异体骨移植、异种骨移植和人工骨材料移植[13]。其中,组织工程骨包括异种骨和同种异体骨两种[14]。随着生物技术的发展,人工肋骨及人工胸膜用于胸壁缺损的修补也取得了良好的效果[15]。比较而言,新鲜的自体骨植骨目前被认为是修补骨缺损的最佳材料[16-17]。自体骨为自身组织,无异物反应,且新鲜的骨组织能够更有效地保障组织存活。近年来,对于直径<5 cm的原发性胸骨肿瘤,部分学者采用自体髂骨移植重建胸廓取得了良好的效果[4,18]。对于本例患者来讲,纵向胸骨缺损在4 cm左右,所需骨质较少,应用自体髂骨移植到缺损的胸骨处,不仅解决了取材的限制,还保证了组织的相容性,促进胸骨愈合。其次,自体组织是最符合人体生理的修复材料,去除内固定后无需长期在体内存留人工材料。但是,移植的髂骨块位于胸骨缺损中间,通过何种内固定方式保证移植骨的存活和维持胸廓的生理功能是重建过程中面临的一项挑战。
2.2 胸骨重建方式的考量
胸骨位于人体正中,不仅承担纵行的支撑力,还有双侧肋骨横向的拉力。部分胸骨切除后,无法提供横向和纵向的力量支持,导致活动障碍的产生。另一方面,物理切除部分胸骨,使人体的十字交叉处空间缺失,难以形成完整的胸壁,不足以保护内脏的器官。因此,认为修复后的胸廓术后短期应能达到以下标准:①能提供足够的支撑力,维持身体纵轴的平衡;②保证胸廓的稳定性,尤其是横向的摆动;③硬度足够,能保护胸骨后的重要脏器;④组织相容性好,无排异反应;⑤能够长期留存,不松动、变形;⑥使形体有良好外观。
钢板硬度足够、稳定性好、支撑力强,因此加压钢板和肋骨接骨板也被广泛应用于胸廓重建的内固定。如肋骨接骨板不需要使用螺钉固定钢板,固定可靠,不伤及骨髓腔,可多点共同环绕肋骨产生环抱力[19]。然而,由于胸骨缺损的个体差异性,单独的制式肋骨接骨板和加压钢板均不能有效满足临床治疗的需求。数字化技术的发展丰富了临床治疗手段,数字化影像资料可以在术前精准地进行胸廓3D重建,提前预估切除和重建的部位、范围,并能据此制作模板进行3D钛合金打印重建钢板。有学者也指出3D打印技术运用于钛合金能够有效兼顾重建材料的形态匹配性及其组织相容性[20]。为此,提出了应用3D技术精准评估胸骨缺损情况及移植髂骨大小,根据患者胸骨缺损情况订制个性化钢板,将经过塑形后的髂骨块嵌入于胸骨缺损处,以订制的数字化钢板固定胸骨及肋骨的重建方法。
由于使用了更有针对性的钢板,术中在连接双侧肋骨接骨板后,可以更精准地确定胸骨处钢板的位置。将设定好的数字化钢板的正中钢板上下极以螺钉分别固定在残余的胸骨两端,使胸骨与钢板融为一体,形成杠杆,共同运动,不会松动,保证了胸骨的纵向支撑力量。同时,得益于术前精确的设计,准确计算出了胸骨缺损的面积,并确保能够取出足够的髂骨满足胸骨缺损修复的需要。在移植的髂骨与胸骨融合生长、彻底愈合以前,术前个体化订制的数字化钢板还可以维持原有胸廓的形态,使愈合后的胸骨与相邻诸肋骨的空间位置关系均保持一致,有利于维持整个形体的完整性。本例患者应用的钢板无需塑形即和患者完全敷贴,钢板固定后,尤其是两侧肋骨固定后,第2、3肋软骨和剩余胸骨的位置关系与术前相比无明显差异,尤其保证了术后胸廓形态的一致性。经过3年的随访,该名患者切口愈合良好,胸廓形态正常,肺活量正常,近远期效果均令人满意,证明数字化订制钢板配合自体髂骨移植能够有效满足重建骨性胸廓的要求,具有临床应用价值。
