小陷胸汤加味联合二甲双胍对肥胖型PCOS痰热证患者胰岛素抵抗及性激素的影响
2022-12-09许建红李路路蔡平平
许建红,侯 晓,沙 婕,李路路,蔡平平
(1. 山东省中医药研究院附属医院,山东 济南 250014;2. 山东省妇幼保健院,山东 济南 250014;3. 山东省康复医院,山东 济南 250000;4. 淄博市张店区中医院,山东 淄博 255020;5. 山东第一医科大学附属省立医院,山东 济南 250021)
多囊卵巢综合征(PCOS)是育龄期女性常见的内分泌与代谢功能障碍性疾病,临床异质性高,多表现为月经稀发、不孕、高雄激素血症,常合并超重/肥胖、胰岛素抵抗(IR)及代谢综合征[1],可增加心血管疾病、子宫内膜癌等的发病风险[2-3]。一项对我国10个省市的15 924名19~45岁育龄女性分层随机抽样调查显示,PCOS的患病率为5.6%[4],占无排卵性不孕的30%~60%,是引起不孕的重要原因[5]。其中合并肥胖的患病率可达30%~60%[6],70%存在血脂代谢异常,31%~35%存在糖代谢异常,罹患糖尿病风险也是正常人群的5~10倍[7]。资料显示,在超重或肥胖人群中PCOS的发病率亦在增加[8]。因此,PCOS作为慢性内分泌代谢性疾病,需要进行长期的疾病管理及并发症的预防,由于临床存在高度异质性及女性各个生理阶段的不同需求,治疗提倡个体化综合治疗[7]。目前,西医对本病的治疗以二甲双胍口服治疗为主,但部分患者易出现消化道不良反应,或存在不敏感现象,依从性亦差,所以临床治疗效果并不理想。笔者从现代人体质出发,结合传统医学理论,针对痰热证PCOS患者,加用小陷胸汤加味治疗,现将结果报道如下。
1 资料与方法
1.1诊断标准
1.1.1西医诊断标准 参照2018年中华医学会妇产科学分会制定的符合中国人群的PCOS诊疗指南[9]。月经稀发、闭经或不规则子宫出血是诊断的必要条件,再符合以下2项中的1项即可诊断为疑似PCOS:①高雄激素的临床表现或高雄激素血症;②超声表现为多囊卵巢。确定为疑似PCOS后,同时逐一排除其他可能引起高雄激素血症、排卵异常的疾病(如甲状腺疾病、高催乳素血症、早发性卵巢功能不全、功能性下丘脑性闭经、21-羟化酶缺乏症、卵巢或肾上腺分泌雄激素肿瘤、先天性肾上腺皮质增生、库欣综合征等)才可确诊。不孕症诊断标准:夫妇同居1年或以上,性生活正常,未避孕未孕,并排除子宫、输卵管等器质性病变者及男方精液异常者[10]。肥胖诊断标准:参照2011年《中国成人肥胖症防治专家共识》[11]的诊断标准,体质指数(BMI)≥25 kg/m2。
1.1.2中医辨证标准 参照《中医妇科学》[12]及《中药新药临床研究指导原则(试行)》[13]中的相关内容,制定痰热证的辨证标准。主症:①月经周期延后,或月经稀发甚至闭经;②月经紊乱、崩漏;③婚久不孕。兼症:①胸脘痞满;②喉间多痰;③口苦口干;④毛发浓密、面部痤疮;⑤急躁易怒;⑥小便黄、大便溏薄或燥结;⑦带下量多、色黄、质稠。舌脉:舌红、苔黄或黄腻,脉弦滑或滑数。具备主症①+③项或②+③项,兼症3项,参照舌脉即可诊断。
1.2纳入标准 符合西医诊断标准及中医辨证标准;年龄在20~40岁;患者知情同意并自愿参与临床研究。
1.3排除标准 其他原因导致的不孕,如输卵管因素、免疫性不孕、先天性卵巢和(或)子宫发育异常、生殖系统器质性病变等;入组前3个月用过激素类药物者;合并心肝肾等其他系统疾病者;男方精液异常者。
1.4一般资料 选择2019年11月—2021年7月就诊于山东省中医药研究院附属医院妇科门诊及山东第一医科大学附属省立医院中医门诊的痰热型PCOS不孕患者60例。按照随机数字表法将患者分为治疗组和对照组,每组各30例。治疗组年龄20~37(27.9±4.8)岁;病程1.5~6(4.38±1.65)年。对照组年龄21~39(26.7±3.7)岁;病程0.8~5(4.70±1.72)年。2组患者年龄、病程比较差异均无统计学意义(P均>0.05)。本研究经山东省妇幼保健院伦理委员会审核通过(2021-108)。
1.5治疗方法
1.5.1对照组 给予盐酸二甲双胍(中美上海施贵宝制药有限公司,国药准字H20023370,规格:500 mg×20片)口服,500 mg/次,3次/d,药物随三餐分次服用,共服用3个月,经期不影响服药。
1.5.2治疗组 在对照组的治疗基础上予小陷胸汤加味口服。药物组成:黄连6 g、清半夏12 g、瓜蒌皮15 g、竹茹12 g、苍术15 g、茯苓15 g、陈皮12 g、香附12 g、牛膝12 g、瞿麦12 g、茺蔚子15 g、甘草6 g。药物来源于山东省中医药研究院附属医院及山东第一医科大学附属省立医院,每日1剂,煎煮成200 mL药液,早晚分服,共服3个月(经期停药,月经第5天继续服药)。患者自月经周期第5天开始服用中药,月经延迟或闭经者则从孕激素撤退出血第5天开始服用。服药期间嘱患者多运动,少食油腻、辛辣及含糖量高、生冷的食物。
1.6观察指标
1.6.1人体测量学指标 治疗前后测量2组患者身高、体重、腰围、臀围,计算BMI、腰臀比(WHR)。
1.6.2实验室指标 分别于治疗前后在月经周期的第2~5天晨起空腹静脉采血,检测2组患者卵泡刺激素(FSH)、黄体生成激素(LH)、睾酮(T)、空腹胰岛素(FINS)、空腹血糖(FPG),计算LH/FSH和胰岛素抵抗指数(HOMA-IR)(FPG×FINS/22.5)。
1.6.3子宫内膜类型、厚度 于排卵日前后采用美国GE LOGIQ E8彩色超声波诊断仪,IC5-9-D经阴道超声探头(5~7.5 MHz)测量2组患者子宫内膜厚度,评估子宫内膜类型。采用Gonen分型标准[14]:A型,三线型或多层子宫内膜,外层和中部强回声、内层低回声,宫腔中线回声明显;B型,弱三线型,中等强度回声均一,宫腔中线回声断续不清;C型,均质强回声,无宫腔中线回声。
1.6.4月经及排卵、妊娠情况 治疗3个月经周期后,比较2组月经周期及排卵率、妊娠率。
1.7统计学方法 应用SPSS 26.0软件对数据进行统计学处理。计量资料组内比较采用配对t检验,组间比较采用独立样本t检验;计数资料采用2检验。P<0.05为差异有统计学意义。
2 结 果
2.12组患者治疗前后BMI、WHR比较 2组患者治疗前BMI、WHR比较差异均无统计学意义(P均>0.05);2组患者治疗后BMI、WHR均较治疗前明显降低,且治疗组BMI明显低于对照组,差异均有统计学意义(P均<0.05),但WHR与对照组比较差异无统计学意义(P>0.05)。见表1。
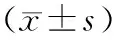
表1 2组肥胖型PCOS痰热证患者治疗前后BMI、WHR比较
2.22组治疗前后FPG、FINS、HOMA-IR比较 2组患者治疗前FPG、FINS、HOMA-IR比较差异均无统计学意义(P均>0.05); 2组患者治疗后FPG、FINS、HOMA-IR均较治疗前明显降低(P均<0.05),且治疗组均明显低于对照组(P均<0.05)。见表2。
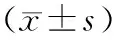
表2 2组肥胖型PCOS痰热证患者治疗前后FPG、FINS、HOMA-IR比较
2.32组治疗前后性激素水平比较 2组患者治疗前性激素水平比较差异均无统计学意义(P均>0.05);2组患者治疗后LH、T水平及LH/FSH均较治疗前明显降低(P均<0.05),且治疗组均明显低于对照组(P均<0.05),2组患者FSH水平治疗前后比较差异均无统计学意义(P均>0.05)。见表3。
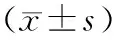
表3 2组肥胖型PCOS痰热证患者治疗前后性激素水平比较
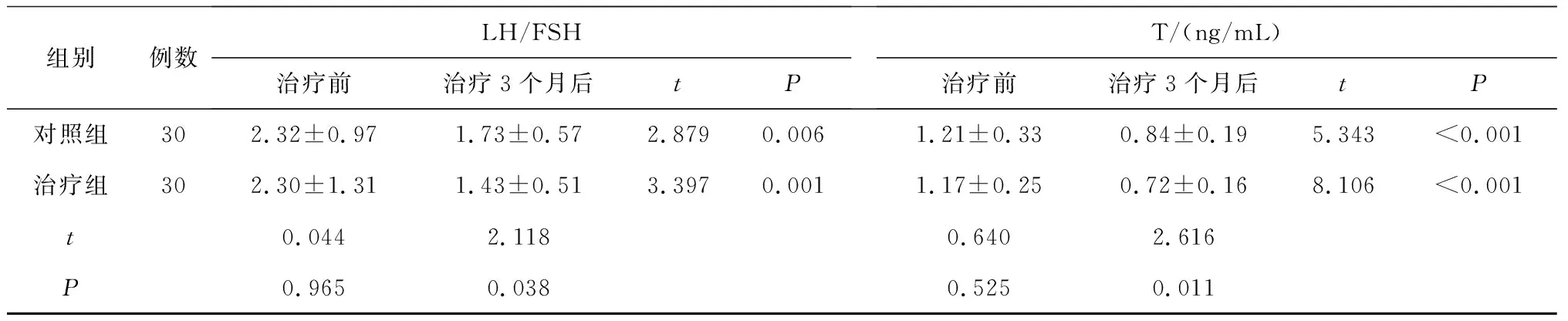
组别例数LH/FSH治疗前治疗3个月后tPT/(ng/mL)治疗前治疗3个月后tP对照组302.32±0.971.73±0.572.8790.0061.21±0.330.84±0.195.343<0.001治疗组302.30±1.311.43±0.513.3970.0011.17±0.250.72±0.168.106<0.001t0.0442.1180.6402.616P0.9650.0380.5250.011
2.42组排卵前后子宫内膜分型及厚度比较 治疗后,治疗组A型内膜比例升高,总体子宫内膜类型分布优于治疗前(2=6.944,P=0.008),亦优于对照组(2=5.554,P=0.018),见表4;治疗组子宫内膜厚度为(0.83±0.15)cm,明显高于对照组的(0.70±0.16)cm(t=3.179,P=0.002)。

表4 2组肥胖型PCOS痰热证患者治疗前后子宫内膜分型比较 例(%)
2.52组月经情况、排卵率及妊娠率比较 对照组治疗后月经周期明显改善,月经周期为(41.7±6.2)d;治疗组治疗月经周期明显改善,月经周期为(38.0±6.6)d,治疗组月经周期较对照组明显缩短(P<0.05)。治疗组排卵率和妊娠率分别为70%(21/30)和53.33%(16/30),均分别明显高于对照组的43.33%(13/30)与26.67%(8/30),差异均有统计学意义(P均<0.05)。
3 讨 论
PCOS是一种内分泌代谢紊乱性疾病,其存在IR、高胰岛素血症及高雄激素血症并存的发病机制,且有高达50%~70%患者合并不同程度的IR[15]。这些因素又通过不同通路影响子宫内膜容受性,导致PCOS患者的低着床率与高流产率。研究发现,伴有IR的PCOS患者子宫内膜中葡萄糖转运蛋白4(GLUT4)及胰岛素受体后信号转导分子表达下降,导致子宫内膜糖利用障碍,阻碍内膜蜕膜化,从而影响胚胎的着床与发育[16-18]。
目前对于肥胖型 PCOS 患者IR的临床治疗,以减轻体重、降低IR程度,纠正糖脂代谢紊乱,并改善生育功能为主要目标。二甲双胍为临床常用的胰岛素增敏剂,2018年国际指南将其作为PCOS治疗的一线用药之一[19],临床常与克罗米芬、来曲唑联合使用。AACE/ACE PCOS临床指南推荐二甲双胍可作为青少年女性患者的单药或联合避孕药、抗雄激素药治疗的一线用药[20]。实验研究发现,二甲双胍通过上调卵巢组织PI3K、PKB、mTOR蛋白的表达,活化PI3K/PKB/mTOR的通路,调节大鼠的性激素水平,改善IR及高雄激素血症[21]。最近有研究发现,PCOS患者血管内皮生长因子(VEGF)水平与卵巢血流量呈正相关,PCOS患者卵巢血管生成增加,提示PCOS患者卵巢血管发育障碍也是PCOS发病的病理生理特征[22]。相关研究显示,二甲双胍可通过调节注射DHEA的PCOS模型大鼠的VEGF、血管生成素及血小板源性生长因子的水平来改善卵巢血管的生成,促进卵泡发育,提高排卵、妊娠及活产率[23]。因此,调节血管生成因子表达也不失为治疗PCOS的新视角。
中医典籍中并无PCOS这一病名,根据其症状一般将其归为“月经后期”“闭经”“不孕”等范畴。既往对肥胖型PCOS的统一认识主要基于脾肾亏虚,并与痰湿、血瘀、气滞等病理产物密切相关。《万氏妇人科 》中云:“惟彼肥硕者,膏脂充满,元室之户不开,挟痰者,痰涎壅滞,血海之波不流,故有过期而经始行,或数月而经一行,及为浊、为滞、为经闭、为无子之病。”《陈素庵妇科补解》中专门提到“妇人体肥者,往往患此”。说明“痰湿”为导致月经后期、育龄期不孕、肥胖的重要因素。随着现代社会经济结构的改变,多数女性饮食结构随之发生变化,喜食辛辣油腻、肥甘厚味之品,再加之生活节奏快,不规律的作息时间、工作学习压力大等,这些因素极易导致痰湿内生、肝郁气滞、火热内蕴,日久痰热互结。所以,笔者在临床工作中发现,痰热证的患者越来越多。
痰之为病,随气升降,上可阻天癸,下可壅冲任胞脉,致月经后期,量少,甚至闭经。加之现代女性容易出现肝气不疏,日久易化热化火,痰与热互结阻于冲任胞宫,以致月经淋漓不尽、崩漏。长期嗜食辛辣肥甘之味,脾胃不堪负重,致脾失健运,胃失升降,水谷精微不归正化,停聚中焦,痰湿内生,日久中满而生内热,痰热互结,充溢机体而生体胖、多毛。此外,肝气过旺还可横克脾土,致脾胃功能失司进一步加重,由此形成痰湿—热—肥胖的恶性循环。痰热相搏阻于肠道,可见大便溏薄或燥结,小便色黄;痰热阻滞冲任,瘀结不通,血瘀与痰浊凝结后挟湿蒸腾于皮肤则见面部痤疮、黑棘皮症;痰浊湿热下注任带二脉,以致任脉不固、带脉失约,出现带下量多、色黄、质稠;舌红、苔黄(腻),脉弦滑亦为痰热互结之征。痰热互结,气机不畅,日久成瘀,结成窠囊,故患者出现卵巢增大、呈多囊样改变,卵泡生长发育受限,卵子无法顺利排出。究其病因,本病与体质、脾失运化、七情内伤密切相关,痰热互结为其主要病理产物,故临床以清热化痰、健脾疏肝为核心治疗原则,但临床对肥胖型PCOS痰热证记载及报道较少。周丽娟[24]提出PCOS主要责之于“痰热瘀互结”,遂治疗上主张以化痰清热、活血化瘀为先,随证辅以扶正健脾、行气疏肝,给予大柴胡汤合桂枝茯苓丸联合达英-35治疗,发现联合治疗通过干预脂肪-胰岛轴,不但能改善糖脂代谢的紊乱,还能减重,改善IR,增加胰岛素敏感性。叶丽芳等[25]提出痰热互结乃PCOS的主要证型,给予三黄汤联合二甲双胍治疗后,患者的临床症状、体质指数和HOME-IR均有明显改善,三酰甘油及T、LH水平显著下降,E2水平明显升高。
小陷胸汤出自《伤寒论》,由“黄连一两、半夏半升、栝蒌实大者一个”三味入药,用于痰热互结于心下或胸膈之小结胸证,具有清热化痰、宽胸散结之义。本研究取“异病同治”之义,在小陷胸汤的基础上加减化裁。黄连苦寒沉降、清热燥湿,半夏辛温升散、化痰消脂,二者共为君药,寒热并用,调畅中焦气机,分消上下湿热之邪,以绝生痰之源,直达病机之要。瓜蒌皮、竹茹甘寒质润,清热化痰,既助黄连泻热,又助半夏涤痰;苍术、茯苓燥湿健脾,与半夏、瓜蒌、竹茹配伍以增强化痰之效;陈皮取气顺痰降、气行痰化之意,增行气之功;香附为血中之气药,具有疏肝理气调经之效,辅以神曲行气导滞;牛膝、瞿麦、茺蔚子活血调经,甘草和中益脾、调和诸药。全方辛开苦降,寒热并用,共奏健脾除湿、清热化痰、理气行滞之功,对痰热证患者切中病机,能较好地改善痰热体质。
仝小林院士运用“态靶结合”的辨证思想提出“中满内热”是肥胖症的核心病机。运用中医经典古方小陷胸汤开郁清热涤痰,同时要根据患者临床伴随症状给予针对性的打靶治疗,对肥、糖、压、酸进行同步调理,最终达到减重、降脂、降压、降糖、调酸的目的[26]。对于PCOS高雄激素血症,仝小林院士提出其核心病机是“热”,具体分为上、中、下三焦3类,同时在辨证基础上结合临证特点选择具有降低血清睾酮作用的“态靶同调”药物,如黄连、清半夏、黄芩、栀子、生地黄等,以提高治疗的精准性及可重复性[27]。IR对PCOS的发生发展具有重要影响,张利民等[28]研究发现,小陷胸汤可保护糖尿病前期痰湿蕴热质患者的β细胞功能,改善IR状态,控制血糖水平,逆转和阻止疾病的进展,相较于阿卡波糖更有效。一项针对小陷胸汤的网络药理学研究发现,小陷胸汤可通过多成分、多靶点、多通路来抑制氧化应激,减轻炎症反应,通过升高细胞内钙离子浓度,阻断胰高血糖素信号通路,激活PI3K/Akt通路来改善IR,提高胰岛素敏感性,降低血糖[29]。黄连素/小檗碱为黄连最主要的提取物,可通过作用于PPAR、MAPK和AMPK关键信号通路来缓解IR,降低雄激素水平,调节脂质代谢,缓解中度慢性炎症,干扰PCOS的发展进程[30]。通过对黄连有效成分的挖掘发现,黄连有多种活性成分共同参与其中,主要包括黄连素、黄柏酮、小檗红碱等多种有机成分,其中在“药物-成分-疾病-靶点”网络中发挥核心作用的成分是槲皮素、黄连素、氢化小檗碱、小檗红碱[31]。临床研究也证实,黄连中的有效成分可改善IVF-PCOS患者的高雄激素血症,降低空腹血糖,改善IR,降低严重卵巢过度刺激综合征的发生率,与二甲双胍获益相当[32]。Dong等[33]研究发现,小檗碱与二甲双胍联用可降低炎症反应,促进胰岛素β细胞分泌胰岛素,提高细胞的胰岛素敏感性,从而达到多种降糖的效果。运用网络药理学方法研究发现,中药复方组药“半夏-苍术-香附”与PCOS共有靶点23个,富集于303条通路,通过主要活性物质槲皮素、山柰酚、β-谷甾醇、木犀草素、汉黄芩素形成系统的调控网络,以增强免疫机制,改善IR,降低炎症因子水平,最终达到系统治疗PCOS的目的[34]。茺蔚子的药理研究中分离到了环肽类、三萜类、黄酮类、甾醇类等化学成分,由于其含大量不饱和脂肪酸,故有抗炎、抗氧化的作用[35]。而多不饱和脂肪酸的摄入对PCOS患者的内分泌水平、BMI、血脂水平均有积极作用[36]。牛膝的主要化学成分为皂苷类与甾酮类,具有抗炎镇痛、调节免疫的作用[37]。甾酮类中蜕皮甾酮在胰岛素抵抗细胞模型中能提高胰岛素介导的葡萄糖的摄取率与利用力,有效改善糖代谢,增加胰岛素敏感性[38]。
本研究结果显示,2组肥胖型PCOS患者治疗3个月后,BMI、FPG、FINS、HMOA-IR均较治疗前明显降低,且治疗组均明显低于对照组,但WHR改善不明显。提示中药联合二甲双胍可改善肥胖患者糖代谢问题,这就有助于降低肥胖患者远期并发心血管等疾病的风险,但因用药周期较短、样本量小,WHR改善不显著;治疗组性激素水平、子宫内膜类型分布、子宫内膜平均厚度改善程度明显优于对照组,且治疗组的排卵率与妊娠率亦都高于对照组,说明中药与二甲双胍可协同调节性激素水平,改善子宫内膜情况,从而提高排卵率及妊娠率。但由于本研究纳入的样本量较少,观察时间较短,缺乏脂代谢指标的检测,故经方小陷胸汤加味的运用对脂代谢紊乱的影响有待进一步研究证实。
利益冲突:所有作者均声明不存在利益冲突。
