ZnO/AgCl/Ag/g-C3N4 复合结构的制备及其光催化性能
2022-12-06杨晓玲常舒婷熊凌竹杨艳春徐文婷童艳花
杨晓玲,常舒婷,熊凌竹,杨艳春,徐文婷,胡 薇,童艳花
(湖州师范学院 工学院,浙江 湖州 313000)
工业化快速发展导致环境问题日益严峻,特别是水体与空气的污染,直接威胁人民生命健康。新型半导体光催化处理技术因成本低、对环境友好,而且能够深度净化水中有机物,在过去几十年中得到了快速发展[1]。
氧化锌(ZnO)是目前应用最广泛的光催化剂之一,具有无毒、无害且导电性良好的特点[2]。更为重要的是,ZnO 具有较大价带顶的势能值,其光生空穴能够将水分子或OH-离子转化成具有强氧化性的羟基自由基(·OH)粒子,能够净化难降解的有毒有机物[3]。然而,纯相ZnO 不但光生电子与空穴容易复合而且容易光腐蚀[4-5],导致纯相ZnO 光催化剂的活性与稳定性均不佳。
两相复合建立内电场是提高光催化剂的光生电子-空穴对分离效率最为普遍的手段。到目前为止,有大量文献报道了ZnO 基异质光催化剂。与ZnO 复合的有:导体,如Au[6]、Ag[7]、石墨烯[8]等;半导体,如TiO2[9]、CuO[10]、BiOI[11]、AgCl[12-17]等。文献中报道的ZnO/AgCl 异质结构都是在可见光下的光催化活性,对于紫外光或太阳光下催化活性很少报道。这是因为AgCl 在紫外光或太阳光照下易分解成单质Ag,随着光照时间延长Ag 颗粒逐渐长大,当Ag 颗粒大到一定程度与基底脱落,最终导致光催化活性与稳定性变差。因此,如何提高ZnO/AgCl 的太阳光稳定性是发挥其应用的关键。
本研究通过对自制ZnO/AgCl 复合物与尿素混合研磨后煅烧处理,得到ZnO/AgCl/Ag/g-C3N4四相复合物,主要成分为ZnO 与AgCl,其次是Ag,g-C3N4的含量较少。并对该复合物的光催化性能进行测试。
1 实验部分
1.1 实验试剂
七水硫酸锌(ZnSO4·7H2O),氨水(NH3·H2O),氯化铵(NH4Cl),硝酸银(AgNO3),无水乙醇(CH3CH2OH),尿素[CO(NH2)2],吡啶(C5H5N),去离子水。
1.2 ZnO/AgCl/Ag/g-C3N4 异质纳米结构的制备
1.2.1 ZnO 的制备
称取1.1258 g ZnSO4溶解于60 mL 超纯水中,记为溶液A。量取3 mL NH3·H2O(26%~28%,质量分数)与7 mL 超纯水,混合均匀形成溶液B。在磁力搅拌下,将溶液B 逐滴加入溶液A 中,直至混合体系pH=9 为止,然后于室温下沉化2 d后放入水浴锅,于80 ℃下水浴2 h,冷却至室温,得到白色絮状沉淀,即为ZnO 前驱体。ZnO 前驱体用去离子水洗涤3 次并离心,备用。将其置于烘箱于60 ℃下干燥10 h,再通过马弗炉于800 ℃下煅烧2 h,即可得到纯相ZnO。
1.2.2 ZnO/AgCl/Ag/g-C3N4异质纳米结构的制备
将上述单个反应釜中得到的ZnO 前驱体分散于90 mL 超纯水中,加入0.048 g NH4Cl,磁力搅拌12 h,促进Cl-在ZnO 前驱体表面吸附。根据Zn:Ag 的摩尔比为10:1,遮光下向上述体系中逐滴加入一定量AgNO3溶液,持续搅拌30 min 后,于60 ℃水浴加热2 h;得到的产物经超纯水与无水乙醇各洗3 次,离心,在电热鼓风干燥箱中于60 ℃下干燥6 h,即可得到ZnO 前驱体与AgCl 的复合物。
将复合物置于马弗炉中以4 ℃/min 升温至800 ℃,煅烧2 h,得到ZnO/AgCl 复合样品。再将一份ZnO/AgCl 复合样品与不同量的尿素混合碾磨后放入马弗炉中,以4 ℃/min 升温至500 ℃,煅烧2 h,此条件连续煅烧两次,即可得到不同比例的ZnO/AgCl/Ag/g-C3N4异质纳米结构。按照煅烧前ZnO 与尿素的物质的量比为10:1、10:3、10:6,最终得到的样品分别记为ZAACN-1、ZAACN-3、ZAACN-6。
1.3 样品表征
采用北京普希仪器有限责任公司的XD-6 型X-射线衍射仪(XRD)表征催化剂的晶体结构,扫描范围为20°~80°,扫描速度为2°/min。
使用JEOL 公司的JEM-F 型透射电子显微镜(TEM)观察样品的形貌,工作电压为200 kV,利用其附件能量色散X 射线光谱(EDX)对样品中元素映像图进行表征。
X 射线光电子能谱由美国PE 公司的PHI-5400 型X 射线光电子能谱仪(XPS)分析获得。
利用Evolution220 固体紫外可见漫反射仪(DRS)对样品进行光吸收测试。
1.4 样品光催化降解活性与稳定性能评价
以太阳光为光源,选用吡啶为目标降解物。分别称取10 mg ZnO、ZnO/AgCl、ZAACN-1、ZAACN-3 和ZAACN-6 加入到60 mL 20 mg/L 的吡啶溶液中,超声分散后避光磁力搅拌30 min,达到吸附平衡,取出5 mL 溶液备测吸附效果。剩余悬浮液置于太阳光下光照,并在光照时间到达20 min、40 min、60 min、80 min、105 min 时各取5 mL溶液离心,吸取上层清液,采用日本岛津UV2600型紫外-可见吸收光谱仪测试吡啶溶液在光催化剂中不同光照时间段的吸光度,波长范围为200~400 nm。取吡啶的最强吸收峰256 nm 处的吸光度,计算其降解率R%,R%=(A0-A)/A0×100%。其中,A0为吡啶溶液初始的吸光度,A 为污染物达到吸附平衡或光照t 时间段的吸光度。将每次光照后的样品收集,分别用去离子水与无水乙醇洗涤两次后离心,在烘箱中于60 ℃下烘干,进行下次同条件光催化循环,测试光催化剂的稳定性。
2 结果与讨论
2.1 晶相结构分析
图1 为ZnO、ZnO/AgCl、ZAACN-3 催化剂的XRD 图。其中,纯ZnO 的所有XRD 衍射峰的位置与六方纤锌矿的标准卡片图谱(JCPDS No.36-1451)完全一致。负载AgCl 后的两个复合样品的XRD 衍射曲线除了具有明显的上述ZnO 衍射峰外,还出现了位于27.8°、32.2°、46.2°、55.2°和57.7°的衍射峰,分别对应于AgCl 标准卡片(JCPDS No.31-1238)的(111)、(200)、(220)、(311)和(222)晶面特征衍射峰。上述AgCl 衍射峰的强度较为明显,表明复合材料中成功引入结晶度较高的AgCl。当ZnO/AgCl 与尿素研磨混合高温煅烧后出现了2θ=38.11°、44.30°与65.0°的新衍射峰,分别对应Ag 标准谱图(JCPDS No.99-0094)中的(111)、(200)与(220)晶面衍射峰。此结果表明样品中部分AgCl 被还原为单质Ag。这可能是由于尿素在分解过程中产生了还原性气体。需要说明的是,ZnO/AgCl 与尿素研磨混合高温煅烧样品(ZAACN-3)并未观察到g-C3N4衍射峰的存在,可能是其含量太少导致的结果。对比3 个样品的XRD 图可以看出,复合AgCl、Ag 和石墨相g-C3N4并未改变原有的ZnO 衍射峰位置,也未出现杂质峰,表明复合后ZnO 的晶体结构保持完整,没有被复合过程破坏。

图1 ZnO、ZnO/AgCl 和ZAACN-3 样品的XRD 图Fig.1 XRD patterns of ZnO,ZnO/AgCl and ZAACN-3
2.2 形貌结构与化学组成分析
为具体观察ZnO/AgCl 和ZAACN-3 光催化剂的微观形貌、尺寸信息以及元素分布,对此两合成样品进行TEM 和EDX 元素映像表征测试。图2(a)与2(b)分别是ZnO/AgCl 和ZAACN-3 样品的TEM 照片,从图2(a)中可以看出,ZnO/AgCl是由约100~600 nm 的纳米颗粒烧结在一起的单个块体。单个块体的表面展现出不同深浅的阴影,中心区域比边缘区域阴影深,这是ZnO 块体表面覆盖了AgCl 产生的。图2(b)也展示了ZAACN-3 样品是由几百纳米的颗粒烧结成的块体,但其深色区不集中而有些分散,且在颗粒的边缘出现了尺寸为几十纳米的小颗粒。除此之外,块体的边缘还有薄片存在。

图2 样品的TEM 照片Fig.2 TEM images of samples
图3(a)为ZAACN 样品暗场扫描透射电子像。图3(b)~3(f)分别对应为Zn、O、Ag、Cl、C、N 元素的映像照片,从中可看出,Zn、O、Cl、C 与N 元素在样品中分布均匀。其中Zn 与O 元素映射信号分布密集且强度高,说明样品主要成分为Zn 与O元素。Ag 元素映像有部分聚集,对应电子像中的小颗粒,说明此小颗粒为Ag 纳米颗粒。这是由于在尿素高温煅烧过程中AgCl 部分还原为Ag 单质。为进一步表征ZAACN-3 样品中有AgCl 与C3N4的存在,对样品进行了XPS 测试,通过元素的价态来确定。

图3 ZAACN-3 样品中各元素映射图Fig.3 Mapping images of elements in ZAACN-3
图4 为ZnO/AgCl 和ZAACN-3 样品的XPS全谱以及相关元素的XPS 特征细谱。谱图中的所有峰均以284.6 eV(C 1s 的结合能)为参考进行了荷电校正。图4(a)中ZAACN-3 样品的XPS 全谱含有ZnO、AgCl、g-C3N4存在的Zn、O、Ag、Cl、C、N 元素的光电子谱线,与预期一致。图4(b)为Zn 2p 的高分辨细谱,两个强峰分别与Zn 2p3/2与Zn 2p1/2相对应,两峰间距为23.0 eV,说明Zn 在2个样品中均仅以+2 价氧化态的形式存在[18]。然而,ZnO/AgCl 与ZAACN-3 的Zn 2p 峰相对纯ZnO的Zn 2p 峰(2p3/2,1021.3 eV;2p1/2,1044.4 eV)均向高结合能方向移动,其中ZnO/AgCl 偏移最多,此现象说明ZnO 与AgCl 之间结合较强。
图4(c)显示的是O 元素的特征细谱。通过对不对称的O1s 能谱曲线进行分峰,可获得3 个不同结合能位置的拟合峰。ZnO/AgCl 样品的3 个拟合峰位置分别位于531.9 eV、533.0 eV、533.74 eV处,而ZAACN 中相应3 个拟合峰的位置为530.1 eV、531.6 eV、532.5 eV 处。3 个拟合峰代表了O 元素的3 种不同结合状态,其中低结合能处的峰属于ZnO 的晶格氧,而中间结合能处的峰属于ZnO 晶格中的缺陷氧,高结合能处的峰则代表吸附于ZnO 表面的H2O 或O2[6]。对比二者中间拟合峰的相对强度,可知ZAACN-3 中缺陷氧的峰相对强度显著高于ZnO/AgCl,则说明ZAACN 中的氧缺陷浓度高于ZnO/AgCl。此外,从整条O 1s 谱线对比,ZAACN-3 的O 1s 峰相对ZnO/AgCl 的峰向低结合能方向偏移了1.5 eV,这可能是由于氧空位的增多引起O 与其他元素键合不平衡从而导致O1s 电子束缚能的降低。
图4(d)展示的是Ag 3d 特征细谱。对于ZnO/AgCl,位于367.8 eV、373.7 eV 峰可指标化为Ag 3d3/2与Ag 3d1/2,对应于+1 价的Ag。因ZAACN-3样品的Ag 3d 能谱峰显示不对称,所以进行了拟合,得到4 个峰。处于低结合能367.2 eV、373.1 eV的峰可归属于金属Ag(0)[19],而在高结合能367.6 eV、373.5 eV 的峰则属于AgCl 的Ag(+1)[20],因此可说明ZAACN-3 复合物中除了AgCl 外,还有单质Ag 存在,与元素映像图相对应。在图4(e)中ZAACN-3 出现了结合能为197.65 eV、199.1 eV的2 个拟合峰,分别对应Cl 2p3/2和Cl 2p1/2[21],可归属于-1 价的Cl,结合+1 价的Ag 离子,可推断样品中存在AgCl。
图4(f)中结合能在284.6 eV 与288.6 eV 对应外来污染碳的峰位,而ZAACN-3 样品在286.0 eV 的峰可以对应C-NH2中的碳键[22]。同时图4(g)也证实N 元素的存在,对其分峰拟合得到398.5 eV、399.5 eV、400.8 eV 分别对应N—C=N、N-(C)3以及N-C-H[23],再结合元素映像图可以证明g-C3N4成功复合在ZnO/AgCl/Ag 上。
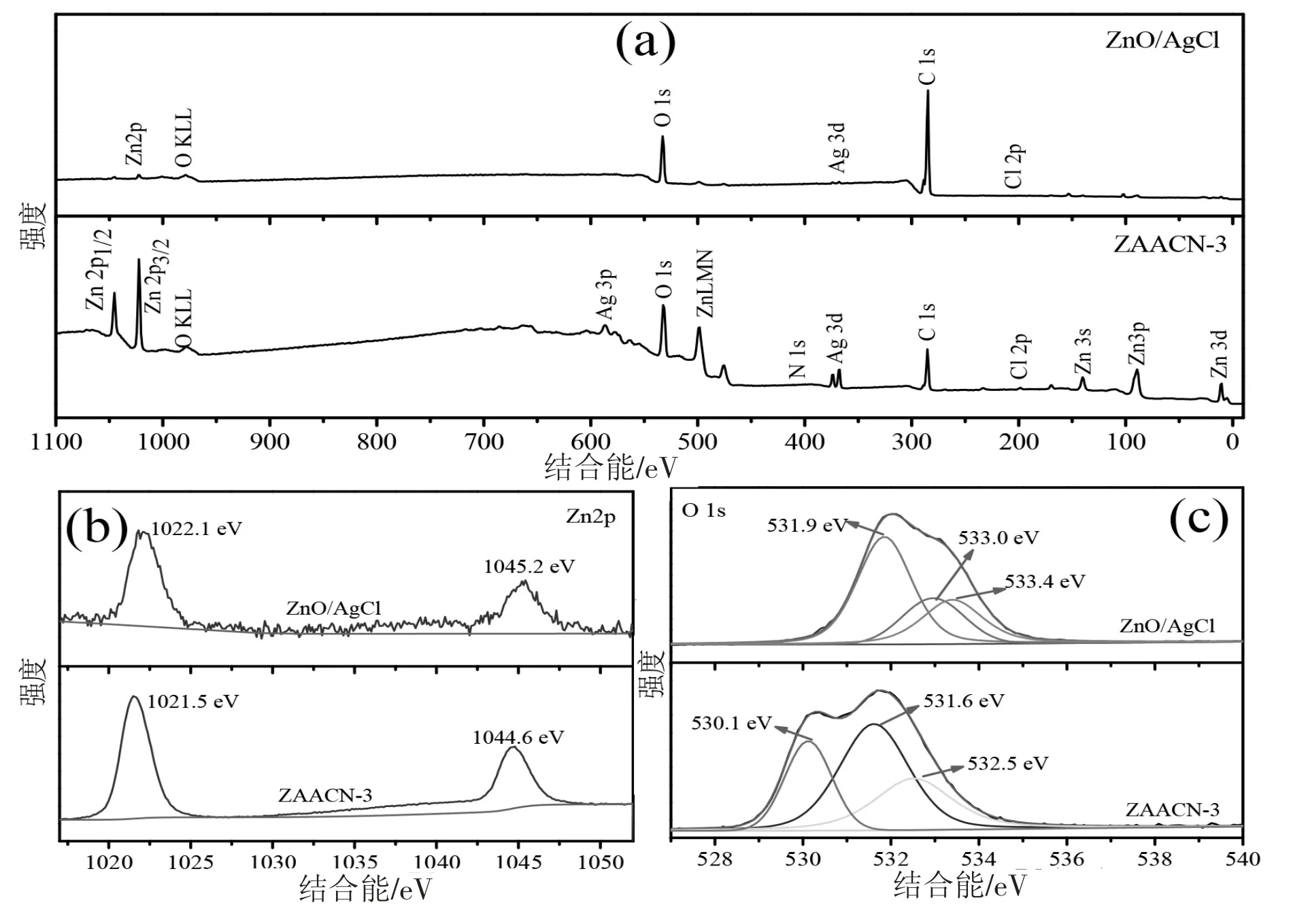
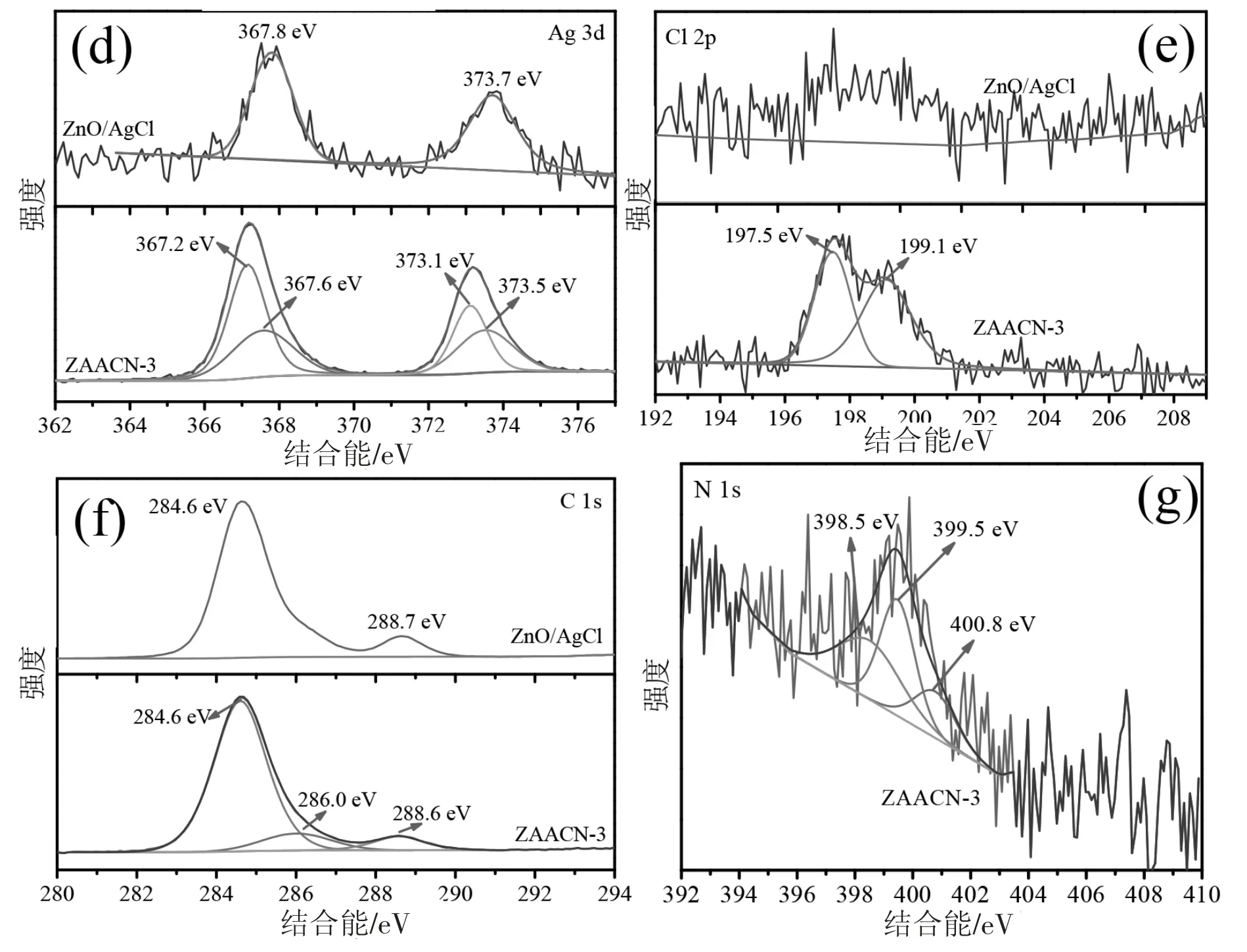
图4 ZnO/AgCl 和ZAACN-3 的全谱以及各自Zn、O、Ag、Cl、N 元素的XPS 精细谱Fig.4 The whole XPS spectra of ZnO/AgCl and ZAACN-3 and fine XPS spectra of Zn,O,Ag,Cl,C and N elements in them
2.3 光学吸收性能
图5 为ZnO、ZnO/AgCl、ZAACN-3 的紫外-可见DRS 光谱图。可以看出纯ZnO 样品的吸收边处于406 nm,说明纯ZnO 只对紫外波段的光区发生响应。当ZnO 与AgCl 复合后,吸收边约为409 nm。与纯ZnO 相比,发生移动较小。不同的是,在420~650 nm 的可见光区有一定的吸收,这可能是在测试过程中,少量AgCl 在光照下分解成Ag 单质造成的可见光区的少量吸收。对于ZAACN 的DRS 曲线,不但吸收边(428 nm)发生了红移,并且在紫外光区的反射率小于ZnO/AgCl和ZnO。除此之外,在450 nm 附近的有较强的吸收峰出现,这是由于纳米Ag 表面等离子效应引起[24],进一步核实了Ag 单质的存在。此结果表明:g-C3N4与Ag 共同修饰的ZnO/AgCl 不仅拓宽了可见光吸收的波段,而且还增强了紫外光的吸收,有利于ZAACN 光催化剂对太阳光的利用。
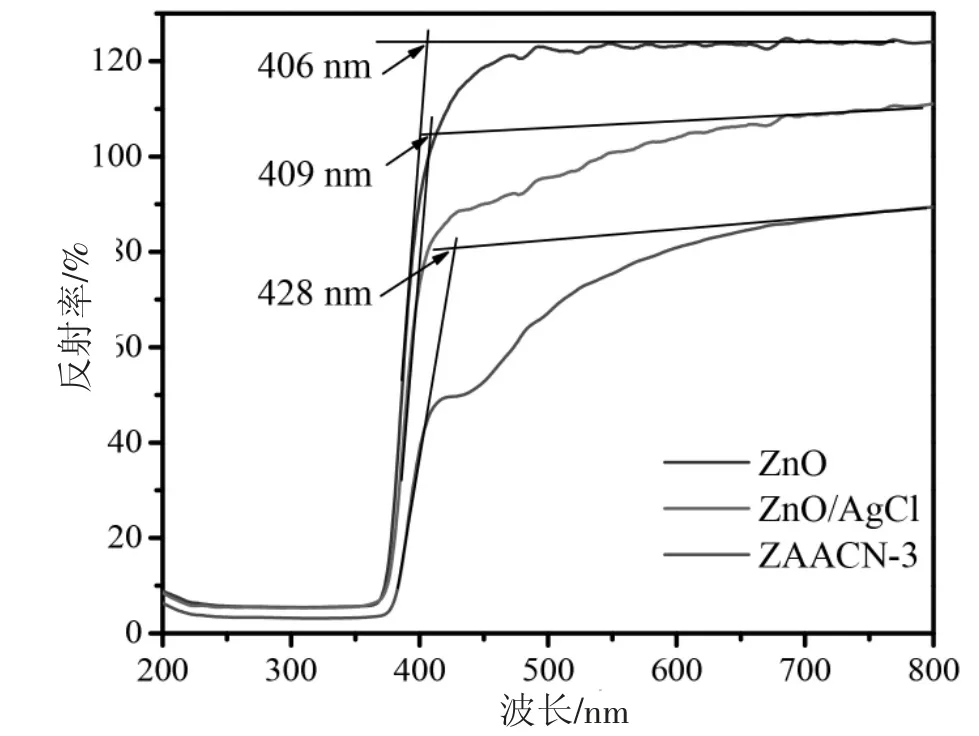
图5 ZnO、ZnO/AgCl 和ZAACN-3 样品紫外-可见漫反射光谱图Fig.5 UV-Vis DRS spectra of ZnO,ZnO/AgCl and ZAACN-3
2.4 ZnO/AgCl/Ag/g-C3N4 复合光催化剂的光催化性能
图6 是不同样品在同等条件下自然日光光催化降解率随时间变化的曲线图。从图中30 min的吸附点,可计算出ZnO、ZnO/AgCl、ZAACN-1、ZAACN-3 和ZAACN-6 的吸附率分别为6.97%、7.37%、12.79%、10.57%和11.81%。由此可看出,各样品对吡啶仅存在少量吸附,ZAACN 样品的吸附效果略优于ZnO/AgCl 和ZnO。这可能是由于ZAACN 表面被超薄的C3N4纳米片包覆,致使表面积有所增大。在太阳光照下,每种样品所在吡啶溶液的瞬时相对含量都随光照时间的延长而降低,表明各样品对光催化降解吡啶都有一定的活性。当光照时间达到105 min 时,ZAACN-1、ZAACN-3、ZAACN-6 所在吡啶的降解率分别为93.37%、97.51%和88.23%,ZnO/AgCl 对应的降解率为73.38%,而纯ZnO 对应的降解率仅为56.78%。此结果说明,g-C3N4与Ag 能够协同提高ZnO/AgCl 的光催化活性,其中ZAACN-3 提高的幅度最大。然而进一步提高g-C3N4的比例,光催化活性提高的幅度开始下降。这可能是由于当尿素的量超过某个值时,部分g-C3N4会独立形成,不全是g-C3N4与ZnO/AgCl 的复合物,而纯g-C3N4的光降解吡啶效果很弱,导致整体光催化效率有所降低。
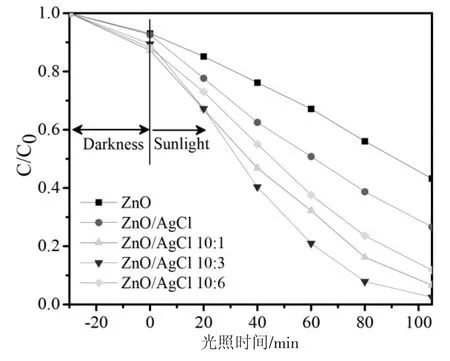
图6 ZnO、ZnO/AgCl、ZAACN-1、ZAACN-3 和ZAACN-6 样品光催化降解吡啶随光照时间的曲线图Fig.6 Time-dependent photocatalytic degradation of pyridine over ZnO,ZnO/AgCl,ZAACN-1,ZAACN-2 and ZAACN-3
图7 是各样品日光光催化后再循环3 次光催化的降解动力学曲线图。ZnO/AgCl 的首次光催化效率比纯ZnO 约高1.3 倍,但在回收第1 次,提高的幅度开始降低,到第2、3 次回收,其光催化效率都比ZnO 低。这应归属于AgCl 在光照下易分解成Ag,当Ag 颗粒长大后,又易与ZnO 基底脱落,导致光催化性能恶化。与之相对比,经过g-C3N4与Ag 共修饰的ZnO/AgCl(即ZAACN-1、ZAACN-3、ZAACN-6)在3 次回收后的光催化效率分别为90.00%、88.59%、83.74%,相比首次光照下降不到10%,说明g-C3N4与Ag 协同修饰ZnO/AgCl 能够提高其光催化活性及稳定性。
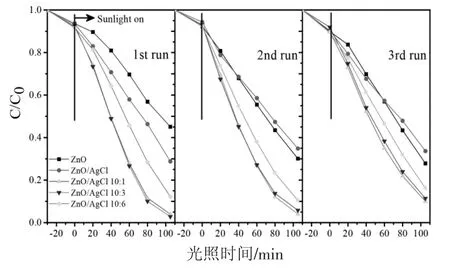
图7 ZnO、ZnO/AgCl、ZAACN-1、ZAACN-3 和ZAACN-6 循环光催化降解PY 的对比图Fig.7 Recycles of photocatalytic degradation of pyridine over ZnO,ZnO/AgCl,ZAACN-1,ZAACN-2 and ZAACN-3
2.5 ZnO/AgCl/Ag/g-C3N4 光催化活性与稳定性同时提高的初步机理
根据文献[17,25]报道的ZnO、AgCl、g-C3N4以及Ag 的能带位置与本研究所制备的g-C3N4包覆ZnO/AgCl/Ag 异质结构,其在太阳光照下产生的光生电子与空穴的传输途径如图8 所示。ZAACN在太阳光照下,因g-C3N4含量极少,主要产生光生电子与空穴的是ZnO 与AgCl。由图8 中各物质的价带顶与导带底能级高低可知,ZnO 与AgCl的光生电子都流向Ag 颗粒;AgCl 的光生空穴流向ZnO 区,ZnO 区的空穴部分流向g-C3N4。因此,g-C3N4与Ag 的协同作用更加促进了ZnO/AgCl异质结的光生电子与空穴分离。特别是Ag 颗粒的存在促进了AgCl 区的光生电子及ZnO 区传送来的电子的驱散,有效抑制光生电子与晶格中Ag+结合生成Ag,从而提高了AgCl 的稳定性。此外,由于ZnO/AgCl/Ag 受到g-C3N4的包裹,不仅可以保护Ag 纳米粒子在光催化中不受空气中氧气氧化,而且可以抑制纳米Ag 粒子从复合材料表面脱落,使得复合光催化剂在后续使用中依旧维持高降解率,能够进行多次循环利用。综上所述,正是因为g-C3N4与Ag 纳米颗粒协同作用,不仅使光生电子与空穴的复合及AgCl 的光腐蚀得到了有效抑制,而且还能防止Ag 纳米颗粒的氧化,最终导致ZAACN 的光催化活性与稳定性都得到提高。
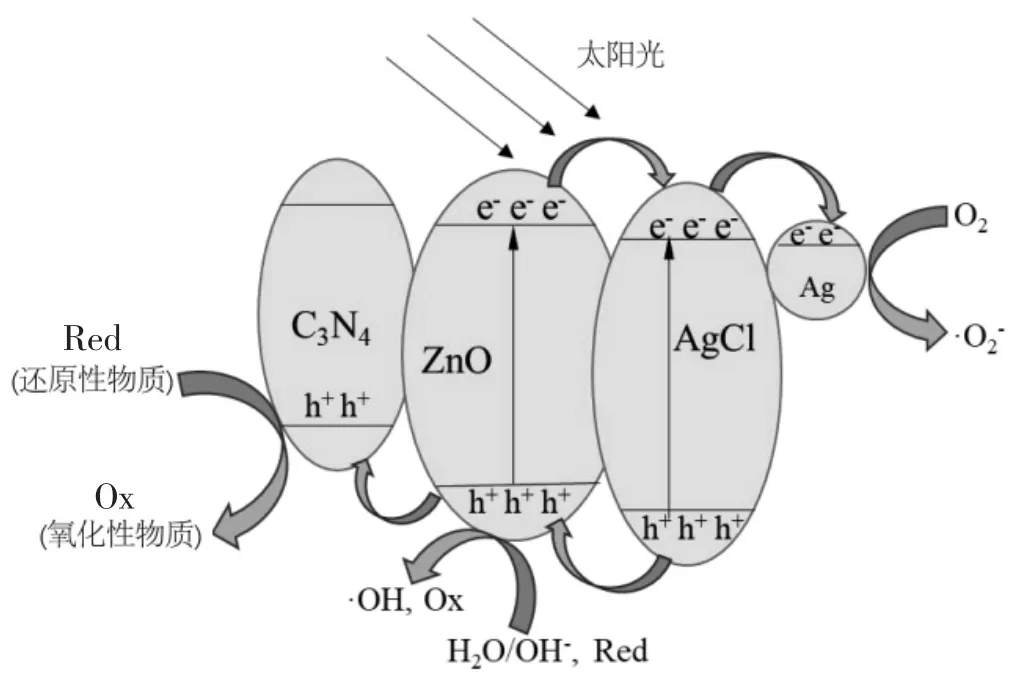
图8 ZnO/AgCl/Ag/g-C3N4 复合结构的光催化机理示意图Fig.8 Schematic of photocatalytic degradation over ZnO/AgCl/Ag/g-C3N4 composite
3 结论
通过沉淀法先制备ZnO 前驱体,负载AgCl后再与尿素研磨混合高温煅烧得到ZnO/AgCl/Ag/g-C3N4复合光催化剂。与ZnO/AgCl 及ZnO 相比,ZnO/AgCl/Ag/g-C3N4复合光催化剂拥有更宽的可见光响应范围及更强的紫外光与可见光的吸收强度,表现出更高的光催化降解吡啶活性与稳定性。ZnO/AgCl/Ag/g-C3N4复合光催化剂的光催化活性与稳定性的提高是由于负载的Ag 与g-C3N4的包覆,不仅促进了光生空穴的转移而且有效控制了纳米Ag 粒子的氧化与脱落,使ZnO/AgCl/Ag/g-C3N4表现出良好的光催化稳定性,经过3 次回收,降解率仍能达到90%。
