乳腺癌调强计划边界外放对靶区和皮肤剂量的影响
2022-12-05沈丹青吴传锋沈裕策
管 建,胡 睿,沈丹青,吴传锋,沈裕策,李 成
受益于体位固定、图像引导和运动管理技术在乳腺癌放射治疗(简称“放疗”)中的发展,包括固定切线野正向和逆向调强、旋转容积调强等放疗技术正逐步应用于临床。当调强计划设计时,乳腺癌放疗临床靶区(clinical target volume,CTV)的外放常会超过体表,尤其是保乳计划为避免其皮肤获得较高的剂量和满足治疗计划系统(treatment planning system,TPS)剂量计算的要求,CTV外放到计划靶区(planning target volume,PTV)的外侧界通常会内收至皮下3~5 mm[1]。而内收后呼吸运动和摆位操作所引起的靶区位移误差不可忽视,受其影响照射范围内靶区和危及器官(organ at risk,OAR)的剂量不确定性增加。相关研究和文献提示[2~5],计划设计时可采用按一定比例混合适形和调强计划、PTV虚拟外放及通量编辑功能等(如Eclipse系统的skin dose)来保证距离PTV外侧界一定范围内的剂量处方和评估要求。
回顾这些研究和文献,无论采用何种方法保证PTV外侧界的剂量要求,都鲜有提及对皮肤剂量的影响,尤其是呼吸运动状态下皮肤剂量的动态影响[6]。而在临床放疗中,表现最直观和患者最敏感的乳腺癌保乳术后放疗副反应就是皮肤损伤。笔者研究的主要目的就是比较现行的几种PTV外侧界剂量处理方法,如直接通量编辑、添加虚拟Bolus等在逆向调强计划设计中对照射野区域内皮肤剂量的影响,重点分析皮肤剂量在自由呼吸运动状态下的变化。
1 资料与方法
1.1 临床资料
选择2019年11月至2020年6月在苏州市立医院东区行乳腺癌(均经病理诊断证实)保乳术后放疗的患者10例,年龄27~69岁,平均年龄46.6岁(标准差15.3岁);病灶位于左侧3例,右侧7例;临床分期为T1~T2。所有患者均被告知相关临床治疗风险。该研究通过笔者所在医院伦理委员会论证。
1.2 方法
1.2.1 体位固定和定位
所有患者均采用乳腺癌常规治疗体位托架固定,平静自由呼吸。采用美国GE公司Discovery 590RT模拟定位CT行常规扫描[三维(three-dimensional,3D)]和动态扫描[四维(four-dimensional,4D)],扫描条件120 kV,自动毫安秒,层厚5 mm。利用“随心呼”功能动态扫描后依据原始图像重建10个时相的CT图像。所有影像资料均归集到美国Varian公司Eclipse 11.0计划系统进行靶区和OAR勾画及计划设计。
1.2.2 临床靶区和危及器官勾画
首先,将每例患者的3D CT静态图像分别与4D CT动态图像利用TPS的Registration功能进行图像配准。其次,在3D CT静态图像勾画CTV和OAR,全乳腺靶区CTV参考美国肿瘤放射治疗协作组织(Radiation Therapy Oncology Group,RTOG)乳腺协作组的标准,并常规勾画双侧肺、心脏、健侧乳腺等OAR。最后,依据患者3D CT静态图像的CTV和OAR轮廓信息建立模板,利用TPS的Smart Segmentation功能自动勾画该患者4D的10组CT图像的CTV和OAR,并由同一名医生依次修改和确认。
1.2.3 计划靶区和皮肤感兴趣区的生成
物理师对每例患者所有CT图像(3D和4D共11组)CTV进行外放,各方向均匀外放5 mm,与体轮廓(BODY)结构“相与”后生成PTV0(图1A);在近体表方向PTV0以BODY为界内收3 mm生成PTV0-0.3,内收5 mm生成PTV0-0.5;PTV0与PTV0-0.3“相减”生成Skin 0.3,PTV0与PTV0-0.5“相减”生成Skin 0.5(图1B、C);PTV0近体表方向外放5 mm生成PTVBolus(添加虚拟Bolus计划方法的优化计算靶区),PTV0近体表方向外放10 mm并与体轮廓“相减”生成V-Bolus(赋予虚拟Bolus区域)(图1D、E)。PTV0-0.5作为计划评估的靶区PTV,Skin 0.3和Skin 0.5作为计划评估的3 mm和5 mm皮肤感兴趣区。
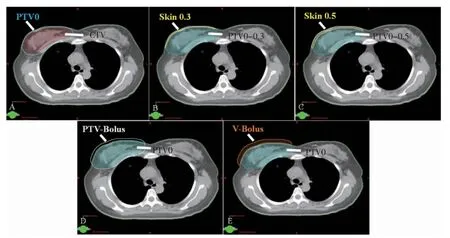
图1 PTV和皮肤感兴趣区的生成Fig.1 Images of generation region of interest in PTV and skin
1.2.4 计划设计
依据试验方案共设计6组计划,根据剂量要求在每例患者3D CT上设计5野逆向调强计划,内切方向2个、外切方向3个照射野,每野间隔10°,命名为Plan3D;复制Plan3D计划,命名为Plan3Dfluence,并在每个射野方向观(beam eye view,BEV)上,沿体表方向利用TPS的Skin Flash Tool功能,直接编辑通量覆盖至V-Bolus外界;复制3D CT图像将V-Bolus和体轮廓“相或”生成新体轮廓,并赋予V-Bolus新的CT密度值为-400 HU,射野同Plan3D,计划优化完成后复制计划到原来的3D CT图像上,生成Plan3DVBolus;将Plan3D、Plan3Dfluence和Plan3DV-Bolus分别复制到每例患者4D CT的10组图像上,各取剂量的十分之一叠加生成新的计划,分别为Plan4D、Plan4Dfluence和Plan4DV-Bolus。
1.2.5 处方剂量
靶区PTV的处方剂量为50 Gy,分25次,同时满足100%处方剂量至少包绕90%靶区体积,95%的处方剂量至少包绕99 %的靶区体积;PTV内大于110%处方剂量体积不超过1%靶区体积,每层CT图像内的最大剂量点均在PTV内。OAR优化条件:脊髓Dmax<40 Gy;患侧肺V20<20%,且V5<40%;心脏Dmax<8 Gy;健侧乳腺Dmax<5 Gy。
1.2.6 计划优化与评估
所有计划均在Eclipse 11.0上设计,计算采用美国Varian公司Truebeam SN型加速器6 MV射线模型,均采用相同优化参数设计,以PTV作为靶区优化目标并归一剂量。优化终止条件为满足相应靶区处方剂量和OAR限值条件。分别评价各计划PTV(V95)、皮肤Skin 0.3和Skin 0.5(V30、V40、Dmean)的体积。
1.3 统计学方法
采用SPSS 22.0统计软件进行分析。对3D CT的Plan3D、Plan3Dfluence和Plan3DV-Bolus,以及4D CT的Plan4D、Plan4Dfluence和Plan4DV-Bolus,共6组计划的PTV、Skin 0.3和Skin 0.5相关剂量评价指标进行正态检验,所有数据均符合正态分布,通过单因素方差分析 (one-way analysis of variance,one-way ANOVA)分别对3D CT和4D CT中不同计划组进行组间比较。通过配对t检验比较同种计划方法下常规组和动态组,分析每例患者自由呼吸状态与皮肤剂量变化的相关性。P<0.05为差异有统计学意义。
2 结果
2.1 不同射野边界外放方法下计划方法的评价指标比较
记录3D CT和4D CT中不同射野边界外放方法下计划的评价指标变化,即PTV(V95)、皮肤Skin 0.3和Skin 0.5(V30、V40、Dmean)。对数据进行统计分析,各数据均服从正态分布。见表1。
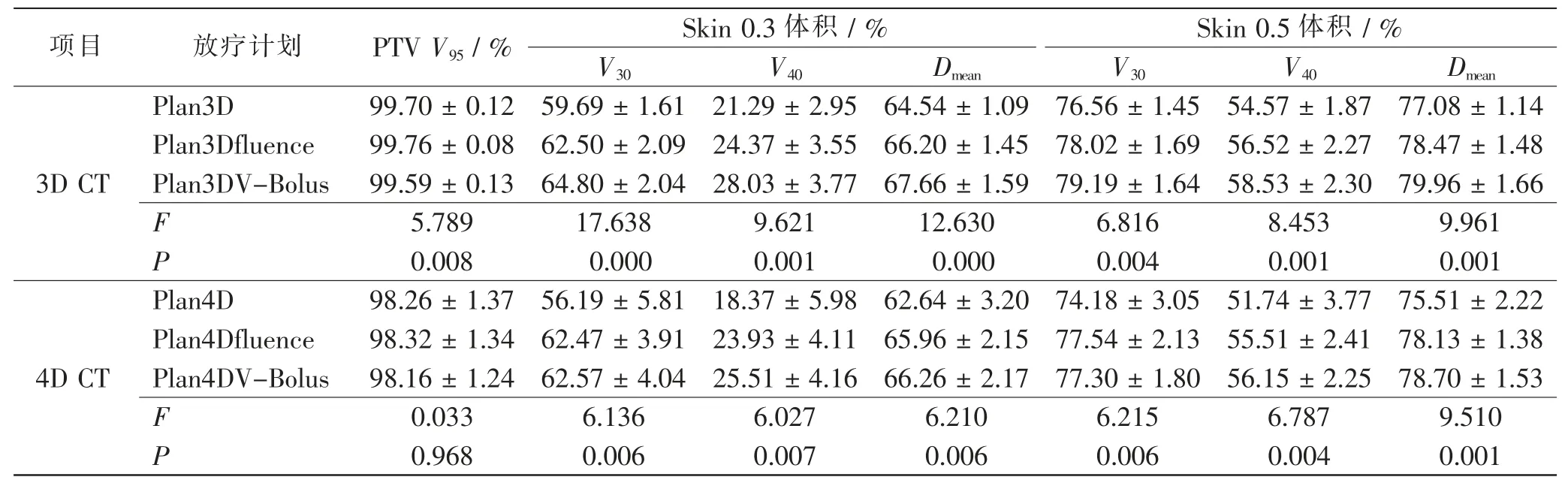
表1 不同射野边界外放方法两种不同扫描下计划的评价指标比较Tab.1 Comparison of evaluation index results of plans under 2 different scans with different field boundary extension methods
利用ANOVA分析方法对比3D CT与4D CT中3种计划方法的相关评价指标变化,其中3D CT中3种计划方法PTV(V95)、皮肤Skin 0.3和Skin 0.5(V30、V40、Dmean)评价指标比较,差异均具有统计学意义(P<0.05)。4D CT中除PTV指标V95的P>0.05外,其余指标均有统计学意义(P<0.05)。10例患者中不同计划方法组间自由度均为2,组内自由度均为27,在显著性水平为0.05时,F分布临界值F(2,27)为3.35,F值均大于临界值,组间的特征差异大。
2.2 同一计划方法下两种扫描方式比较
使用配对t检验方法分别对3D-MENDIAS和4D-MENDIAS同一计划方法下靶区和皮肤剂量进行分析(表2)。3种计划方法在组间比较中PTV指标V95差异有统计学意义(P<0.05);皮肤剂量指标只有在添加V-Bolus计划方法下,Skin 0.5中V30和V40的比较结果,差异有统计学意义(P<0.05)。
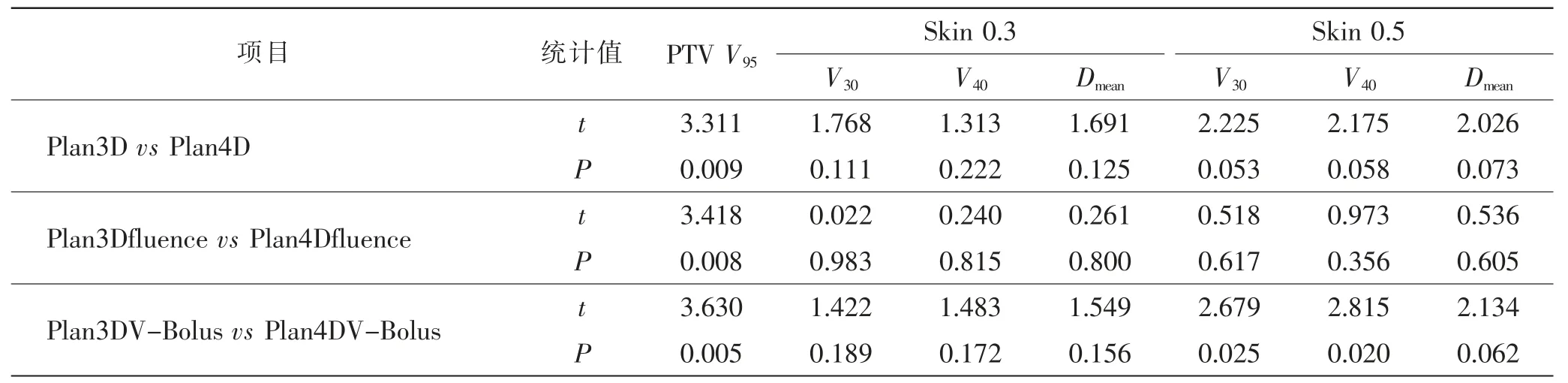
表2 3D CT与4D CT同一计划方法靶区和皮肤剂量比较Tab.2 Comparison results of PTV and skin dose of routine group and dynamic group in the same plan mode
在3D CT的Skin 0.3和Skin 0.5中,两种计划方法皮肤剂量较5野切线方向调强计划均有增加,其中直接通量编辑方法皮肤V30增加了4.71%和1.91%,皮肤V40增加了14.47%和3.57%,皮肤Dmean增加了2.57%和1.80%;添加虚拟Bolus方法皮肤V30增加了8.56 %和3.44 %,皮肤V40增加了31.66 %和7.26 %,皮肤Dmean增加了4.83%和3.74%。在4D CT的Skin 0.3和Skin 0.5中,相较5野切线方向调强计划,直接通量编辑方法皮肤V30增加了11.18 %和4.53%,皮肤V40增加了30.27%和7.29%,皮肤Dmean增加了5.30%和3.47%;添加虚拟Bolus方法皮肤V30增加了11.35%和4.21%,皮肤V40增加了38.87%和8.52%,皮肤Dmean增加了5.78%和4.22%。
3 讨论
放疗是乳腺癌常见的治疗手段之一,但在治疗肿瘤的同时,也引起一些临床并发症,皮肤放射性损伤是乳腺癌患者放疗中最常见的副作用之一[7~9]。皮肤放射性损伤主要症状有红斑、湿性脱皮等,严重时会影响放疗进程甚至中止,同时治疗过程中对患者心理的负面影响不可低估[10,11]。笔者研究就调强放疗对该问题进行讨论,从而指导实际临床操作。
相关研究均证实放疗中皮肤受照剂量升高是增加皮肤放射性损伤风险的高危因素[6],为了减少皮肤放射性损伤的发生概率,在不影响治疗目标的前提下,接受剂量超过40 Gy的皮肤体积应达到尽可能低的水平[12]。基于相关文献中对皮肤剂量毒性反应的研究结果,笔者在研究中将皮肤剂量的评价指标定义为处方剂量(50 Gy)的60%(30 Gy)和80%(40 Gy)[13],皮肤定义为照射野范围内体轮廓下3 mm和5 mm,即Skin 0.3和Skin 0.5。
笔者研究中采用了两种用于补偿PTV剂量的乳腺调强计划射野边界外放方法对靶区和皮肤剂量的影响。一种为直接通量编辑,即利用Skin Flash Tool功能在每个野的射野方向BEV上[14],沿体表方向编辑通量覆盖皮肤外界10 mm;另一种为添加虚拟Bolus,即在乳腺靶区层面向体轮廓外扩10 mm,并赋予外扩区域新的CT密度值(-400 HU),CTV进行常规外放并且不再对外侧界内收处理[4,14]。同时,笔者设立了3D CT(即不考虑呼吸运动影响)和4D CT(利用4D重建模拟患者临床实际照射过程中呼吸运动)。在3D CT中,对于5野切线方向调强计划和采用两种边界外放方法后,其PTV指标V95的影响存在统计学意义,3种计划方法PTV指标V95差异有统计学意义,4D CT中3种计划方法PTV指标V95差异无统计学意义,但无论3D CT还是4D CT,PTV指标V95均满足临床治疗需求。而使用直接通量编辑和添加虚拟Bolus的方法均增加了体表皮肤受照剂量,在3D CT的Skin 0.3和Skin 0.5中,两种计划方法皮肤剂量较5野切线方向调强计划均有增加。在4D CT的Skin 0.3和Skin 0.5中,相较5野切线方向调强计划,直接通量编辑方法皮肤V30、V40、Dmean均增加;添加虚拟Bolus方法皮肤V30、V40、Dmean也增加。
同时笔者也研究了同种计划方法在3D CT和4D CT间的剂量变化。4D CT中各计划方法的PTV指标V95均小于相对应3D CT,下降了约1.5%,虽然差异具有统计学意义,但进一步临床评价其降低程度不大,仍能满足临床治疗要求。Veldeman L等[15]研究也提示乳腺癌其呼吸运动幅度不大,冠状轴方向为1.49 mm,矢状轴方向为1.44 mm。笔者试验中患者平静呼吸下呼吸动度冠状轴方向最大为1.08 mm,平均为0.32 mm,矢状轴方向最大为2.21 mm,平均为1.24 mm,考虑笔者研究的病例采用乳腺托架或翼型板固定体位,患侧手臂均上举,一定程度上对乳腺起到牵拉固定的作用,故患者呼吸运动幅度受到限制。如果呼吸幅度增加,其靶区剂量的减少将相应增加,应引起临床的重视。而体表皮肤Skin 0.3和Skin 0.5的受照剂量变化无统计学意义,且相应Dmean的下降程度均不超过3%,呼吸运动对患者乳腺表面皮肤剂量影响不大。
上述直接通量编辑和添加虚拟Bolus的方法制定的初衷,都是考虑患者放疗过程中的呼吸运动和器官内运动等因素可能会造成靶区实际受照剂量缺失。笔者的研究表明,参照3D定位CT设计的调强计划,患者实际接受的靶区剂量略低,但仍能满足放疗需求,而直接编辑通量和添加虚拟Bolus的方法,对靶区剂量补偿作用不大,且在一定程度上增加了患者乳腺表面的皮肤剂量毒性,相应地增加了患者发生放射性皮肤损伤的风险。
4 结论
笔者研究主要比较了静态和动态下两种常用射野边界外放方法对靶区和皮肤剂量的影响。两种方法即体表直接通量编辑和添加虚拟Bolus,在3D CT图像下相比常规无剂量补偿的5野切线调强计划,对靶区剂量有所改变,但对实际临床治疗影响不大;4D CT图像下虽受呼吸运动影响靶区剂量有所下降,但仍满足临床评估要求,当呼吸幅度进一步增大时靶区剂量的改变需待进一步的研究。同时,这两种剂量补偿方法无论在静态还是动态下,均会增加照射野范围内乳腺的皮肤剂量,在临床应用中应评估和关注其对皮肤的损伤,酌情使用。
