中国全膝关节置换术围手术期疼痛管理指南(2022)
2022-12-05中华医学会骨科学分会关节外科学组北京医学会骨科专业委员会关节外科学组
中华医学会骨科学分会关节外科学组,北京医学会骨科专业委员会关节外科学组
1 本指南制订背景
全膝关节置换术(total knee arthroplasty,TKA)是目前治疗终末期膝关节疾病的主要方法。Feng 等[1]研究显示,我国TKA病例数迅速增长,从2011年的53 880例增加到2019年的374 833例,增长了 5.9倍。然而,TKA术后常伴有中度至重度疼痛[2- 4],严重影响患者术后康复、患者满意度和总体疗效[5- 7]。多模式镇痛被认为是缓解TKA术后疼痛的理想方案[8- 10]。充分的围手术期镇痛不仅可以减少疼痛及阿片类药物的使用,进而减少阿片类药物相关不良事件,还可以缩短住院时间、减少医疗费用、促进患者康复,并改善患者满意度[9,11- 12]。因此,临床医师有必要充分了解TKA围手术期的疼痛管理方案,以改善患者的治疗效果。
目前存在的挑战是:①国内尚无 TKA围手术期疼痛管理的指南,在《中国髋、膝关节置换术加速康复——围术期管理策略专家共识》[13]及《中国骨科手术加速康复围手术期疼痛管理指南》[14]中部分提及优化镇痛方案,但并未严格按照美国国家科学院医学研究所(Institute of Medicine,IOM)的标准来制订,未通过系统评价的方法来形成证据,循证医学证据级别不高;②国外指南[2,15]同样将 TKA围手术期镇痛作为加速康复管理的一部分,但对于镇痛措施细节推荐不够[16],影响临床应用;③在TKA加速康复外科(enhanced recovery after surgery,ERAS)背景下[15],疼痛管理既是其核心环节,又与其他措施关系紧密,疼痛管理的最高目标从单纯镇痛转变为患者整体的加速康复,减少阿片类药物的使用也成为疼痛管理的重要目标,疼痛管理要求考虑其对于整个ERAS体系的影响;④在国内中医学领域,中医药镇痛是临床实践的一部分,需要评估其价值;⑤多模式镇痛措施复杂,对于技术细节优化的研究层出不穷,临床应用的措施(含药物)也愈来愈多。但是,临床上,尤其是国内基层医院,尚缺乏规范化的简单易行的且可以推广的指南。因此,制订TKA围手术期疼痛管理指南十分重要和必要。
2 本指南推荐总则
2.1 疼痛管理目标
本指南推荐疼痛管理以减轻患者术后疼痛,加速恢复患者膝关节功能,提高患者生活质量,同时兼顾减少阿片类药物的使用,以减少药物不良反应为目标;在美国,阿片类药物通常被用来治疗TKA术后膝关节疼痛。文献报道,在创伤或矫形外科手术后,多达 20% 的患者长期使用阿片类药物[17- 18]。目前国内患者TKA围手术期应用阿片类药物的数据缺乏,但长期使用阿片类药物可能对个人和社会产生重大影响[19]。基于健康宣教、多模式镇痛和心理干预等措施有望减少围手术期吗啡的使用[20]。
2.2 适用人群
接受初次TKA手术的患者。
2.3 应用时限
TKA围手术期。围手术期用于描述任何外科手术的术前、术中和术后阶段。依据 Zhuang 等[21]的研究,本指南将围手术期定义为从最初的术前评估至术后6周。
2.4 干预措施
包括非药物(如患者教育、心理干预、冰敷)、药物及辅助镇痛措施(由外科、麻醉科、疼痛科医师实施),不包括为处理疼痛而实施的外科手术。
2.5 围手术期疼痛的诊断与量化
疼痛依据患者主诉诊断。疼痛程度会影响干预措施的选择,对其进行量化将直接影响疼痛的管理决策。本指南推荐选择视觉模拟评分(visual analogue scale,VAS)对骨关节疼痛进行评分与分级,1~3分为轻度疼痛,4~6分为中度疼痛,7~10分为重度疼痛[22]。
2.6 多模式镇痛的定义及理念
多模式镇痛包括非药物(如患者教育、心理干预、冰敷)与药物措施,后者是几种药物和给药途径的结合,包括预防镇痛、周围神经阻滞(regional nerve block,RNB)、患者自控镇痛(patient controlled analgesia,PCA)、关节周围混合药物注射(periarti-cular multimodal drug injection,PMI)镇痛及口服/静脉使用非甾体抗炎药(nonsteroidal anti-inflammatory drug,NSAID)和阿片类药物[12]。
2.7 疼痛评估指标及最小临床有效值(minimal clinically important differences,MCID)
评估TKA围手术期疼痛管理的有效性指标主要包括VAS评分、阿片类药物用量、恶心或呕吐等不良反应、膝关节活动度(range of motion,ROM)、患者膝关节功能评分及满意度评分。基于系统综述,本指南设定的术后 0~24 h内阿片类药物消耗绝对减少量的MCID 中位数为10 mg静注注射吗啡当量(QR为6.8~14.5 mg),阿片类药物消耗相对减少量为40%(QR为30%~50%)。VAS 评分(0~100 mm计数)的 MCID绝对值为静息状态减少 15 mm(QR为 10~20 mm)和运动状态减少 18 mm(QR为 10~20 mm),相对值减少30%(QR为20%~30%)[23]。
2.8 临床问题、推荐意见、证据概述及推荐说明
本指南采用推荐意见的分级评估、制定及评价(Grading of Recommendations Assessment,Development,and Evaluation,GRADE)方法对证据体的证据质量和推荐意见的推荐强度进行分级。GRADE证据质量和推荐强度分级与定义见表1和表2。采用德尔菲法进行4轮函询后形成专家意见,专家对推荐意见可根据赞同程度选择“同意”“不确定”或“不同意”。

表1 本指南中涉及的证据质量分级与定义

表2 本指南中涉及的推荐强度分级与定义
3 TKA围手术期疼痛管理措施
临床问题1:对患者开展术前健康教育,包括疼痛相关知识与患者自我管理,是否可以减轻患者TKA术后疼痛?
推荐意见:现阶段无明确证据表明术前宣教可以减轻TKA术后疼痛,但可以缓解患者围手术期焦虑,改善膝关节功能,故推荐术前开展健康教育以助力TKA术后康复。(证据等级:C;推荐强度:1)(专家意见:同意100%,不确定0,不同意0)
原理:术前开展健康教育可能有利于缓解患者焦虑及术后疼痛。有报道显示系统性的术前教育对术后疼痛、焦虑和康复有益[24],也有报道显示术前焦虑与术后疼痛相关[25],因而开展术前健康教育从理论上来讲可以缓解术前患者焦虑和改善术后疼痛。
证据总结:2017 年的一篇系统综述/荟萃分析发现,开展术前健康教育项目后,患者TKA术后疼痛无显著减轻,术后膝关节功能显著改善,术后股四头肌力显著增强,术后腘绳肌力无显著差异,术后住院时间明显缩短[26]。2020年的一篇系统综述对TKA术前健康教育的影响进行了分析,提出术前咨询和宣教的推荐强度为1,但证据等级为C,并未对TKA术后疼痛单独进行分析[15]。术前健康教育是患者知情同意权和医学人道主义精神的体现,而疼痛知识及自我管理方法的讲解是术前健康教育不可缺少的一部分。术前健康教育可以缓解患者围手术期焦虑,而焦虑又与疼痛有密切关系[25],只是由于目前TKA镇痛前瞻性对照研究中对于观测焦虑设置的亚组数量偏少并且不甚完善,故没有显现出由缓解焦虑而减轻疼痛的显著作用。总的来说,术前健康教育是全世界各级医院实践中的产物和人文关怀的体现,总体上取得了良好成效,因此推荐术前开展健康教育以期减轻TKA术后疼痛。
临床问题2:术前预防镇痛加入TKA多模式镇痛方案的有效性与安全性?
推荐意见:建议术前使用预防镇痛,可以减轻TKA术后疼痛,目前对于药物的构成尚无标准方案。(证据等级:C;推荐强度:2)(专家意见:同意 100%,不确定0,不同意0)
原理:预防镇痛是指在术前给予一种或几种药物干预,降低外周和中枢敏化,从而降低伤害性刺激引起的痛觉过敏和痛觉异常,达到减少术后镇痛药物使用的一种镇痛方法[27]。在TKA术前进行预防镇痛,目的是降低由手术切口或手术操作引起的外周和中枢神经系统的疼痛敏感性[28],可改善患者术后疼痛反应,降低术后慢性神经性疼痛的风险[27]。
证据总结:2021年的一篇系统综述纳入了6项前瞻性临床研究,结果显示术后24 h与术后72 h的VAS评分差异有统计学意义;与术前相比,实验组术后 24 h屈曲VAS评分差异有统计学意义,而术后 72 h 屈曲VAS评分差异则无统计学意义。组间阿片类药物用量差异有统计学意义,但手术时间或术后恶心/呕吐发生率差异均无统计学意义[29];证据等级为C。
预防镇痛的药物构成尚无标准方案,文献报道常用的药物为:①环氧合酶-2(cyclooxygenase-2,COX- 2)抑制剂(选择性 NSAID)。2013年一项荟萃分析包含8组随机对照研究(randomized controlled trial,RCT),纳入 571 例接受TKA的患者,围手术期预防镇痛使用COX- 2抑制剂,结果显示,围手术期使用 COX- 2 抑制剂可以有效降低 VAS 评分,获得更大的膝关节ROM,减少术后3 d内阿片类药物用量及阿片类药物不良反应(瘙痒),以及术后恶心呕吐的发生[30]。②加巴喷丁类药物。围手术期使用这些药物治疗急性疼痛是超适应证的[31]。Buvanendran等[32]的研究表明,9 例接受TKA的患者术前一次性给予 150 mg 普瑞巴林,在给药 2 h 内迅速达到脑脊液峰值浓度,相当于抗惊厥药物水平。一项 RCT 结果表明,普瑞巴林治疗组在术后急性期消耗更少的阿片类药物,并在术后30 d获得更大的膝关节ROM,术后6个月的慢性神经性疼痛显著减少[33]。常规使用此类药物仍存在争议,证据将在临床问题13详细讨论。③对乙酰氨基酚(acetaminophen,AP):静脉注射 AP 效果与静脉注射吗啡当量10 mg相同,且能避免阿片类药物相关不良反应[34]。它在术前镇痛同样作用明显,给药后 30 min 内迅速达到脑脊液峰值浓度,而且不受口服药物吸收延迟的影响[35]。但是目前在国内尚无注射用 AP 剂型;口服 AP 需关注肝功能损害。证据将在临床问题11详细讨论。
临床问题3:术前实施预康复是否可以减轻TKA术后疼痛?
推荐意见:现阶段无明确证据表明术前预康复可以减轻TKA术后疼痛,但其可能有助于术后膝关节功能的恢复,故建议对患者给予预康复以利于TKA术后加速康复。(证据等级:C;推荐强度:2)(专家意见:同意80%,不确定17%,不同意3%)。
原理:预康复指在TKA术前进行的一系列康复训练或治疗手段,其目的是加速术后康复过程,改善关节功能,减轻术后疼痛等[36]。有观点提出,预康复可以轻度缓解患者术后疼痛,增强下肢肌力,提高TKA术后膝关节 ROM 及功能[37]。但也有研究持相反意见[38]。
证据总结:2022年的一篇荟萃分析结果显示,在疼痛方面,预康复组与对照组的 VAS 评分差异并无统计学意义。术后膝关节总的ROM差异无统计学意义,术后6周预康复组膝关节屈曲功能明显优于对照组,但术后 12 周及术后 1 年后两组差异均无统计学意义。术后12周6 min行走测试也未发现两组差异有统计学意义。术后6周预康复组膝关节损伤与骨关节炎评分(knee injury and osteoarthritis outcome score,KOOS)均明显优于对照组;但术后6周、术后12周、术后1年两组KOOS及西大略湖和麦克马斯特大学骨关节炎指数(Western Ontario and McMaster Universities osteoarthritis index,WOMAC)差异均无统计学意义。研究也发现预康复可以显著缩短患者的住院时间[39]。现阶段,预康复的方式包括关节屈曲伸展活动、肌肉力量训练、平衡能力训练、神经肌肉电刺激等[40]。2020年的系统综述结果提示术前伸膝训练并不能显著提高术后的伸肌力量[41]。2021年的系统综述发现术前感觉运动训练对术后的疼痛没有缓解作用,且并没有明显增加 ROM,但对患者术后的功能表现有一定的提升作用[42]。因大部分预康复训练操作简单、不额外增加患者经济负担,本指南建议通过门诊或电话方式指导患者预康复训练,包括关节屈曲伸展活动及肌肉力量训练(如床上滑移屈膝动作、坐位屈膝动作、伸膝压腿动作、直腿抬高训练、坐位伸膝训练、支撑辅助下的提踵训练等),时间为 4~6 周,以助于加速康复[43- 44]。
临床问题4:TKA术中减少应用止血带时间是否减轻术后疼痛?
推荐意见:推荐尽量减少TKA术中应用止血带的时间,以减少患者术后疼痛,降低其他不良事件发生的风险。(证据等级:B;推荐强度:1)(专家意见:同意90%,不确定10%,不同意0)
原理:止血带是TKA术中常用的辅助装置,原理是在大腿近端利用压力限制远端手术部位的血液供应,达到减少手术区域出血的目的[45]。有观点认为,术中应用止血带可以提供更清晰的手术视野,同时利于骨与假体之间的骨水泥黏合[46]。但有作者认为其可能增加术后下肢疼痛甚至血栓形成的风险,并且可能影响手术切口的愈合[47]。《中国髋、膝关节置换术加速康复——围术期管理策略专家共识》[13]提出:术中不用止血带可以减轻TKA术后大腿肌肉疼痛,加快膝关节功能恢复。但也有研究认为,止血带的使用并不增加TKA术后疼痛程度及相关不良事件的发生[48]。
证据总结:2021年一项系统综述结果显示,在疼痛方面,止血带组术后第1天的疼痛评分较对照组增加了 1.25分,术后 3 d内的平均疼痛评分较对照组增加0.78分,但仍在最小临床差异水平之下,说明患者在临床中可能体会不到这种差异;在手术时间方面,使用止血带平均减少了3.7 min,但平均住院日延长了0.34 d;在并发症方面,使用止血带发生严重不良事件(包括下肢深静脉血栓形成、肺栓塞、感染、再次手术等)的危险更高[相对危险度(risk ratio,RR)=1.73,95%置信区间(95% confidence interval,95% CI):1.10~2.73][49]。2022年的一项RCT发现,止血带可以节省机器人辅助TKA的手术时间,但并不能减少出血量;同时,非止血带组在术后能更早地完成直腿抬高动作,并且平均住院日更短[50]。2019年的一项系统综述对比了部分时间使用止血带及不使用止血带两种情况,结果提示二者术后疼痛评分差异无统计学意义[51]。部分时间使用止血带理论上有助于降低假体松动的风险,然而尚无长期随访结果[52]。
综合考虑使用止血带的利弊,推荐在常规TKA或机器人辅助TKA术中尽量减少使用止血带时间,以减轻术后疼痛及减少不良事件,缩短住院时间,促进功能恢复,达到ERAS的目的。但是对于特殊复杂的初次TKA,考虑到止血带可以提供更清晰的手术视野,利于手术进行,建议按需使用。
临床问题5:术中常规行PMI镇痛的安全性及有效性?
推荐意见:推荐术中常规使用 PMI 以减轻TKA术后疼痛及减少阿片类药物的使用。(证据等级:A;推荐强度:1)(专家意见:同意 100%,不确定 0,不同意0)
原理:PMI 镇痛在临床上又称“鸡尾酒”注射镇痛,原理是消除手术伤口对疼痛的刺激与传导,以达到预防和控制术后疼痛的目的[53],由于其效果肯定,不影响运动神经传导,且操作简便,镇痛效果显著,全身副作用小,已广泛应用[2]。
证据总结:2016年的一篇系统评价和荟萃分析发现,与未注射或安慰剂组相比,PMI组疼痛评分、阿片类药物用量和术后恶心呕吐发生率更低,24 h膝关节 ROM 更大,住院时间更短。PMI组在术后 24 h和48 h的 VAS 评分低于无注射组或安慰剂组,具有高度异质性。亚组分析显示,术中 PMI 而非关节腔内注射的 24 h疼痛评分低于未注射组或安慰剂组。因此,PMI对TKA术后24 h内的急性疼痛治疗有效,能够减少阿片类药物使用,降低术后恶心呕吐发生率,缩短住院时间,并且增加术后24 h膝关节ROM[54]。
一项系统评价和荟萃分析表明,PMI在TKA术后早期缓解疼痛、减少阿片类药物使用、减少恶心呕吐发生率等方面具有优势,在手术时间、伤口并发症、深静脉血栓形成发生率方面与非PMI组差异无统计学意义[55]。2022 年一项系统综述显示,术中 PMI 显著降低术后24 h内VAS评分,显著减少术后 24 h 内吗啡用量[56];证据等级为A。
但 PMI的药物配方、剂量尚未形成共识[57- 58]。配方中最基本的药物为长效局部麻醉药,但多大剂量和浓度的局部麻醉药才能产生最佳的治疗效果目前没有统一标准,并且由于个体对局部麻醉药毒性的敏感性各不相同,局部麻醉药的最大安全剂量也尚无相应标准。虽然局部麻醉药引起的全身毒性反应相对较少,但由于接受TKA的患者,特别是进行一期双侧TKA的患者,可能因高龄或合并肝、肾功能不全等疾病,应警惕大剂量使用增加局部麻醉药中毒的风险。与传统局部麻醉药相比,新型布比卡因脂质体并未体现其优势[59]。一项荟萃分析发现,与普通局部麻醉药相比,注射布比卡因脂质体在术后 24 h、48 h、72 h 并不能带来更强的镇痛效果[60]。考虑到在国内的可获得性及经济性,不建议加入混合药物配方。三项高质量研究汇总结果显示,PMI中加入酮洛酸能够减轻术后疼痛及减少阿片类药物使用[61]。阿片类药物加入配方并未减轻TKA术后疼痛及减少阿片类药物用量[62- 63],同时吗啡等阿片类药物有呼吸抑制作用,对于全身麻醉或呼吸障碍患者需慎用。本指南建议常规的 PMI配方包括长效局部麻醉药、长效糖皮质激素(证据将在临床问题6详细讨论)及 NSAID[61]。但 PMI 操作也应关注相关不良反应(如腓总神经麻痹、膝关节后方血管神经损伤)。
临床问题6:PMI药物配方中添加糖皮质激素的安全性及有效性?
推荐意见:对于无禁忌证的患者,推荐在 PMI药物配方中添加长效糖皮质激素以减轻TKA术后疼痛,并不增加围手术期并发症发生率。(证据等级:B;推荐强度:1)(专家意见:同意 91%,不确定 3%,不同意6%)
原理:PMI混合药物中加入激素能减少术后炎症反应、减轻疼痛,但同时具有增加感染的风险[55,64]。多项研究证实,添加糖皮质激素的“鸡尾酒”配方局部浸润麻醉在TKA术后疼痛控制和早期康复方面具有显著优势,且不会增加术后并发症的发生[65- 66]。相反,三项RCT显示,在“鸡尾酒”配方中应用糖皮质激素对术后早期疼痛的缓解、关节活动范围和功能评分并无显著改善[65,67- 68]。
证据总结:2021 年的一篇系统评价和荟萃分析发现,糖皮质激素组术后 48 h 内的 VAS 评分显著低于对照组,术后 24 h的膝关节 ROM 较对照组显著改善,术后24 h内吗啡用量及术后C反应蛋白水平显著降低,差异均有统计学意义。住院时间和长期美国膝关节协会评分(Knee Society score,KSS)差异均无统计学意义。在TKA患者术后并发症(如伤口感染、假体感染、血糖水平异常、髌腱断裂、下肢深静脉血栓形成等)发生率方面差异无统计学意义。亚组分析结果显示,在术后VAS评分和膝关节活动范围方面,长效激素(倍他米松)优于短效激素[69]。但应关注应用糖皮质激素相关副作用,注意避免注射入切口周围的皮肤及髌腱;同时对于患有糖尿病、类风湿关节炎等感染高风险患者,应用糖皮质激素应当慎重。
临床问题7:TKA围手术期镇痛,PMI能否获得相当于或者优于单次股神经阻滞(femoral nerve block,FNB)的临床效果?
推荐意见:FNB相比 PMI在术后镇痛效果、吗啡用量及并发症发生率方面无显著差异,前者影响术后康复,后者简便经济,建议在相同条件下优先选择PMI。(证据等级:C;推荐强度:2)(专家意见:同意94%,不确定3%,不同意3%)
原理:FNB 既往被认为是TKA术后镇痛的金标准[70],但因为其固有的运动神经阻滞及伴随的跌倒风险限制了其临床应用[71]。PMI由于其效果肯定、简单易行,而且因为不影响运动神经,在 ERAS 背景下相比FNB有潜在的优势。
证据总结:2018 年一项系统评价进行荟萃分析后发现,FNB相比PMI,术后VAS评分[术后 24 h(P=0.52)、术后 48 h(P=0.36)和术后72 h(P=0.27)]、术后吗啡用量(P=0.27)、术后ROM(P=0.45)、术后KSS评分(P=0.51)、术后并发症发生率(P=0.81)和住院时间(P=0.75)等差异均无统计学意义,提示二者镇痛效果相当[72]。所有证据等级均为C。
PMI存在的问题是药物配方及注射技术尚无统一的标准。2022年一项 RCT发现,在北欧国家,PMI的麻醉费用、材料费用都显著低于 FNB[73]。基于ERAS 要求,同时综合考虑镇痛措施卫生经济学、时间成本和技术可及性等因素,本指南建议相同条件下优先选择 PMI。另外,因担心单用 FNB 不能阻断膝关节后侧的疼痛感受器,可联合使用PMI。
临床问题8:TKA围手术期镇痛,收肌管阻滞(adductor canal block,ACB)是否优于FNB?
推荐意见:ACB 相比 FNB 在术后镇痛效果及并发症发生率方面无显著差异,但 ACB 对术后股四头肌肌力影响较小,在ERAS背景下,建议优先选择ACB,也可联合使用 PMI。(证据等级:C;推荐强度:2)(专家意见:同意100%,不确定0,不同意0)
原理:ACB 仅阻断股神经的感觉支-隐神经(根据个体解剖特征,可能还包括闭孔神经后支和股内侧肌支),具有理论上不影响股神经运动分支即股四头肌肌力的优点,但也有阻滞不完全镇痛效果欠佳的担忧。临床往往结合超声引导下腘动脉和膝关节后囊间隙(interspace between the popliteal artery and capsule of the posterior knee,iPACK)阻滞使用;多个RCT比较ACB与FNB的镇痛效果及并发症发生率,但结果并不一致[74]。尤其是在ERAS背景下,ACB是否可以降低FNB所固有的股四头肌无力的发生率和跌倒风险并不清楚[75- 76]。
证据总结:2017 年一项荟萃分析结果显示,虽然ACB组相比FNB组术后VAS评分(术后8 h、24 h、48 h)、吗啡用量等差异均无统计学意义(P均>0.05),但ACB组各时间点股四头肌肌力(术后 8 h、24 h 和 48 h)和行走能力(以术后 24 h和 48 h 的站立-行走计时试验评估)均优于FNB组[77]。2019年一项系统评价发现,ACB相比FNB术后各时间点VAS评分差异均无统计学意义,术后恶心的发生率、住院期间跌倒风险差异也均无统计学意义[78];证据等级为C。
另外,为了延长单次注射的效果,不论是 ACB,还是 FNB,均可选择留置导管持续给药。有研究提示股神经区域置管持续给药相比单次注射有更好的镇痛效果[79]。但也有研究发现,持续与单次给药镇痛效果并无明显差异[80]。无论何种给药方式,均需要仔细识别高风险患者和评估跌倒风险,另外,置管的管理也需要关注。
对于ACB是否联合使用 PMI,2021 年一项系统综述显示,在存在PMI的情况下,在ACB的基础上添加 iPACK阻滞并没有改善术后 6 h 的疼痛。然而在没有PMI的情况下,ACB联合iPACK阻滞可减少疼痛,但并未达到MCID。对于次要结果,在有PMI的情况下进行比较,ACB联合iPACK阻滞并没有改善术后疼痛、阿片类药物使用及功能恢复。相反,在没有PMI的情况下,ACB 联合iPACK阻滞减轻了术后12 h和24 h的疼痛,功能恢复也得到改善,但未减少阿片类药物的用量[81]。本指南建议优先选择单次ACB结合iPACK阻滞,可联合使用术中PMI;对术后疼痛控制不佳的患者可考虑连续的ACB。
临床问题9:TKA围手术期全身应用糖皮质激素镇痛的有效性与安全性?
推荐意见:由于TKA围手术期全身应用糖皮质激素镇痛的有效剂量及其安全性仍存在争议,故不建议将其常规纳入TKA多模式镇痛方案。(证据等级:B;推荐强度:2)(专家意见:同意 74%,不确定20%,不同意6%)
原理:糖皮质激素可以抑制体内炎症反应、减轻伤害感受,在临床上具有减轻术后疼痛、减少围手术期恶心呕吐的作用[82]。糖皮质激素的应用不仅途径繁多,而且剂量各异,在临床规范镇痛治疗的应用上存在争议[83]。
证据总结:2020 年发表的一篇系统综述结果显示,围手术期静脉应用或口服糖皮质激素(≤15 mg地塞米松或相同效量的糖皮质激素)可以明显降低术后1~3 d 的疼痛评分(包括静息及运动状态),并有效减少术后恶心呕吐的发生,但其却在最小临床差异水平之下。更大剂量的糖皮质激素(>15 mg地塞米松或相同效量的糖皮质激素)的镇痛效果更为明显,高于最小临床差异[84]。2022 年发表的另一篇系统综述单独对静脉应用地塞米松在TKA围手术期的作用进行了评估,结果提示,围手术期静脉应用地塞米松可以降低TKA术后第1天及第2天静息或运动状态下的疼痛评分,但二者均在最小临床差异水平之下[85]。2020年发表的系统综述指出,术后24 h以后再次追加糖皮质激素并不能显著降低患者的疼痛评分[84]。2022 年发表的系统综述也指出,单次使用与多次使用地塞米松并没有明显差异[85]。近期的一项前瞻性RCT结果表明,在术后第1天及第2天,单次应用 20 mg 地塞米松组的疼痛评分及炎症因子水平均明显低于两次应用10 mg地塞米松[86]。
现有研究提示全身应用糖皮质激素并不增加TKA术后早期感染、消化道出血、下肢深静脉血栓形成、伤口愈合不良风险[84]。但糖皮质激素的应用会短期增加患者术后血糖水平,且血糖的增加与糖皮质激素用量密切相关,这种影响一般会持续超过 48 h[87]。在有多种基础疾病的高风险患者群体中,糖皮质激素使用所带来的不良影响仍是临床医师的主要顾虑。尽管TKA术后感染等并发症的发生率相对较低,但由于现有的RCT样本量有限,并不能充分证实围手术期全身应用糖皮质激素是否增加感染风险,尤其是否增加远期假体周围感染的风险。
综上,围手术期全身应用糖皮质激素镇痛的有效剂量及其安全性仍存在争议,故不建议将其常规纳入TKA多模式镇痛方案。
临床问题10:TKA术后是否常规应用 NSAID镇痛?
推荐意见:对无禁忌证的患者,推荐术后常规使用 NSAID 镇痛,优先选择 COX- 2 抑制剂。(证据等级:A;推荐强度:1)(专家意见:同意100%,不确定0,不同意0)
原理:传统的非选择性 NSAID 和选择性 COX- 2抑制剂通过抑制COX- 2和前列腺素用于围手术期镇痛[16]。选择性 COX- 2抑制剂减少了对胃肠道的影响和失血风险。此外选择性COX- 2抑制剂通过减少外周前列腺素的合成来缓解炎症,并抑制外周和中枢COX- 2的表达,最终防止中枢神经系统的敏感化,从而发挥镇痛的效果[88]。
证据总结:Jiang 等[89]对 3014 例患者进行的荟萃分析显示,NSAID选择性COX- 2抑制剂相比对照组降低了术后 24 h、48 h 和 72 h 的 VAS 评分。亚组分析显示,静脉使用帕瑞昔布显著降低VAS评分;目前,国内外专家共识[13,90]推荐将 COX- 2抑制剂(塞来昔布、艾瑞昔布)加入多模式镇痛中,以减少阿片类药物的使用,同时无严重并发症。两项RCT得出结论,使用COX- 2抑制剂对比安慰剂明显改善TKA术后疼痛,并推荐其作为多模式镇痛方案的一部分[91- 92]。另外一项RCT发现,COX- 2抑制剂在TKA术前使用,能带来更好的镇痛效果和膝关节功能[93]。Schroer等[94]实施的RCT 表明,与安慰剂相比,使用 6 周的选择性 COX- 2抑制剂可以减轻疼痛和/或减少阿片类药物的使用。但没有研究评估出院后使用非选择性 NSAID 的情况。Fillingham 等[88]的系统综述结果显示,围手术期的 NSAID、出院后的选择性 COX- 2抑制剂和静脉注射的酮咯酸在术后并发症方面差异无统计学意义;围手术期 NSAID 与安慰剂相比的直接荟萃分析显示,二者任何不良事件发生率差异均无统计学意义;另外,围手术期的 NSAID 被证明具有降低发热的风险;但需要注意,要避免合并肾脏疾病的患者中不当使用 NSAID[95]。NSAID 不宜超量使用;且药物血浆蛋白结合率高,不推荐二种联用;一种效果不佳时,可考虑更换为另一种。NSAID的主要不良反应包括胃肠道、心血管、血小板功能异常和肾损伤等。在患者用药前需对其进行消化系统损伤和心血管损伤危险进行评估,再根据不同风险程度采取不同方案[96]。
临床问题11:TKA围手术期静脉注射或口服AP镇痛的有效性、可行性及安全性?
推荐意见:不建议常规将AP纳入TKA术后多模式镇痛方案。(证据等级:B;推荐强度:2)(专家意见:同意67%,不确定20%,不同意13%)
原理:AP具有解热镇痛作用但无明显抗炎作用。多数观点认为 AP通过介导一系列通路起效,包括大麻素受体激动剂、COX- 2抑制剂的同工酶、瞬时受体
电位阳离子通道激动剂等[97]。静脉注射AP与静脉注射吗啡10 mg的效果相当,且避免了阿片类药物不良反应。AP 在术前镇痛同样作用明显,国内目前主要应用口服剂型。
证据总结:一项Cochrane系统综述表明,AP单次口服给药可为约一半的术后急性疼痛患者提供有效镇痛,持续时间约 4 h,且很少出现不良反应,但是该研究以口腔科手术为主,骨科手术研究数量有限[98]。相比口服剂型,静脉注射剂型达到最大浓度的速度更快,但费用更高[99]。一项系统综述表明,对于接受TKA和全髋关节置换术(total hip arthroplasty,THA)的患者,不同研究对口服 AP 是否具有术后镇痛效果判断不一;静脉注射 AP与安慰剂对比能够明显减轻术后 24 h、48 h 疼痛,减少术后 24 h 吗啡用量;静脉注射和口服 AP 对术后疼痛程度、阿片类药物用量的影响无显著差异;静脉注射 AP、口服AP 和安慰剂在术后并发症发生率方面无显著差异。但是该综述将TKA和 THA患者混合比较,且未详细列出定量结果[100]。2018年发表的一篇系统综述结果显示,静脉注射AP组相比安慰剂组,阿片类药物用量明显下降,而术后第 1、2、3天疼痛评分、术后第 1 天阿片类药物用量及术后住院时间则未发现明显差异[101];证据等级为B。2020年的一篇系统综述结果显示,AP静脉注射和口服用药在术后24 h、48 h疼痛评分,术后24 h阿片类药物用量方面均无显著差异,仅术后住院时间缩短[102];证据等级为D。一项针对103万例TKA或THA患者的大型回顾性研究不支持静脉注射AP制剂减少阿片类药物使用量[103]。另一项包含190 691例TKA患者的大型回顾性研究表明,静脉注射AP患者的30 d再入院率低于口服AP组(0.04%比0.14%)[104]。值得注意的是,不当应用AP可能会导致严重肝损伤,一些罕见的皮肤不良反应(如重症多形红斑、中毒性表皮坏死松解症)也可能与AP有关,因此需要严格控制药物用量。指南建议,口服AP最大剂量为4 g/d[105]。
综上,AP可以作为TKA围手术期多模式镇痛方案的一部分,静脉注射 AP 与口服 AP 相比对疼痛评分无明显改善,对术后阿片类药物用量的减少效果也不明显,有可能会缩短患者术后住院时间。其安全性值得警惕,且现有证据的质量等级低,且当前静脉注射 AP 剂型在国内大部分医院无法获得。在可静脉注射其他种类NSAID的情况下,不建议常规将AP纳入多模式镇痛方案。
临床问题12:TKA术后是否常规使用PCA?
推荐意见:不建议TKA术后常规使用静脉PCA,对于无条件开展区域阻滞镇痛或不适宜局部浸润镇痛的病例,仍可选用静脉PCA。(证据等级:B;推荐强度:2)(专家意见:同意94%,不确定3%,不同意3%)
原理:静脉PCA通常指采用PCA泵为术后患者提供静脉注射阿片类镇痛药物,患者可根据自身需要控制药物的使用时机,可同时通过PCA泵持续给予背景药量药物,是TKA术后镇痛的一种经典方式[99,106]。2015 年Cochrane系统综述表明,PCA 相比其他常规给药方式在控制外科术后疼痛方面效果更好,无明显的安全性问题[107]。但是该研究中骨科手术研究数量很少,且证据质量有限(证据等级为B或C)。近年来,由于恶心、呕吐等不良反应,以及影响术后康复锻炼,在其他多模式镇痛方法有效情况下,是否常规应用静脉PCA存在争议。
证据总结:2014 年一篇Cochrane系统综述结果显示,FNB组在术后24 h静息痛、24 h运动痛、24 h阿片类药物用量、术后恶心呕吐发生率、术后膝关节ROM及患者满意度方面均优于PCA组,且差异有统计学意义[70]。2021年发表的网状荟萃分析结果显示,单纯PCA患者术后尿潴留风险升高[比值比(odd ratio,OR)=1.08,95% CI:1.08~5.16][75]。综上,静脉PCA可将TKA术后静息痛控制在轻度至中度,但对运动痛控制效果有限,且恶心、呕吐等并发症发生率高。因而推荐采用ACB等区域阻滞镇痛方式联合PMI,以逐步取代静脉 PCA。但是 RNB 的实施需要超声辅助和具备一定经验的麻醉医师。我国各级医院发展不均衡,因此建议仅在暂不具备开展 RNB 条件的医疗机构,或对于不能使用 PMI镇痛的患者,仍可将PCA作为TKA术后镇痛的选择,但需要合理计算药物用量,避免阿片类药物不良反应。
临床问题13:TKA术后使用加巴喷丁类药物镇痛的有效性与安全性?
推荐意见:不推荐将加巴喷丁类药物(如加巴喷丁、普瑞巴林等)常规纳入TKA术后多模式镇痛方案。(证据等级:C;推荐强度:1)(专家意见:同意94%,不确定6%,不同意0)
原理:加巴喷丁类药物(如加巴喷丁、普瑞巴林等)作为TKA围手术期镇痛的辅助用药,最初是为了应对阿片类药物过度使用而导致的成瘾等副作用。作为辅助用药,用于治疗神经病理性疼痛,通过抑制中枢神经敏感性以达到镇痛的作用[33,108],并减少阿片类药物的用量。但同时这类药物有一定的致抑郁作用。
证据总结:2016 年一项系统评价及荟萃分析显示,TKA术后 12 h、24 h 及 48 h 吗啡药物用量明显下降[109]。但同一研究团队 Kang 等[110]在 2020 年进行的系统综述及荟萃分析,将受试者人群扩大到髋/膝关节置换患者,结果显示术后24 h(P=0.87)、术后48 h(P=0.15)、术后72 h(P=0.85)的疼痛评分加巴喷丁组与对照组无显著区别,且术后48 h后的累积吗啡用量也无显著区别;证据等级为C。2020年一项系统评价及荟萃分析结果显示,术后早期(至出院前)普瑞巴林可降低术后阿片类药物用量及减轻术后疼痛,但均未达MCID。出院后,加巴喷丁既不减轻疼痛也不降低阿片类药物用量,但普瑞巴林可同时减轻疼痛及阿片类药物用量(但未达 MCID)[111]。2018 年Hah等[112]的RCT显示,加巴喷丁并不影响术后(不局限于TKA)疼痛的时间,但会在一定程度上降低对阿片类药物的使用需求;不良事件无显著差异(安慰剂组20.8%;加巴喷丁组 25.0%)。综上,TKA患者使用加巴喷丁类药物,虽然较安慰剂有一定的间接镇痛作用,但作用效果较弱,现有证据异质性较大,且并发症如恶心、抑郁等均有发生,故对接受TKA的患者不推荐常规使用加巴喷丁类药物辅助镇痛。
临床问题14:TKA术后是否常规使用阿片类药物镇痛及补救镇痛是否推荐阿片类药物?
推荐意见:不推荐TKA术后常规使用阿片类药物镇痛,在补救镇痛情况下可使用阿片类药物。(无证据等级;推荐强度为专家建议)(专家意见:同意90%,不确定0,不同意10%)
原理:阿片类药物通过外周和中枢阿片类受体结合发挥镇痛作用。ERAS应用于TKA,强调减少术后阿片类药物使用,这是出于对其副作用的担忧,如嗜睡、呼吸抑制、恶心呕吐、瘙痒、尿潴留及成瘾的潜在风险[19]。阿片类药物的副作用将延缓患者术后康复进展。国外指南和国内专家共识[2,16]均不推荐常规经PCA静脉使用阿片类药物进行术后镇痛。在患者出现术后爆发性疼痛的情况下,补救镇痛可使用阿片类药物。
证据总结:大量研究显示术后常规经PCA静脉输注阿片类药物并未改善术后疼痛[113- 115],并且会增加患者术后恶心呕吐等不良反应;同时需警惕呼吸抑制等并发症。但这些研究的循证医学等级非常低,阿片类药物在TKA术后常规应用的临床证据尚缺乏。2020 年一项系统综述结果显示,术后常规使用阿片类药物,在术后出现爆发性疼痛时消耗的阿片类药物更少;但在恶心呕吐、呼吸抑制、头痛等不良反应方面两组无明显差异[116]。但是,此研究并未区分单独TKA术后使用阿片类药物的结果。一项 2019年的高质量 RCT 对比两组 THA/TKA术后常规处方不同剂量羟考酮患者,结果显示,术后 30 d两组患者疼痛评分无显著差异,术后6周两组患者临床结果也无显著差异。提示更多剂量的阿片类药物并不必要[117]。2022 年一项 RCT 发现,术前预防镇痛使用阿片类药物并无获益[118]。Trasolini 等[19]认为需要进一步优化镇痛方案以减少阿片类药物的应用,只有当其他所有镇痛途径都无效之后,才可使用阿片类药物治疗术后疼痛。
临床科室已经将阿片类药物广泛应用于TKA术后补救镇痛,并取得良好的疼痛缓解效果。其中,较为常用的补救镇痛阿片类药物包括吗啡、氢吗啡酮、盐酸吗啡、盐酸哌替啶、羟考酮等。目前主张单次给药,常用剂量为吗啡 2 mg[119]、盐酸吗啡 10 mg[120]、盐酸哌替啶50 mg[121]。为避免不良反应,不建议哌替啶多次给药。
临床问题15:TKA术后使用椎管内置管镇痛的有效性与安全性?
推荐意见:不建议将椎管内置管镇痛常规纳入TKA术后多模式镇痛方案。(证据等级:B;推荐强度:2)(专家意见:同意88%,不确定6%,不同意6%)
原理:椎管内麻醉若在术后使用椎管内置管镇痛,与全身麻醉相比有持续镇痛的作用;阿片类药物和局部麻醉药均可以注入到硬膜外间隙,以发挥镇痛作用。多个RCT显示这种方法在TKA术后早期有较好的疼痛控制,减少阿片类药物用量[122- 123]。但阿片类药物硬膜外给药常引起皮肤瘙痒症,而且吗啡还可引起迟发性呼吸抑制,因而具有较大风险[124]。且TKA术后早期需预防抗凝,将会增加椎管内留置管周围出血风险,直接影响患者安全及康复速度。随着多模式镇痛的不断发展,如 PMI[61]与 ACB[81]等方式,越来越不依赖于椎管内麻醉后的留置管镇痛。
证据总结:2018 年有 RCT 报道椎管内镇痛对于TKA术后早期疼痛有减轻作用,减少早期吗啡类药物的使用[122]。《中国髋、膝关节置换加速康复——围术期管理策略专家共识》[13]提出,麻醉方式并不直接影响TKA术后早期患者运动功能和并发症发生率。2003年的 Cochrane 系统综述结果显示,术后早期静息痛椎管内镇痛组较对照组显著降低。术后晚期静息痛、术后早期运动痛减轻[6]。综上,相对于全身麻醉,椎管内置管镇痛可以减轻术后早期静息痛及运动痛,但对术后晚期,即术后 18 h后的疼痛程度影响不大。2018 年一项系统综述对比椎管内置管镇痛与 PMI 镇痛,结果显示,术后 12 h、24 h 静息 VAS 评分,术后 24 h、48 h及72 h运动VAS评分差异均无统计学意义(P>0.05);PMI 组术后 24 h、48 h 膝关节 ROM 更优(P<0.05),同时术后恶心呕吐也更少[125]。考虑到药物预防抗凝治疗所致的潜在出血风险,并限制了患者的早期活动,故不建议常规将椎管内置管镇痛纳入多模式镇痛方案。建议仅在暂不具备开展区域阻滞镇痛条件的医疗机构,或对于不能使用 PMI镇痛的病例,仍可将其作为TKA术后镇痛的选择。
临床问题16:中医耳贴镇痛是否可以减轻TKA术后早期疼痛?
推荐意见:建议仅在有条件开展耳贴镇痛的机构,术后辅助使用耳穴贴以减轻TKA术后早期疼痛。(证据等级:D;推荐强度:2)(专家意见:同意77%,不确定23%,不同意0)
原理:耳穴贴是我国传统医学手段,越来越多的循证医学工作证实其有一定辅助镇痛疗效[126- 127]。目前世界范围内对耳穴疗法逐渐有了一定认识。其主要机制是通过刺激耳部特定穴位,刺激痛觉感受器释放内啡肽、脑啡肽等物质,提高痛阈,减轻疼痛程度[126,128- 129]。
证据总结:2018年的一篇系统综述结果显示,辅助耳贴镇痛能降低术后6 h、12 h、24 h疼痛评分(低于MCID),术后48 h及72 h疼痛评分无显著差异[128]。综上,TKA患者应用耳穴贴辅助围手术期镇痛,可以减轻术后早期(24 h内)的疼痛。但由于不同研究的耳贴穴位、按压时间、频次等均不一致,无法给出标准化操作指导,且研究对象基本上全是华人,有出现人群偏倚的可能,建议仅在有条件开展的机构对进行TKA的患者辅助使用耳穴贴镇痛以减轻术后早期疼痛。
临床问题17:针灸镇痛减轻TKA术后早期疼痛的有效性与安全性?
推荐意见:建议仅在有条件开展针灸镇痛的机构,术后辅助使用针灸/电针灸以减轻TKA术后早期疼痛。(证据等级:D;推荐强度:2)(专家意见:同意83%,不确定13%;不同意4%)
原理:针灸是我国传统医学技术的瑰宝,目前世界范围内对电针灸即针灸配合电刺激手段的认可度较高,用于治疗急慢性疼痛。其主要机制是电针灸通过刺激外周-中枢神经产生一系列生物活性化学物质,下调疼痛信号传导,调节神经-免疫-内分泌系统进而产生镇痛、抗炎的作用[130]。
证据总结:2021年的3篇系统综述结果显示,进行TKA的患者应用电针灸辅助围手术期镇痛,可以减轻术后3~14 d的疼痛,不增加恶心呕吐的发生[131- 133];证据等级为D。但由于不同研究的针灸穴位、时间、频率等均不一致,无法给出标准化操作指导,且研究对象基本上全是华人,有出现人群偏倚的可能,故仅建议在有开展条件且经验丰富的机构,对进行TKA的患者辅助使用电针灸镇痛治疗以减轻疼痛。实施过程中需关注医源性感染风险。
临床问题18:围手术期改善患者睡眠是否可以减轻TKA术后疼痛?
推荐意见:推荐在围手术期改善患者睡眠以减轻TKA术后早期疼痛。(证据等级:B;推荐强度:1)(专家意见:同意96%,不确定4%,不同意0)
原理:接受TKA的患者术前多伴有睡眠障碍。有研究显示81%的接受TKA的患者术后会经历夜间痛[134]。术后的功能康复与睡眠的质量或时长呈正相关[135- 136]。
证据总结:《中国髋、膝关节置换术加速康复——围术期疼痛与睡眠管理专家共识》[90]提出:在优化镇痛方案时应评估患者围手术期的睡眠障碍、同时进行必要的催眠及抗焦虑治疗。2021年的一篇系统综述结果,显示睡眠改善组相比对照组在术后第1天、第3天的静息状态及运动状态疼痛程度,以及恶心呕吐的发生率均有降低[137]。故推荐对拟接受TKA手术的患者要重视并积极改善其睡眠状态。目前常用于改善TKA患者围手术期睡眠的药物有艾司唑仑、唑吡坦、佐匹克隆、褪黑素等。同时需关注患者使用后的跌倒风险。
临床问题19:TKA术后应用冷疗镇痛的有效性与安全性?
推荐意见:建议在有条件开展冷疗的机构,在TKA术后对术侧膝关节应用冷疗以减轻术后疼痛。(证据等级:B;推荐强度:2)(专家意见:同意96%,不确定4%,不同意0)
原理:冷疗是一种简单经济的物理治疗手段,通过在皮肤外围使用冰袋或冷水等手段降低皮肤温度,有效减少创伤局部的炎症反应 、水肿和失血[138- 139]。有研究指出,冷疗能够在减少局部炎症递质释放的同时,减慢神经信号的传导,从而减轻患者疼痛,但其有效性和安全性仍然存在争议[140]。
证据总结:2020年的一篇系统性综述显示,应用冷疗组术后1周内的疼痛评分较对照组减少0.83分,术后第2周的疼痛评分较对照组减少0.63分,术后阿片类药物用量较对照组减少(P=0.92)[141]。2021年的一篇 RCT结果显示,无论静息或行走状态下,冷疗组术后1周内的疼痛数字评价量表(nume-ric rating scale,NRS)评分较对照组显著降低,冷疗组患者的阿片类药物使用比例和用量也较对照组显著减少(P<0.001)。在术后第2周、第6周两组间的 NRS 评分无显著差异,冷疗组患者 KOOS量表中的疼痛评分显著低于对照组,但差异低于MCID[142]。冷疗的副作用也值得关注。有研究显示,2例接受TKA的患者在术后长时间使用冷冻疗法后出现髌骨前方皮肤坏死[143]。此类并发症可以通过避免皮肤直接接触冷疗设备、限制使用时间进行预防。现有临床冷疗设备及生产公司较多,各医院购置设备存在多样性,基于设备操作手册及已发表的临床研究,建议在TKA术后 3 h 内开始应用,每应用2 h间隔1 h后继续,每日完成4次,患者出院后改为每持续应用 1 h后间隔 30 min进行,每日完成 4 次至术后 2 周。但应注意由于不同公司冷疗设备设计理念和参数存在差异。
综上,建议将冷疗用于减轻TKA术后疼痛,疗程可适当延长至术后2周,但应注意避免皮肤直接接触冷疗设备和长时间使用。
临床问题20:TKA术后应用神经肌肉电刺激(neuromuscular electrical stimulation,NMES)镇痛的有效性与安全性?
推荐意见:建议在有条件开展NMES的机构,在术后4~6周内当其他治疗不能获得满意镇痛效果时,可辅助使用NMES以减轻患肢疼痛。(证据等级:B;推荐强度:2)(专家意见:同意78%,不确定18%,不同意4%)
原理:NMES作为一种促进四肢创伤和手术患者术后康复的物理治疗技术,能够将电流传递到神经肌肉接头和周围的神经纤维,通过引起强直性肌肉收缩的方式,恢复和改善术后患肢的肌肉力量、减轻疼痛并促进功能恢复[144- 145]。它在增强股四头肌肌力和功能的效果已得到认可,但在减轻TKA术后患者疼痛方面的有效性仍然存在争议。
证据总结:2021年一篇RCT结果显示,在静息状态下,围手术期NMES组患者术后第3周、第 6 周的疼痛评分较对照组无明显降低。尽管在术后第12周NMES组疼痛评分较对照组减少0.5分,两组患者间的疼痛评分差异无统计学意义(P=0.381)。NMES组患者基于KOOS量表的疼痛评分在术后第3周较对照组降低2.46分,但差异无统计学意义(P=0.773)。研究未对术后阿片类药物使用情况进行评估[146]。2021 年的一篇系统性综述结果显示,NMES 组在术后1个月内的疼痛评分较对照组减少0.47分,术后1~2个月的疼痛评分较对照组减少0.62分,术后3~6个月的疼痛评分较对照组减少0.44分,术后6个月以上的疼痛评分较对照组减少 0.03 分,但以上两组间疼痛评分差异均无统计学意义[147]。结合指南总则对TKA围手术期时间范围的限定(术后 6 周),建议在有条件开展NMES的机构,在TKA术后 4~6周,其他镇痛方式不能获得满意镇痛效果时,将其作为镇痛的一种物理治疗方式供选择。由于不同设备的差异化,NMES 的最佳电流大小、频率等参数设置无统一方案,建议以略微引起患者不适但可耐受的刺激强度为佳,不建议对带有心脏起搏器的TKA患者应用NMES疗法[148]。
4 本指南的制订过程与方法
本指南严格遵循 IOM 最新指南定义,同时参考世界卫生组织(World Health Organization,WHO)和国际指南联盟(Guidelines International Network,GIN)对高质量指南的要求,并符合指南研究与评价工 具(Appraisal of Guidelines for Research and Evaluation Ⅱ,AGREE Ⅱ)的六大领域。本指南按照加拿大医学会提出的指南制订清单2.0版和国际实践指南报告规范(Reporting Items for Practice Guidelines in Healthcare,RIGHT)制作了指南计划书和正式指南文件,并遵循《中国制订/修订临床诊疗指南的指导原则(2022版)》[149]。
4.1 指南制订机构
本指南由北京协和医院骨科发起,北京医学会骨科专业委员会关节外科学组和中华医学会骨科学分会关节外科学组批准制定该指南,北京协和医院流行病学教研室、兰州大学GRADE中国中心给予方法学支持。
4.2 指南注册
本指南已在国际实践指南注册平台(Global Practice Guidelines Registry Platform)进行注册(注册号:IPGRP- 2021CN405)。
4.3 指南项目组构成
指南项目组由指南指导委员会、指南共识专家组、指南制订工作组和指南外审组构成。
4.3.1 指南指导委员会
指南指导委员会的职责是:①确定指南范围;②组建指南共识专家组、指南制订工作组和指南外审组;③组织指南相关会议;④批准问题和结局指标排序;⑤审核利益声明表;⑥监督指南制订流程;⑦批准推荐意见和指南发布。
4.3.2 指南共识专家组
在考虑了地域代表性和性别因素的基础上,指南共识专家组的成员主要由 25 位多学科的专家组成。指南共识专家组的职责是:①形成问题,为结局指标排序;②指导指南制订工作组完成系统评价、证据分级、患者偏好与价值观调查;③形成推荐意见;④修改指南全文初稿。
4.3.3 指南制订工作组
指南制订工作组由11位具有资质的研究人员构成,并设指南秘书处。指南制订工作组的职责是:①制作系统评价,完成证据分级,开展患者偏好与价值观调查;②完成 GRADE 分级;③采用德尔菲法开展指南会议;④撰写指南全文初稿。
4.3.4 指南外审组
指南外审组的成员由指南的利益相关者构成。他们并不直接参与指南的制订。指南推荐意见形成后,将接收他们的反馈意见,并提交指南指导委员会和指南共识专家组审定。
4.4 指南使用者及适用人群
本指南终端使用者:骨科医师、风湿科医师、麻醉/疼痛科医师、康复科医师、护理人员等。指南适用人群:接受初次TKA手术的患者。
4.5 利益冲突与基金资助
指南指导委员会、指南共识专家组和指南制订工作组成员均要求填写利益声明表,并对存在利益冲突的成员进行管理。所有成员的利益声明都会在最终的指南文件中以附件形式呈现。
4.6 构建问题
指南工作组通过第1轮开放性问卷调查收集了30份问卷共计34个临床问题。对收集到的临床问题进行汇总去重后,最终得到 30个临床问题。对 30个临床问题进行分类,归纳为三个方面:①TKA围手术期疼痛的定义及管理目标;②疼痛管理模式及理念;③术前、术中、术后疼痛管理的具体干预措施。接下来进行第2轮问卷调查,拟对临床问题的重要性进行评估,调研的对象为全国多个省市、不同级别医院的各级别医师。每个临床问题的重要性分为五个等级,即非常重要(5级)、比较重要(4级)、一般重要(3级)、不太重要(2级)及不确定(1级)。
经指南共识专家组达成共识,指南指导委员会审定通过,通过对每个临床问题重要性级别进行赋值和汇总,最终将三个方面共 20 个临床问题进行了重要性排序。
4.7 临床问题解构与证据检索
针对纳入的临床问题,按照 PICO 原则(人群、干预措施、对照、结局指标)进行解构。根据解构的临床问题进行证据检索:①检索数据库包括 Medline、Embase及Cochrane Library;②检索研究类型:优先检索5年内已发表的系统评价、Meta分析及随机对照研究。当最新证据不足或证据水平较低时,检索已发表5 年以上的系统评价、Meta分析、前瞻性RCT及全部队列研究、病例对照研究等;③检索时间为建库至2021年12月30日;④草拟指南正文前对最近发表的证据开展进一步检索,检索时间至2022年3月15日。
4.8 证据评价
针对系统评价和Meta分析,使用系统评价的方法学质量评价工具(assessing methodological quality of systematic reviews,AMSTAR)进行方法学质量评价;针对随机对照试验,使用 Cochrane风险偏倚评价工具进行评价;针对观察性研究,使用纽卡斯尔-渥太华量表(Newcastle-Ottawa scale,NOS)对相应类型的研究进行方法学质量评价。使用 GRADE 方法对证据体的质量进行评价并对推荐意见进行分级。
4.9 推荐意见形成
指南制订工作组按证据评价结果,初步形成31条推 荐意见。先后经过一轮面对面讨论会、一轮德尔菲法共识会及一轮终审会后,最终确定了20条推荐意见的推荐强度和推荐方向。指南推荐意见形成后,为方便指南的传阅和应用,将指南推荐意见以表格的形式精简展示(表3、表4)。
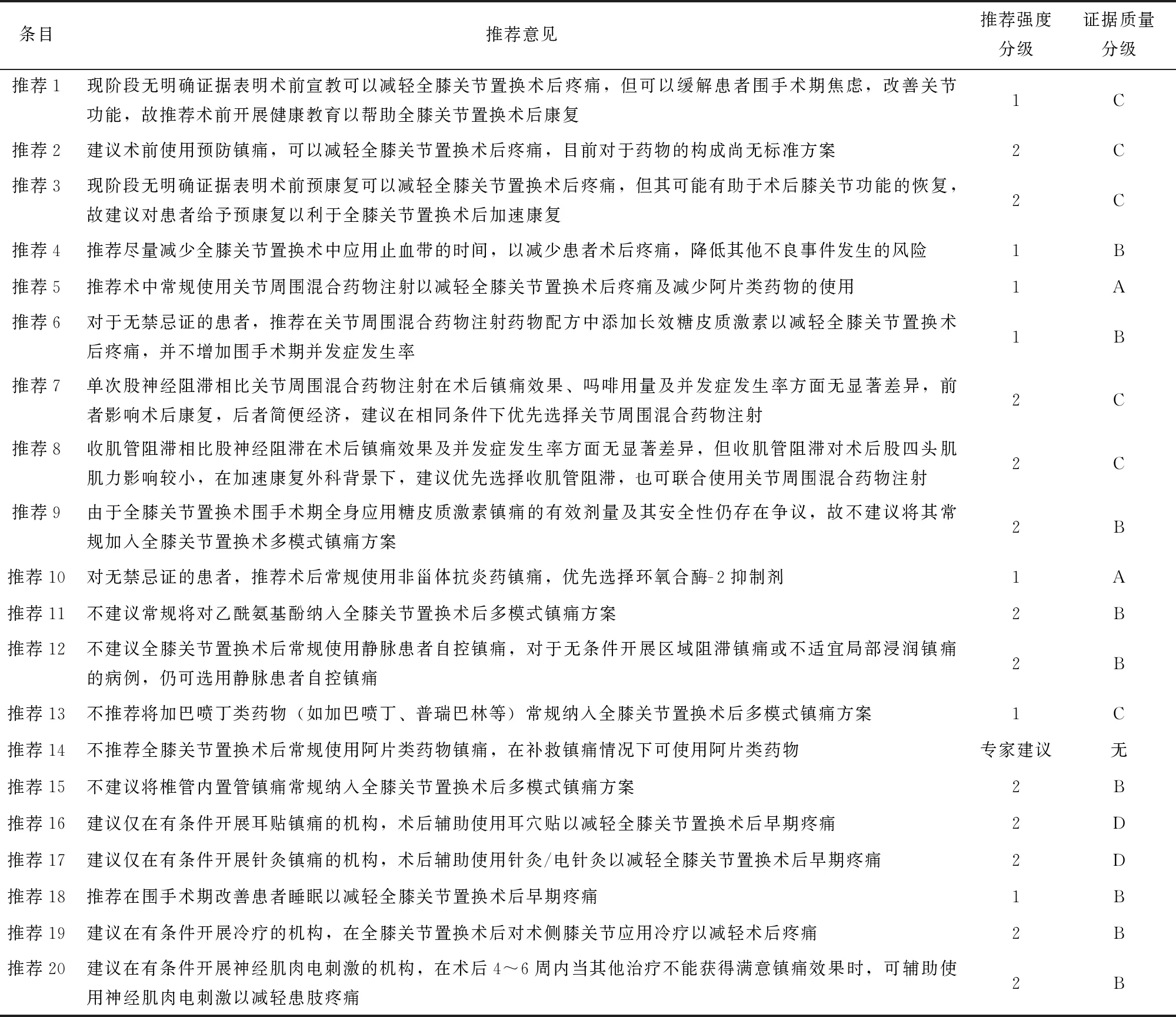
表3 《中国全膝关节置换术围手术期疼痛管理指南(2022)》推荐意见

表4 本指南干预措施推荐意见及证据质量分级
4.10 指南外审
本指南在发布前进行了同行评议,并对评审意见进行了回复和修改。
4.11 指南发布与更新
本指南全文发布在《中华骨与关节外科杂志》,并同期发布在《协和医学杂志》。指南制订小组计划每2~3 年对指南进行一次更新。
4.12 指南实施与传播
本指南出版后,将通过学术会议或学习班等方式进行传播。具体传播方式包括:①在骨科会议和TKA学习班上传播 1~2年;②指南的正文将以报纸、期刊、单行本、手册等形式出版传播;③指南将以中、英文方式宣传,并在专业网站传播;④针对指南的实施和评价,拟通过发布指南相关解读文章或视频进一步促进指南的实施。
作者贡献:翁习生、王坤正牵头制订指南框架;彭慧明负责组建指南制订工作组;指南制订工作组成员负责查阅文献、撰写指南初稿;张丽帆负责方法学指导及文献评价;其他成员对指南内容进行审校、修订和补充。
利益冲突:所有参与制订该指南的专家组成员均声明不存在利益冲突
附:《中国全膝关节置换术围手术期疼痛管理指南(2022)》项目组成员
指南指导委员组
邱贵兴 中国医学科学院 北京协和医学院 北京协和医院
裴福兴 四川大学华西医院
王坤正 西安交通大学第二附属医院
指南共识专家组(以姓氏汉语拼音排序)
蔡 谞 清华大学附属北京长庚医院
曹光磊 首都医科大学附属北京宣武医院
曹永平 北京大学第一医院
柴 伟 中国人民解放军总医院骨科医学部
陈继营 中国人民解放军总医院骨科医学部
崔旭蕾 中国医学科学院 北京协和医学院 北京协和医院
冯 宾 中国医学科学院 北京协和医学院 北京协和医院
关振鹏 北京大学首钢医院
郭 艾 首都医科大学附属北京友谊医院
郭万首 中日友好医院
黄迅悟 中国人民解放军总医院第九医学中心
林剑浩 北京大学人民医院
林 源 首都医科大学附属朝阳医院
马璐璐 中国医学科学院 北京协和医学院 北京协和医院
梅 丹 中国医学科学院 北京协和医学院 北京协和医院
申 乐 中国医学科学院 北京协和医学院 北京协和医院
孙祯杰 北京市第六医院
田 华 北京大学第三医院
翁习生 中国医学科学院 北京协和医学院 北京协和医院
姚建华 中国人民解放军总医院第七医学中心
张 洪 中国人民解放军总医院骨科医学部
张洪美 中国中医科学院望京医院
张星火 首都医科大学附属北京潞河医院
张耀南 北京医院
张轶超 首都医科大学附属北京同仁医院
周一新 北京积水潭医院
指南制订工作组(以姓氏汉语拼音排序)
李 曾 广东省人民医院
李 辉 西安交通大学医学院附属红会医院
李 涛 青岛大学附属医院崂山院区
李子全 中国医学科学院 北京协和医学院 北京协和医院
彭慧明 中国医学科学院 北京协和医学院 北京协和医院
沈松坡 首都医科大学同仁医院
孙 洋 吉林大学第二医院
王英杰 中国医学科学院 北京协和医学院 北京协和医院
肖 刻 四川大学华西医院
徐溢明 中国医学科学院 北京协和医学院 北京协和医院
朱 威 中国医学科学院 北京协和医学院 北京协和医院
指南外审组(以姓氏汉语拼音排序)
曹 力 新疆医科大学附属第一医院
胡懿郃 浙江大学医学院附属第一医院
黄 伟 重庆医科大学附属第一医院
蒋 青 南京大学医学院附属鼓楼医院
雷光华 中南大学湘雅医院
刘 军 天津医院
刘培来 山东大学齐鲁医院
吕松岑 哈尔滨医科大学附属第二医院
毛新展 中南大学湘雅二医院
钱齐荣 海军军医大学第二附属医院(上海长征医院)
尚希福 中国科学技术大学附属第一医院(安徽省立医院)
沈 彬 四川大学华西医院
史占军 南方医科大学附属第一医院
孙 水 山东第一医科大学附属省立医院(山东省立医院)
孙 炜 深圳市第二人民医院
王 飞 河北医科大学附属第三医院
王金成 吉林大学第二医院
王英振 青岛大学附属医院
夏亚一 兰州大学第二医院
肖 骏 华中科技大学同济医学院附属同济医院
徐耀增 苏州大学第一附属医院
许 鹏 西安交通大学医学院附属红会医院
许伟华 华中科技大学同济医学院附属协和医院
严世贵 浙江大学医学院附属第二医院
杨 佩 西安交通大学第二附属医院
姚振钧 复旦大学中山医院
尹宗生 安徽医科大学第一附属医院
郑 稼 河南省人民医院
郑秋坚 广东省人民医院
周宗科 四川大学华西医院
指南秘书
彭慧明 中国医学科学院 北京协和医学院 北京协和医院
李 曾 广东省人民医院
方法学专家
张丽帆 中国医学科学院 北京协和医学院 北京协和医院
刘晓清 中国医学科学院 北京协和医学院 北京协和医院
执笔
彭慧明 中国医学科学院 北京协和医学院 北京协和医院
翁习生 中国医学科学院 北京协和医学院 北京协和医院
