对比增强T1加权成像纹理分析鉴别小脑毛细胞型星形细胞瘤与血管母细胞瘤
2022-12-03王新东沈潮
王新东,沈潮
(1.淮安市肿瘤医院儿科,江苏 淮安 223200;2.影像科)
毛细胞型星形细胞瘤(pilocytic astrocytoma,PA)是小脑最常见的肿瘤之一,手术完全切除对降低复发率、提高生存率具有重要作用[1]。血管母细胞瘤(hemangioblastoma,HB)是一种生长缓慢且血液供应丰富的肿瘤,术后复发少见[2-3]。由于PA与HB的治疗方案及预后不同,故影像学诊断对临床具有重要的参考价值。当PA或HB具有特征性影像表现时,两者的鉴别并不困难,但重叠的影像特征仍常造成误诊[4]。磁共振扩散成像与灌注成像可有效地鉴别小脑PA与HB,但扫描时间较长等原因限制其在临床中的应用[5]。纹理分析可定量分析图像内的灰阶信息,获取肉眼无法观察的灰度分布信息[6],但尚鲜见运用于小脑PA与HB鉴别的相关报道,本研究尝试通过基于对比增强T1加权成像(contrast-enhanced T1-weighted imaging,CE-T1W)纹理分析鉴别PA与HB,并与影像特征的鉴别效能比较。
1 资料与方法
1.1 临床资料 回顾性分析我院2014年1月至2021年6月经组织病理学确诊的32例PA和38例HB。纳入标准:(1)入院前未进行药物或手术治疗;(2)已完成T1WI、T2WI、扩散加权成像(diffusion weighted imaging,DWI)及CE-T1W扫描;(3)图像质量良好;(4)无其他肿瘤病史。排除标准:(1)本研究所需序列不齐;(2)图像内存在运动伪影。本研究经医院伦理委员会批准,患者均知情同意本研究。
1.2 检查方法 均采用美国GE公司Discovery MR750 3.0T超导磁共振扫描仪,信号采集使用8通道头部相控阵表面线圈,采集T1WI、T2WI、DWI及CE-T1W。T1WI:TR 2 000 ms,TE 25 ms,层厚5 mm,层间距1 mm,FOV 240 mm×240 mm,矩阵160×160;T2WI:TR 4 300 ms,TE 100 ms,层厚5 mm,层间距1 mm,FOV 240 mm×240 mm,矩阵160×160;DWI:采用自旋回波平面回波序列,单次激发,TR 3 000 ms,TE 65.5 ms,b值分别为0和1 000 s/mm2,层厚5 mm,层间距1 mm,FOV 240 mm×240 mm,矩阵160×160;CE-T1W:参数同T1WI,采用高压注射器以流率2.0 ml/s经肘正中静脉团注钆喷酸葡胺(Gd-DTPA)(广州康臣药业有限公司,15 ml∶7.04 g)0.1 mmol/kg。
1.3 纹理分析与影像特征 选出肿瘤CE-T1W序列横断面最大层面图像以DICOM格式导出并转成BMP格式,由2名放射科医师分别使用MaZda ver.4.6软件沿肿瘤边缘勾画感兴趣区(region of interest,ROI),尽量包含整个肿瘤,避免画入周围正常组织。为了平衡图像之间的亮度和对比度,将图像标准化为μ±3σ(μ:图像强度的平均值;σ:标准差)后提取肿瘤的直方图分析(histogram analysis,HA)、灰度共生矩阵(graylevel co-occurrence matrix,GLCM)、灰度游程矩阵(gray-level run length matrix,GLRLM))、绝对梯度(absolute gradient,AG)、自回归模型(autoregressive model,AR)和小波变换(wavelet transform,WT)6种纹理特征,GLCM的步长从1~5个像素,GLCM与GLRLM均包含4个方向(0°、45°、90°和135°),共279个参数。肿瘤的影像特征由2名放射科医师共同分析后得出,包括实性(是或否)、大囊小结节(有或无)、囊内分隔(有或无)、流空血管(有或无)、实性均匀强化(是或否)、囊壁强化(是或否)、瘤周水肿(有或无),见图1~2。

图1 1例7岁女性患者左侧小脑半球内PA
1.4 统计学分析与模型构建 数据分析、特征筛选及模型建立使用R语言(4.0.3)。使用组内相关系数(intraclass correlation coefficient,ICC)分析2名医师提取的纹理特征,选取ICC>0.75重复性良好的特征[7]。组间的特征参数比较取2名医师提取的平均值,将差异有统计学意义的参数归一化在(0,1)之间后再通过LASSO回归分析进一步筛选,LASSO回归模型的最优λ值通过十折交叉验证获得。利用筛选出的特征及影像特征分别构建支持向量机(support vector machine,SVM)模型,分别使用线性核(linear kernel,LK)、多项式核(polynomial kernel,PK)和径向基函数核(radial basis function kernel,RBFK),验证方式选择十折交叉验证。采用受试者工作特征(ROC)曲线评估模型的效能,模型的AUC比较使用Z检验。计量资料以均数±标准差表示,采用独立样本t检验(通过正态分布与方差齐性检验)或以M(P25,P75)表示,采用秩和检验;计数资料比较采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。

图2 1例42岁女性左侧小脑半球HB
2 结果
2.1 2组一般资料比较 PA组男19例,女13例,年龄6~27岁,平均(10.09±4.52)岁;HB组男20例,女18例,年龄15~83岁,平均(46.63±19.29)岁,2组年龄比较差异有统计学意义(t=-10.472,P<0.01),性别差异无统计学意义(χ2=0.320,P>0.05)。
2.2 构建模型的纹理特征参数 选出重复性良好的173个特征参数,其中2组间差异有统计学意义的特征参数共128个,LASSO选出10个特征参数见表1,图3右边的黑色垂直线对应的横坐标代表模型的最优λ值,此时LASSO模型最精确,图4代表选出的各特征系数绝对值。

图3 LASSO模型最优λ值时对应的特征数量
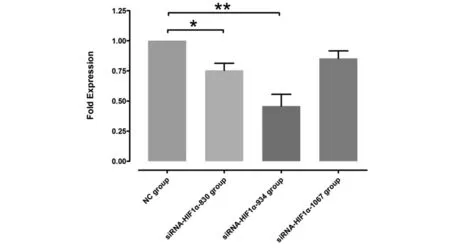
图4 LASSO模型选出的10个特征参数(直方图越长,代表系数绝对值越大)
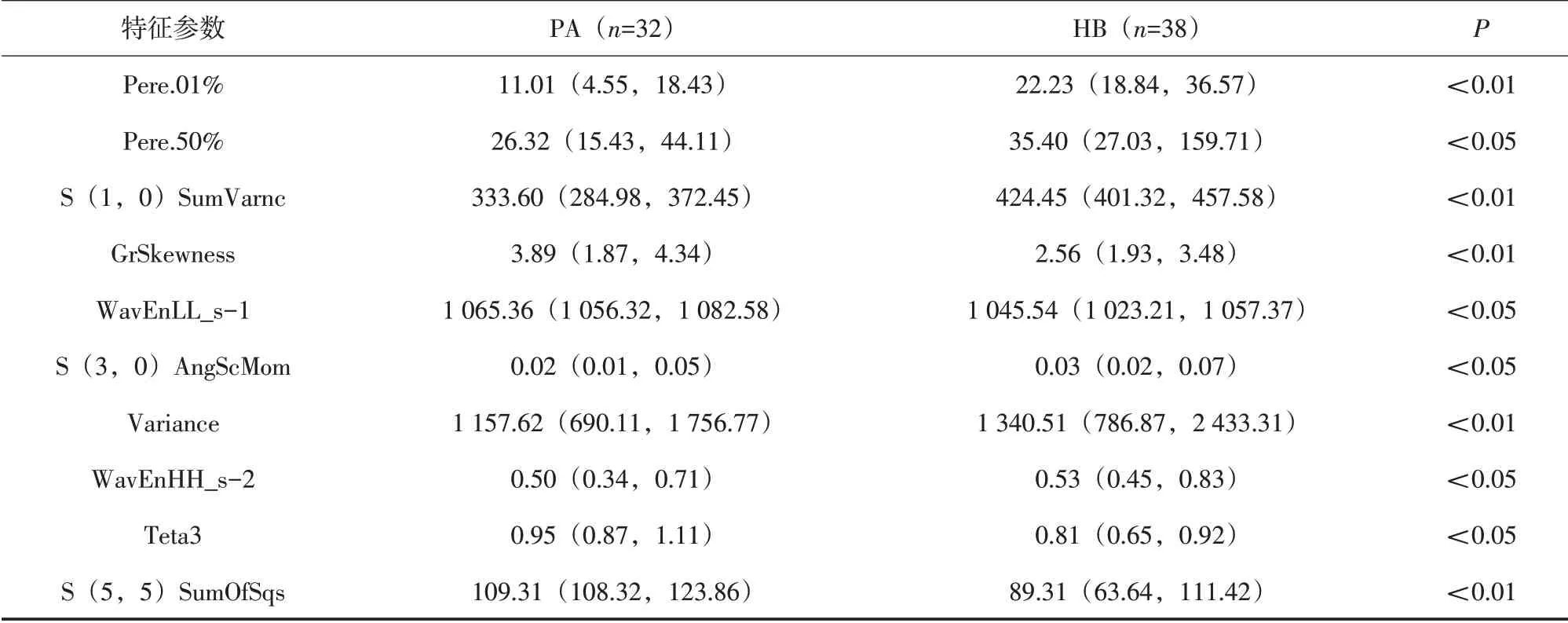
表1 2组筛选出的纹理特征参数的比较[M(P25,P75)]
2.3 2组影像特征比较 相较于PA组,HB组更易形成大囊小结节、存在更多流空血管、实性强化更均匀(P<0.01),而2组是否呈实性、有无囊内分隔、囊壁是否强化、有无瘤周水肿差异无统计学意义(P>0.05),见表2。
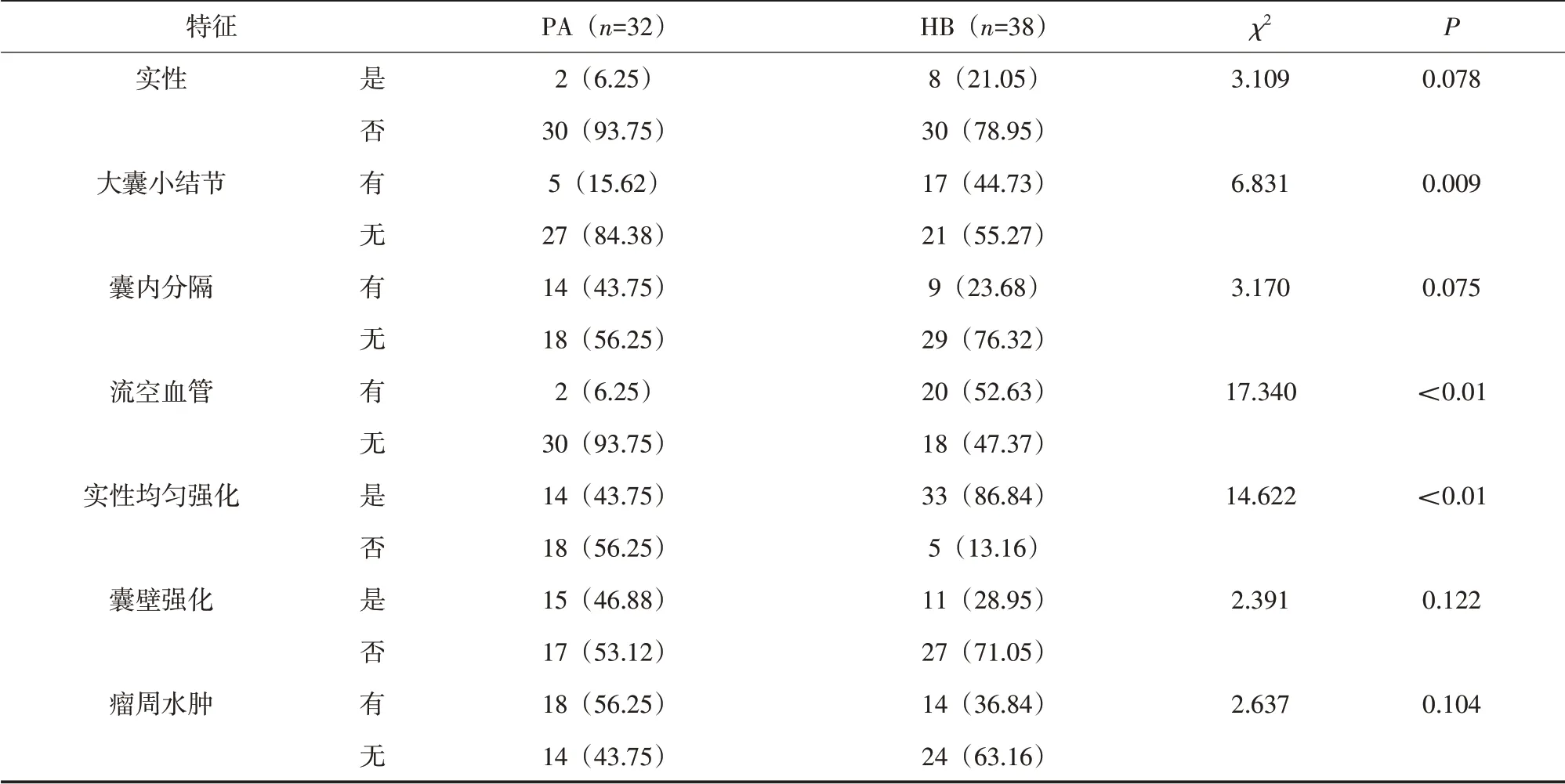
表2 2组间影像特征比较[n(%)]
2.4 纹理特征与影像特征构建的SVM分类模型效能 纹理特征建立的SVM分类模型中,PK核的模型分类效能最佳,敏感度、特异度、准确率及AUC最优,其中AUC优于以3个影像特征建立的3种SVM分类模型,差异均有统计学意义(Z=2.972、2.561、2.783,P<0.05),见表3。

表3 纹理特征与影像特征构建的SVM分类模型区分PA与HB的效能
3 讨论
PA是儿童最常见的中枢神经系统胶质瘤,属于Ⅰ级星形细胞瘤,最常发生于小脑,占儿童星形细胞瘤的60%[1,5],而HB好发于小脑,属于中枢神经系统血管源性的良性肿瘤,好发于成年女性[2],本研究结果显示PA组的年龄低于HB组(P<0.01),而2组性别比较差异无统计学意义,与既往研究结果[1-2]一致。
影像特征中,大囊小结节在HB中具有特征性,表现为肿瘤光滑的囊壁上出现明显均匀强化的小结节,而PA中这种特征相对少见且强化程度低,主要由于HB结节内存在丰富的毛细血管网,而PA结节内的毛细血管所占比例不高[8-9],本研究也发现HB组出现大囊小结节这一特征的比例明显高于PA组(P<0.01)。另外,在HB肿瘤实性部分可出现低信号的流空血管信号,并可显示肿瘤内存在的粗大供血动脉[10]。本研究中HB组内亦多次出现流空血管信号,而PA组内未出现此特征,也印证了HB较PA具有更加丰富的血供。最后,HB实性强化较PA更均匀,推测由于HB主要由薄壁的毛细血管与间质细胞构成[11],造影剂能顺着血管均匀充盈整个肿瘤,而PA的实性部分由增生的胶质、肿瘤细胞及增生的毛细血管等多种成分构成,各种成分比例不恒定使强化方式呈现出多样化[4-5],即更易表现出不均匀强化的特征。本研究以2组间差异有统计学意义的影像特征建立SVM分类模型,但3个模型的效能一般,AUC仅分别达0.764、0.726、0.740。
SVM是一种有效的二分类工具,利用医学图像的纹理特征建立模型对疾病进行诊断,在临床研究中已有广泛运用[12-14]。本研究利用磁共振CE-T1W序列图像提取279个纹理特征,共筛选出10个特征参数建立了3种SVM分类模型,且均得到了良好的分类效果,其中使用PK核的模型分类效能最佳,与既往研究[13]类似,但与Mahato等[14]的研究结果并不一致,这可能与研究的数据类型不同有关。比较后发现,纹理特征建立的PK核SVM分类模型效能优于以3个影像特征建立的3种SVM分类模型(P<0.05),说明在PA或HB不具备特征性影像表现时,纹理分析可为PA与HB的鉴别诊断提供重要参考信息。
综述所述,基于CE-T1W的纹理特征建立的SVM分类模型可有效鉴别小脑PA与HB,且效能优于影像特征所建立的模型。本研究主要的不足之处:纳入样本量较少,仍需扩大样本量以提高分类模型的可信度;仅分析了CE-T1W序列图像的纹理特征,而未研究其他序列;仅利用纹理特征建立了SVM分类模型,而未研究其他模型。
