基于网络药理学和分子对接筛选杜仲治疗抑郁症的潜在靶点和活性成分
2022-12-03杨萍刘萍
杨萍,刘萍
(遵义医科大学药学院,贵州 遵义 563000)
抑郁症是世界范围内精神致残的主要原因,2017年世界卫生组织数据显示,全球已有约3.22亿抑郁症患者[1],且患病人数还在随社会高速发展、老龄化加剧等持续上升[2]。目前,抑郁症的病理生理学机制包括单胺假说、下丘脑-垂体-肾上腺(HPA)轴功能亢进等,但并不完善。在治疗方面,临床一线治疗仅对1/3的患者显现出明显的改善作用,并且药物起效作用存在数周至数月的潜伏期、药物不良反应严重[3]。传统中医理论认为,抑郁症属情志病范畴,正常的情志活动依赖于五脏气、血和精的充盈与阴阳平衡,与肝肾功能及相互调节密切相关[4],通过调节肝肾功能治疗抑郁症的疗效也已得到认可。杜仲,经典补益药,有补肝肾、强筋骨和安胎的功效。已有研究发现,杜仲可以显著改善小鼠抑郁样行为[5],但作用靶点和主要的抗抑郁活性成分尚不完善。本研究借助网络药理学研究方法,筛选杜仲治疗抑郁症的重要靶点,并运用分子对接考察杜仲主要活性成分基于该靶点治疗抑郁症的可能性,以期为后续研究提供思路。
1 材料与方法
1.1 获取抑郁症靶基因 运用在线人类孟德尔遗传数据库(OMIM,https://omim.org/)和人类基因数据库(GeneCards,https://www.genecards.org/)获取疾病靶标,并对结果进行汇总去重。本文采用数据库及软件涉及“物种”选项均设置为“Homo Sapien(Human)”。
1.2 杜仲靶基因预测 在中药系统药理学分析平台(Traditional Chinese Medicines Systems Pharmacology,TCMSP,http://tcmspw.com/tcmsp.php)检索“杜仲”,获得的“Ingredients”特指所检索药物的活性成分。口服生物利用度(oral bio‐availability,OB)是衡量药物体内药代动力学过程及成药性的重要参数,类药性(drug-like,DL)代表其成分和已知药物化学结构的相似度,对分析中药活性成分是否可对机体产生作用具有重要参考价值。有研究显示,OB≥30%且DL≥0.18对于活性成分成药至关重要[6],故本研究选取OB值≥30%且DL值≥0.18的活性成分,并在“Related Targets”项下查询其对应靶标。后通过Universal Protein(UniProt,https://www.uniprot.org/)在线数据库将获得的靶标转换为基因名称。
1.3 获取交集基因并构建活性成分-靶点-药物-疾病的可视化网络 将前述所得杜仲和抑郁靶基因分别输入Venn在线工具,即可获取两者交集基因。使用Cytoscape 3.6.1软件(http://www.cyto‐scape.org/)构建可视化的活性成分-靶点-药物-疾病网络。
1.4 获取交集基因并构建蛋白相互作用(PPI)网络 交集基因导入STRING 11.5在线数据库(https://string-db.org/)构建PPI网络、获取核心基因。
1.5 基因本体论(GO)和基因百科全书(KEGG)通路富集分析 联合生物信息注释数据库(DA‐VID,https://david.ncifcrf.gov/)和R语言对核心基因进行GO和KEGG通路富集分析。
1.6 重要靶点与杜仲主要活性成分的分子对接通过数据库查找杜仲主要活性成分,使用PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)下载杜仲主要活性成分的二维结构,依次在AutoDock‐Tools-1.5.6、Chem3D为其添加氢和电荷、修改使其能量最小化并以PDBQT格式保存。糖皮质激素受体基因(NR3C1)(PDBID:1NHZ)的晶体结构从蛋白质数据库PCSB PDB(http://www.rcsb.org)下载,下载的复合物使用PyMol 1.7软件修饰以去除原始配体和水分子并保存为PDBQT格式。将以上准备好的文件导入到Discovery Studio 3.5软件进行杜仲主要活性成分与NR3C1的分子对接和相互作用力分析,选择能量最低的构象作为分析的最优构象。
2 结果
2.1 抑郁症靶标 将2个数据库获得的基因进行汇总去重后共得到抑郁症基因9 720个,其中有1个来源于OMIM数据库,其余来源于GeneCards数据库。
2.2 杜仲靶标 共获得杜仲活性成分28个,后得到靶基因共181个。
2.3 交集基因及活性成分-靶点-药物-疾病网络杜仲和抑郁症交集基因共170个。使用Cytoscape 3.6.1软件以展示药物活性成分与靶基因(交集基因)之间的关系,见图1,其中有4个活性成分与交集基因无连接,予以删除。
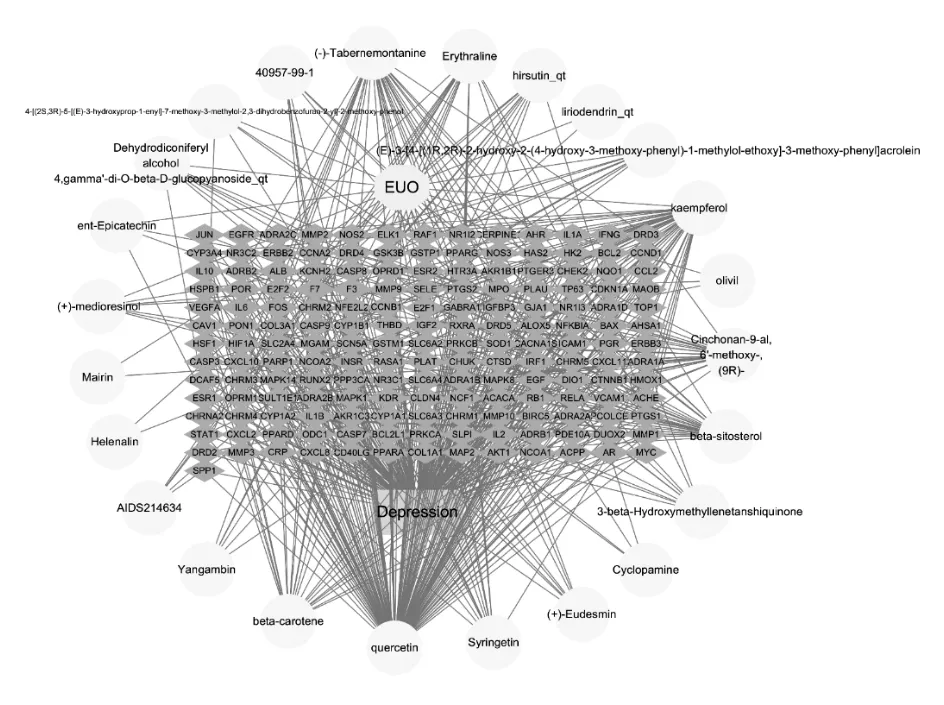
图1 杜仲主要活性成分-靶点-药物-疾病网络
2.4 PPI网络 将交集基因导入STRING11.5在线数据库以获取核心靶点。通过设置最低相互作用得分为0.990,隐藏与主网络无连接的点,得到PPI网络,见图2。图中连线代表2个基因关联,即基因共同促成或具备某功能。每一根连线代表一个该关联的证据来源,如实验、数据库等,连线越多则证明两者之间的关联证据越充分,总连线越多的基因在网络中的作用越核心,经筛选后得到的此网络中的基因即为杜仲治疗抑郁症的核心基因,共44个。

图2 杜仲与抑郁症PPI网络图
2.5 GO和KEGG通路富集分析结果 GO富集分析从细胞成分、生物途径和分子功能3个方面对基因进行描述,根据网络药理学预测可知,杜仲治疗抑郁症的核心基因存在于核质、细胞质、转录因子复合体、细胞周期蛋白依赖性蛋白激酶全酶复合物和微管中心,通过参与机体对脂质、有机物、有机环状化合物的反应,调控生物发育,从而起到影响转录因子、酶、大分子复合物、染色质、转录调控区DNA结合的作用,见图3。KEGG通路富集分析见图4,图中P值代表富集程度,越小则富集程度越高,从上往下,P值逐渐增大。结果显示,杜仲通过多通路协同作用治疗抑郁症,此处仅列出P值较小的前20个,其中包括内分泌抵抗和凋亡信号通路。
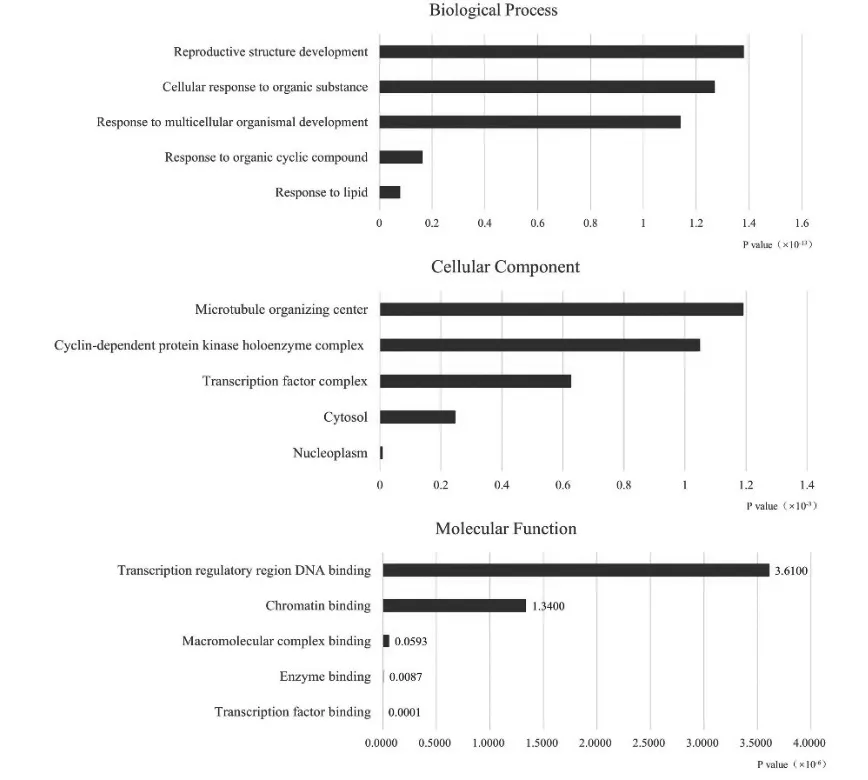
图3 杜仲治疗抑郁症的药物-疾病核心基因GO分析图
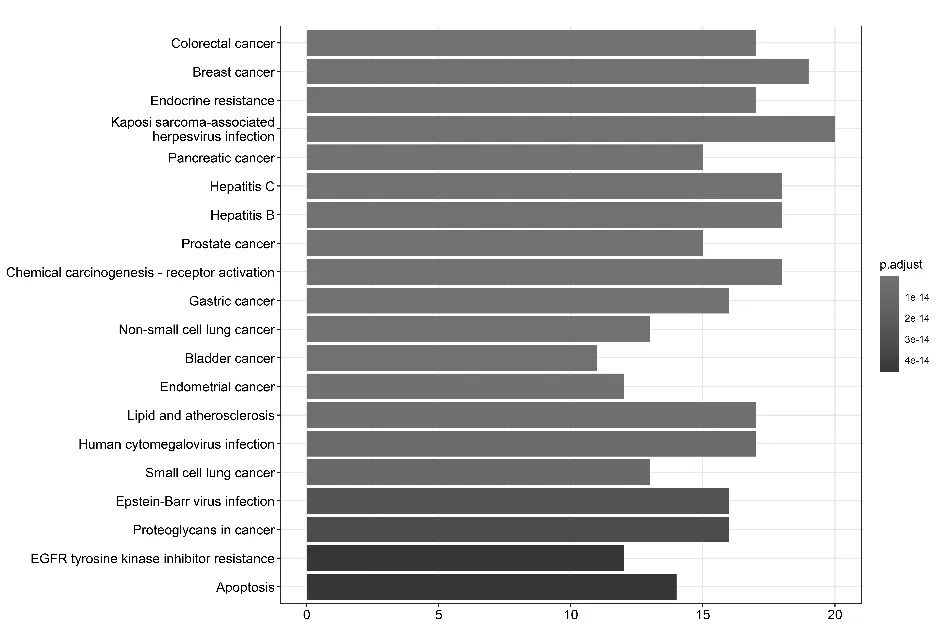
图4 杜仲治疗抑郁症药物-疾病核心基因KEGG分析
2.6NR3C1与杜仲主要活性成分的分子对接 本研究基于网络药理学研究筛选得到杜仲治疗抑郁症的潜在调控靶标共44个,并可通过PPI网络对每个靶标在网络中的重要性进行简单分析。但网络药理学是基于数据库和文献的研究,因为选择方法、参数设置和计算模型的不完善使得一些作用靶点的得分排名较低甚至被剔除,结合文献研究筛选靶点能部分减少这种错误。文献研究发现,HPA轴功能紊乱是研究最深入、公认对抑郁症的发生发展极其重要的机制,在HPA轴的调控中,糖皮质激素受体(glucocorticoid receptor,GR)发挥了重要作用,故本研究选取其调控基因NR3C1与杜仲主要活性成分进行分子对接验证。通过数据库查找并得到杜仲主要活性成分7种,包括桃叶珊瑚苷、筋骨草苷、车前草苷、二氢查耳酮、哈帕苷丁酸酯、京尼平和马钱苷。
Uniport网站查询到NR3C1的(UniProtKBP04150(GCR_HUMAN))的氨基酸序列(500-777),该序列对应的晶体结构是NRLBD(图6),PDB编号1NHZ,分辨率2.3A。NR3C1与各活性成分的分子对接结果见表1,可视化结果见图5。
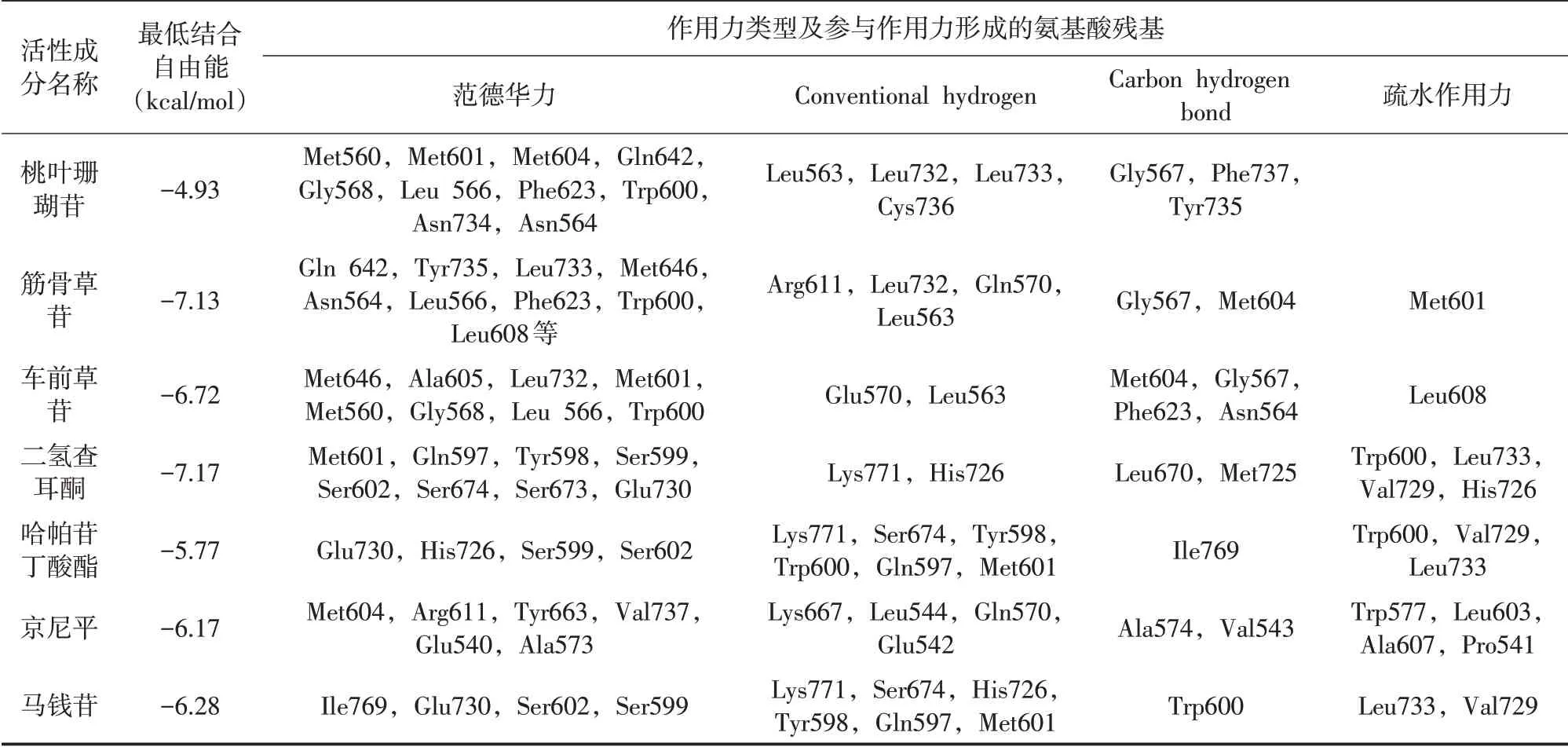
表1 NR3C1与杜仲主要活性成分的分子对接结果
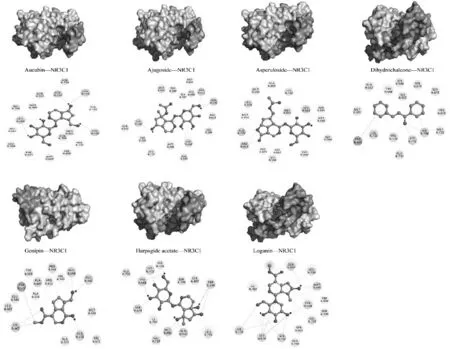
图5 NR3C1与杜仲主要活性成分的分子对接(3D结构为NR3C1的NRLBD结构域)
3 讨论
本研究基于网络药理学研究方法,探讨杜仲治疗抑郁症的作用机制发现,杜仲中OB≥30%且DL≥0.18的活性成分共28个,24个与交集基因有连接;与抑郁症的交集基因共170个,通过STRING在线数据库筛选出杜仲治疗抑郁症的核心基因共44个。文献研究发现,核心基因中的NR3C1也是调控HPA轴的重要靶点,可能对抑郁症有重要影响,故以其作为重要调控靶点进行后续研究。为了进一步发掘杜仲中基于NR3C1调控抑郁症的成分,进行分子对接发现,桃叶珊瑚苷、筋骨草苷、车前草苷、二氢查耳酮、哈帕苷丁酸酯、京尼平和马钱苷与NR3C1结合能均小于0 kcal/mol,分子之间有结合活性,具有进一步研究的价值。
肝为将军之官,一主疏泄、升发,调节全身气机,使人体之气向上向外,通而不滞,散而不郁,具有“阳”的生理特点,与抑郁症情绪低落、悲伤易哭等“阴”性特征相互制约,彼此消涨;二主藏血,为神志活动提供物质基础,具有收敛之性,可化生和涵养肝气[4]。肝之疏泄和藏血功能互为前提,维持人体气、血的正常运行,从而保证机体发挥正常的情志活动。肾为作强之官,一主藏精,精是神志活动的根本,肾精充盈,可化生为血液,保证肝的藏血功能;二主闭藏,防止肝疏气太过;另外,肾之阴阳为五脏阴阳之根本,肾阳是一切活动的动力之源,而抑郁症表现出活动减少、兴趣丧失等“不动”现象,可能与肾阳气亏虚有关[4]。肝肾相互制约、相互影响,共同维持和调节五脏六腑阴阳气血的平衡,在抑郁症的发生发展中起到重要的调节作用。目前,中医理论讨论肝郁为基础,通过肝肾同调可能具有更好的应用前景。但不论是从时间、物料投入等方面,都应具充分的理论论证。本研究通过网络药理学进行深入分析,一方面论证补肝肾药物治疗抑郁症的可行性;一方面预测可能的机制,二者相互验证寻找研究具有抑郁症治疗前景的中药活性成分。虽然网络药理学筛选的研究已经初具规模,但是通过网络药理学将中医理论与现代药理学结合还处于探索阶段。深入的网络药理学研究可以为二者有机结合提供思路,并可以减少盲目投入,节约成本,提高研究效率。
检索以上7种成分的抗抑郁研究发现,桃叶珊瑚苷[7]、京尼平[8]、马钱苷[9]具有抗抑郁作用,但其作用机制不包括调控GR/NR3C1,进一步梳理肝肾同调与HPA轴的关系,研究以上7种活性成分基于该轴的抗抑郁作用,或可为抑郁症的机制和治疗提供新的方案。本研究中使用的网络药理学研究方法不仅节约了人力、物力,更重要的是让中医理论能够通过现代药理学来解释,其基于多成分、多靶点的相互结合的分析方法可能是中药研究的突破点[10]。
