钾矿与不同钙质原料制备的硅钙钾肥中有效钙的性质对比研究
2022-12-02王朝军江远萍朱云勤
王朝军, 李 波, 江远萍, 朱云勤
(1.瓮安生态环境监测站 贵州瓮安 550400;2.贵州大学资源化工研究所 贵州贵阳 550025)
施用钙肥不仅可以给农作物提供营养元素钙,还可以改善农作物生长的土壤环境,改良冷烂泥田及酸性土壤;中和农作物体内代谢过程中过多的有机酸,消除有机酸的毒害;有助于提高细胞膜的稳定性,促进植物对钾离子的吸收;消除因某些离子(如H+、Al3+、Na+)过多而产生的毒害[1]。
传统的硅钙钾肥是以不溶性含钾硅酸盐岩石与石灰石为钙质原料在1 160 ℃高温下烧制而成,大量开采石灰石不仅要排放大量的粉尘颗粒,而且会破坏地表的生态平衡,产生水土流失等严重问题,因此寻找新型的钙质原料来制备硅钙钾肥,是目前急切需要解决的问题。磷酸生产企业在制备磷酸的工艺中,用硫酸处理磷矿时会产生大量的固体废弃物(磷石膏),并且在磷石膏综合利用制备硫酸铵时会产生大量的二次固体废弃物(磷石膏钙渣),这些废弃物(磷石膏、磷石膏钙渣)长时间暴露在空气中会对大气和土壤造成严重的污染。磷石膏、磷石膏钙渣中含有丰富的钙元素,若能以磷石膏、磷石膏钙渣为钙质原料制备硅钙钾肥,既解决了我国不溶性钾资源缺乏的问题,又解决了我国因大量开采石灰石和大量堆存磷石膏、磷石膏钙渣而带来的环境污染问题。本研究以不溶性含钾硅酸盐岩石(简称钾矿,K2O的质量分数为9.85%)与3种钙质原料按一定的比例[磷石膏-钾矿(1∶2.2)、磷石膏钙渣-钾矿(1∶1.45)、石灰石-钾矿(1∶1.0)]混合制备的硅钙钾肥为研究对象,探讨了在一定浓度的酸性溶液中及在模拟酸性土壤中钙的溶出规律,以期对新型硅钙钾肥(不溶性含钾硅酸盐岩石与磷石膏钙渣制备)的推广使用提供参考[2]。
1 试验部分
1.1 主要仪器与试剂
SP-3580AA型火焰原子吸收分光光度计,上海光谱仪器有限公司;钙空心阴极灯;CP214型电子天平(万分之一),奥豪斯仪器(常州)有限公司;DK-98-ⅡA型恒温水浴锅,天津市泰斯特仪器有限公司;HY4型调速多用振荡器,苏州威尔实验用品有限公司。
1.4 g/cm3硝酸溶液(硝酸为分析纯,国药集团化学试剂有限公司),硝酸(1+1)溶液,0.1 g/mL镧溶液,50 mg/L钙标准溶液(北京坛墨质检科技有限公司),20 g/L柠檬酸溶液(柠檬酸为分析纯,无锡市展望化工试剂有限公司)。
1.2 钙分析试液制备
准确称取1 g(精确至±0.000 2 g)经120 ℃干燥的硅钙钾肥试样置于250 mL磨口锥形瓶中,用移液管准确加入100 mL 20 g/L柠檬酸溶液,立即塞紧瓶塞,用HY4型调速多用振荡器在一定温度下振荡一定时间(振荡频率120次/min,不同条件对振荡温度和振荡时间要求不同),用定量滤纸过滤于干燥的150 mL烧杯中,得到含钙分析试液[3]。
2 钙含量的测定
2.1 测定方法
硅钙钾肥中钙的含量采用火焰原子吸收分光光度法测定[4]。其原理为:在酸性条件下,将试液喷入空气-乙炔火焰中,使钙原子化,采用422.7 nm共振线的吸收测定钙含量。
用1.4 g/cm3硝酸溶液酸化钙分析试液的pH为1~2,准确吸取1.00~10.00 mL(含钙不超过250 μg)试液于50 mL容量瓶中,加入硝酸(1+1)溶液1 mL和0.1 g/mL镧溶液1 mL,用蒸馏水稀释至刻度,摇匀。用50 mL水取代试样进行空白试验。
2.2 标准曲线的制作
准确移取钙标准溶液0、0.50、1.00、2.00、3.00、5.00、6.00 mL于7只50 mL容量瓶中,依次从低到高测量吸光度,以钙的质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线。按式(1)计算钙的质量浓度ρCa:
ρCa=f·ρCa标
(1)
式中:ρCa——钙的质量浓度,以CaO计,mg/L;
f——试样定容体积与试样体积之比;
ρCa标——由标准曲线查得钙的质量浓度,mg/L。
3 试验结果与分析
3.1 有效钙含量对比
分别准确称取1 g(精确至±0.000 2 g)经120 ℃干燥的3种不同钙质原料制备的硅钙钾肥试样,然后加入12 g氢氧化钠于镍坩埚中,温度设置为700 ℃,熔融时间25 min,待制备成分析试样后,用火焰原子吸收分光光度法测定有效钙含量,测定结果见表1。

表1 3种不同硅钙钾肥中的有效钙含量
3.2 稳定性
将2015年自制的3种硅钙钾肥(石灰石、磷石膏、磷石膏钙渣分别与不溶性含钾硅酸盐岩石制备)产品在2021年取样检测其中的有效钙含量,测定结果见表2。

表2 3种硅钙钾肥稳定性试验结果
由表2可以看出,3种硅钙钾肥中钙元素性质稳定,均能长期放置,不受年限的影响。
3.3 有效钙缓释性对比
分别将浸取3种不同硅钙钾肥的浸取液(水和20 g/L柠檬酸溶液)取出1/2体积(取出的1/2体积溶液模拟成被植物所吸收),然后加入等量的浸取溶液(水和20 g/L柠檬酸溶液)继续浸取,浸取温度均为常温(25 ℃),振荡时间均为30 min(120次/min),持续重复5次[4-6]。3种硅钙钾肥在20 g/L柠檬酸溶液中的有效钙累积溶出率曲线见图1。

图1 3种硅钙钾肥在20 g/L柠檬酸溶液中的有效钙累积溶出率曲线
由图1可知,3种硅钙钾肥在20 g/L柠檬酸溶液中的有效钙累积溶出率均呈增加的趋势,且钙素能维持养分平衡。试验结果表明,磷石膏和磷石膏钙渣分别与不溶性含钾硅酸盐岩石制备的硅钙钾肥中的钙符合缓释性肥料的检验标准要求[7-8],肥料中的钙具有缓释性。
3.4 试验条件的影响
试验考察了酸度(pH)、振荡温度和振荡时间对有效钙溶出率的影响。按试验操作步骤,分别绘制了不同酸度、不同振荡温度、不同振荡时间下3种不同硅钙钾肥中有效钙的溶出率,结果分别见图2、图3和图4。

图2 3种硅钙钾肥中有效钙的溶出率随酸度的变化

图3 3种硅钙钾肥在20 g/L柠檬酸溶液中有效钙溶出率随振荡温度的变化

图4 3种硅钙钾肥在20 g/L柠檬酸溶液中有效钙溶出率随振荡时间的变化
由图2可以看出,在振荡温度为常温(25 ℃)、振荡时间为30 min、振荡频率为120次/min时,当pH<3时,3种硅钙钾肥中有效钙的溶出率变化明显,酸度越大,有效钙的溶出率越大。
由图3可以看出,在振荡时间为30 min、振荡频率为120次/min、酸度一定(pH为2~3)时,3种硅钙钾肥中有效钙的溶出率均随振荡温度的升高而增大,但增加量不明显。
由图4可知,在振荡温度为常温(25 ℃)、振荡频率为120次/min、酸度一定(pH为2~3)时,3种硅钙钾肥中有效钙的溶出率均随振荡时间的延长而逐渐增大。
4 讨论
4.1 正交试验设计
根据硅钙钾肥有效钙溶出行为的影响因素,确定振荡温度、振荡时间和酸度为三因素,分别选定3个水平进行正交试验[9],结果见表3。
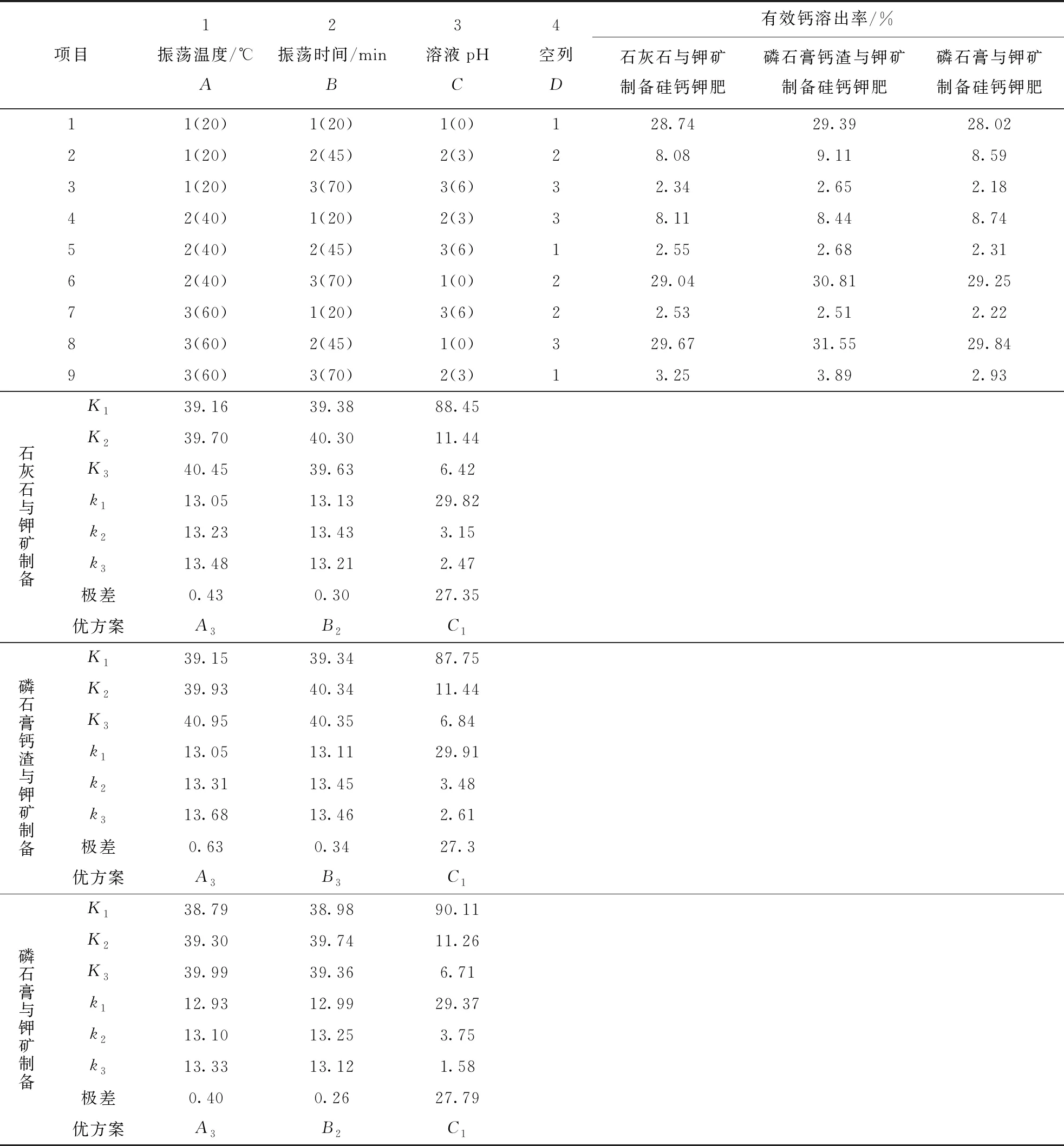
表3 L9(34)正交试验设计表
由表3可知,3种不同硅钙钾肥中有效钙的溶出率受酸度影响较大,振荡温度和振荡时间对有效钙溶出率影响不大。
4.2 方差分析
对表3试验结果进行方差分析[10],数据见表4。
由表4可知,探索硅钙钾肥中有效钙的溶出行为时,其溶出量受酸度的影响具有高显著性,振荡温度和振荡时间无显著性。
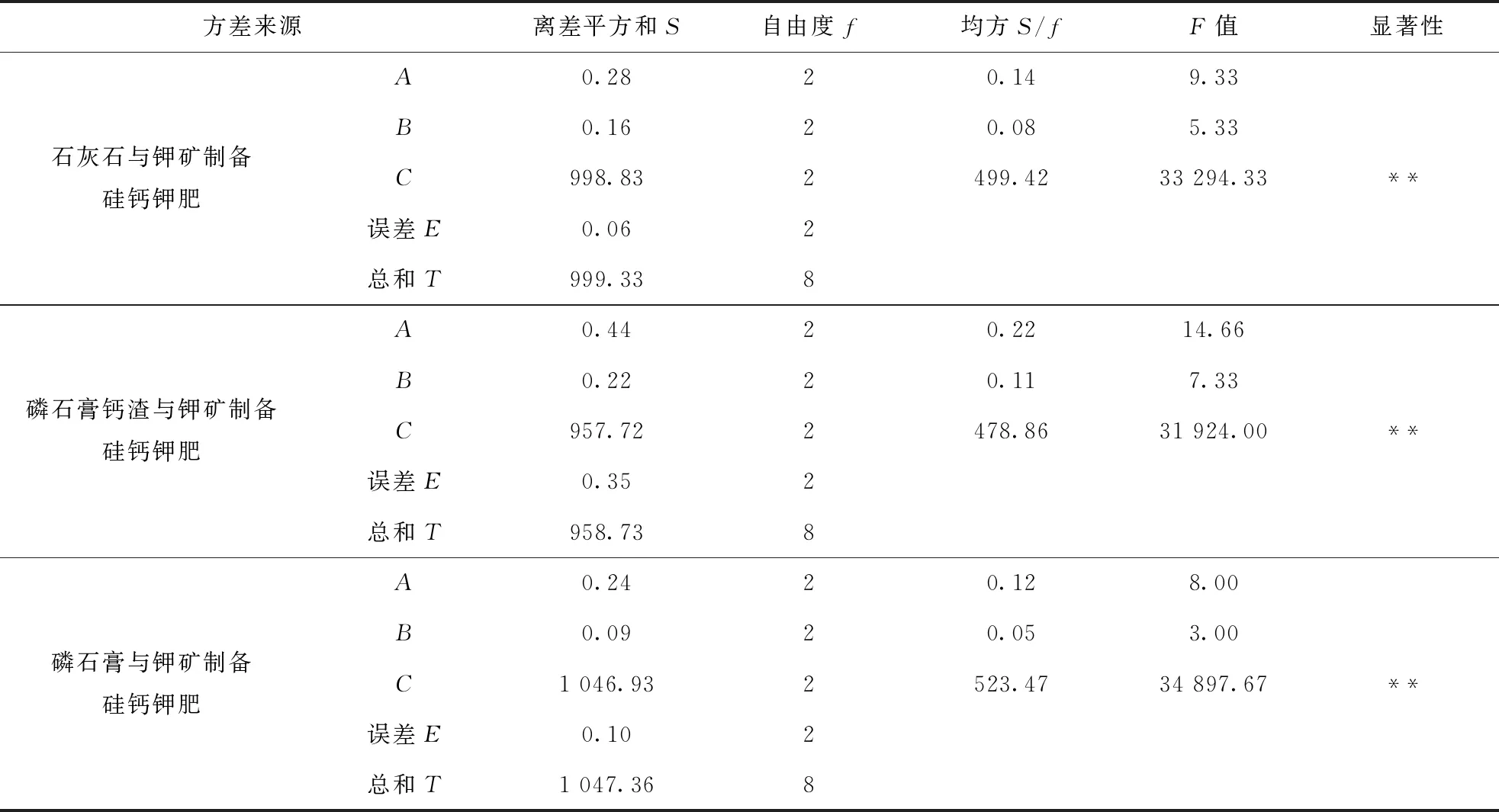
表4 方差分析结果统计
5 结语
(1)由试验可知,3种原料制备的硅钙钾肥中的钙均具有较好的缓释性,能有效改良酸性土壤,对农作物具有持久供肥的效果。
(2)综合单因素法和正交试验结果可知,施肥后温度和时间变化对硅钙钾肥中有效钙溶出率的影响不存在显著差异,而酸度对硅钙钾肥中有效钙的溶出率存在显著性差异,土壤的酸性越强,溶出率越大。
(3)经对比分析表明,3种硅钙钾肥中钙的释放特征具有相似性,这不但解决了开采石灰石需要排放大量粉尘和颗粒物,及对地表植被带来毁灭性损毁,导致水土流失、生物量和生物多样性锐减等生态环境问题,而且为磷石膏、磷石膏钙渣寻找到了新的合理利用途径,可变废为宝,实现对磷石膏、磷石膏钙渣中钙的资源化利用,将有害的工业废渣转化为对农作物有用的肥料。
