过敏原特异性免疫治疗过敏性鼻炎的疗效观察及作用机制研究
2022-11-29项清华
项清华
(朝阳市中心医院耳鼻咽喉科,辽宁 朝阳 122000)
过敏性鼻炎是一种与过敏原接触后诱发的耳鼻喉科常见病,该症是基因与环境相互作用后的结果,其在各年龄段均可发病,尤以过敏体质和老年人为高发群体。近年来,随着环境改变,全球过敏性鼻炎发病率有所提高,相关数据调查显示,过敏性鼻炎在全球的发病率为10%~25%[1]。患病后,主要表现为流涕、鼻痒、打喷嚏等症状,对患者正常学习、生活造成严重影响。临床治疗该症以防治结合为原则,即环境控制、药物治疗、免疫治疗及健康教育为一体。特异性免疫治疗(ASIT)被认为是过敏性鼻炎的对因治疗方法,且效果较好[2]。ASIT根据不同给药途径可分为舌下含服免疫治疗(SLIT)和皮下免疫治疗(SCIT),相较SCIT,SLIT给药方便,且安全无创,患者依从性高,更有优势。研究指出,SLIT能减少患者对药物依赖,且停药后不易复发[3]。虽然SLIT治疗过敏性鼻炎的效果已受到临床认可,但其具体作用机制尚不明确。鉴于此,本研究选取146例患者进行分组观察,并对用药前后免疫球蛋白水平、Th1/Th2细胞水平变化等指标,旨在探索其可能药理机制,为今后治疗该症提供参考依据。
1 对象与方法
1.1 研究对象
采用随机、对照试验,从2019年2月至2021年2月在耳鼻喉科就诊的过敏性鼻炎患者中随机选出146例作为观察对象,经随机数字表法分为两组,每组73例。观察组中男39例,女34例;年龄19~63(41.07±6.13)岁;病程1~7(4.05±0.14)年。对照组中男37例,女36例;年龄21~64(42.04±6.31)岁;病 程1~8(4.49±0.25)年。两组患者临床资料比较,无明显差异(P>0.05),有可比性。
纳入标准:(1)患者粉尘螨皮肤点刺试验结果呈阳性,符合过敏性鼻炎诊断标准[4];(2)年龄18~65岁;(3)单一粉尘螨过敏或多重变应原过敏;(4)入组前未接受过其他抗过敏治疗;(5)患者自愿参与研究,其家属知情。
排除标准:(1)合并支气管哮喘、鼻窦炎、鼻息肉等疾病;(2)存在其他部位过敏症状;(3)合并急、慢性感染性疾病或全身性疾病;(4)妊娠期或哺乳期女性;(5)合并恶性肿瘤。
1.2 方法
对照组患者服用枸地氯雷他定片(扬子江药业集团广州海瑞药业有限公司,国药准字H20090138,规格8.8 mg×6 s),1片/次,1次/d;同时用盐酸氮卓斯汀鼻喷剂(维亚瑞股份有限公司,注册证号H20050251,规格10 mL/瓶/盒)喷鼻孔,喷药时保持头部直立,2次/d,早晚各1次。疗程为6个月。
观察组患者在对照组用药基础上加用畅迪粉尘螨滴剂(浙江我武生物科技股份有限公司,国药准字S20060012,规格2 mL∶1000 μg/瓶),该滴剂分为1、2、3、4、5号。将滴剂滴于舌下,含1~3 min吞咽,1次/d,每日于同一时间用药。起始阶段:于1~3周,用1、2、3号滴剂,每周7天剂量依此为1、2、4、6、8和10滴/次;第4、5周用4号滴剂,4滴/次。维持阶段为自第6周起,用5号滴剂,2滴/次。疗程为6个月。
1.3 观察指标
(1)鼻部症状和药物评分。参照鼻部症状总评分(TNSS)[5]评估,根据喷嚏、鼻痒、鼻塞和流涕症状由轻至重计1~3分,4项评分总和为最终得分,得分越高症状越严重。采用对症治疗药物评分(TMS)[6]评估,分别用抗组胺及抗白三烯药(均为1分)、局部用糖皮质激素(2分)、口服糖皮质激素(3分)评估,各项评分之和为最终得分。(2)实验室指标。于用药前和用药后采集患者清晨空腹(>8 h)静脉血3 mL,按3000 r/min离心15 min,分离血清,采用酶联免疫吸附试验检测尘螨特异性IgE(sIgE)、尘螨特异性IgG4(sIgG4)和尘螨总IgE(T-IgE)。采用EP-icsXL型流式细胞仪检测Th1、Th2细胞水平。
1.4 疗效评估标准
用药后,参照《变应性鼻炎特异性免疫治疗专家共识》[7]评估临床治疗效果,鼻塞、流涕、喷嚏等症状完全消失,TNSS减分率≥66%,半年内未复发评为显效;患者症状较用药前明显缓解,TNSS减分率为26%~65%,随访半年发现无复发评为有效;患者症状与治疗前相比,无改变或加重,TNSS减分率≤25%,随访半年,发现复发。总有效率=[(显效例数+有效例数)/总例数]×100.00%。TNSS减分率=[(用药前总分-用药后总分)/治疗前总分]×100.00%。
1.5 统计学方法
本次研究数据均由SPSS 23.0统计学软件处理。符合正态分布的计量资料以(±s)表示,经t检验,组间及组内数据比较分别采用独立样本t检验及配对t检验;计数资料以[n(%)]描述,两组间比较用χ2检验或校正χ2检验。检验水准α=0.05。以P<0.05提示有统计学差异。
2 结果
2.1 两组TNSS和TMS评分对比
两组患者用药前TNSS评分、TMS评分相当(P>0.05); 用药后,两组TNSS评分、TMS评分降低,且与对照组比较,观察组各项评分减少更明显(P<0.05),见表1。
表1 两组患者用药前和用药后TNSS、TMS评分对比(±s,分)
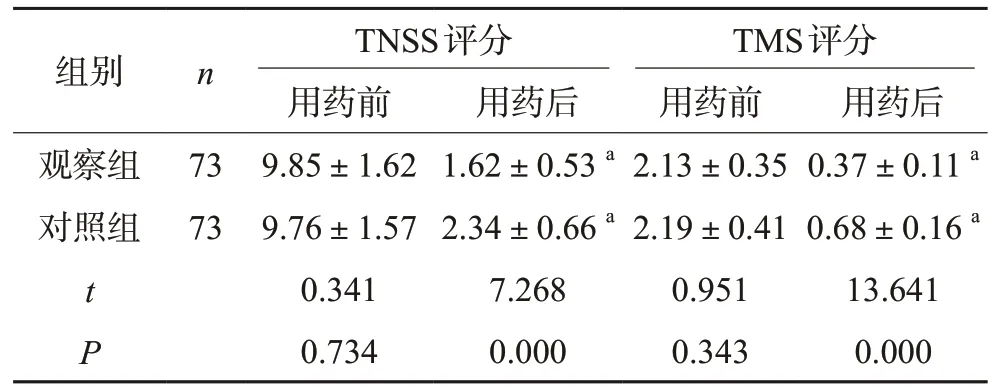
表1 两组患者用药前和用药后TNSS、TMS评分对比(±s,分)
注:与同组用药前比较,aP<0.05
组别 n TNSS评分TMS评分用药前 用药后 用药前 用药后观察组73 9.85±1.62 1.62±0.53 a 2.13±0.35 0.37±0.11 a对照组73 9.76±1.57 2.34±0.66 a 2.19±0.41 0.68±0.16 a t 0.341 7.268 0.951 13.641 P 0.734 0.000 0.343 0.000
2.2 两组免疫球蛋白水平水平对比
两组患者用药前的sIgE、sIgG4及T-IgE水平相近(P>0.05);用药后复检,两组患者的sIgE和T-IgE水平降低,sIgG4水平升高(P<0.05),且与对照组相比,观察组各项指标改善情况更明显(P<0.05),见表2。
表2 两组患者免疫球蛋白指标水平对比(±s)
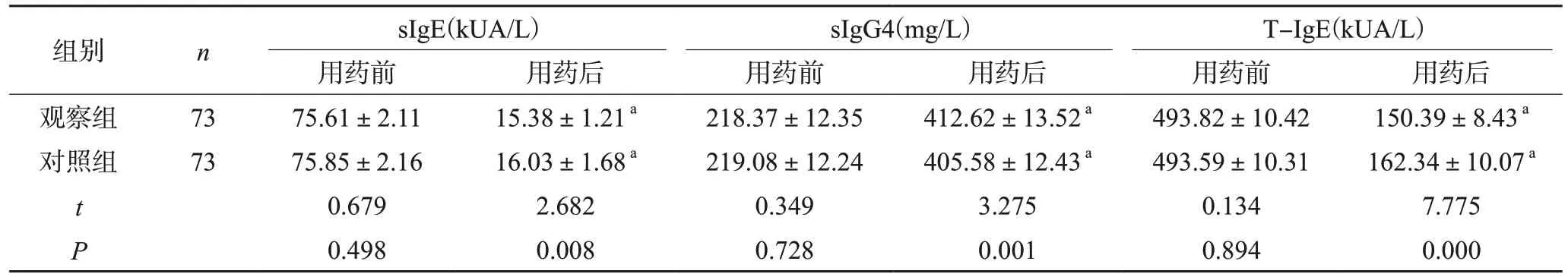
表2 两组患者免疫球蛋白指标水平对比(±s)
注:与同组用药前比较,aP<0.05
组别 n sIgE(kUA/L)sIgG4(mg/L)T-IgE(kUA/L)用药前 用药后 用药前 用药后 用药前 用药后观察组 73 75.61±2.11 15.38±1.21 a 218.37±12.35 412.62±13.52 a 493.82±10.42 150.39±8.43 a对照组 73 75.85±2.16 16.03±1.68 a 219.08±12.24 405.58±12.43 a 493.59±10.31 162.34±10.07 a t 0.679 2.682 0.349 3.275 0.134 7.775 P 0.498 0.008 0.728 0.001 0.894 0.000
2.3 两组Th1/Th2细胞水平对比
两组患者用药前的Th1、Th2细胞水平对比,无明显差异(P>0.05);用药后复检,两组患者的Th1降低,Th2细胞水平下降(P<0.05),且与对照组相比,观察组Th1、Th2细胞水平改善更明显(P<0.05),见表3。
表3 两组患者Th1/Th2细胞水平对比(±s,%)
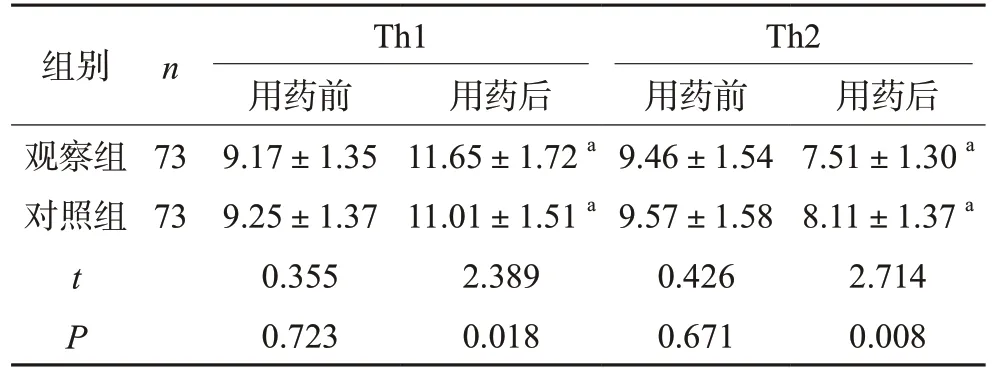
表3 两组患者Th1/Th2细胞水平对比(±s,%)
注:与同组用药前比较,aP<0.05
组别n Th1 Th2用药前 用药后 用药前 用药后观察组73 9.17±1.35 11.65±1.72 a 9.46±1.54 7.51±1.30 a对照组73 9.25±1.37 11.01±1.51 a 9.57±1.58 8.11±1.37 a t 0.355 2.389 0.426 2.714 P 0.723 0.018 0.671 0.008
2.4 两组总有效率对比
两组总有效率对比,观察组高于对照组(91.78%比82.19%,P<0.05),见表4。
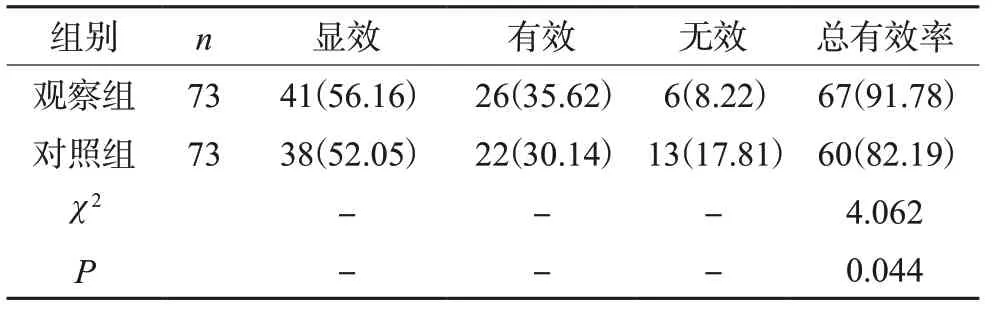
表4 两组患者临床治疗效果对比[n(%)]
3 讨论
过敏性鼻炎是一种以鼻腔黏膜Th2免疫反应为主的变应性炎症反应,其免疫病理学特征以组织中Th2细胞因子过量表达为主。尘螨是该症主要致敏源,相关调查研究显示,过敏性鼻炎患者变应原皮肤点刺试验尘螨阳性率高达70%[8]。而该类患者,在实际生活中无法彻底避免与致敏源接触,传统药物治疗虽能缓解疾病症状,但难以彻底阻断疾病发展,且停药后易复发,整体疗效不甚理想。ASIT是对过敏患者使用针对性过敏原制剂进行反复、逐渐加量刺激,诱导患者脱敏或能耐受过敏原,最终起到缓解过敏症状,遏制疾病进展的一种治疗方式[9]。其优点在于减少患者对药物的依赖,且能在ASIT终止后几年内不复发,现已成为治疗过敏性疾病的可靠方法,但其确切作用机制尚不明确。
氯雷他定为组胺H1受体拮抗剂,常用于过敏性鼻炎的治疗,该药能选择性抑制组胺H1释放,以及肥大细胞分泌白三烯作用,该药可作用于毛细血管,通过将其血管壁通透性缓解过敏性鼻炎相关症状。盐酸氮卓斯汀鼻喷剂是一种新型长效抗过敏化合物,其具备H1受体拮抗剂特点,该药能抑制过敏反应中的白三烯、5-羟色胺、组胺等化学介质的合成及释放,发挥抗过敏作用。针对过敏性鼻炎患者,内服枸地氯雷他定片,外用盐酸氮卓斯汀鼻喷剂喷鼻,可起到内外协同作用,缓解症状。但该治疗方案存在一定局限性,如药物不良反应,停药后复发率高等。研究认为,ASIT是目前唯一一种通过调节免疫机制以此阻断变应性疾病自然进行,继而实现对因治疗的方法[10]。畅迪粉尘螨滴剂是一种特异性免疫治疗类药物,其主要成分为粉尘螨疫苗,通过舌下含服吞咽方式给药,给药剂量按照依次递增直到最大剂量后维持治疗,通过刺激机体对变应原的免疫反应,使Th1、Th2细胞水平处于平衡状态,诱导B细胞分泌阻断性抗体;同时还能抑制炎症递质及细胞因子释放,促使机体产生免疫耐受,降低变应原速发或迟发性反应,最终发挥治疗作用,并在停药后仍能持续产生远期治疗作用。孙熙燕等[11]结果显示,在单纯抗过敏药物治疗基础上,联合SLIT治疗能进一步缓解变应性鼻炎伴过敏性咳嗽患者的鼻部和咳嗽症状,同时能显著改善生活质量。李蕾等[12]在研究舌下含服粉尘螨滴剂治疗变应性鼻炎的疗效中发现,其治疗总有效率达89.62%,患者治疗后症状及生活质量较治疗前显著改善,且治疗过程中未见严重不良反应,疗效肯定,安全可靠。本研究结果表明,两组用药后TNSS和TMS评分均较用药前明显降低,且观察组各项评分明显低于对照组,提示在药物治疗基础上联合SLIT治疗过敏性鼻炎患者有效,且能进一步减轻鼻部症状。
本研究中,观察组用药后sIgE、T-IgE和Th2细胞水平明显低于对照组,sIgG4和Th1细胞水平明显高于对照组。过敏性鼻炎是一种由IgE介导的速发型变态反应性疾病,多数学者认为多种原因所致的免疫调控失衡与该症发病相关,表现为Th1、Th2免疫失衡,继而出现以鼻腔黏膜Th2为主的变态反应性炎症。IgE在过敏性鼻炎发病中发挥着关键作用,其能一定程度反映机体致敏状态,通过检测过敏原的sIgE可明确过敏原,为临床诊疗提供依据。梁灼萍等[13]通过分析过敏性鼻炎患者sIgE和T-IgE阳性率及其水平发现,患者sIgE阳性率为80.04%,T-IgE阳性率为75.05%,且血清sIgE和T-IgE水平呈高表达。SIgG4能对IgE介导的嗜酸性粒细胞及肥大细胞释放的炎性介质起到阻断作用,同时通过抑制过敏原-IgE复合物与B细胞表现的受体结合而阻止了B细胞将过敏原呈递给特异性T细胞,从而缓解过敏性鼻炎症状。在常规用药基础上,加用SLIT治疗,通过诱导机体生成特异性IgG(sIgE、SIgG4、T-IgE)类循环抗体,并与过敏原结合,通过阻断致敏源与肥大细胞表面IgG作用,最终抑制I型超敏反应,发挥治疗作用。本研究显示,联用SLIT治疗观察组患者的sIgE、T-IgE和Th2细胞水平降低更明显,sIgG4和Th1细胞水平升高更明显,证实SLIT治疗能进一步改善患者免疫球蛋白水平,维持Th1、Th2平衡。本研究中,观察组治疗总有效率显著高于对照组,进一步肯定了SLIT治疗过敏性鼻炎的疗效。孙楚东等[14]研究亦证实,SLIT在单一和多重变应原过敏的过敏性鼻炎患者均有效,且二者疗效相当,本研究结果与其结论相符。
综上所述,针对过敏性鼻炎患者,采用SLIT治疗能明显改善症状,疗效肯定,其作用机制可能与调节免疫机制,维持Th1/Th2细胞平衡有关。
