废旧锂离子电池钴酸锂正极材料回收研究进展
2022-11-28曹远鹏张艺博段建国
曹远鹏,张艺博,段建国,董 鹏
(昆明理工大学冶金与能源工程学院,云南昆明 650221)
20世纪以来,随着全球工业化水平的不断提高,全球环境问题不断凸显出来,气候变化、臭氧层破坏、温室效应、资源浪费等问题已经愈发受到国际组织以及各国政府的关注。新能源产业成为应对环境问题的重要举措,近年来,随着各国政府对其大力支持,锂二次电池产业得到了强有力的发展。2021年,我国钴酸锂正极材料产量为10.1万t,相比2020年增长36.8%。钴酸锂电池广泛应用于3C产品、智能穿戴、无人机航拍、启动电源和汽车领域,然而,锂离子电池寿命一般为3~5年,随着其大规模的应用,退役的钴酸锂正极材料电池如何处理成为迫在眉睫的问题。据EVTank联合伊维经济研究院发布的《中国废旧锂离子电池回收拆解与梯次利用行业发展白皮书(2022年)》指出,2021年中国理论废旧锂离子电池回收量高达59.1万t,其中废旧动力电池理论回收量为29.4万t,3C及小动力废旧锂离子电池理论回收量为24.2万t,其他相关的废料理论回收量为5.5万t。EVTank在白皮书中预计2026年中国理论废旧锂离子电池回收量将达到231.2万t。据统计,随着新能源产业深入发展,2019年全球锂离子电池回收市场规模约为15亿美元,预计在2025年这一数据将增至122亿美元,年均复合增长率超过50%,潜在的回收价值巨大[1]。
随着我国不断出台相关环境保护治理政策,环保压力与日俱增。相关研究人员愈发重视开发合适的锂离子电池处理技术和电池部件的回收利用技术,特别是针对地壳中储量较低的元素(如Co、Li等元素)。Fan等[2]在近些年对废旧锂离子电池回收的研究方向进行了高度概括,提出3R策略和4H原则,即再设计、再使用、再循环策略和高效、高经济收益、高环境效益、高安全性能原则。
锂离子电池的总造价很大程度取决于正极材料,因此合理、高效地回收废旧电池中的正极材料具有巨大的潜在经济价值。目前针对废旧锂离子电池正极材料的回收工艺正在被逐步完善,改良后的回收工艺可以使整个回收体系在趋近零污染的情况下具有更加可观的经济效益,本文总结了近年来几种主流的废旧钴酸锂正极材料回收工艺,并对其优劣做出对比。
1 废旧钴酸锂回收的主要工艺
LiCoO2在锂离子电池市场中占据了非常大的比例[3]。因此,随着新能源产业的不断发展,LiCoO2的退役量也会随之增加。同时,考虑到Co是一种稀有元素,具有潜在的经济价值,但处理不当会对环境有不利影响,所以提出一些有效的方法来回收和再生废弃的LiCoO2极为重要。关于从废旧LiCoO2中再生LiCoO2正极材料的相关研究已经开展了许多。按照回收结果分为两大类,回收“元素”和回收“材料”。回收“元素”,即将废旧钴酸锂正极材料通过一系列回收工艺处理后得到的回收产品是含有价金属的离子化合物(如Co3O4、CoO、CoCO3等)。回收“材料”,即废旧钴酸锂正极材料经回收工艺处理后得到的回收产品是可用于直接装配电池的再生正极材料(如LiCoO2、LiNixCoyMnzO2等)。
废旧钴酸锂正极材料回收的主要工艺路线有3种:①湿法冶金工艺,将废旧钴酸锂电池的正极材料进行粉碎并煅烧,然后经过碱浸、酸浸以及萃取等工艺得到有价金属化合物;②火法冶金提取金属元素工艺,主要是在高温熔融状态下通过添加碳还原剂获得有价金属合金,然后结合湿法工艺对其进行分离;③直接再生正极材料工艺,主要是通过添加一定的元素以及包覆材料对混合浆料进行焙烧,在修复废旧正极材料的晶体结构的同时对其进行改性,使得到的再生正极材料满足电池的再次装配要求。
2 湿法工艺回收废旧钴酸锂正极材料
为实现回收为含有价金属的离子化合物产品,一般采用湿法冶金的方法。湿法冶金处理的机理是将预处理过的正极材料中有价金属浸出并在溶液中呈离子形态,然后进行金属离子分离,生成金属盐或其他产品。因此,各种有价金属从废旧正极被浸出到溶液中是湿法冶金过程的关键步骤,因为只有在溶液状态下才能方便地实现后续的分离回收。根据浸出剂的不同,浸出工艺可分为无机酸浸出、有机酸浸出、氨浸出和生物浸出。浸出速率(浸出过程的反应动力学)、浸出效率(浸出液中离子含量与原废旧正极中该离子总量的比值)、环境友好性、经济价值、回收效率是评价一种回收体系的重要指标。浸出后还需经过分离过程提取有价金属,并进行材料合成才能得到再生正极材料。
湿法工艺的一般流程如图1所示。
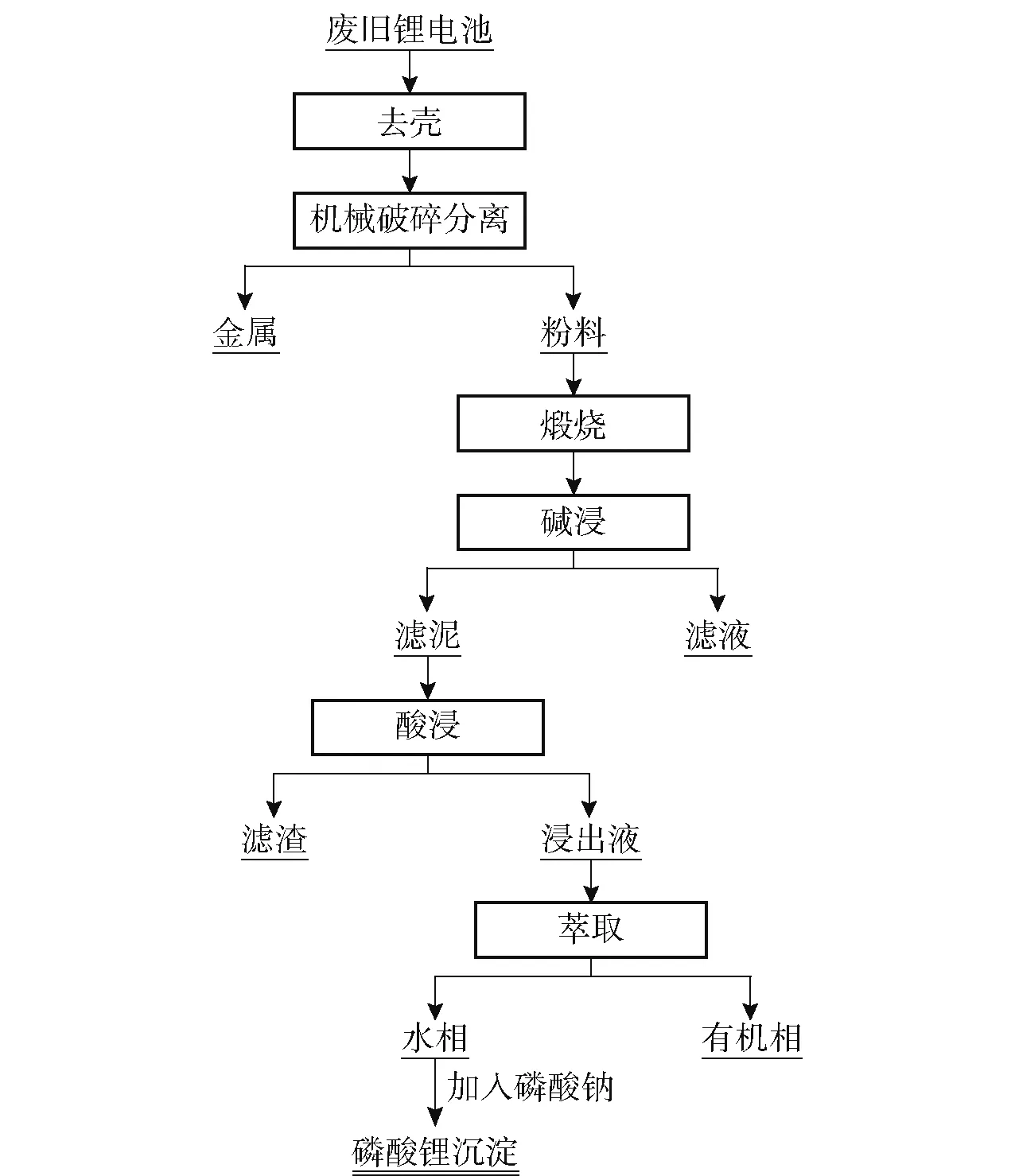
图1 湿法工艺处理废旧锂电池流程简图Fig.1 Flow chart of hydrometallurgy process treating waste lithium battery
2.1 浸出过程
浸出过程主要分为无机酸浸出、有机酸浸出、氨浸出以及生物浸出4种浸出工艺。
2.1.1 无机酸浸出
无机酸浸出是传统浸出方法,浸出效率高。常用的无机酸有HCl、H2SO4、HNO3和H3PO4。Tao等[4]在反应没有还原剂的条件下采用酸浸来对LiCoO2正极材料进行处理,来实现锂和钴的选择性回收,在最佳工艺条件下,锂浸出率为87.9%,钴浸出率为99.1%,并采用蒸发结晶法制备碳酸锂和硫酸钴。
表1展示了不同无机酸浸出剂以及无机酸配合氧化剂浸出对LiCoO2正极材料的回收效果。大量研究表明,采用无机酸对废LiCoO2电池进行全组分回收是一种经济、高效的方法。

表1 不同无机酸浸出LiCoO2正极材料结果Table 1 Leaching results of LiCoO2 cathode materials by different inorganic acid
另外,在无机酸浸出过程中也可采用机械化学方法强化浸出,其主要操作是使用高能球磨来促进正极材料粉末和试剂(如螯合试剂)之间的反应使正极材料颗粒尺寸减小、比表面积增加、晶体结构发生畸变,出现各种缺陷,由于在机械力的作用下晶体结构以及表面状况发生明显改变,其物理化学性质也发生了明显的改变,比如溶解度升高、表面能升高等等,从而提高化学反应活性。屈莉莉等[9]以石英为助磨剂与LiCoO2共同研磨,采用机械化学法提高废弃锂离子电池中Co和Li的浸出率,在SiO2与Li-CoO2质量比为1∶1、在研磨转速500 r/min、研磨时间30 min的条件下LiCoO2转化为无定形态,其反应活性大大提升,在该条件下,Co和Li在柠檬酸中的浸出率分别达到94.91%和97.22%,有效地从Li-CoO2中回收了Li和Co元素。
2.1.2 有机酸浸出
无机酸浸出虽然具有优良的浸出性能,但由于副反应产品较多,不可避免地会带来严重污染问题。而有机酸由于其原料丰富、易降解,成为一种较为理想、环境友好的浸出剂,并得到了广泛的应用。虽然有机酸的酸度较无机酸低,但有些有机酸在浸出过程中仍表现出较好的浸出效率,其能使有价金属阳离子与阴离子形成配合物,使溶液中的金属离子更加稳定。
表2展示了不同有机酸浸出剂对LiCoO2正极材料的浸出效果。大量研究指出,虽然实验室规模的有机酸浸出具有较好浸出性能。然而,由于有机酸的价格相对较高,对其复杂的浸出机理认识还不成熟,因此在工业规模上有机酸实际应用还有待进一步探索。

表2 不同有机酸浸出LiCoO2正极材料结果Table 2 Leaching results of LiCoO2 cathode materials by different organic acids
2.1.3 氨浸出
该方法的独特优势在于NH3的螯合特性,氨浸出后的产物为螯合物,NH3在目标金属(Li、Ni、Co)和非目标金属(Fe、Mg、Al、Mn)之间具有选择性浸出的效果[14],NH3浸出Ni、Co、Mn的化学反应方程式见式(1)~(3)。

可以利用NH3选择性浸出金属离子来分离Ni2+、Co2+和Mn2+离子。虽然过渡金属具有非常相似的性质,但氨化剂更容易溶解Ni2+和Co2+离子,而不是Mn2+离子。图2为Co-NH3·H2O系E-pH图,由图可以看出,当Co离子浓度在不是过高的水平下,[Co(NH3)n]2+配合物在7.5~11.0的pH值范围内均有较好的稳定性。值得注意的是,氨浸出是一种很有前途的闭环回收方法,使用过的浸出剂中的氨可以通过氨蒸馏回收再利用,该工艺具有独特的环境友好性[15]。
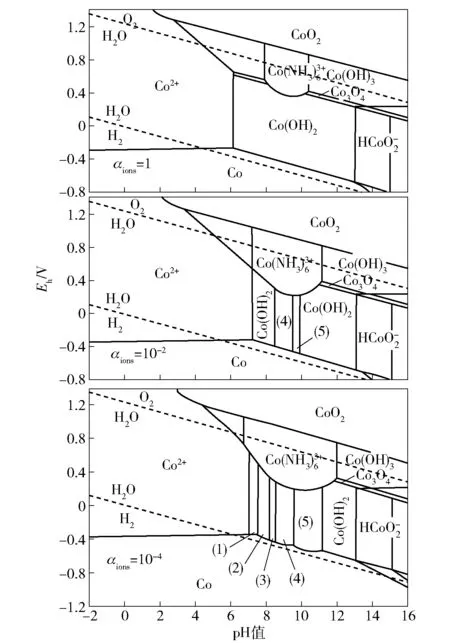
图2 标准状态(101.325 kPa,25℃)下Co-NH3-H2O系E-pH图[16]Fig.2 E-pH diagram of Co-NH3-H2O system in standard state(101.325 kPa,25℃)
Wang等[14]通过研究退役三元正极材料中有价金属在不同还原剂和缓冲溶液体系下的浸出行为差异,详细分析了氨浸出过程中的不同机制,发现在不额外加入缓冲溶液的情况下,还原剂对三元材料中的金属浸出有促进作用,但是添加亚硫酸铵作为还原剂时Al溶解受到抑制,但是促进Al以外其他金属的溶解。通过对NH3-(NH4)2CO3-Na2SO3选择性氨浸体系的研究,发现单级浸出可以实现79.1%Li、86.4% Co、85.3% Ni选择性浸出,仅有1.45%Mn进入溶液,多级浸出可以实现98.4% Li、99.4%Co和97.3% Ni被溶解,由此实现Li、Co、Ni与Mn、Al的有效分离,从而实现有价金属的高效回收。
2.1.4 生物浸出
生物浸出方法利用微生物(如细菌和真菌)的代谢物回收金属,由于其环境友好、成本低廉以及对矿石中微量有价金属元素有较好的富集效果,已被应用于低品位矿浸出的工业化生产,但是在退役锂离子电池回收行业尚在实验室研究阶段。
在生物浸出过程中,首先配制有营养物质、适当pH值和微生物的生物浸出介质。用于生物浸出的微生物主要是嗜酸细菌或真菌。通常,这些微生物会产生酸(例如H2SO4或有机酸),可以溶解金属离子,类似于湿法冶金过程[17]。在金属溶解过程中,生物浸出机制通过3种途径发生,即氧化还原、酸解和复合溶解。生物浸出过程的动力学依赖于:①细菌如何促进氧化还原反应;②细菌产生的代谢物与金属的复合;③与金属底物的结合能力。生物浸出工艺被认为是一种有望取代传统冶金工艺的方法[18]。
目前微生物培养最棘手的问题是细菌在重金属离子丰富的环境中难以繁殖和生存。关于微生物从矿石和废料中提取金属的确切机制仍在争论中。锂、钴、镍、铜和锰等金属以金属单质及其化合物形式存在于LIB中的复合物。微生物需要额外的能量来源,如化石生自养细菌需要铁或元素硫,异养真菌需要额外的碳源(糖)来打破这些元素复合物[19]。
生物浸出一个明显的缺陷是浸出速率低,通常需要数天才能完成,限制了其工业化推广应用。为了提高浸出率,Zeng等[20]通过研究发现Cu离子可以加快Co的浸出速率。在无Cu离子时,经过10 d Co的浸出率只有43.1%,但是添加0.75 g/L的Cu离子后,经过6 d,Co的浸出率已经达到了99.9%;同样在添加Ag离子后也可以提高Co的浸出率,仅需要添加0.02 g/L的Ag离子,经过7 d,Co的浸出率可以提升到98.4%。
2.1.5 机械化学法浸出
机械化学法被应用于正极材料的前处理,其使用高能球磨来促进阴极粉末和试剂(如螯合试剂)之间的反应,反应过程中正极材料颗粒尺寸减小、比表面积增加、晶体结构发生畸变,出现各种缺陷。由于在机械力的作用下晶体结构以及表面状况发生明显改变,其物理化学性质也发生了明显的改变,比如密度减小、溶解度升高、表面能升高、熔点降低,因此,金属萃取过程所需的活化能降低,正极活性物质与浸出试剂之间的反应活性增加。该方法有利于提高金属离子的浸出效率,降低酸耗[21]。
屈莉莉等[9]以石英为助磨剂与LiCoO2共同研磨,采用机械化学法提高废弃锂离子电池中Co和Li的浸出率。在SiO2与LiCoO2质量比为1∶1、研磨转速500 r/min、研磨时间30 min的条件下,LiCoO2转化为无定形态,其反应活性大大提升,Co和Li在柠檬酸中的浸出率分别达到94.91%和97.22%,有效地回收了Li和Co元素。
2.2 分离过程
废旧钴酸锂正极材料经过浸出后,金属离子分离过程是决定回收材料纯度的关键性步骤,该阶段的方法主要为沉淀法、萃取法、溶胶-凝胶法。
1)沉淀法。沉淀法是向浸出液中加入沉淀剂使Li、Co金属离子发生选择性沉淀,进而提取有价金属离子。该过程中需要控制适当的温度以及pH值,来保证回收离子高效沉淀同时避免杂质离子的沉淀。邹海凤等[22]通过在含有Li+、Cu2+、Ti4+、Zr4+、Co2+、Ni2+、Mn2+、Fe2+等元素的浸出液中加入Na2S使Cu2+沉淀,随后加入NaClO3使Fe2+氧化为Fe3+,进而加入NaOH控制pH=5.0,使Ti4+、Zr4+、Fe3+去除率达到98%以上,最后得到的镍钴锰盐溶液,可用于重新制备正极材料。但是这种方法在生产过程中使用大量的H2SO4、NaOH等强酸强碱来控制pH值使金属元素溶解与沉淀分离,产生大量的三废,增加了后续处理难度。
2)萃取法。萃取法是通过向浸出液中添加有机溶剂,使待回收有价金属进入有机相后进行萃取、反萃取,并调节pH值回收金属。对于简单成分的正极材料LiCoO2,通过萃取法可较容易从该材料的浸出液中分离提取有价组分。徐军等[23]采用P204萃取剂对含Co2+、Cu2+、Mn2+、Ni2+的水溶液中的Co2+以及Ni2+进行提纯,当P204的皂化率为20%时,第一次萃取pH值控制在2.7,第二次萃取pH值控制在2.5时,溶液中残留的Cu2+、Mn2+浓度为0.006 μg/mL,接近ICP检出限,得到了仅含Co2+、Ni2+的水溶液,但是这种方法流程较为冗长,且萃取剂需要进行反萃之后才可以回收利用,产能较低。
3 火法冶金回收废旧钴酸锂正极材料
火法冶炼回收是一种高温冶炼工艺,是指在高温条件下,利用燃料燃烧、原料自身的潜热、电能产生的热以及某种化学反应放出的热,使含有价金属的原料经历一系列物理化学变化,令其中的金属与其他杂质分离的过程。其主要工艺流程包括废旧电池破碎、还原焙烧、渣金分离、合金材料的分离等工序,具体流程如图3所示。
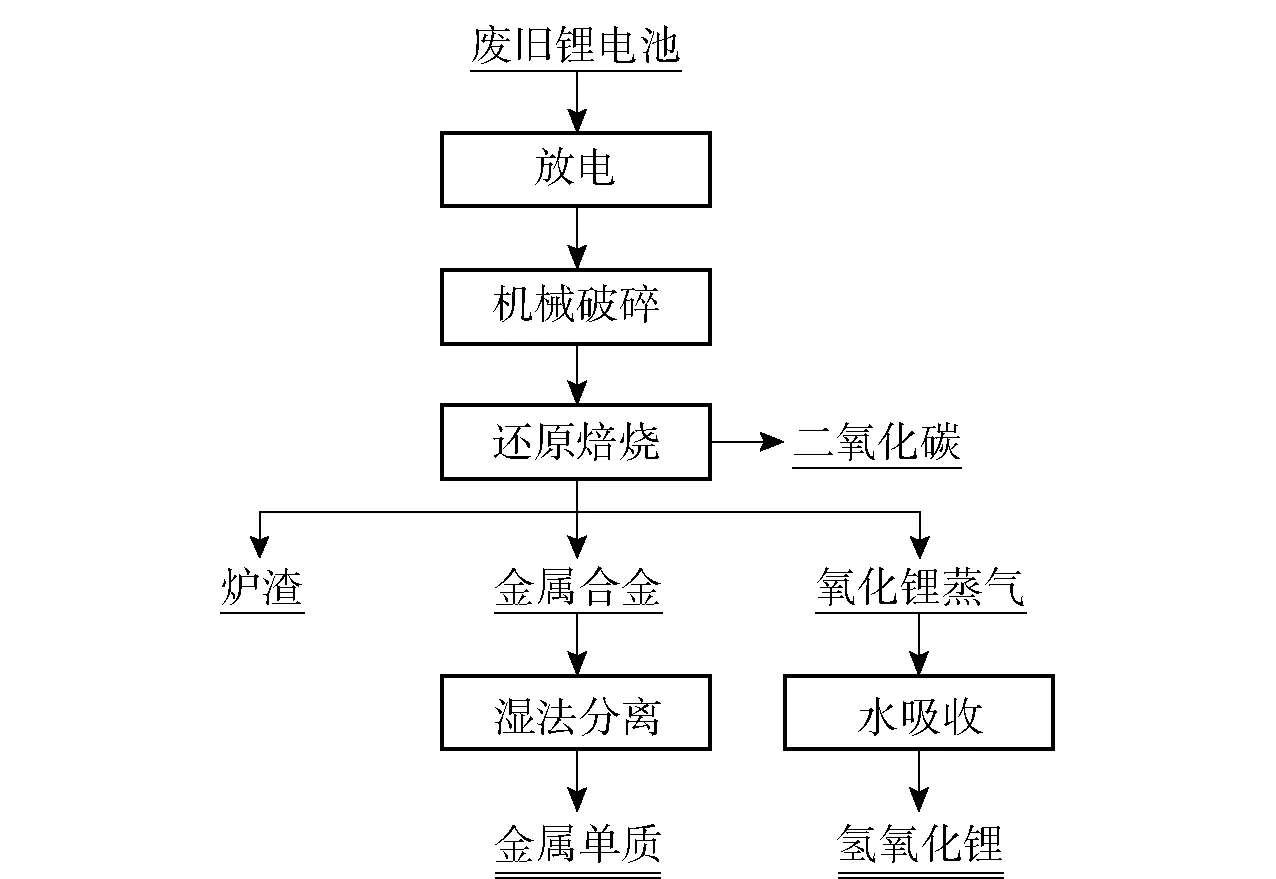
图3 火法工艺处理废旧锂电池流程简图Fig.3 Flow chart of pyrometallurgy process treating waste lithium battery
1)电池破碎。将充分放电的锂离子电池进行机械破碎,得到50目左右的小颗粒物料。
2)还原焙烧。钴酸锂电池在熔炉中焙烧,通过添加碳还原剂,将有价金属Co、Cu等还原为金属合金,有机物以及电池壳在该过程中被氧化燃烧,可为反应体系提供一定的能量,而Li无法被还原,大部分以氧化物的形式挥发并被收集,少量Li残留在炉渣中,可以通过附加工序进行回收。
3)合金材料分离。根据Cu、Co、Al等金属元素化学性质的差异,采用湿法工艺,首先将其酸溶,随后通过控制电位、pH值对其进行分离或者通过以上萃取工艺对其进行分离。陈亮[24]等通过在含有Al3+、Cu2+、Fe2+、Mn2+等杂质离子的钴酸锂浸出液中加入碳酸氢铵使Al3+和Cu2+水解沉淀,随后采用次氯酸钠使Fe2+和Mn2+氧化为高价而水解沉淀,在此过程中不断加入NaOH以中和生成的H+,最后得到的浸出液中Fe浓度为0.006 g/L,Cu、Al以及Mn浓度低于0.005 g/L,而Co的损失率仅为1.2%,从而使杂质离子得到高效去除,在此期间发生如下化学反应:
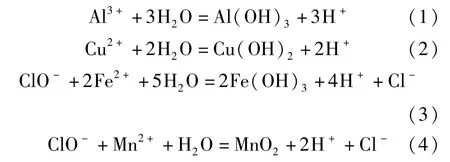
由于便携式电子产品中使用的锂盐中钴含量高,迄今为止,火法冶金工艺已经产生了相对成功的产业模式。然而,随着电动汽车电池钴含量越来越低,该产业模式的吸引力将会下降。火法冶金工艺的主要优点是:①工艺简单而成熟;②无需分选和研磨;③产品为合成多种不同化学性质的新型正极材料的基本构件。主要缺点是:①冶炼过程中产生CO2,能耗高;②合金需要进一步加工,增加了总回收成本;③商业模式可能不适合电动汽车电池,因为Co浓度低。此外,该行业正朝着还原钴或最终无钴正极材料的方向发展。
4 废旧钴酸锂正极材料的直接再生
一般来说,正极材料在长期使用过程中锂的损耗以及结构发生不可逆相变是其失效的主要原因之一。对于一些杂质含量较低的退役锂离子电池,在不破坏其化学结构、不造成二次污染的情况下,通过补锂和焙烧有可能实现材料的直接再生[25]。近些年,为了避免回收工艺较长而引起的三废处理难度大以及经济效益下降等问题,简化流程是解决上述问题最有效的方法。因此,将重心从废旧正极材料中提取金属转移到直接修复废旧材料获取再生正极材料是未来回收体系的发展方向。
直接回收是一种直接收集和回收锂离子电池活性物质,同时保留其原有化合物结构的回收方法。直接回收方法有以下优点:流程短;回收产品无需二次加工;三废排放少,降低了环境污染。直接回收工艺的主要缺点包括:需要严格的分类/预处理;难以保证始终如一的高纯度和纯净的晶体结构。目前的分离技术可能达不到电池行业直接回收严格的标准要求。
在短期内,这种技术更有可能被电池制造商采用,用于回收化学成分已知的电极废料。直接再生技术通常采用固相反应法和水热法。
4.1 固相反应法
固相反应法主要通过测定废旧LiCoO2正极材料各元素含量,随后补充缺少的元素,最后通过高温煅烧直接生成LiCoO2。采用不含酸浸的固相反应法再生LiCoO2正极能够缩短回收路线,简化再生过程,避免酸浸产生的“三废”污染。
YunjianLiu等[26]首先提出了直接从废旧钴酸锂正极材料中再生出LiCoO2的固相反应方法。从含有DMAC的Al箔中分离出LiCoO2,然后通过高温煅烧去除活性材料中的聚偏氟乙烯(PVDF)和碳粉,随后在残留的粉料中加入Li2CO3,调整Li/Co摩尔比为1。在850℃的空气中煅烧12 h合成再生的LiCoO2。再生的LiCoO2首次放电容量为151 mAh·g-1,经过30次循环后,其放电容量仍有141 mAh·g-1。Nie等[27]仔细比较了再生LiCoO2与商用LiCoO2的性能。测试数据表明,在900℃下,再生LiCoO2的放电容量可达152.4 mAh·g-1,表现出优异的物理化学性能,能够满足商用电池的要求。
ErshaFan等[28]提出了一种不需要额外的合成步骤直接通过固相烧结实现废旧LiCoO2的回收方法,通过高温补充Li和Mg掺杂来恢复和提高Li1-xCoO2的层状结构稳定性的实用方法。再生的复合材料与商用正极材料相比,再生产物具有更好的电化学性能。3.0~4.6 V的电压窗口内,放电倍率0.2C下,掺Mg 5%的LiCoO2(LMCO)展现出高放电容量202.9 mAh·g-1,同时掺Mg 3%的LiCoO2显示出更可观的循环稳定性,在0.2C下循环50周期后容量保持率为99.5%,在1C下循环100周期后容量保持率为96.8%。因为高温补充金属离子有利于消除废旧材料表面的裂纹和纳米杂质颗粒,从而恢复层状结构和电化学性能。Mg离子的掺杂抑制了晶格氧的释放,稳定了表面结构,进一步提高再生材料的电化学性能。因此,固相法辅助表面掺杂Mg改性回收LiCoO2具有实际意义。
随着回收技术的不断创新和改良,再生产品的性能也在逐渐提升,同时在简化流程的基础上有价金属的回收率达到100%,这有助于为回收工艺减轻环保压力、提升经济价值,有助于实际应用的推广。
4.2 水热法
LiCoO2再生过程中也可采用水热法。早在2004年,Kim等[29]采用水热法从废LiCoO2电极中再生出LiCoO2正极材料,再生LiCoO2样品的首次放电容量为144.0 mAhg-1。YangShi等[30]通过水热处理和退火联合工艺,开发了一种回收LiCoO2正极材料的新工艺,热液锂化可以部分恢复正极材料的结构,然后再进行退火处理,结构恢复进一步增强。再生LiCoO2正极经过短时间的退火后,结晶度更好,阳离子无序性更少,缺陷更少。水热修复的Li-CoO2在0.1C下放电容量为153.1 mAhg-1,在1C下循环100圈后容量保有率为91.2%,将该结果与通过单独热处理回收的LiCoO2样品进行比较,水热修复的样品显示出优异的倍率性能。
4.3 溶胶-凝胶法
溶胶-凝胶法可以从有机酸浸出过程产生的渗滤液中重新合成正极活性物质,渗滤液中的有机酸同时。作为螯合剂,因此,溶胶-凝胶法不需要额外的螯合试剂,在一定程度上具有经济可行性。溶胶-凝胶法一般是将金属离子比例调整到所需数量后进行合成。最初,金属离子以溶胶态均匀分布;然后,通过水解前驱体混合物,溶胶逐渐转变成凝胶状态;最后,将凝胶经过干燥以及焙烧之后可获得固态的正极材料粉末。张飞等[31]通过以柠檬酸为螯合剂,根据浸出液中Co2+和Li+的浓度添加相应的钴源(碱式碳酸钴)或锂源(氢氧化锂),调节锂钴元素浓度比为1∶1。再用NH3·H2O溶液调节浸出液pH值至7.0,在80℃下搅拌直至形成溶胶,然后溶胶在100℃下真空干燥24 h后得到干凝胶。干凝胶通过700℃烧结得到再生Li-CoO2。再生的LiCoO2在3.0~4.2 V的电压范围内首次充放电容量达到128.3 mAh·g-1。
5 结论与展望
随着退役动力锂电池规模的持续扩大,经济安全、高效环保、绿色低碳的电池回收技术亟待开发利用。
1)湿法工艺包括无机酸浸出、有机酸浸出、氨浸出及生物浸出4种浸出工艺。传统无机酸浸出工艺比较成熟,且经济高效,但存在工艺冗长、试剂消耗量大、机理复杂、产生废液量大等问题;有机酸虽然浸出性能较好,但价格相对较高,对其复杂的浸出机理的认识还不成熟,因此在工业规模利用上还有待进一步探索;氨浸出工艺中浸出剂中的氨可以通过氨蒸馏回收再利用,是一种很有前途的闭环工艺;生物浸出由于其成本低廉、环境友好而备受关注,但是目前生物浸出速率较慢且微生物只在低浓度的矿浆中保持较高活性,工业化推广还有很长的路要走;机械化学法被应用于正极材料的前处理,可以使萃取过程所需的活化能降低,有利于提高金属离子的浸出效率。
2)火法工艺适用于处理钴含量高的材料,且在生产过程中会消耗大量的能源,排放大量的CO2,不利于环境保护。退役锂离子电池回收是一个复杂的过程,火法工艺只是其中的一个步骤,经高温处理后,仍需要采用各种物理化学方法进行有价金属分离。随着未来锂离子电池正极材料中有价金属朝着多元化、低成本化方向发展,火法工艺势必会与湿法工艺相结合,在节能环保、增强原料适应性上做出更多努力。
3)直接再生由于其工艺流程简单,回收经济性较高,再生后的材料可直接利用,与其他工艺流程相比,三废产生较少。但是由于该工艺制备的产品性能与退役锂离子本身状态密切相关,对原料杂质含量要求较高,且在工业生产中需要严格将相同或者相近成分的原料预分类,不适用于处理不同类型正极材料的混合废料,从而对其工业化带来较大挑战,因此该工艺在原材料的适应性与杂质的分离上需要做出更多的努力。
