巯基功能化纤维素气凝胶材料的制备及其对Cr(Ⅲ)的吸附
2022-11-28杨文玲张鹏瑞李虎林邸博洋郭清华崔洪誉
杨文玲,张鹏瑞,李虎林,邸博洋,郭清华,崔洪誉
(河北科技大学化学与制药工程学院,河北石家庄 050031)
制革废水中Cr(Ⅲ)难以得到有效处理,是制约制革行业可持续发展的根本原因,制革工业中大多以碱式硫酸铬作为鞣剂,主要成分为Cr(Ⅲ),但利用率只有30%~70%[1],剩余大量的Cr(Ⅲ)和微量的Cr(Ⅵ)进入到制革废水中,在氧化剂的存在下,Cr(Ⅲ)会转化为Cr(Ⅵ),Cr(Ⅵ)的毒性是Cr(Ⅲ)的100倍以上,具有很强的致癌致畸变性。按照《制革及毛皮加工工业水污染物排放标准》(GB 30486—2013)规定[2],废水中总铬的排放质量浓度不得超过1.5 mg/L,六价铬的排放质量浓度不得超过0.2 mg/L。目前,国内外研究人员已经对制革废水中Cr(Ⅲ)的去除做了许多工作,主要采用化学沉淀法、离子交换法、萃取法、膜分离法、电解法、循环利用法、吸附法[3]等,最常用的加碱沉淀法处理后的废水中仍含有2.0~20 mg/L的Cr(Ⅲ),同时产生大量含铬污泥需进一步处理。以上方法大都存在处理不彻底、处理效果较差、易造成二次污染、运行成本较高等缺点,难以被大规模应用到生产中。其中,吸附法是一种简单高效、费用低廉的处理方法,因此,制备一种廉价高效的吸附材料成为了研究重点。
利用微晶纤维素易构建多孔、质轻、比表面积大的气凝胶材料[4-6]。生活中大量纤维素材料的堆积,也造成了环境污染和资源浪费,且其分子中含有大量羟基,对其进行适当改性,用于吸附重金属,可以达到以废治废的效果。近些年来,大量纤维素吸附材料已被应用到水体重金属的处理[7-9]。SINGH等[10]研究表明,改性纤维素对Cr3+和Cr6+的吸附能力分别达到了62.40%和5.98%,而天然纤维素对Cr3+和Cr6+离子的吸附能力仅为42.02%和5.79%。相比于含O基团,含S基团对重金属离子吸附效果更好[11]。闫荣荣等[12]以废弃茶叶渣为原料,制备纤维素黄原酸酯,用以吸附水中的Cd(Ⅱ),最大吸附容量为45.46 mg/g;其次,Cr(Ⅲ)极易与羟基等基团形成配合物而很少以单一金属离子形式存在,相比于其他,如Cu2+,Pb2+等金属离子更难去除[13]。上述改性纤维素材料多以固体粉末状呈现,导致纤维素材料的再生利用性能不足、应用成本偏高。利用CS2对微晶纤维素进行巯基化改性,制备多孔、比表面积大、易于分离的气凝胶材料的研究鲜见报道。
针对上述问题,本研究以脱脂棉为原料,经过碱处理、酸处理,得到微晶纤维素(MCC),以NaOH/尿素/H2O为溶剂[14],CS2为改性剂,对纤维素分子中羟基进行功能化改性,制备巯基功能化纤维素气凝胶材料(CS2-MCC),以Cr(Ⅲ)为吸附对象,研究CS2-MCC对Cr(Ⅲ)的吸附能力。
1 实验材料与方法
1.1 实验材料
医用脱脂棉;氢氧化钠、尿素、无水硫酸镁、无水乙醇、二硫化碳、二苯基碳酰二肼,均购自天津市大茂化学试剂厂;碱式硫酸铬,购自上海麦克林生化科技有限公司。以上试剂均为分析纯。
1.2 微晶纤维素(MCC)的制备
将脱脂棉剪碎后置于2%(质量分数,下同)的NaOH水溶液中浸泡处理,随后用酸液中和,洗涤、干燥,将其置于8%的硫酸中,于80 ℃下水解2 h,然后用碱液中和,充分洗涤、干燥得到微晶纤维素(MCC)。
1.3 CS2-MCC的制备
将1 g MCC分散于20.25 mL 质量比为7∶12∶81的NaOH/尿素/H2O溶液中,放入冰箱冷冻12 h后取出,在常温下剧烈搅拌至澄清透明的纤维素溶液,在一定温度下,加入一定量CS2溶液,密封反应一定时间后,加入一定量的5% MgSO4溶液反应15 min,转移至24孔细胞培养板,以1% HCl溶液为凝固浴,中和多余的NaOH,使纤维素凝胶化。再用去离子水对纤维素水凝胶进行反复浸泡,置换出剩余的NaOH和尿素分子,使纤维素水凝胶进一步老化,浸泡至中性为止。随后冷冻干燥即可得到CS2-MCC气凝胶材料。图1为CS2-MCC制备流程图。
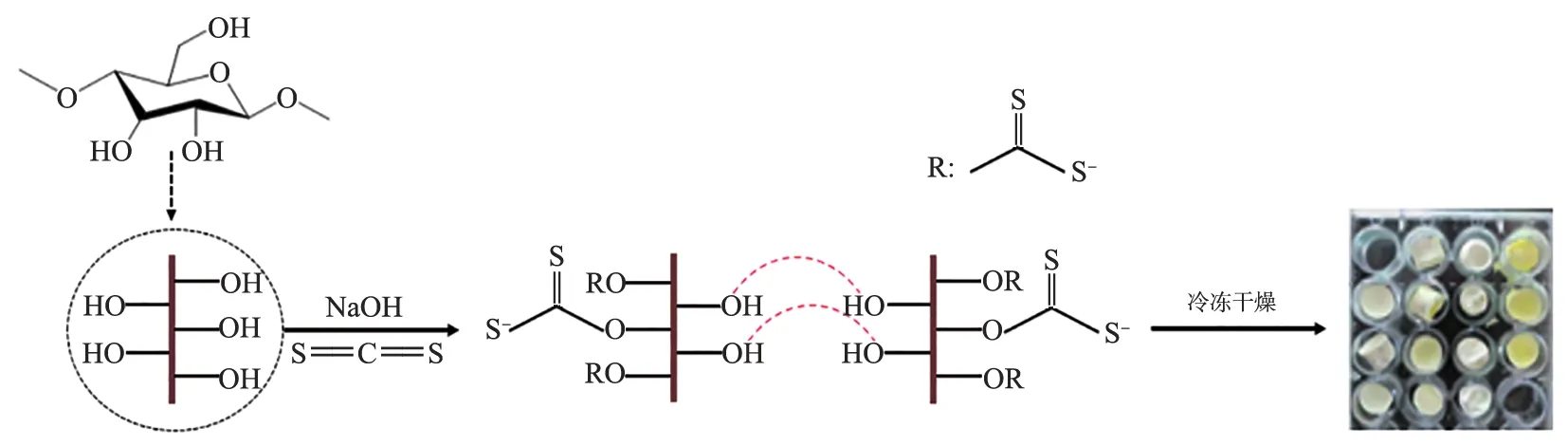
图1 CS2-MCC制备流程图
1.4 吸附实验
(1)
(2)
式中:qt为t时刻,单位质量吸附材料对Cr(Ⅲ)的吸附容量,mg/g;C0与Ct分别为溶液初始Cr(Ⅲ)离子质量浓度和t时刻Cr(Ⅲ)质量浓度,mg/L;V为处理溶液体积,L;M为吸附材料的质量,g;η为去除率,%。
2 结果与分析
2.1 最佳制备条件的确定
2.1.1 单因素实验
对CS2-MCC的制备条件进行优化。以CS2用量、改性温度、MgSO4用量和改性时间为主要影响因素,考察其对Cr(Ⅲ)的吸附能力和材料机械性能的影响。
CS2作为材料制备的关键改性试剂,当用量不足时,无法对纤维素中羟基进行有效改性,当用量过多时又会加剧与NaOH产生的副反应,使CS2的利用率降低。同时,过量的CS2会取代纤维素分子中大多数羟基,使其难以形成气凝胶材料。单因素实验结果如图2所示。由图2 a)可知,当CS2用量为0.6 mL/g时,CS2-MCC对Cr(Ⅲ)的吸附率达到最大。本研究使用万能实验机测定不同CS2用量下所制备的气凝胶材料的压缩回弹性能。实验结果如图2 b)所示,随着CS2用量的增加,气凝胶材料的压缩回弹性能变差,综合考虑对Cr(Ⅲ)吸附能力与压缩回弹性能2个方面,确定当CS2用量为0.5 mL/g时吸附性能最佳。由图2 c)可知,随着温度的升高,CS2-MCC对Cr(Ⅲ)的吸附能力呈现先上升后下降的趋势,当改性温度为40 ℃时,CS2-MCC对Cr(Ⅲ)的去除率最大,为96.47%。升高温度有利于CS2与纤维素分子中的羟基接触,但当温度过高时,CS2气化严重,与纤维素的接触面积反而减少,改性效果变差,且过高的温度也促使CS2与NaOH生成二硫代碳酸钠的副反应加剧,不利于纤维素改性;反应初始生成的是钠离子型[12]黄原酸酯,钠离子极化能力较低,产物稳定性较差,以MgSO4溶液作为稳定剂,使Mg2+和Na+进行交换,生成更稳定的镁离子型黄原酸酯,增强CS2-MCC的稳定性和使用寿命。由图2 d)可知,当MgSO4溶液用量为20 mL/g时,CS2-MCC对Cr(Ⅲ)的吸附能力达到最大,去除率为96.49%。由图2 e)可知,当改性时间大于6 h,吸附率趋于平衡,为节约时间成本,选择6 h为最佳改性时间。
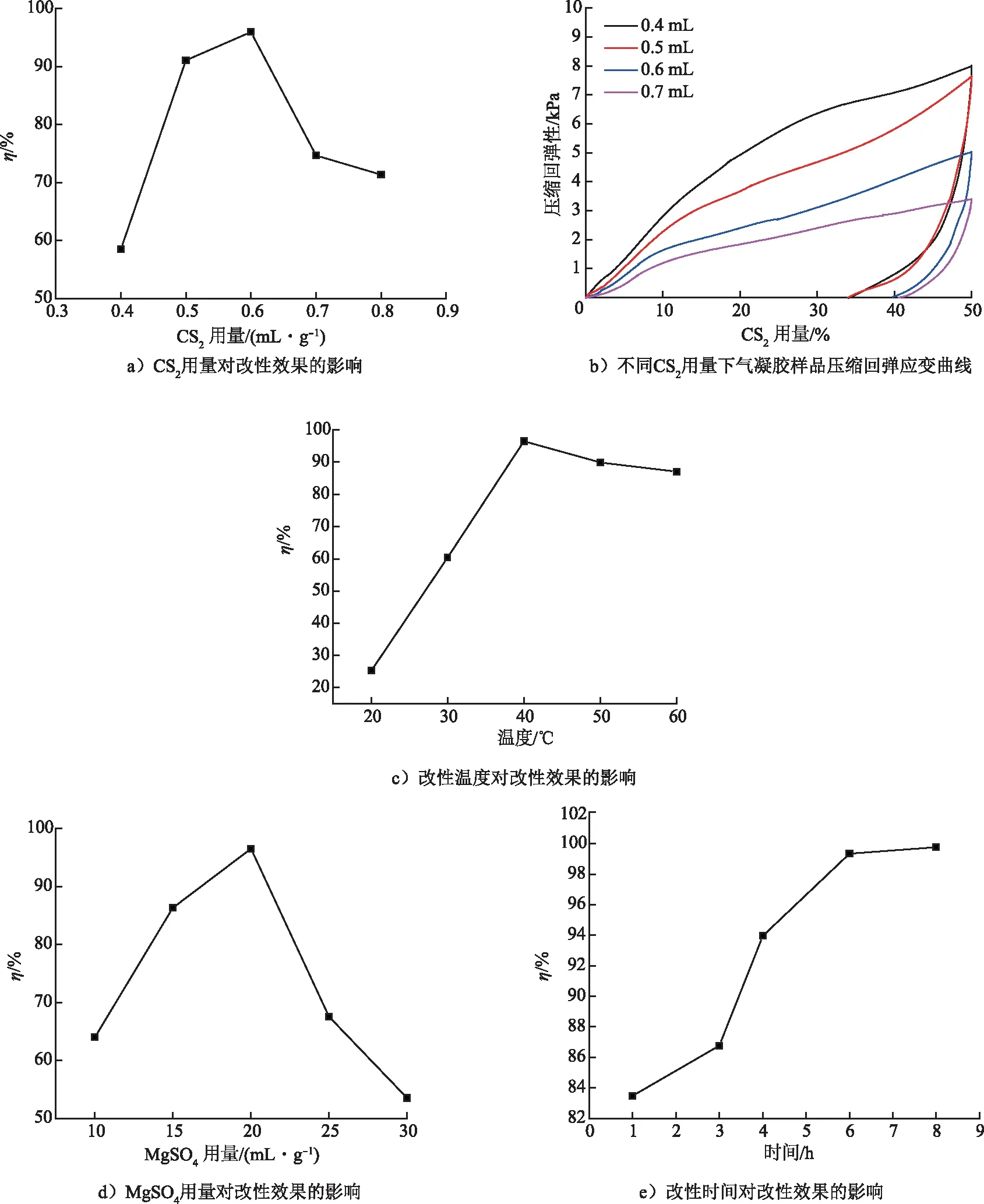
图2 单因素实验结果
2.1.2 正交试验
根据单因素试验得出的结果,确定正交试验的研究范围,设计L9(34)的正交试验,如表1所示。
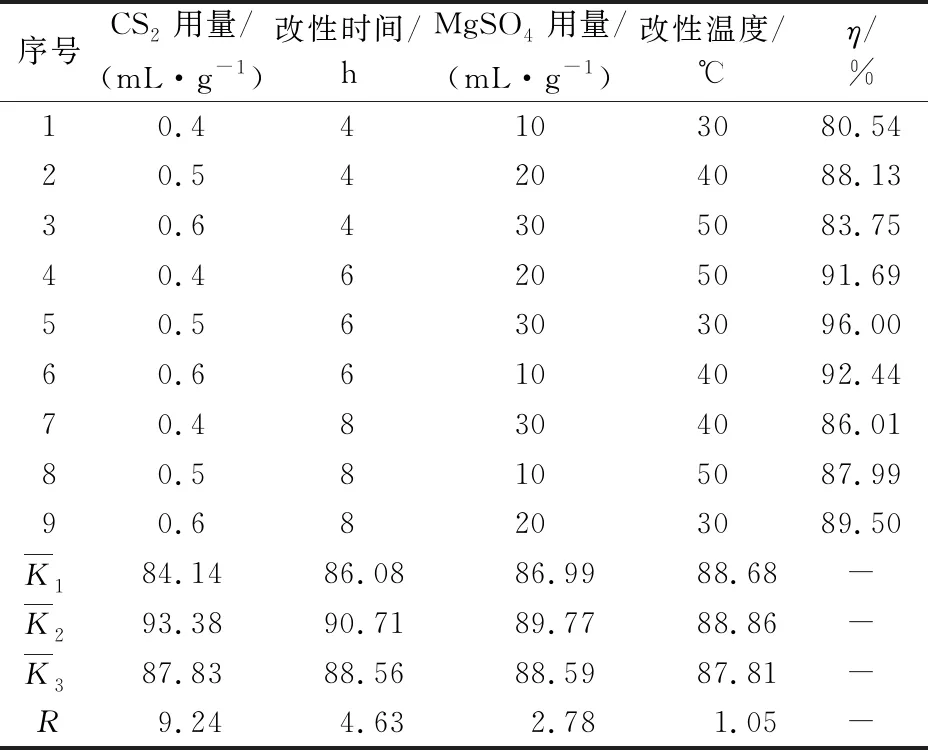
表1 正交试验结果分析
由正交试验得出影响CS2-MCC对Cr(Ⅲ)吸附能力大小的因素依次为CS2用量>改性时间>硫酸镁用量>改性温度。
根据单因素试验与正交试验确定CS2-MCC的最优制备条件为CS2用量为0.5 mL/g、改性时间为6 h、改性温度控制在40 ℃,此外用20 mL,5%的硫酸镁溶液促进稳定。
2.2 材料的表征分析
2.2.1 傅里叶红外光谱分析(FT-IR)
如图3所示,CS2-MCC与MCC均在1 000~1 500 cm-1有尖锐的红外吸收峰,且在3 300~3 450 cm-1出现羟基的伸缩振动峰,在2 924 cm-1出现亚甲基中C-H的伸缩振动峰,在1 630 cm-1出现C-O的伸缩振动峰,这些都是纤维素的特征吸收峰[17],说明经过CS2改性后仍保持纤维素的主要结构,但CS2-MCC分别在1 057 cm-1和2 521 cm-1出现了较弱的吸收峰,对应着C=S和-SH的特征吸收峰,且在844 cm-1处出现了与C-S有关的伸缩振动峰[18],说明经过CS2改性后的纤维素分子链中引入了巯基。
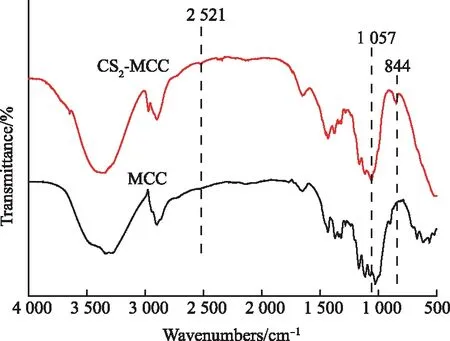
图3 CS2-MCC与MCC红外光谱分析图
2.2.2 X射线能谱分析(EDS)
通过X射线能谱 (EDS)分析了纤维素改性前后各元素的含量以及能谱图。由图4可知,经过CS2改性后的纤维素相比原始纤维素出现了硫元素,占总元素质量的9.3%,结合傅里叶红外光谱分析,说明成功地在纤维素链上引入了巯基,巯基对Cr(Ⅲ)的吸附起主要作用,说明CS2对纤维素改性成功。
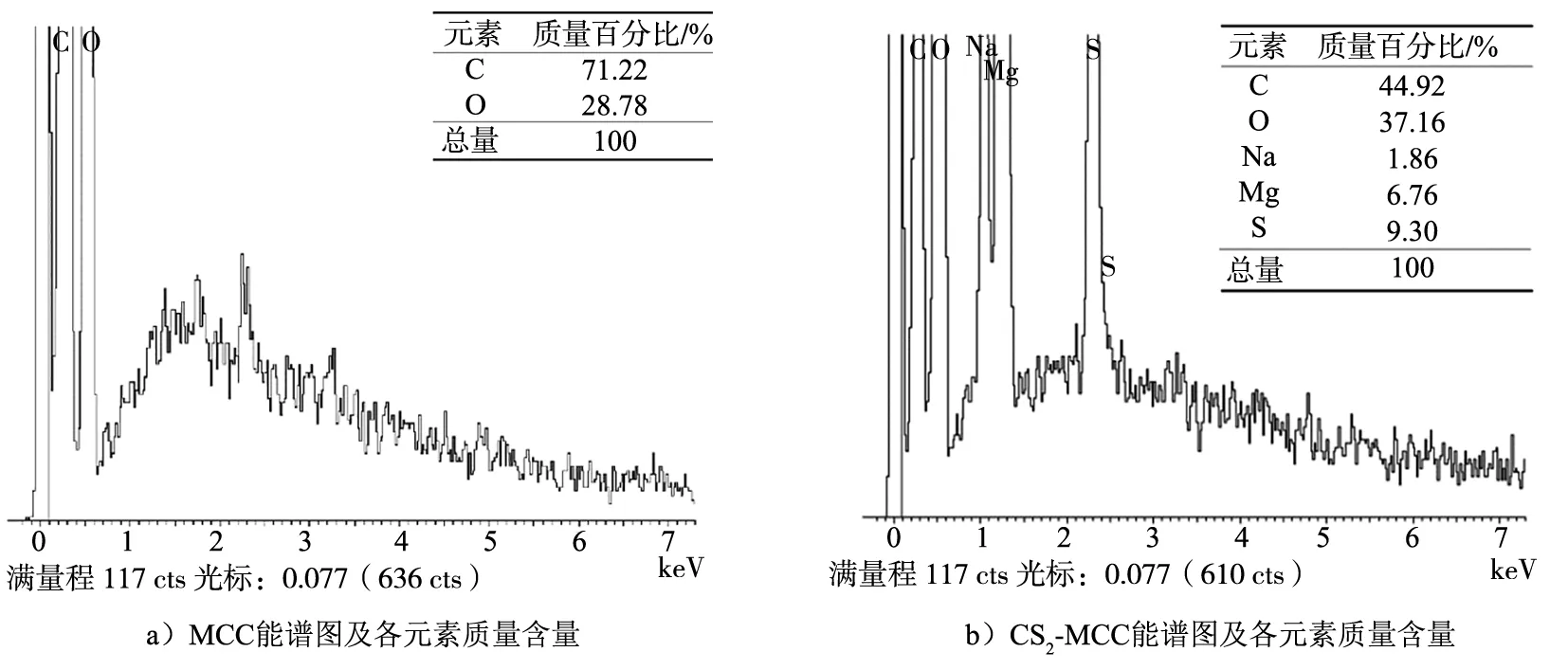
图4 MCC 和CS2-MCC EDS图谱
2.2.3 X射线衍射分析(XRD)
通过X射线衍射仪对改性前后的纤维素内部结构进行分析,如图5所示。纤维素在2θ=16.34°和2θ=22.68°处出现相对吸收强度分别为6 224.7和11 182.8的衍射峰,CS2-MCC在2θ=17.38°和2θ=20.88°处出现相对吸收强度分别为2 373和3 970的衍射峰,相比于纤维素衍射峰强度大幅降低,说明经过CS2改性制得的CS2-MCC结晶度下降,纤维素分子间氢键被破坏,经过凝胶化处理,重新构建为气凝胶材料。

图5 MCC及CS2-MCC的XRD分析结果
2.2.4 扫描电镜(SEM)分析
利用SEM观察纤维素气凝胶和CS2-MCC的表面形貌,结果如图6所示。纤维气凝胶表面形貌如图6 a)和图6 b)所示,纤维素经过凝胶化处理后形成的气凝胶材料呈现多孔结构,但由于纤维素分子中含有大量氢键,导致纤维素气凝胶聚合度较高,孔道结构较少,孔径较小。经过CS2改性,再经纤维素再生后的CS2-MCC表面形貌如图6 c)和图6 e)所示,相对于纤维素气凝胶,CS2-MCC表面形貌发生了巨大变化,表面结构无序性增大,纤维素气凝胶中的氢键被破坏,材料表面出现许多粗糙的鳞片结构,并且相互堆积形成三维网状的多孔结构,含有大量孔径在几百纳米到几微米的孔道结构,极大增加了材料的比表面积,增大了CS2-MCC的吸附活性和吸附能力。
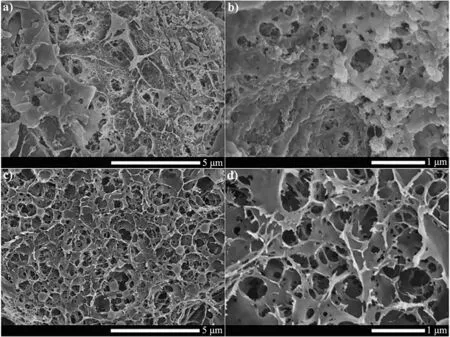
图6 纤维素气凝胶和CS2-MCC 的扫描电镜图
2.2.5 孔隙率与比表面积分析
对干燥彻底的柱状气凝胶样品的质量(m0)进行测定,使用游标卡尺对其半径(r)及高度(h)进行测定,计算其表观密度(ρ0),ρ0计算公式如式(3)所示,进一步通过式(4)计算气凝胶材料的孔隙率,相关物理参数如表2所示。采用比表面积及孔径分析仪对气凝胶材料进行测定,气凝胶的氮气吸附-脱附曲线及孔径分布曲线如图7所示,具体物理参数如表2所示。

图7 纤维素气凝胶与CS2-MCC 样品的氮气吸附-脱附曲线及孔径分布曲线

表2 纤维素气凝胶与CS2-MCC气凝胶物理结构参数
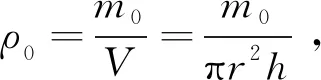
(3)
(4)
从图7和表2可以看出,纤维素气凝胶材料与CS2-MCC均属于介孔材料。与纤维素气凝胶相比,CS2-MCC材料拥有更低的表观密度、更高的孔隙率和更高的比表面积,这是由于经过改性后,原有纤维素分子中氢键体系被破坏,形成比表面积更大、孔道结构更多、孔径更大的三维网状结构,CS2-MCC的比表面积为59.340 7 m2/g,存在极少的微孔分布,整体分布为介孔材料,平均孔径为37.09 nm,与SEM结果较为吻合。
2.3 吸附条件的确定
2.3.1 pH值对 Cr(Ⅲ)吸附的影响
如图8所示,随着pH值的增大,CS2-MCC对Cr(Ⅲ)的去除率呈先上升后下降的趋势;pH值对Cr(Ⅲ)吸附的影响是2方面的:一方面,Cr(Ⅲ)的存在形态在很大程度上受溶液pH值的影响;另一方面,pH值影响着CS2-MCC表面的电荷分布和活性基团的形态[11]。当pH值在1~3范围内时,Cr(Ⅲ)主要以Cr3+和Cr[(OH)]2+2种形态存在,溶液中过多的H+会与Cr3+和Cr[(OH)]2+争夺吸附位点,且过低的pH值会使CS2-MCC表面质子化,导致CS2-MCC显阳离子性,不利于Cr(Ⅲ)的去除。当溶液pH值为4时,Cr(Ⅲ)主要以Cr[(OH)]2+形式存在,同时CS2-MCC逐渐去质子化,此时CS2-MCC对Cr(Ⅲ)的吸附效果较好。当pH值继续增大时,Cr(Ⅲ)会与-OH形成体积更大、电荷更高的配合物而难以被吸附,去除率有所降低。当pH值>6时,Cr(Ⅲ)开始以Cr(OH)3沉淀存在,对Cr(Ⅲ)的去除是吸附与沉淀的共同结果。考虑绿色化学发展理念,选取pH值为6为最佳吸附条件。
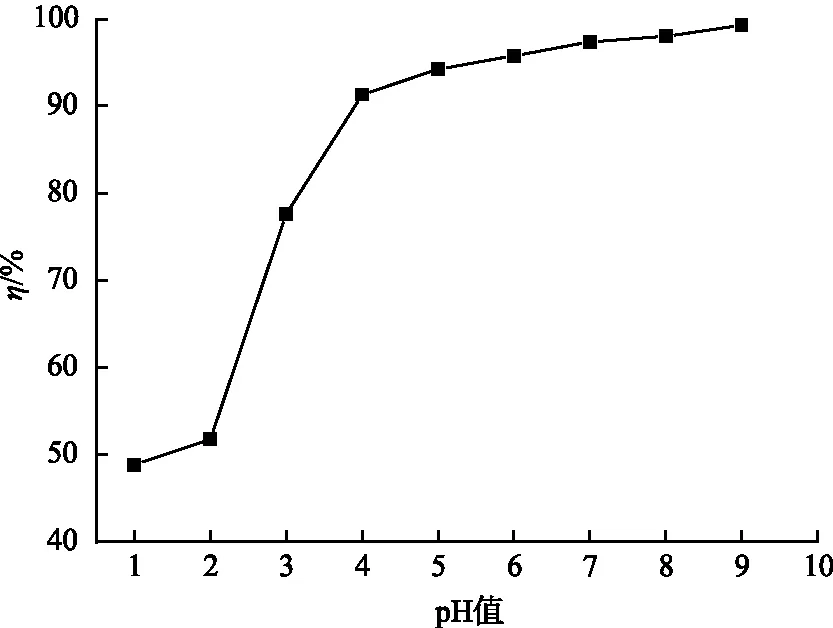
图8 溶液初始pH值对Cr(Ⅲ)吸附的影响
2.3.2 CS2-MCC投加量对Cr(Ⅲ)吸附的影响
由图9可知,当CS2-MCC投加量从0.4 g/L增加到1.3 g/L时,对Cr(Ⅲ)的去除率从12.37%迅速增加至98.33%,吸附容量由30.932 mg/g上升至75.638 mg/g,当增加CS2-MCC的用量时,CS2-MCC有效吸附位点数也随之增加,对Cr(Ⅲ)去除率增大;随后继续增加CS2-MCC投加量,去除率变化趋于稳定,相对应的吸附容量开始下降,说明此时溶液中Cr(Ⅲ)含量不足以使过量的CS2-MCC达到饱和。因此考虑材料应用成本等问题,CS2-MCC的投加量选择1.3 g/L较好。
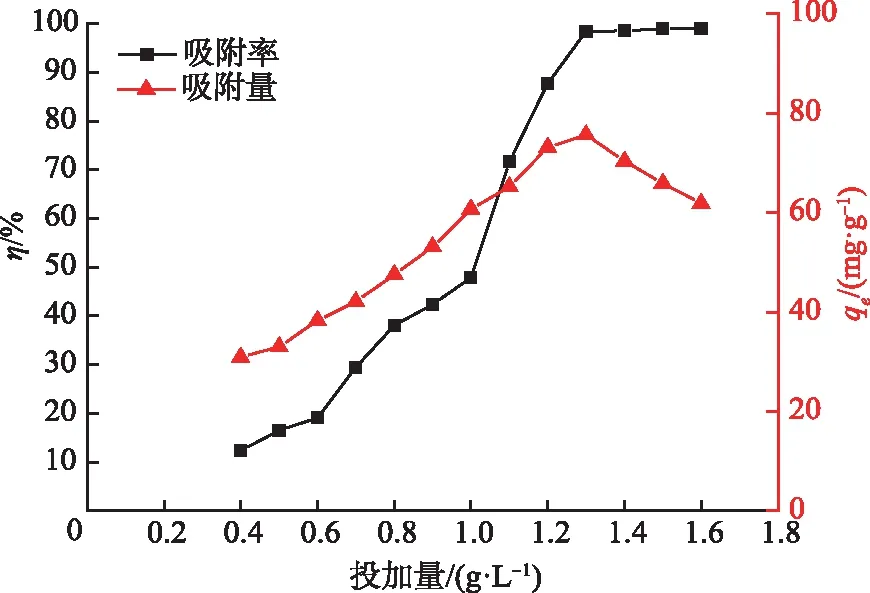
图9 CS2-MCC投加量对Cr(Ⅲ)吸附的影响
2.3.3 吸附时间对Cr(Ⅲ)吸附的影响
由图10可知,随着时间的推移CS2-MCC对Cr(Ⅲ)的去除率迅速增加,当吸附时间达到120 min时,去除率达到98.53%,对Cr(Ⅲ)的平衡吸附容量达到75.792 mg/g,溶液中Cr(Ⅲ)浓度降至1.47 mg/L,已达到排放标准,继续增加吸附时间时去除率变化趋于稳定,均达到99%以上,为节约时间成本,吸附时长选择120 min即可。

图10 吸附时间对Cr(Ⅲ)吸附的影响
2.3.4 吸附材料对Cr(Ⅲ)吸附的影响
调研了不用类型吸附材料对Cr(Ⅲ)的吸附性能,见表3[19-28]。由表3可发现,不同吸附材料对Cr(Ⅲ)的吸附能力有很大差别,CS2-MCC对Cr(Ⅲ)的平衡吸附容量为75.79 mg/g,吸附能力高于人工沸石[20]、虾壳和松树皮[21]、磁性纳米粒子负载没食子酸[22]、氨基功能化SBA-15介孔分子筛[23]、木质素[24]、中孔活性炭[25]、商品化活性炭[26]、TEMPO氧化纳米纤维素(CNF)[27]、羧甲基纤维素(CMC)/氧化石墨烯/四氧化三铁复合颗粒[28]。

表3 不同类型吸附材料对Cr(Ⅲ)的吸附[19-28]
2.4 CS2-MCC循环利用性能研究
以0.1 mol/L H2SO4溶液为洗脱液对吸附Cr(Ⅲ)后的CS2-MCC进行多次洗脱,并对洗脱液中Cr(Ⅲ)含量进行测定,直到检测含量为0。再用去离子水将CS2-MCC冲洗干净,于40 ℃烘箱中烘干备用,研究其循环利用性能。
由图11可知,经过4次吸附-洗脱后,CS2-MCC对Cr(Ⅲ)的吸附容量仍可达到64.721 mg/g,但经过第5次吸附-洗脱吸附容量下降至52.385 mg/g,但此时CS2-MCC开始分解,变得松散难以回收,因此,CS2-MCC循环使用次数保持在4次,CS2-MCC可以得到最有效利用。经过洗脱后,含有Cr2(SO4)3的洗脱液可回用于铬鞣工段,继续参与鞣制过程。
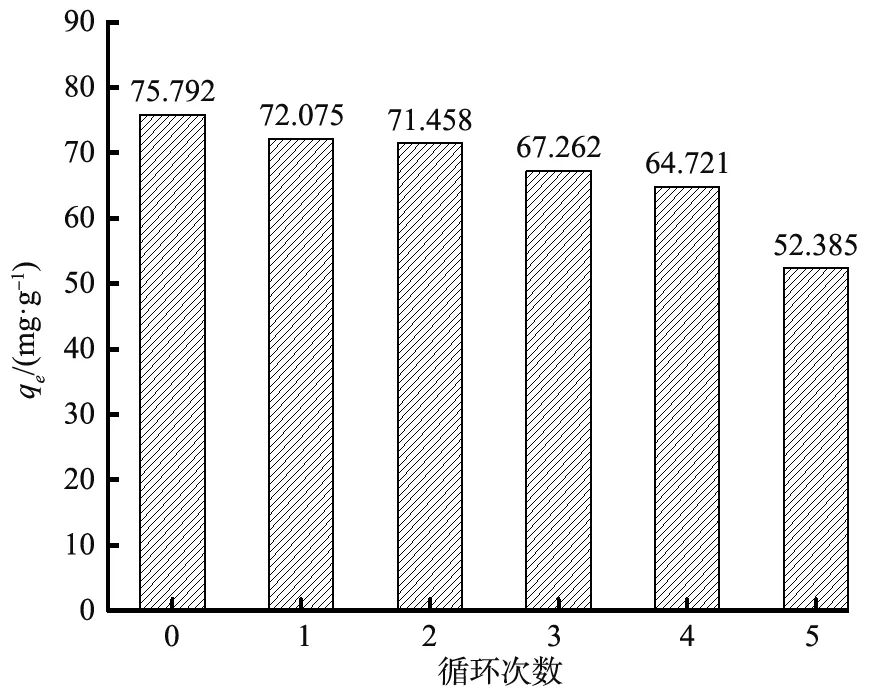
图11 CS2-MCC循环再生
2.5 吸附动力学分析
建立适宜良好的动力学模型,可以反映出CS2-MCC对Cr(Ⅲ)的吸附过程。本文采取准一级动力学[29]和准二级动力学[30]研究CS2-MCC对Cr(Ⅲ)的吸附过程与其内在的吸附动力。
ln(qe-qt)=-K1t+lnqe,
(5)
(6)
式中:qe为达到吸附平衡时吸附材料对Cr(Ⅲ)的吸附容量,mg/g;K1为准一级动力学常数,min-1;K2为准二级动力学常数,g·(mg-1·min-1)。


图12 不同温度下CS2-MCC对Cr(Ⅲ) 的吸附动力学模型拟合图

表4 CS2-MCC对Cr(Ⅲ) 吸附的动力学模型参数
2.6 吸附等温模型分析
采用Langmuir吸附等温线模型[31]和Freundlich吸附等温线模型[32]对Cr(Ⅲ)吸附过程进行拟合,探索其吸附机制。二者模型可用以下方程来表示:
(7)
(8)
式中:qm为吸附材料对Cr(Ⅲ)单层分子吸附的理论最大吸附容量,mg/g;Ce为达到吸附平衡时溶液中Cr(Ⅲ)的质量浓度,mg/L;n为经验常数,反映了吸附材料的不均匀性,表示吸附材料吸附能力的优劣,n值越大材料吸附性能越好,n>1为优惠吸附,n=1为线性吸附,n<1为非优惠吸附或多分子吸附;KL为Langmuir吸附常数,L/mg;KF为Freundlich吸附常数,mg/(g·(mg·L-1)n)。
在温度为298.15 K下进行实验,实验结果如图13和表5所示,其中通过Langmuir吸附等温线模型进行拟合的R2大于Freundlich吸附等温线模型的R2,说明CS2-MCC对Cr(Ⅲ)吸附行为更符合Langmuir吸附,即单分子层吸附,且由Langmuir等温吸附模型计算得CS2-MCC对Cr(Ⅲ)的最大吸附容量为78.247 mg/g,与实验测得的最大吸附容量相差不大。
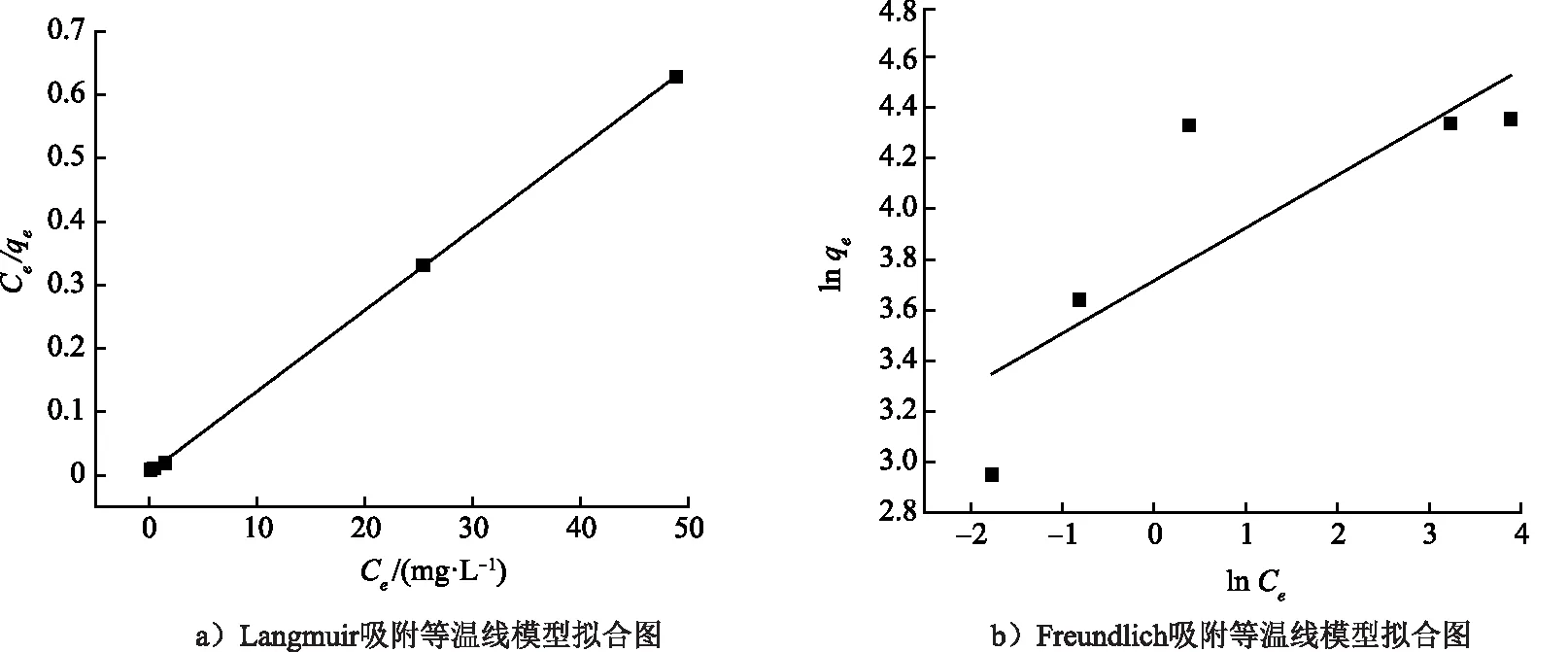
图13 Langmuir与Freundlich吸附等温线模型线性拟合图

表5 Langmuir与Freundlich吸附等温方程线性拟合参数
2.7 吸附热力学实验
为进一步探索吸附过程机理,以100 mg/L Cr(Ⅲ)离子模拟废水作为吸附对象进行吸附。分别在温度为293.15,298.15,308.15,318.15,328.15 K下,吸附6 h,进行热力学实验。通过式(9)和式(10),以lnKd对1/T作图,如图14所示。

图14 ln (Kd)-T-1关系图
(9)
ΔGθ=ΔHθ-TΔSθ,
(10)

表6为CS2-MCC吸附Cr(Ⅲ)的热力学参数。由表6可知,CS2-MCC对Cr(Ⅲ)吸附过程的焓变(ΔHθ)为321.943 J/mol,熵变(ΔSθ)为45.355 J/mol·K,ΔGθ变化范围为-12.973~-14.355 kJ/mol。ΔHθ>0,表明吸附过程为吸热过程,ΔGθ<0,说明吸附为自发吸附过程,且ΔGθ的数值随着温度上升而减小,再次表明升高温度有利于吸附过程的进行。

表6 CS2-MCC吸附Cr(Ⅲ)的热力学参数
2.8 对实际制革废水的处理效果
以1.4所述的实际制革废水作为处理对象,于298.15 K温度下,保持原水的pH值不变,进一步研究CS2-MCC对实际制革废水中Cr(Ⅲ)的吸附性能。
图15为不同CS2-MCC投加量下,对实际制革废水中Cr(Ⅲ)吸附的η-t关系图和qt-t关系图。如图15 a)所示,由于实际制革水中Cr(Ⅲ)的存在形式复杂多样,导致材料对Cr(Ⅲ)去除能力下降。通过进一步增加CS2-MCC投加量实现对Cr(Ⅲ)的有效去除,当CS2-MCC投加量增加至1.5 g/L时,在吸附160 min后,对Cr(Ⅲ)的去除率为98.524%,材料对应的吸附容量为 65.299 mg/g,此时制革废水中Cr(Ⅲ)含量降低至1.464 mg/L,实现了对废水中Cr(Ⅲ)的有效去除。

图15 不同CS2-MCC投加量对实际制革废水中Cr(Ⅲ)吸附效果的影响
3 结 语
本文以脱脂棉为原料,以质量比为7∶12∶81的NaOH/ 尿素/ H2O为纤维素溶剂,CS2为改性剂,对纤维素分子中羟基进行巯基化改性,再经纤维素再生与冷冻干燥,制备出巯基功能化纤维素气凝胶材料(CS2-MCC)。通过单因素试验及正交试验确定了制备CS2-MCC最佳工艺条件:CS2用量为0.5 mL/g,改性时间为6 h,硫酸镁用量为20 mL/g,改性温度为40 ℃。各因素对CS2-MCC吸附能力大小的影响依次为CS2用量>改性时间>硫酸镁用量>改性温度。
吸附实验表明:在298.15 K,pH值为6,CS2-MCC投加量为1.3 g/L,吸附120 min后,对Cr(Ⅲ)最大吸附容量为75.792 mg/g,溶液中Cr(Ⅲ)含量降低至1.470 mg/L,达到排放标准。吸附过程符合准二级动力学模型和Langmuir等温吸附模型,ΔGθ<0,表明对Cr(Ⅲ)的吸附为自发进行的单分子层吸附及化学吸附。重复使用4次后,对Cr(Ⅲ)的吸附容量仍可达到52.385 mg/g。当CS2-MCC投加量为1.5 g/L时,可实现对实际制革废水的有效处理,对实际制革废水中Cr(Ⅲ)的吸附容量可达65.299 mg/g。
研究首次制备出质轻、多孔、比表面积大的巯基功能化纤维素气凝胶材料(CS2-MCC),解决了大多数纤维素材料呈现固体粉末状难以分离和吸附性能较差的问题,将其用于制革废水中Cr(Ⅲ)的吸附,可实现对废水中Cr(Ⅲ)有效吸附并达到含铬废水的排放标准。
对CS2-MCC吸附机理的研究,本文仅从吸附动力学和热力学以及脱附过程等方面进行了推测,在CS2-MCC吸附机理的测定方面还有待进一步研究。
