市售乳酸菌制品中乳酸菌耐药基因分析
2022-11-28梁媛媛黄甜甜夏琪琪杨云斌刘鹏鹏
梁媛媛,黄甜甜,夏琪琪,杨云斌,刘鹏鹏*
1.浙江方圆检测集团股份有限公司(杭州 310018);2.浙江省市场监管生物安全重点实验室(杭州 310018);3.长兴县食品药品检验检测中心(湖州 313100)
乳酸菌是一类发酵糖类产物为乳酸的革兰阳性菌,与维护肠道微生物平衡、提高机体免疫力、维持宿主健康密切相关[1]。美国食品药品管理局(Food and Drug Administration,FDA)将其评价为“普遍安全(generally regarded as safe,GRAS)”的一类。乳酸菌长期以来作为安全的无致病性的益生菌种被广泛应用于食品、保健品和药品,如发酵酸奶、固体饮料、肠道微生态制剂等[2-3]。
近年来,随着抗生素新品种的大量问世及抗菌药物的大量使用,细菌耐药性问题越发严重。早期的耐药性研究主要集中在病原微生物领域[4-5],近期关于乳酸菌的耐药性所带来的安全性问题引起广泛关注[6-7]。FAO/WHO指出,随着消费者大量食用乳酸菌制品,存在的一种可能的危害是造成菌种携带的耐药基因的转移,即乳酸菌的耐药性会通过食物链转移到人体肠道[8]。在体内形成耐药基因库,耐药基因在致病菌和正常菌株之间无屏障传递,容易形成天然的耐药基因池,导致超级细菌的产生,给疾病治疗和生命安全带来潜在的安全风险,也可能成为制约发酵乳制品行业发展的重大安全隐患[9-12]。因此,是否携带耐药基因可成为乳酸菌的安全性评价的依据之一。
β-内酰胺类抗生素系指化学结构中具有β-内酰胺环的一大类抗生素,其通过共价键与青霉素结合蛋白结合,从而抑制细菌细胞壁的合成,是临床使用最为广泛的一类抗生素,也是目前研究报道中耐受性较普遍存在的一类抗生素。有报道表明,在生产乳制品用的乳杆菌、嗜热链球菌等菌株中检测到对相关抗生素的耐药性[13-16],β-内酰胺酶基因作为耐药性基因则鲜有检出。鉴于此,试验对市售乳酸菌制品中添加的活菌数量和菌种进行分析鉴定,同时考察β-内酰胺酶基因blaZ在这些菌株中的分布和多重耐药基因的情况,从而为市售乳酸菌制品的安全性评价提供依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
随机选取国内市售发酵乳、乳酸菌饮品等77批乳酸菌制品,用琼脂平板稀释法对样品中的乳酸菌进行分离培养。
嗜热链球菌、乳杆菌、双歧杆菌(均采用MRS琼脂,北京陆桥生物技术有限责任公司);莫匹罗星、半胱氨酸盐酸盐(均为青岛海博生物技术有限公司);DL500 DNA Marker、10×TBE缓冲溶液(Tris-EDTA)、1 000×D-HelixRed核酸染料和双蒸馏水(ddH2O)[均为宝日医生物技术(北京)有限公司];细菌基因组DNA提取试剂盒[天根生化科技(北京)有限公司];2×PCR Taq Mix预混液(北京美莱博医学科技有限公司);琼脂糖(Agarose Regular)、PCR引物、DNA测序、2×高保真PCR Mix预混液和阳性质粒[均为生工生物工程(上海)有限公司]。
1.1.2 仪器与设备
Anoxomat MARK Ⅱ智能厌氧培养系统(美国Gene Science公司);Beckman Microfuge 16台式微量离心机(美国贝克曼库尔特有限公司);Nano-300超微量分光光度计(杭州奥盛仪器有限公司);D1200板式加热器(美国Labnet’s公司);ABI Veriti梯度PCR仪(美国应用生物系统公司);Powerpac HC 1645052伯乐高流核酸电泳仪、Gel-Doc-XR+凝胶成像系统(均为美国Bio-Rad公司);VITEK MS全自动快速微生物质谱检测系统(法国生物梅里埃公司)。
1.2 方法
1.2.1 乳酸菌的分离和培养
乳酸菌制品中的乳酸菌菌株培养按照GB 4789.34—2016《食品微生物学检验双歧杆菌检验》和GB 4789.35—2016《食品微生物学检验乳酸菌检验》进行。
1.2.2 乳酸菌的鉴定
乳酸菌的快速鉴定采用激光解析电离飞行质谱VITEK MS进行。用接种环挑取单个菌落,点在样品靶板孔中,涂抹均匀并在室温自然晾干。吸取1 μL基质CHCA溶液与样品混合,自然晾干,形成结晶,上机测定。
1.2.3 引物设计
参考NCBI数据库blaZ基因(基因库序列号MT906815.1),使用Primer Premier 5.0软件设计上游引物blaZ-F和下游引物blaZ-R;实验室自行合成链霉素耐药基因strA、strB,四环素耐药基因tetM、tetK,卡那霉素耐药基因aph3-Ⅲa和万古霉素耐药基因vanX,引物序列如表1所示。

表1 PCR扩增耐药基因所用引物及扩增产物长度
1.2.4 样品DNA提取
将培养的单菌落进行扩大培养。用接种环5 μL接种环收集一环菌落,DNA提取方法参考天根细菌基因组DNA提取试剂盒。
1.2.5 PCR反应体系和程序
反应体系:2×PCR反应预混液12.5 μL,正向引物和反向引物各1 μL,挑取单菌落作为DNA模板或者取DNA(10~50 ng/μL)1 μL。反应条件:95 ℃预变性5 min,95 ℃变性15 s,55 ℃退火15 s,72 ℃延伸30 s,进行40个循环;72 ℃延伸2 min,反应结束4 ℃保存。
2 结果与分析
2.1 乳酸菌样品活菌计数
共采集包括发酵乳、固体饮料等在内的市售乳制品样品77批。每批样品按照国标方法进行乳酸菌的培养及活菌计数,计数结果如图1所示。77批样品中76批样品添加活菌数均符合标准要求或者超过标识菌数。据Morovic等[21]报道,67.3%的市售益生菌制品(n=50)在保质期内经活菌计数发现,添加的益生菌活菌数均符合或超过商品标识菌种数,其余样品的活菌计数值均低于标识。在国内,王绮等[22]利用傅里叶变换近红外分析仪与紫外-可见分光光度计结合快速测定市售145个乳酸菌样品,活菌数均超过国家标准(106CFU/mL),与试验数据较为接近。

图1 乳酸菌制品活菌数与标识菌数的比较
2.2 耐药基因分析
通过随机挑选涵盖77个样品的640个菌落进行PCR初步鉴定,得到一批携带耐药基因blaZ的可疑阳性菌。扩大培养后,提取可疑阳性菌菌株的基因组gDNA,利用高保真Taq酶再次进行耐药基因的PCR鉴定,筛选出携带blaZ的菌株47株。结果如表2所示,47株乳酸菌均携带耐药基因blaZ,检出率为7.34%。其中,24株菌(51.06%)经鉴定只携带blaZ,18株菌(38.29%)含有双重耐药基因blaZ和tetM,2株菌含有双重耐药基因blaZ和aph3-Ⅲa,3株(6.38%)携带含有三重耐药基因blaZ、tetM和aph3-Ⅲa。另外,试验用同样方法进行表1中其他耐药基因的鉴定,结果发现链霉素抗性基因(strA和strB)、四环素抗性基因(tetK)及万古霉素抗性基因(vanX)在试验中均未检出。

表2 乳酸菌菌种及其携带的耐药基因
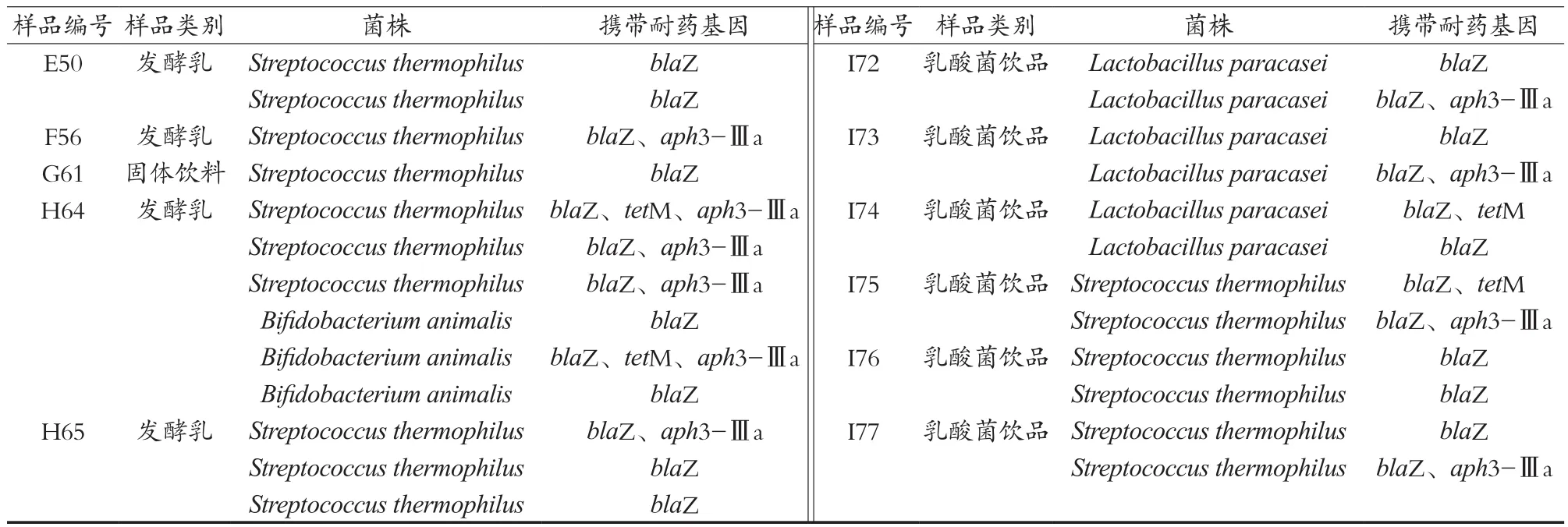
接表2
2.3 菌株鉴定
对携带blaZ耐药基因的47个菌株采用MALDI-TOF MS进行菌种鉴定,结果表明blaZ阳性菌株均为样品中标识添加的乳酸菌(图2)。携带耐药基因blaZ的阳性菌主要集中在嗜热链球菌(63.83%),其次是副干酪乳杆菌(17.02%)和动物双歧杆菌(14.89%),鼠李糖乳杆菌则携带blaZ基因的情况较少(4.26%)。对blaZ阳性菌株是否携带其他抗生素耐药基因也进行鉴定和分析。通过各耐药基因相对丰度的比较结果(表2、图3)可以看出,所有类型的乳酸菌中,数量仅次于blaZ基因的是氨基糖苷类耐药基因aph3-Ⅲa,携带最少的是四环素类耐药基因tetM。含有三重耐药基因的3株菌分别是嗜热链球菌、鼠李糖乳杆菌和动物双歧杆菌(表2)。
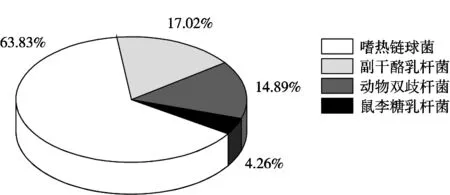
图2 飞行质谱鉴定菌种组成
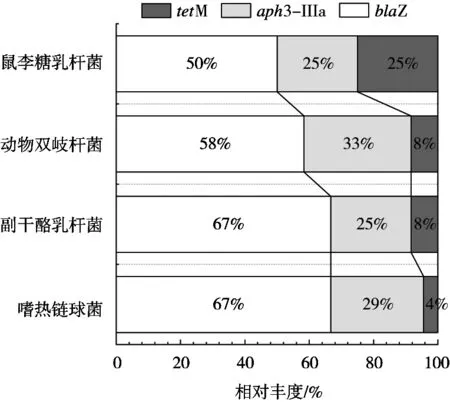
图3 耐药基因组成的相对丰度分析
3 结论
试验对随机选取的市售乳酸菌制品样品(n=77)进行乳酸菌活菌计数,结果显示共计76份样品添加活菌数超过标准要求或者商品标识菌种数,合格率为98.70%。这表明我国对乳酸菌市场加强行业监管已初见成效,但仍存在个别乳酸菌制品的活菌数添加不符合要求的现象。试验以市售乳酸菌制品为研究对象,调查发现耐药基因blaZ在样品中的检出率为28.57%。氨基糖苷类耐药基因aph3-Ⅲa在研究中也有检出,47株blaZ阳性乳酸菌菌株中检出率为44.68%。四环素耐药基因tetM和tetK的鉴定中,前者在此次调查中有检出(10.64%),即5株blaZ阳性乳酸菌菌株中有检出tetM,而后者在试验中未检出。
通过对市售乳酸菌制品中的乳酸菌活菌添加情况的调查及耐药基因的鉴定和分析显示,市售乳酸菌制品添加活菌数基本符合标准或者标识要求。同时,乳酸菌菌种具有携带一种甚至多种耐药基因的情况,可能成为耐药基因的贮存库,今后需要持续加强食用菌株安全性评价。试验受传统PCR方法的局限,检测的灵敏度和准确度均有待提高。另外据以往报道,耐药基因和耐药表型的关联度较低。因此,对乳酸菌制品中的菌株耐药表型及其耐药机理展开调查将成为今后工作的主要方向。
