经皮肾动脉支架置入术治疗动脉粥样硬化性肾动脉狭窄长期临床效果观察
2022-11-26周海鹏张志强王亚松周铁楠王效增
周海鹏, 张志强, 王亚松, 周铁楠, 王效增
北部战区总医院 心血管内科,辽宁 沈阳 110016
肾动脉狭窄常由动脉粥样硬化及纤维肌性发育不全、大动脉炎引起[1-3]。在我国年龄>40岁的肾动脉狭窄患者中,动脉粥样硬化是常见病因,约占总数的94.7%[4]。动脉粥样硬化性肾动脉狭窄(atherosclerotic renal artery stenosis,ARAS)可引起肾血管性高血压及缺血性肾病,进而导致难治性高血压、肾损害及肾功能缓慢性减退[5]。ARAS也可引起肾外系统表现,如脑卒中、冠心病及外周动脉硬化等[6]。在肾动脉狭窄的诊断和处理中国专家共识中推荐经皮介入治疗作为肾动脉血管重建的首选方法[4],但其能否长期改善肾动脉狭窄患者的高血压及肾功能,目前仍存在争议。本研究旨在观察经皮肾动脉支架置入术(percutaneous renal artery stenting,PTRAS)治疗ARAS的长期临床效果。现报道如下。
1 对象与方法
1.1 研究对象 选取北部战区总医院自2016年5月至2016年9月收治的行肾动脉造影明确诊断ARAS的238例患者为研究对象。纳入标准:肾动脉主干直径狭窄≥70%;肾功能快速恶化,存在残余肾功能或患侧肾长度>7 cm;顽固性高血压或不用降压药物高血压达3级水平;合并慢性肾功能减退的双侧或单侧ARAS。排除标准:大动脉炎、纤维肌性发育不良引起的肾动脉狭窄;肾动脉瘤,腹主动脉瘤压迫,肾动脉栓塞压迫,肾移植术后移植肾动脉狭窄;存在抗凝、抗血小板药物禁忌;对比剂过敏;失访。根据纳入和排除标准,剔除失访41例,最终纳入197例。根据治疗方式不同,将患者分入优化药物组(n=78)和药物联合PTRAS组(n=119)。患者及其家属均签署知情同意书。本研究经医院伦理委员会批准。
1.2 肾动脉造影及支架置入术 穿刺股动脉成功后,留置7F股动脉鞘管,肝素钠注射液2 000 U鞘入,选用JR3.5 7F指引导管行肾动脉造影,记录肾动脉狭窄处直径及病变长度、参考血管直径,优化药物组术毕;药物联合PTRAS组补充肝素3 000 U,按照标准操作置入肾动脉支架。对比剂为威视派克(GE320,上海通用公司)。
1.3 药物治疗 所有患者肾动脉造影前1天口服肠溶阿司匹林300 mg+硫酸氢氯吡格雷300 mg/替格瑞洛180 mg。优化药物组术后长期口服阿司匹林、调脂药物。药物联合PTRAS组术后长期口服阿司匹林、调脂药物,以及硫酸氢氯吡格雷75 mg/次,每天1次或替格瑞洛90 mg/次,每天2次,至少服用6个月。两组患者均在密切监测血压变化的基础上调整降压药物,由研究者酌情决定是否继续服用其他药物。
1.4 随访及观察指标 所有患者均由专人以门诊、电话、微信等方式随访,收集患者肾动脉造影或肾动脉介入术后第3天和术后6、12、36、60个月的随访资料,记录随访过程中血液透析、新发脑卒中、心源性死亡、全因死亡、肾移植、肾动脉靶血管血运重建等临床事件的发生情况。
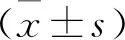
2 结果
2.1 两组患者临床资料比较 药物联合PTRAS组年龄、肾小球滤过率、低密度脂蛋白及既往冠心病史比例均低于优化药物组,入院收缩压、入院舒张压及既往高血压史、单侧肾动脉狭窄比例均高于优化药物组,差异有统计学意义(P<0.05)。见表1。

表1 两组患者临床资料比较
2.2 两组患者术前术后血压水平比较 两组术后第3天和术后6、12、36、60个月的收缩压均低于术前,差异有统计学意义(P<0.05);两组术后第3天和术后6、12、36、60个月的收缩压和舒张压比较,差异无统计学意义(P>0.05)。见表2~3。与优化药物组比较,药物联合PTRAS组舒张压在术后6、12、60个月时降低明显,差异有统计学意义(P<0.05);两组术后不同观察时间收缩压改善程度差异无统计学意义(P>0.05)。见表4~5。
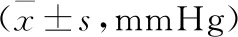
表2 两组患者术前术后收缩压水平比较
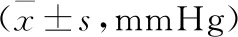
表3 两组患者术前术后舒张压水平比较

表4 两组患者术后不同观察时间与术前收缩压差值比较[M(Q1,Q3),mmHg]
2.3 两组患者术后肾功能指标比较 优化药物组术后第3天、12个月、36个月的肾小球滤过率分别为(102.17±34.88)ml/(min·1.73 m2)、(91.13±36.86)ml/(min·1.73 m2)、(84.13±29.77)ml/(min·1.73 m2),药物联合PTRAS组分别为(84.13±29.77)ml/(min·1.73 m2)、(65.11±28.32)ml/(min·1.73 m2)、(77.08±34.27)ml/(min·1.73 m2),差异无统计学意义(P>0.05)。优化药物组术后第3天、12个月、36个月的肾小球滤过率与基线差值分别为(4.44±20.92)ml/(min·1.73 m2)、(-1.57±16.36)ml/(min·1.73 m2)、(-1.92±17.13)ml/(min·1.73 m2),药物联合PTRAS组分别为(-0.61±14.22)ml/(min·1.73 m2)、(-7.90±27.55)ml/(min·1.73 m2)、(2.12±24.57)ml/(min·1.73 m2),差异无统计学意义(P>0.05)。
2.4 两组患者终点事件发生率比较 药物联合PTRAS组靶血管血运重建、肾移植、血液透析发生率高于优化药物组,但差异无统计学意义(P>0.05)。优化药物组心源性死亡、肾源性死亡发生率高于药物联合PTRAS组,但差异无统计学意义(P>0.05)。见表6。

表5 两组患者术后不同观察时间与术前舒张压差值比较[M(Q1,Q3),mmHg]
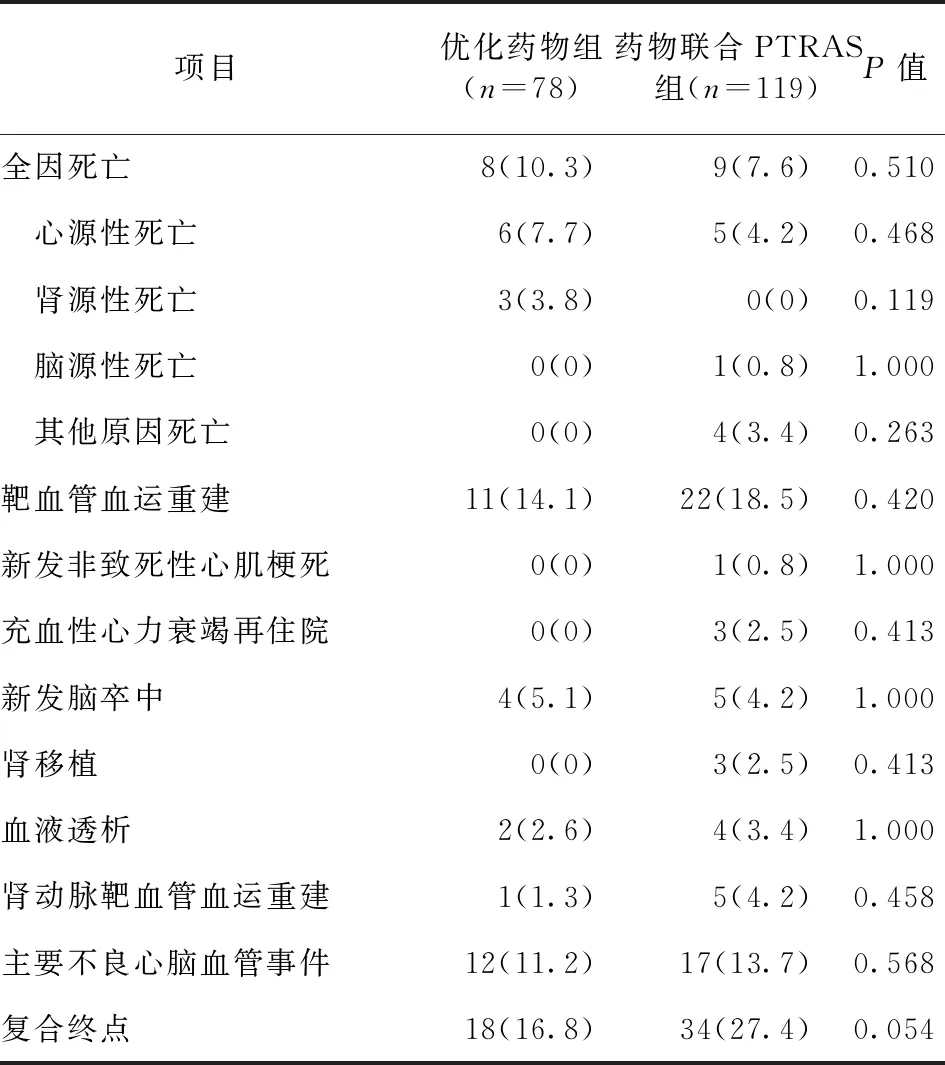
表6 两组患者终点事件发生率比较/例(百分率/%)
2.5 两组患者术后60个月内全因死亡危险因素分析 术前肾小球滤过率<60 ml/(min·1.73 m2)、低密度脂蛋白水平升高、双侧肾动脉狭窄、肾动脉最重狭窄程度增加是优化药物组全因死亡的危险因素(P<0.05)。糖尿病史、左室射血分数降低、双侧肾动脉狭窄、肌酸激酶同工酶水平升高是药物联合PTRAS组全因死亡的危险因素(P<0.05)。肾小球滤过率<60 ml/(min·1.73 m2)、低密度脂蛋白水平升高、双侧肾动脉狭窄、最重狭窄程度增加对全因死亡发生率的影响存在显著交互作用(P<0.05)。见图1。

图1 两组患者术后60个月内全因死亡危险因素Logistic分析
3 讨论
ARAS是一种进行性疾病,随着血管狭窄严重程度增加,肾功能逐渐恶化,发生慢性肾衰竭的可能性较大[7]。目前,PTRAS因其微创、高效、并发症少等优点已广泛应用于治疗ARAS。ARAS血运重建的主要目标为改善高血压和肾功能,以及治疗肾动脉狭窄严重的病理生理效应[8]。但国内外对于应用肾动脉支架治疗ARAS的术后肾功能改善和降压作用仍存在争议[9-11]。
肾动脉狭窄常引起肾血管性高血压,可使血压正常者出现高血压后迅速进展或原有高血压的中老年患者血压迅速恶化,重症患者会出现恶性高血压[8,12-14]。单侧肾动脉狭窄所致肾血管性高血压若长久不能良好控制,还能引起对侧肾损害[12]。PTRAS血运重建对肾血管性高血压有效,但不能改变原发性高血压[15]。因此,PTRAS后患者血压较术前降低或服用降压药种类减少均属于PTRAS治疗的临床效果[16]。本研究结果显示:两组术后第3天和术后6、12、36、60个月的收缩压均低于术前,差异有统计学意义(P<0.05)。可认为本研究中PTRAS临床治疗有效。但本研究结果还显示:与优化药物组比较,药物联合PTRAS组舒张压在术后6、12、60个月时降低明显,差异有统计学意义(P<0.05);但两组术后不同观察时间收缩压改善程度差异无统计学意义(P>0.05)。这可能与药物联合PTRAS组中合并原发性高血压的患者比例较高有关。
肾动脉狭窄是缺血性肾病的根源,主要表现为肾功能缓慢进行性减退,肾小球功能受损,肾小球滤过率下降,血肌酐升高,后期肾体积缩小[17-18]。本研究中,PTRAS对肾功能的改善并不明显,这可能与纳入对象多为单侧肾动脉狭窄,健侧肾尚有代偿功能有关。
本研究的Logistic回归分析结果显示,双侧肾动脉狭窄为优化药物组和药物联合PTRAS组全因死亡的危险因素(P<0.05)。因此,临床医师应高度重视肾动脉狭窄检出及合理化治疗,解除病变狭窄,控制血压,改善预后。
综上所述,优化药物治疗和药物联合PTRAS治疗均可有效改善ARAS患者血压;与优化药物治疗比较,联合PTRAS不能明显改善肾功能及减少终点事件发生;肾动脉狭窄程度较重为ARAS患者全因死亡的危险因素,在临床工作中应高度重视。
