二尖瓣经导管缘对缘修复的超声心动图操作规范中国专家共识
2022-11-23中国医师协会超声分会超声心动图专业委员会
中国医师协会超声分会超声心动图专业委员会
中国医师协会心血管内科医师分会结构性心脏病学组
二尖瓣反流/关闭不全(mitral regurgitati on,MR)是最常见的心脏瓣膜疾病之一[1]。超声心动图是目前诊断和评价MR最重要的影像学方法。经导管缘对缘修复(transcatheter edge-to-edge repair,TEER)为目前最成熟、指南唯一推荐的MR介入技术。与其他心脏介入手术不同,超声心动图在TEER术中具有无可替代的导航及监测作用。随着TEER代表性器械MitraClip在全世界的发展和在我国上市推广[2-5],以及我国研发的国产TEER器械陆续进入临床试验[6-10],我国临床对TEER超声心动图的指导性文件及规范化培训的需求急剧增加。虽然 国际上已经发布了有关MR超声心动图评价的指导性文献[11-13],我国也于2019年初发布了《二尖瓣反流介入治疗的超声心动图评价中国专家共识》(简称《共识2019》)[14],但该共识有些内容侧重于术前评估,对术中导航监测阐述不详,且部分内容需要更新。为推进我国二尖瓣TEER(简称M-TEER,下文TEER特指M-TEER)的安全、规范、快速发展,作为《共识2019》的更新版及补充版,我们编写了本共识,为TEER术前评估和筛选、手术策略制定、术中导航和监测及术后随访提供更全面的指导。
1 二尖瓣解剖结构概述
二尖瓣装置由前叶、后叶、腱索、乳头肌、瓣环和左心房壁、左心室壁组成。两个瓣叶在前外交界和后 内交界处相连接,均有相应的腱索和乳头肌。在《共识2019》里,二尖瓣前叶和后叶分别分成3个扇区,一般情况下后叶天然的二个切迹将后叶分成3个部分,从前外交界向后内交界方向,依次为外侧叶P1、中间 叶P2、内侧叶P3,前叶与之对应的区域依次为外侧叶A1、中间叶A2、内侧叶A3以及前外交界AC、后内交界PC;少见情况下的二尖瓣后叶有三个切迹将后叶分为4个部分,从前外交界向后内交界方向,依次为外侧叶P1、中间叶P2L(偏外侧)、P2M(偏内侧)、内侧叶P3;另一种较少见的二尖瓣后叶有一个深的切迹,将后叶分为2个部分,从前外交界向后内交界方向,依次 为外侧叶P1、内侧叶P3,无P2部分[15]。
2 MR的病因及功能分型
2. 1 MR病因分型
《共识2019》中将MR的病因分为原发性瓣膜病变和继发性瓣膜病变。本共识将MR的病因分为原发性瓣膜病变(瓣膜本身结构的病变导致)、继发性瓣膜病变(心脏本身或瓣膜支撑结构病变导致)和混合性二尖瓣病变(既有原发性二尖瓣病变,又有继发性二尖瓣病变),见表1。

表1 二尖瓣反流病因分型
2. 2 MR功能分型
二尖瓣修复技术的创始人Carpenter教授提出了MR“功能分型”[16],从而帮助规范定义及指导后续的外科修复治疗。《共识2019》引用 了Carpenter分型。Carpenter分型主要根据瓣叶活动情况来划分,其本质是一种 机制分型。本共识大体沿用了Carpenter分型,但在该基础上增加了Ⅳ型(混合性包括原发性和继发性并存),同时将Carpenter Ⅱ型进一步分为脱垂、假性脱垂、连枷、脱垂合并连枷四种亚型[17-18](图1~4)。所谓脱垂就是瓣叶活动度增加,瓣体关闭时超过前后瓣环平面;假性脱垂,即瓣叶活动度增加,但关闭时瓣体未超过前后瓣环平面;连枷,即瓣尖部因主腱索断裂错入左心房、呈“连枷”运动(大幅度的关节样甩动);脱垂合并连枷,即在脱垂基础上合并主腱索断裂呈连枷运动。具体见表2。Carpenter分型最初是用于指导外科二尖瓣修复,但这类分型方法对指导MR介入治疗也具有一定指导意义,TEER对不同分型效果可能不同。目前认为TEER对Ⅱ型和Ⅲb型效果较好,对Ⅰ型较差,而Ⅲa型不适合TEER,但这需要将来更严谨的研究进行证实。

表2 二尖瓣反流功能分型
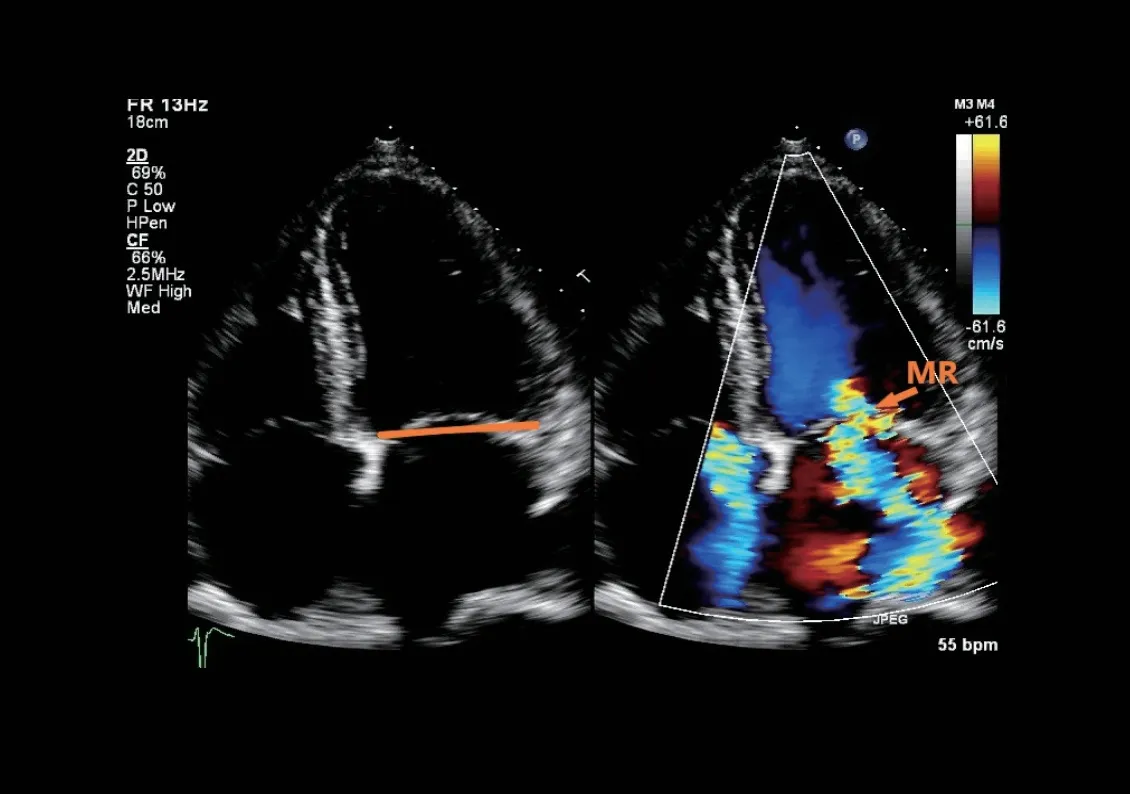
图1 Ⅰ型,正常瓣膜运动,因瓣环扩大,导致MR(箭头所示)

图2 Ⅱ型脱垂、假性脱垂、连枷、脱垂合并连枷 A. 脱垂,食管中段左心室长轴切面,显示二尖瓣后叶P2 处脱入左心房,且瓣体部超过二尖瓣瓣环平面;B. 假性脱垂,食管中段左心室长轴切面,显示P2 处脱向左心房、瓣尖骑跨后叶,但瓣体部未超过二尖瓣瓣环平面;C.连枷,食管中段左心室长轴切面,显示前叶体尖部因腱索断裂错入左心房、在二尖瓣口来回甩动即“连枷”运动;D. 脱垂合并连枷,食管中段左心室长轴切面,显示P3 处脱垂、连枷,且体尖部超过瓣环平面
3 MR的定量
《共识2019》[14]摒弃了传统轻度、中度、重度分型,提出以数字为基准的反流分级,将MR程度划分为无(0+)、轻度(1+)、中度(2+)、中重度(3+)、重度(4+)及极重度(5+)六个等级。对于评估流程进行适当的、标准化的简化,提出以反流颈宽度(vena contracta width,VCW)为主要指标、反流分数(regurgitation fraction,RF)为第二指标的简化评估方法。与此同时,也依据测量可重复性、精确度的多个角度,提出了MR定量标准评估方法以及相关参数,包括VCW、RF、反流容积(regurgitation vol u me,RVol)、有效反流口面积(ef f ective regurgitant orifice area,EROA)以及EROA等几种测量方式及其可能误差及参数推荐设定。
上述的定量评估方案主要针对原发性MR患者,对于功能性MR(functional mitral regurgitation,FMR)患者,存在着不同的评价体系,且争议较大[19]。新近,有学者提出一个量化FMR严重程度的新概念体系,根据EROA和左心室舒张末期体积(left ventricular end-diastolic volume,LVEDV)的比值关系将FMR分为成比例型(EROA/LVEDV<0.14)和非成比例型(EROA/LVEDV≥0.14)FMR[20]。本共识认为该分类可能影响患者TEER术后效果,是目前FMR患者行TEER术前评估需要考虑的指标,但这需要进一步研究证实。
4 TEER的超声心动图适应证
TEER最佳的二尖瓣解剖结构的具体超声心动图指标包括:(1)二尖瓣中央区,即A2/P2区病变;(2)夹合处瓣叶没有钙化、裂隙;(3)二尖瓣瓣口面积(mitral valve area,MVA)>4 cm2;(4)可活动的后叶长度>10 mm;(5)前后瓣叶的对合高度<11 mm;(6)存在瓣叶脱垂和连枷的,连枷间距<10 mm,脱垂范围<15 mm。对于FMR除了解剖学符合要求外,其他条件包括:心力衰竭(心衰)规范化药物治疗后症状仍持续,与左心室重构程度不成比例的严重FMR,左心室射血分数(left ventricular ejection f raction,LVEF)介于20%~50%、左心室收缩末期内径(lef t ventricular end systolic diameter,LVESD)≤70 mm,肺动脉收缩压≤70 mmHg(1 mmHg=0.133 kPa),没有右心功能受损(三尖瓣环收缩期位移TAPSE≥17 mm或S波峰值速度≥10 cm/s)或没有重度三尖瓣反流。MR的TEER治疗的解剖学评估推荐使用“适合的、有挑战的、不适合的”三分区策略(表3)[21]。以上的解剖适应证主要是针对经股静脉TEER,对于经心尖的TEER具体的适应证可能略有差别,但目前尚无足够研究证实。
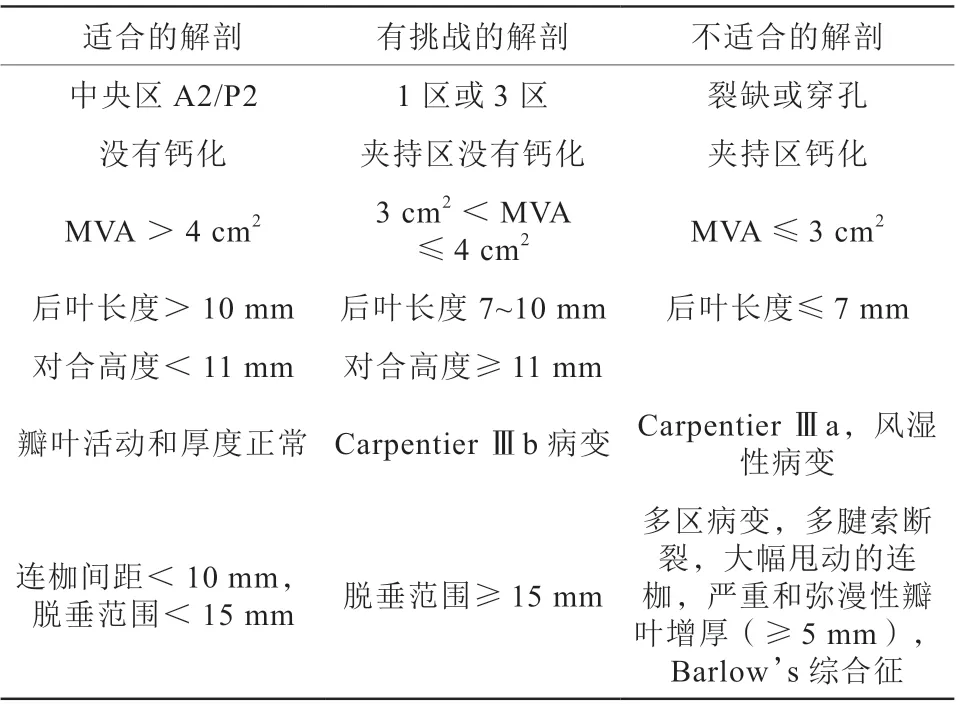
表3 TEER 术前解剖适合的、有挑战的、不适合的超声评估分类

图3 Ⅲ型限制瓣膜运动 A. 瓣叶开放和关闭时均受到限制,导致二尖瓣狭窄和反流;B. 瓣叶关闭时受到限制,导致二尖瓣反流
5 经股静脉TEER术中的超声心动图操作规范
5. 1 TEER术的硬件要求及切面定义
TEER手术对超声仪器的要求比较高,一般建议使用具有支持食管三维探头,具备实时双切面、三切面、3D ZOOM(可以局部显示某一特殊结构的三维显像,主要用来显示二尖瓣口的三维“外科视野”)、实时三维显像等,且具备二尖瓣专用分析软件。
在二尖瓣进行夹合时,常使用X-plane切面同时显示食管中段二尖瓣交界处二腔心切面和左心室长轴切面,其中食管中段二尖瓣交界处二腔心切面显示器械与二尖瓣口是前外和后内的关系,而食管中段左心室长轴切面显示器械与二尖瓣口是前后关系,因此本共识将上述X-plane切面称为“X-Plane工作切面”。
常使用3D ZOOM技术,清楚地显示二尖瓣的三维结构,该切面称之为二尖瓣“外科视野”或“左心房观”切面。有时,可以 将X-Plane工作切面和二尖瓣左心房观切面同时显像,本共识将这样的显示方式定义为“工作三切面”;某些超声机器还可以同时显示短轴切面,可定义为“工作四切面”(本共识中工作三切面定义包含了工作四切面)。以上两个工作切面主要使用在A2、P2区病变,对于非A2、P2区的非中央区病变,因X-Plane工作切面的取样线不能与输送系统同轴,因此无法很好地显示整体输送系统及器械,此时需要使用Multi-Vue多切面,它可以在非A2、P2病变部位处实现取样线与输送系统同轴且垂直于二尖瓣关闭线(图5)。

图4 Ⅳ型(混合性二尖瓣反流) A. 食管中段左心室长轴切面,显示二尖瓣前后叶因腱索牵拉均不能退至瓣环水平,导致关闭时二尖瓣前后叶瓣尖错位;B. 与A切面相同,彩色多普勒显示该处重度二尖瓣反流;C. 食管中段二尖瓣交界处二腔心切面,显示P3 处连枷;D. 与C 切面相同,彩色多普勒示该处重度二尖瓣反流

图5 A. 食管中段二尖瓣交界处二腔心切面,显示输送系统及夹合器位于A3、P3处;B. 在图A、图C中红色取样线放置于A3、P3且与输送系统同轴,并与二尖瓣关闭线垂直获得图B 食管中段左心室长轴切面;C. 在图A、图B中蓝色取样线放置于二尖瓣环获得图C 二尖瓣瓣环短轴切面;D. 二尖瓣口的三维“外科视野”,显示夹合器位于A3、P3 处且与二尖瓣关闭线垂直
经股静脉TEER术是一个慢节奏的手术,需要介入医师和心脏超声医师的精诚合作。经食管三维超声心动图的工作三切面、Multi-Vue切面及X-Plane工作切面克服以往单平面显像需要在食管中段二尖瓣交界处二腔心切面和食管中段左心室长轴切面、食管中段上下腔切面和食管中段大血管短轴切面、以及二维和三维之间的转换,同时实时监测术中并发症,早期监测术中血流动力学变化的情况。其具体步骤见表4。

表4 经股静脉TEER 超声引导的所需切面及超声评估要点
5. 2 引导房间隔穿刺
房间隔穿刺的监测是2D、3D经食管超声心动图(trans esophageal echocardiography,TEE)引导的第一个目标,合适的穿刺点是经股静脉TEER术成功及难易的基本影响因素。其操作规范为:(1)术中应用X-plane双切面(食管中段上下腔切面和大血管短轴切面)同时显示房间隔的上、下和前、后,监测和引导房间隔穿刺(图6);(2)食管中段四腔心切面(角度0°~10°)或食管中段反四腔心切面(角度140°~160°)定量房间隔穿刺点平面距二尖瓣瓣环平面的高度(正常范围在4.0~5.0 cm)(图7),且房间隔穿刺点在前后方向、上下方向位置合适(食管中段四腔心切面可以观察到)。但是不同二尖瓣病变部位对于穿刺点的高度要求稍有不同:如果病变部位偏外交界,穿刺点高度稍微低一点;病变部位偏内交界,穿刺点稍微高一点。

图6 X-Plane 双切面 A. 为食管中段上、下腔静脉,显示穿刺点位于房间隔中段卵圆窝偏上靠近上腔静脉(★所示);B. 食管中段大血管短轴切面,显示穿刺点位于房间隔中段卵圆窝偏后处靠近左心房顶(★所示)

图7 A. 食管中段四腔心切面,显示房间隔穿刺平面距二尖瓣瓣环平面的高度为4.6 cm(★显示房间隔穿刺点位置);B. 应用三维定量软件测量房间隔穿刺平面距二尖瓣瓣环平面的高度为5.35 cm(★显示房间隔穿刺点位置)
5. 3 引导鞘管和夹合系统进入左心房
其步骤及规范为:(1)置入Superstiff超硬导丝至左上肺静脉;(2)在TEE引导下沿导丝送可调弯大鞘至左心房内并测量其顶端距房间隔的距离,一般为2.0~2.5 cm,若深度不合适应该及时提醒手术医师;(3)选择合适夹子沿可调弯大鞘进入输送系统。此时要求2D TEE、3D TEE 清晰显示输送系统顶端在左心房内的位置,避免与后侧、侧面的左心房壁及左心耳接触(图8);(4)调整弹道。调整输送系统,使之与左心室长轴平行,在X-Plane工作切面显示位于左心房的输送系统与二尖瓣平面垂直,且位于反流区正上方,应用二尖瓣口的三维“外科视野”,可立体观察二尖瓣结构与输送系统的空间立体关系[22](图9),引导介入医师 调整输送系统的方向。也可应用三维成像的X-Plane工作切面法同时显示来引导和监测。弹道建立满意后,可以将输送系统往左心室推送,测试弹道运动轨迹是否符合预期。

图8 A. 大血管短轴切面的三维图像,显示大鞘顶端与周围结构的空间关系(★显示大鞘顶端);B. 大血管短轴切面,显示大鞘穿过房间隔进入左心房,顶端(★所示)距房间隔穿刺点的距离为2.6 cm;C. 应用三维定量软件测量大鞘顶端距房间隔穿刺点的距离约2.6 cm
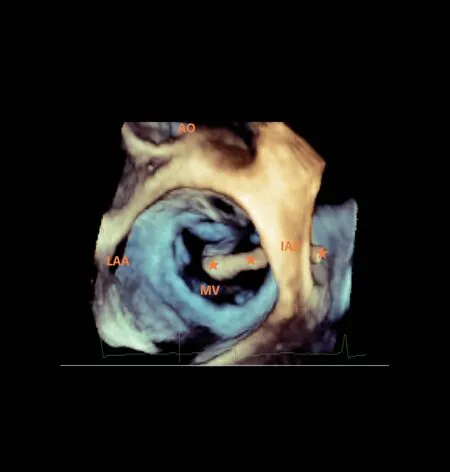
图9 二尖瓣左心房观切面,从左心房俯视鞘管在二尖瓣口上方的前后、左右关系,引导介入医师调整鞘管的方向(★所示鞘管)
5. 4 引导夹合器在二尖瓣口上方的定位
一旦输送系统的顶端置于二尖瓣口上方,首先应用二尖瓣口的三维“外科视野”或X-Plane工作切面测试弹道系统即输送系统与二尖瓣环垂直并位于二尖瓣口中央(图10)。然后打开夹合臂(60°~120°),应用二尖瓣口的三维“外科视野”引导(图11),或者应用X-Plane工作切面引导旋转夹合臂与二尖瓣关闭线垂直,且位于二尖瓣病变处或反流束最大处,夹合器能平均分裂二尖瓣反流束,且到前后瓣叶距离均衡。虽然经胃的二尖瓣水平短轴切面在大约1/3的患者中较难获得,但是当实时二尖瓣口的三维“外科视野”无法显示满意的图像时,可应用经胃的二尖瓣水平短轴切面来显示。

图10 A~B. 二尖瓣口的三维“外科视野”显示输送系统位于二尖瓣口的中央,并与橙色二尖瓣关闭线垂直(★所示鞘管);C. X-Plane 工作切面,显示输送系统位于二尖瓣口中央并与二尖瓣环垂直(★所示鞘管)

图11 二尖瓣口的三维“外科视野”显示打开的夹合臂与橙色关闭线垂直,并位于病变部位(5 点和12 点处)
5. 5 引导夹合器在二尖瓣口下定位
在应用X-Plane工作切面引导下,将夹合器送入左心室中 上段,并在X-Plane工作切面或“工作三切 面”或Multi-Vue多切面(适合于非A2、P2中央区病变)监测和引导下,将夹合器缓慢回撤至二尖瓣叶下方并微调整夹合位置,使其位于二尖瓣病变处或二尖瓣反流最大束位置,并且保证夹合臂仍与二尖瓣关闭线垂直(图12),且到前后瓣叶距离均衡,且在深度上可以轻易捕获二尖瓣叶,并预估前后叶夹合量足够。在A2、P2处及附近夹合时,在食管中段X-Plane工作切面的二尖瓣交界处二腔心切面,夹合器的两个臂翼被侧面显示呈“线状”,而在食管中段X-Plane工作切面的左心室长轴切面,夹合器的两个臂翼被正面显示,呈打开的“倒伞状”(图13)。
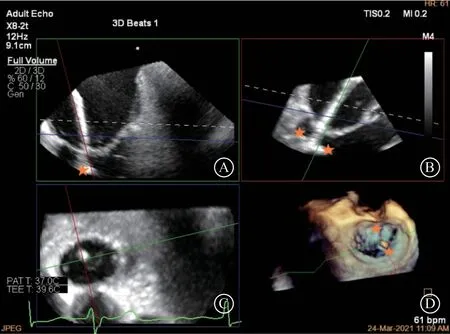
图12 Multi-Vue 多切面 A. 食管中段二尖瓣交界处二腔心切面显示夹合臂位于A2、P2 偏内交界处(★显示夹合臂);B. 食管中段与左上图垂直并偏内交界处的左心室长轴切面,显示夹合臂与二尖瓣关闭线垂直;C. 与图A、B 切面相垂直的横切面;D.二尖瓣口的三维“外科视野”显示夹合臂位于A2、P2 偏内交界处并与二尖瓣关闭线垂直
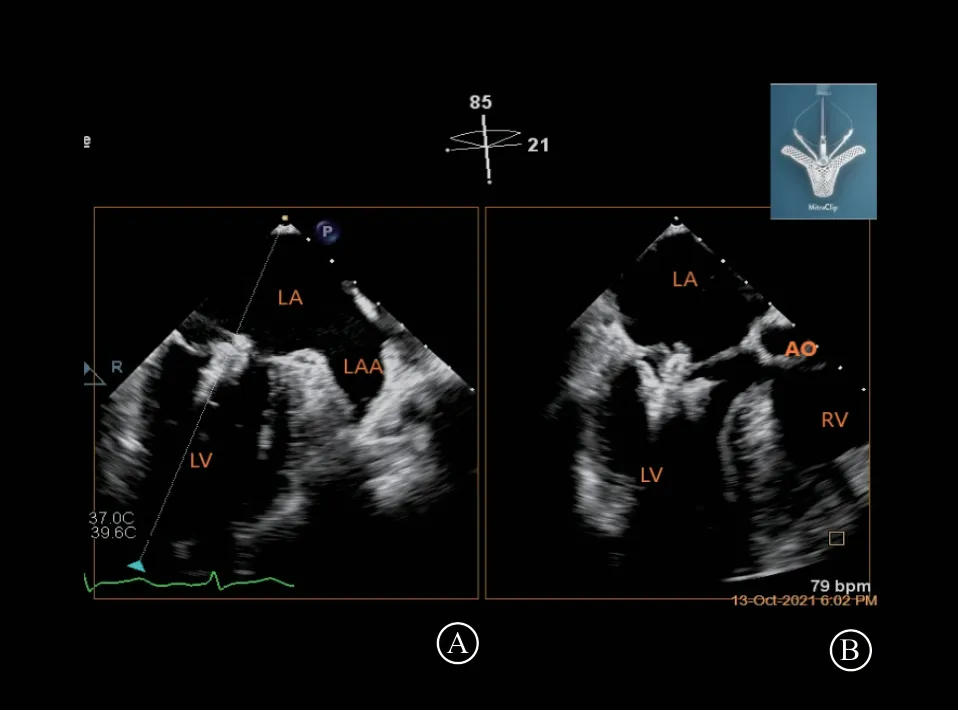
图13 X-Plane 工作切面 A. X-Plane 工作切面的二尖瓣交界处二腔心切面,显示夹合器的侧面呈“线状”;B.X-Plane 工作切面的左心室长轴切面,显示夹合器的正面,由两个夹合臂和中央两个带有倒刺的夹合片组成,呈打开的“倒伞状”
5. 6 引导夹合器夹合
当夹合器定位满意后,充分打开夹合器(120°~150°),当二尖瓣前后叶在舒张期时落在夹合器的下夹臂上,预估前后叶夹合量及夹合钟向合适,放下上夹捕获瓣膜,确认上夹已捕获瓣膜(上夹随着瓣叶跳动)夹合量合适,夹合器无发生旋转,闭合夹合器夹合瓣膜,监测夹合器闭合情况,此过程应用Multi-Vue切面或X-Plane工作切面来监测。
5. 7 引导夹合器释放
评估夹合效果、夹合器装置能否释放是术中TEE评价的重要步骤,包括四个方面评价:(1)形态学观察。二尖瓣口的三维“外科视野”和从左心室面观察二尖瓣口均显示双口二尖瓣,并且仔细观察由二尖瓣前叶、夹合器和后叶组成的“桥”结构(图14),如果组织桥较宽,桥组织稳定,前后叶夹合量均衡,表明瓣叶的良好捕获,夹合器解离后,“桥”结构稳定;如果前后叶夹合量不均衡,一侧的桥组织较细,或瓣膜张力很大,分别表明瓣叶夹合量过少或过多,夹合器解离后,“桥”结构将会前后或左右晃动(受力不均所致),或有撕裂瓣叶风险。(2)夹合量测量。对于12 mm长夹子理想夹持长度为9 mm以上,对于9 mm短夹子理想夹持长度为6 mm以上。但是无论长、短夹子,夹合长度至少达到5 mm,否则有脱落风险。评估夹合量常用方法包括①减法,即对比夹持前后前瓣叶和后瓣叶长度(图15);②直接测量法,TEE测量夹合瞬间夹住的瓣叶长度。(3)评估残余反流程度及机制。彩色多普勒多切面评估二尖瓣残余反流的程度,并关注肺静脉内是否存在收缩期反向血流。对于残余反流详细评估,应用彩色多普勒根据X-Plane工作切面的食管中段二尖瓣交界处二腔心切面将取样线从夹合器装置外侧(P1、A1处)、夹合器装置处(P2、A2处)及夹合器内侧(P3、A3处)进行移动,得到不同位置的食管中段左心室长轴切面,判断残余反流的程度及机制,为下一步手术策略提供建议(调整夹子位置、钟向、夹合量或置入第二枚夹子)。(4)评价二尖瓣夹合后二尖瓣狭窄的情况。如果二尖瓣平均跨瓣压差≤5 mmHg,且心率和血压正常,表明夹合术后未引起二尖瓣狭窄;如果二尖瓣平均跨瓣压差升高,则必须排除高动力状态、心动过速、残余MR或者狭窄,以明确是否夹合后引起二尖瓣狭窄。但文献表明,在FMR患者中,根据COAPT的数据显示,稍微增高的术后二尖瓣平均跨瓣压差并未显示较差的预后[23]。对于血压较低者,应在注射肾上腺素提升血压后,应用TEE再次评价MR的程度和二尖瓣平均跨瓣压差[24-25]。对于夹合效果满意者,可释放夹合器(表5)。在释放夹子过程中,要观察瓣膜张力是否过大、瓣叶是否滑脱,夹合器是否张开、反流是否变多,需及时提醒术者;最后要确认夹合器是否完全解脱。如果夹合效果不满意,可重新打开夹子,在左心室微调整夹合器的位置,或者夹合器反转并退回到左心房重新调整后,重复上述步骤,或者考虑置入第二枚夹子。总而言之,术中TEE对夹合器是否可以释放以及制定下一步手术策略是至关重要的。
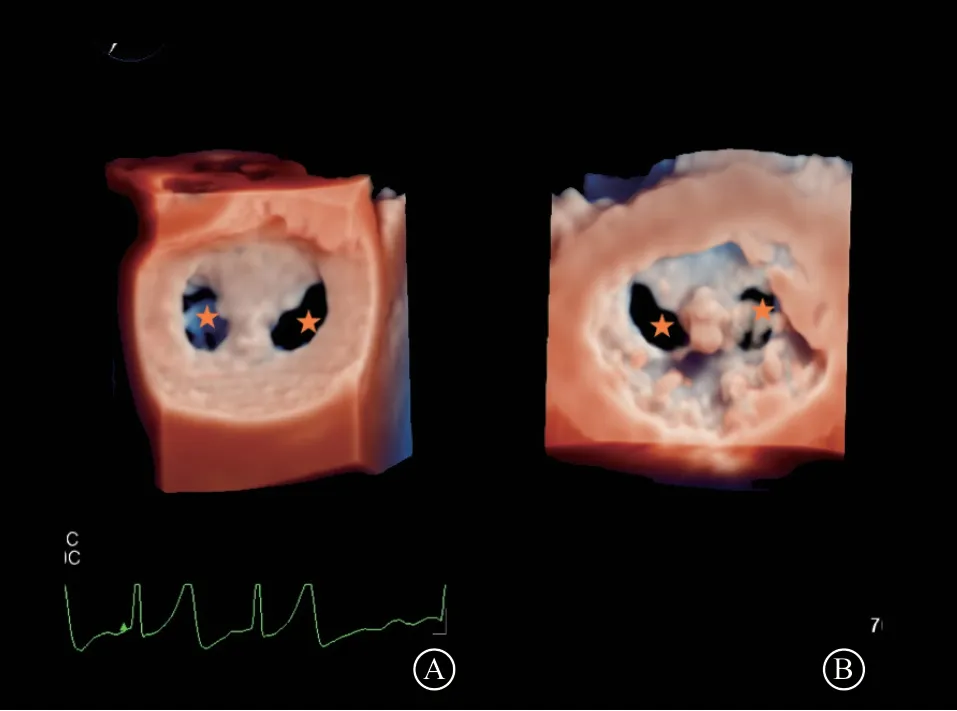
图14 A. 二尖瓣口的三维“外科视野”,显示大小基本相等的双口二尖瓣和由前叶、夹合器、后叶组成的“桥”结构;B. 从左心室面观察二尖瓣口,同样显示大小基本相等的双口二尖瓣和“桥”结构

图15 A.食管中段左心室长轴切面,显示二尖瓣夹合术前A2、P2 处长度;B.与A 图相同切面,显示二尖瓣夹合术后A2、P2 处长度。然后术前、术后两者相减,得到二尖瓣前后叶的夹合量(>7 mm)

表5 TEER 术中是否可以释放夹子的经食管超声心动图建议标准
5. 8 引导输送鞘管 撤离
在食管中段大血管短轴切面或食管中段上下腔切面或食管中段四腔心切面实时监测输送系统安全后撤至大鞘内,然后食管中段大血管短轴切面监测过房间隔大鞘安全撤离至右心房,即刻以彩色多普勒评估房水平分流,最后食管中段多切面判断心包腔内有无心包积液,如果无心包积液术中TEE监测完成。
6 经心尖TEER术中的超声心动图操作规范
6. 1 确定心尖穿刺点
经胸探头置于第五肋间或第六肋间,显示标准的心尖四腔心切面,尽量使左心房上下径 、左心室上下径最大,根据探头位置选择合适的心尖穿刺点,并于相应肋间体表标记。经体表标记处切开,暴露心尖,扩大手术视野后,术者以指尖触压心尖预穿刺部位,结合 X-Plane工作切面定位心尖穿刺点,要求手指触压心尖部位,在X-Plane工作切面上同时显示心尖部凹陷,并指向二尖瓣口中央(图16),该手指触压部位确定为心尖穿刺点[26]。
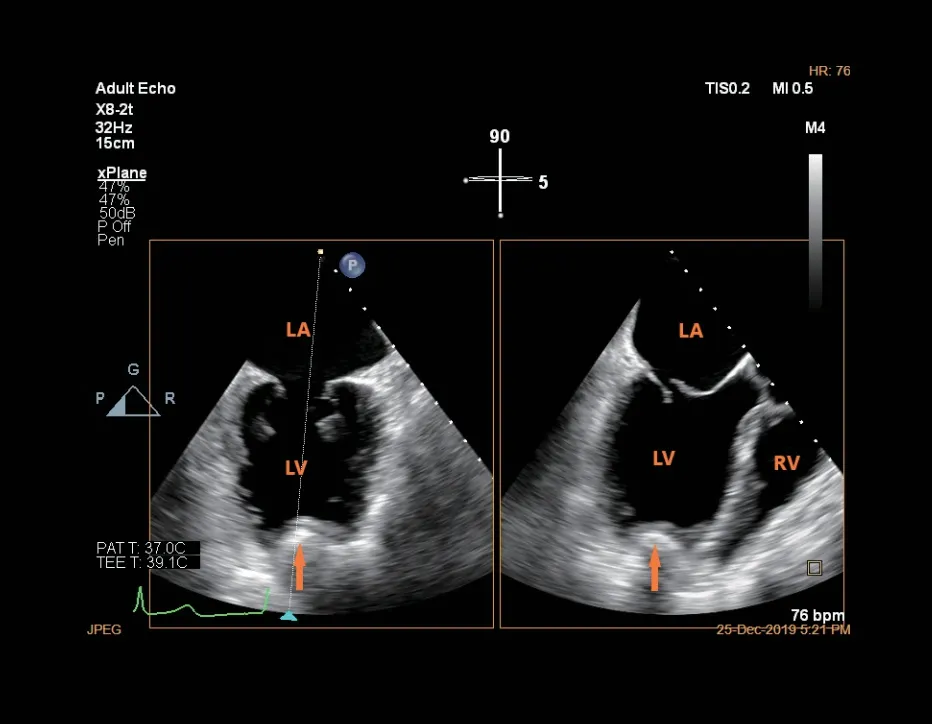
图16 X-Plane 工作切面显示手指在心尖触压点(橙色箭头所示)
6. 2 穿刺心尖
围绕预穿刺点缝合带有垫片荷包,使用微穿刺针穿刺。在X-Plane工作切面或工作三切面引导和监测下,导丝从心尖穿刺点进入左心室,并缓慢向上穿过二尖瓣口至左心房,观察导丝指向是否指向二尖瓣口中央,再次确认穿刺点位置的准确性。
6. 3 跨瓣器及大鞘入左心房
经导丝引导送入16 F输送鞘,在X-Plane工作切面监测下,将16 F输送鞘慢慢地推送至左心室近乳头肌水平。退出导丝,将跨瓣器输送至16 F鞘管内,在 X-Pla ne工作切面监测下将跨瓣器在左心室中央慢慢推送至二尖瓣口,并在舒张期二尖瓣打开时跨过二尖瓣进入左心房(图17)。在X-Plane工作切面监测下,术者将跨瓣器做前(A2)、后(P2)、左(外交界C1)、右(内交界C2)四个方向自由度测试,观察跨瓣器在左心房内有无形变以及是否缠绕二尖瓣腱索。沿跨瓣器输送鞘管进入左心房,在X-Plane工作切面和(或)工作三切面下实时监测输送鞘管顶端和左心房壁的位置关系(图18),确认输送鞘管深度合适后撤出跨瓣器。

图17 跨瓣器入左心房的过程 A. X-Plane 工作切面显示跨瓣器慢慢从鞘管内推出(★所示);B. X-Plane 工作切面显示跨瓣器慢慢推送至二尖瓣口(★所示);C. X-Plane 工作切面显示跨瓣器在二尖瓣开放时入左心房(★所示)

图18 输送鞘管入左心房后撤出“跨瓣器” A. 工作三切面显示输送鞘管沿“跨瓣器”钢杆入左心房(★所示“跨瓣器” 所示鞘管);B.工作三切面显示“跨瓣器”已从输送鞘管撤出( 所示鞘管)
6. 4 输送、打开夹合器
在X-Plane工作切面或工作三切面监测和引导下,将夹合器装置送入输送鞘管内,并慢慢推送至鞘管顶端,打开上夹,缓慢回撤输送鞘管后,再打开下夹,并将夹合器在左心房内完全展开,根据X-Plane工作切面“中心线”原则或工作三切面调整夹合臂的方向,使夹合器在二尖瓣口上方左心房内位于最大反流区正上方与二尖瓣关闭线垂直(常规二尖瓣的病变部位位于A2或P2处),即工作三切面(图19)的上图二尖瓣左心房观切面显示打开的上下夹指向二尖瓣口12点和6点,左下图食管中段二尖瓣交界处二腔心切面,显示打开的上下夹,呈“线状”并位于A2处;右下图食管中段左心室长轴切面,显示打开的上下夹,呈“工”字状并位于A2、P2对合处[24-25]。

图19 工作三切面显示左心房内完全打开的上下夹,位于二尖瓣口中央并与二尖瓣关闭线垂直(上图为二尖瓣左心房观切面,显示打开的二尖瓣位于瓣口中央并与二尖瓣关闭线垂直(★所示) ;左下图为食管中段二尖瓣交界处二腔心切面,侧面显示打开的上下夹,呈“线状”(★所示);右下图为食管中段左心室长轴切面,正面显示打开的上下夹,呈“工”字状(★所示)
6. 5 定位、捕获、夹合及释放
这些步骤基本原则同经股静脉TEER,不做详细介绍。在X-Plane工作切面或工作三切面监测和引导下缓慢回撤整个夹合系统,使下夹跨过二尖瓣口退至左心室,但上夹仍在左心房,夹合器到前后瓣叶距离均衡,且保持夹合臂的钟向不变,然后缓慢将下夹上移托住前、后瓣叶病变部位或反流束最大处,此时将上夹回撤,夹合并收拢夹合臂(图20)。评估效果满意后,释放夹合器。经心尖的TEER的超声心动图切面及要求总结为表6。

表6 经心尖TEER 超声心动图引导的所需切面及评估要点

图20 工作三切面监测和引导下二尖瓣的夹合过程 A. 工作三切面显示上、下夹位于二尖瓣口上方( 所示);B. 工作三切面显示下夹位于左心室二尖瓣口下方,上夹位于左心房二尖瓣口上方( 所示);C. 工作三切面显示下夹上移并托住二尖瓣前后叶( 所示);D. 工作三切面显示上、下夹夹合并收拢夹合臂,形成双口二尖瓣( 所示)
7 TEER术后随访评价
在TEER术后,患者必须定期进行常规经胸超声心动图检查,包括出院前、术后1个月、术后3个月、术后6个月、术后1年、术后2年、术后3年、术后4年、术后5年。随访内容包括:MR程度、平均跨瓣压差、MVA,夹合器位置是否移位或脱落、心腔大小、肺动脉压力、肺静脉血流、房间隔残余分流(TEER经股静脉房间隔穿刺)、LVEF等参数指标。如果经胸超声心动图检查因透声差不能明确诊断,则需要进行TEE检查以明确诊断。
执笔专家:潘翠珍(复旦大学附属中山医院),潘文志(复旦大学附属中山医院),周达新(复旦大学附属中山医院),刘先宝(浙江大学医学院附属第二医院),宋光远(首都医科大学附属北京安贞医院)
专家组成员(按姓氏拼音排序):陈良龙(福建医科大学附属协和医院),陈茂(四川大学华西医院),陈海燕(复旦大学附属中山医院),陈韵岱(中国人民解放军总医院心血管病医学部),段福建(中国医学科学院阜外医院),方臻飞(中南大学湘雅二医院),冯沅(四川大学华西医院),葛均波(复旦大学附属中山医院),郭应强(四川大学华西医院),何奔(上海交通大学医学院附属胸科医院),姜正明(郑州大学第一附属医院),孔祥清(南京医科大学第一附属医院),李飞(中国人民解放军空军军医大学第一附属医院),李捷(广东省人民医院),李伟(复旦大学附属中山医院),陆方林(中国人民解放军海军军医大学第一附属医院),罗建方(广东省人民医院),马为(北京大学第一医院),马小静(武汉亚心总医院),孟欣(中国人民解放军空军军医大学第一附属医院),孟旭(首都医科大学附属北京安贞医院),潘湘斌(中国医学科学院阜外医院),彭小平(南昌大学第一附属医院),蒲朝霞(浙江大学医学院附属第二医院),秦永文(中国人民解放军海军军医大学第一附属医院),尚小珂(华中科技大学同济医学院附属协和医院),舒先红(复旦大学附属中山医院),宋治远(中国人民解放军陆军军医大学第一附属医院),苏茂龙(厦门大学附属心血病管医院),苏晞(武汉亚心总医院),孙旭东(福建医科大学附属协和医院),唐红(四川大学华西医院),唐熠达(北京大学第三医院),陶凌(中国人民解放军空军军医大学第一附属医院),田家玮(哈尔滨医科大学附属第二医院),修建成(南方医科大学南方医院),徐凯(中国人民解放军北部战区总医院),王建安(浙江大学医学院附属第二医院),王建德(中国医学科学院阜外医院),王浩(中国医学科学院阜外医院),王焱(厦门大学附属心血管病医院),魏来(复旦大学附属中山医院),吴永健(中国医学科学院阜外医院),伍广伟(广西壮族自治区人民医院),伍伟峰(广西医科大学第一附属医院),谢明星(华中科技大学同济医学院附属协和医院),杨剑(中国人民解放军空军军医大学第一附属医院),于波(哈尔滨医科大学附属第二医院),曾杰(四川省人民医院),张戈军(中国医学科学院阜外医院),张海波(首都医科大学附属北京安贞医院),张俊杰(南京市第一医院),张奇(同济大学附属东方医院),张瑞岩(上海交通大学医学院附属瑞金医院),张玉顺(西安交通大学附属第一医院),赵仙先(中国人民解放军海军军医大学第一附属医院),周玉杰(首都医科大学附属北京安贞医院),朱达(云南省阜外心血管病医院)。
利益冲突所有作者均声明不存在利益冲突
