十二指肠与空回肠间质瘤临床病理特征比较及预后影响因素
2022-11-18单治理
单治理
苏州市独墅湖医院(苏州大学附属独墅湖医院)普外科,江苏苏州 215000
胃肠道间质瘤(gastrointestinal stromal tumor,GIST)是最常见的胃肠道间叶源性肿瘤,大多具有CKIT或血小板源性生长因子受体的基因活化突变[1]。GIST可发生在胃肠道任何部位,小肠是其发生的第二大部位[2]。小肠GIST因临床症状隐匿,且诊断主要依赖于影像学检查,多数患者确诊时已处于中高危险度。因此小肠GIST更具侵袭性,预后更差[3]。在小肠GIST中,十二指肠GIST(duodenal stromal tumor,D-GIST)因其解剖部位、临床表现、诊断方法以及手术方式同空回肠GIST(jejunoileal stromal tumor,JI-GIST)都有一定差异,所以两者的临床病理特征和预后可能不同[4-5],本研究旨在通过回顾性分析92例小肠GIST患者的临床资料,探讨D-GIST和JI-GIST的临床病理特征及预后的差异,以提高小肠GIST的诊治水平。
1 资料与方法
1.1 一般资料
回顾性分析2008年1月至2017年8月苏州市独墅湖医院收治的92例小肠间质瘤患者资料。纳入标准:①病理诊断为原发小肠GIST;②经手术治疗;③临床、病理及随访资料完整。排除标准:①合并其他恶性肿瘤;②不可手术、初始转移无法切除、复发转移再次手术;③因手术并发症死亡;④临床、病理及随访资料不完整。92例小肠GIST患者中,男51例(55.4%),女41例(44.6%);年龄27~84岁,平均(57.8±1.2)岁;D-GIST 23例,JI-GIST 69例;术后危险度分级参照美国国立卫生研究院(National Insti tutes of Health,NIH)改良版[6],极低危5例(5.4%),低危21例(22.8%),中危2例(2.1%),高危64例(69.6%)。本研究经苏州大学附属第一医院伦理委员会审查通过(伦理号:2020205)。
1.2 观察指标及随访
统计患者年龄、性别、肿瘤部位、首发症状、手术方式、肿瘤大小、核分裂象、免疫组化、基因检测、伊马替尼治疗与否等资料。采用门诊、网络、电话等方式随访,末次随访时间为2020年8月1日,中位随访时间56.2个月。
1.3 统计学方法
采用SPSS 24和Graphpad 5进行统计学分析,计量资料用均数±标准差(±s)表示,两组间比较采用t检验;计数资料用率表示,组间比较采用χ2检验。Kaplan-Meier法绘制生存曲线并计算生存率,采用log-rank检验进行单因素分析,当单因素分析P<0.05,则纳入Cox比例风险模型,采用逐步回归方法进行多因素分析。以P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者临床病理特征的比较
两组患者的年龄、性别、核分裂象、免疫组化阳性率、CKIT基因突变情况以及伊马替尼治疗年限时间等,差异无统计学意义(P>0.05)。D-GIST最常见的首发症状为消化道出血(52.2%),其次是腹痛(26.1%),而JI-GIST最常见的首发症状为腹痛(39.1%)及腹部肿物(15.9%)。JI-GIST组中,肿瘤直径>5cm患者比例高于D-GIST组(P<0.001)。JI-GIST组高危患者比例高于D-GIST组(P<0.001)。
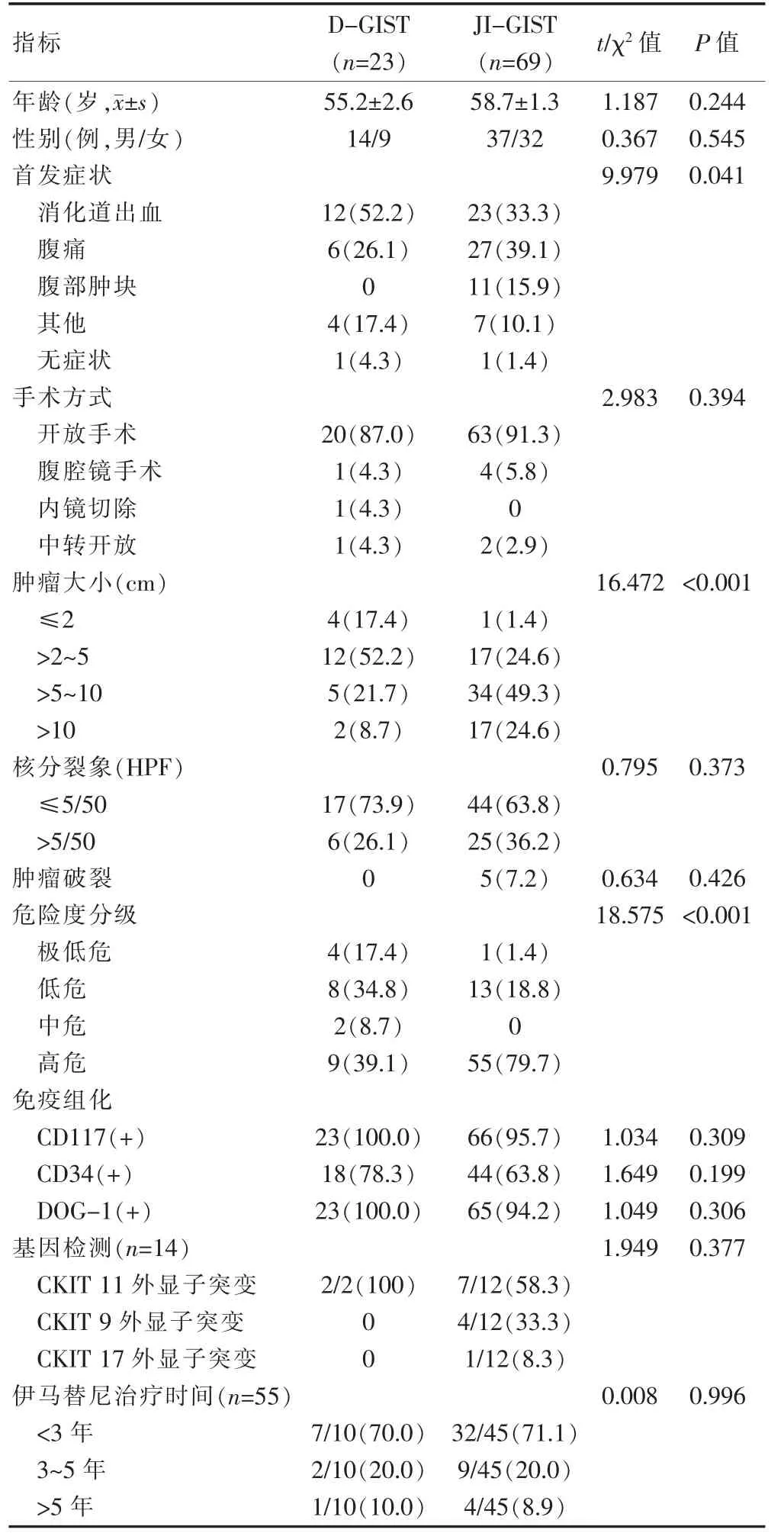
表1 两组患者临床病理特征的比较[n(%)]
2.2 两组患者复发及生存情况分析
92例患者中位随访时间为56.2个月(5.7~128.4个月)。术后总复发率39.1%(36/92),其中JI-GIST术后复发率为47.8%(33/69),D-GIST术后复发率为13.0(3/23);JI-GIST中位无复发生存时间(relapse free survival,RFS)为80.6月,D-GIST中位RFS未达到;JI-GIST与D-GIST的3年无复发生存率为72.0%、95.7%(HR:2.506,95%CI:1.183~5.305,P=0.016)。JIGIST与D-GIST的3年总体生存率为89.9%、100%(HR:2.666,95%CI:0.874~8.131,P=0.085)(图1)。
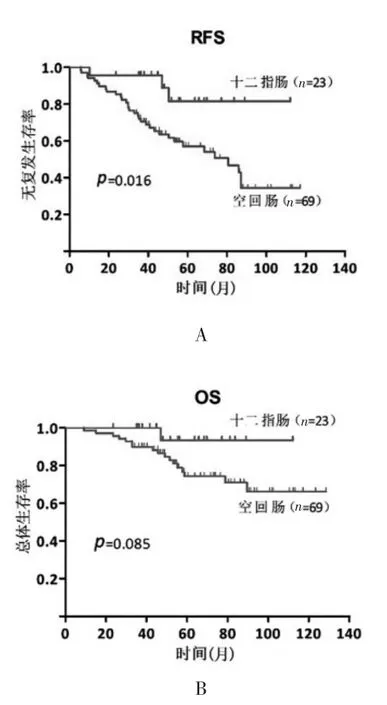
图1 D-GIST和JI-GIST患者的复发及生存曲线
2.3 影响小肠GIST预后的单因素分析
单因素分析结果显示:性别、肿瘤部位、肿瘤大小、核分裂象和危险度分级与3年无复发生存率有关(P<0.05);年龄、性别、肿瘤大小、核分裂象和危险度分级与3年总体生存率有关(P<0.05)(表2)。
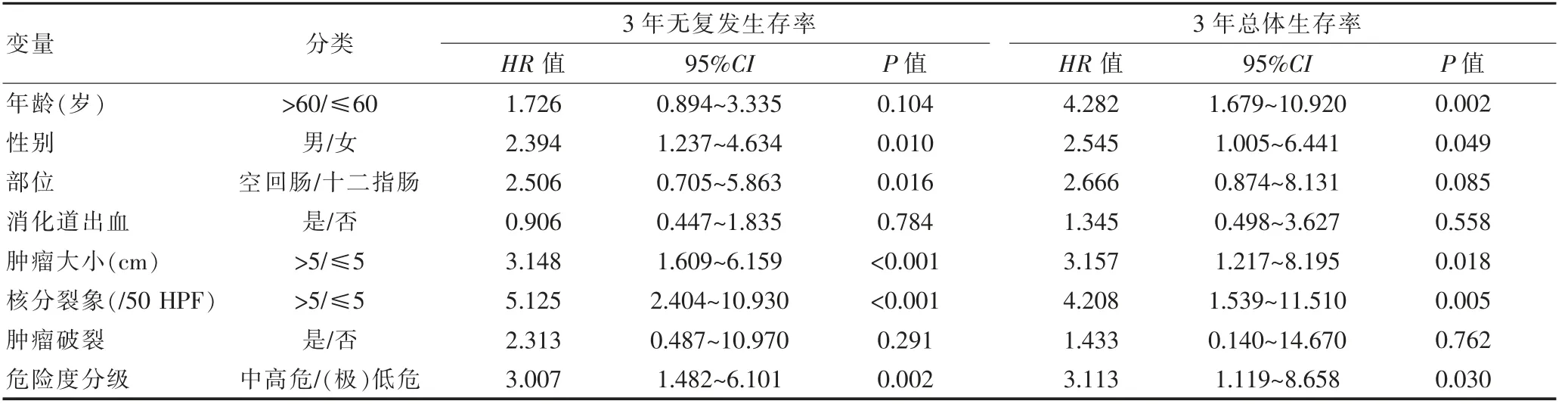
表2 92例小肠GIST复发和生存预后的单因素分析
2.4 影响小肠GIST预后的多因素Cox分析
对单因素分析中有意义的指标进行赋值(表3),纳入多因素Cox分析。结果显示:肿瘤直径>5 cm、核分裂象>5/50 HPF是影响患者复发的独立危险因素(表4);年龄>60岁、肿瘤直径>5 cm、核分裂象>5/50 HPF是影响患者生存预后的独立危险因素(表5)。

表3 各变量赋值情况

表4 影响小肠GIST复发的多因素分析

表5 影响小肠GIST生存预后的多因素分析
3 讨论
胃肠道间质瘤可发生于全消化道任何部位,胃部发生率最高,小肠次之。对于食管、胃以及结直肠GIST,可通过内镜检查及活检以明确诊断[7]。而对于小肠GIST,普通消化内镜检查难以实现,诊断主要依赖于影像学检查[8]。且小肠GIST临床症状隐匿、无特异性,当出现腹痛、消化道出血、腹部包块、腹胀等临床症状就诊时,多数患者已处于中高危险度[9]。消化道出血症状更易引起患者重视[10],且D-GIST可通过胃镜检查明确,本研究中23例D-GIST患者中有14例通过内镜检查明确。而JI-GIST患者最常见的轻度腹部隐痛不适症状往往不够引起重视。此外,因腹腔空间大,JI-GIST出现临床症状也往往比D-GIST晚,就诊时肿瘤体积已比较大。这些综合因素使得JI-GIST较D-GIST更难以发现,且JI-GIST患者就诊时肿瘤分期也较D-GIST晚。小肠GIST误诊率为39.3%,当患者出现腹痛、消化道出血、腹胀症状,内镜检查无阳性发现时,应根据临床症状和体格检查并结合腹部超声、消化道造影、CT或者MRI等检查综合判断,以防漏诊、误诊[11]。
胃肠道出血是否意味着胃肠间质瘤破裂以及对肿瘤预后的影响存在争议。陶凯雄[10]通过对800例原发性GIST患者进行回顾性分析后发现,存在消化道出血症状的小肠GIST患者的RFS和OS均优于非消化道出血组。但在胃和结直肠GIST中则不存在这种差异。对于难行内镜检查的小肠GIST而言,这可能与消化道出血症状易引起警觉和重视,从而较早发现病灶有关[12]。对本研究中存在消化道出血症状的35例患者进行分析可知,消化道出血对患者预后并无影响。但因本研究样本量较小,这可能是结果同前述研究结果不同的主要原因。
本研究发现JI-GIST的复发率高于D-GIST,这和JI-GIST确诊时肿瘤直径较大、危险度分级为高危比例更高有关。在69例JI-GIST中,有5例发生肿瘤破裂,D-GIST无肿瘤破裂。对于GIST而言,手术应完整切除肿瘤,避免肿瘤破裂,较多研究都表明肿瘤破裂是GIST复发的危险因素[13]。两组患者总生存率虽无统计学差异,但从生存曲线来看,随着随访时间延长,JI-GIST的预后较D-GIST差。危险因素分析显示,影响复发和预后的独立危险因素主要为肿瘤大小和核分裂象大小,这和以往诸多研究结果一致[14-15]。国内一项研究也得出相似结论:肿瘤最大径≥5.3 cm和核分裂象>5/50 HPF可作为预测GIST术后不良结局的独立危险因素[16]。Cox多因素分析发现年龄也是影响预后的独立危险因素,一项针对40例GIST研究显示,60岁以上的患者的死亡率风险是≤60岁患者的4.5倍[17]。
以往研究已经证实术后伊马替尼辅助治疗可降低复发率,延长生存时间[18]。本研究中部分患者早期因经济原因,没有术后服用伊马替尼辅助治疗,而是在肿瘤复发后再次服药,因此本研究未将伊马替尼治疗纳入因素分析。
综上所述,D-GIST比JI-GIST更易早期确诊,因此术后复发风险较JI-GIST低。肿瘤直径>5cm和核分裂象>5/50HPF是影响小肠GIST复发和预后的独立危险因素。
