靶向B淋巴细胞治疗系统性红斑狼疮的生物制剂:贝利尤单抗与泰它西普
2022-11-16张莹莹王世颖束庆严晶葛卫红华冰珠中国药科大学南京鼓楼医院南京0008南京鼓楼医院风湿免疫科南京0008南京鼓楼医院药学部南京0008南京临床药学中心南京0008
张莹莹,王世颖,束庆,严晶,葛卫红,华冰珠*(.中国药科大学南京鼓楼医院,南京 0008;.南京鼓楼医院风湿免疫科,南京 0008;3.南京鼓楼医院药学部,南京 0008;4.南京临床药学中心,南京 0008)
系统性红斑狼疮(systemic lupus erythematosus,SLE)是一种系统性自身免疫病,以全身多系统多脏器受累、反复复发与缓解、体内存在大量自身抗体为主要临床特点,如不及时治疗,会造成受累脏器的不可逆损害,最终导致患者死亡[1]。SLE 致病原因较为复杂,其中B 淋巴细胞过度激活导致的免疫复合物(IgM、IgA、IgG)大量沉积至关重要[2]。目前临床的传统治疗药物主要为糖皮质激素、免疫抑制剂、抗疟药等[3]。但是以上传统的药物治疗存在以下几点问题:①除糖皮质激素外,绝大多数药物治疗起效较慢;② 约有60%的患者疗效不佳;③ 药物不良反应多等[4]。因此,临床亟待发现新的治疗药物。
随着SLE 发病机制的研究进展,研究者发现使用靶向B 淋巴细胞的治疗不仅能达到与传统疗法相似甚至更好的疗效,且不良反应更小,起效更快[5]。目前国内批准靶向B 淋巴细胞治疗SLE的生物制剂仅有贝利尤单抗及泰它西普两种。本文将从作用机制、用法用量、药动学、有效性、安全性等方面讨论两者的临床特征,帮助临床医师了解最新的研究进展。
1 作用机制
B 淋巴细胞刺激物(B lymphocytes timulator,BLyS)又称B 细胞激活因子(B-cell activation factor,BAFF),与增殖诱导配体(a proliferation inducing ligand,APRIL)同属肿瘤坏死因子配体家族[6]。研究表明在SLE 患者中BLyS 与APRIL水平升高,且高水平的BLyS 及APRIL 与SLE 患者的高疾病活动度和高复发率密切相关,可能原因为BLyS 与APRIL 共同调控B 淋巴细胞存活、增殖、分化及抗体分泌[7-8]。具体作用机制主要与BLyS 和APRIL 的下游调控靶点有关,研究显示按照结合强度由强至弱BLyS 依次与BAFF 受体(BAFF receptor,BAFFR)、B 淋巴细胞成熟抗原(B-cell maturation antigen,BCMA)及跨膜蛋白活化物(transmembrane activator and calciummodulator and cyclophilin ligand interactor,TACI)结合,APRIL 依次与BCMA、TACI 结合[9]。其中BAFFR 分布于除浆细胞外的所有B 淋巴细胞中,研究表明BAFFR 通过介导IκB 激酶 1 和IκB 激酶 2 激活非经典和经典NF-κB 通路,该通路能够维持B 淋巴细胞凋亡抑制因子水平,从而促使幼稚B 淋巴细胞成熟和记忆细胞存活[10-11];BAFFR 缺乏或抗BLyS 治疗将阻滞未成熟B 淋巴细胞发育和抑制记忆细胞的存活,这导致成熟B 淋巴细胞、浆细胞和记忆细胞循环量减少,进一步降低IgM(主要由从头激活的幼稚B 淋巴细胞分泌)及IgG(主要由记忆细胞重新激活分泌)水平,而IgA 的分泌不受BAFFR 的影响,表现为IgA 水平正常或升高[10,12]。TACI 主要分布于边缘区B 淋巴细胞、滤泡性B 淋巴细胞和浆细胞中[6],研究表明TACI 可介导B 淋巴细胞转录因子诱导浆细胞分化,影响NF-κB 通路和抑制促凋亡蛋白共同促进浆细胞存活[13-15];此外,边缘区B 淋巴细胞和滤泡性B 淋巴细胞中TACI 水平上调后,IgA 和 IgG 分泌随之增加[6,16],原因可能是BLyS 和/或APRIL 与TACI 的结合增加了激活诱导的胞苷脱氨酶转录水平,导致多糖特异性抗体同种型转换为IgA 和IgG[6];记忆细胞中虽表达TACI,但其如何影响记忆细胞尚未可知[6]。BCMA 主要分布于浆细胞,研究表明BCMA 也可以通过影响NF-κB 通路及上调抗凋亡蛋白促进浆细胞的存活[6,15],尤其是长寿浆细胞的存活[17]。BAFFR、BCMA、TACI 三种受体作用于B 淋巴细胞发育的不同时期,共同发挥促进SLE患者抗体异常分泌的作用。泰它西普及贝利尤单抗均为靶向B 淋巴细胞的生物制剂,具体作用机制见图1。
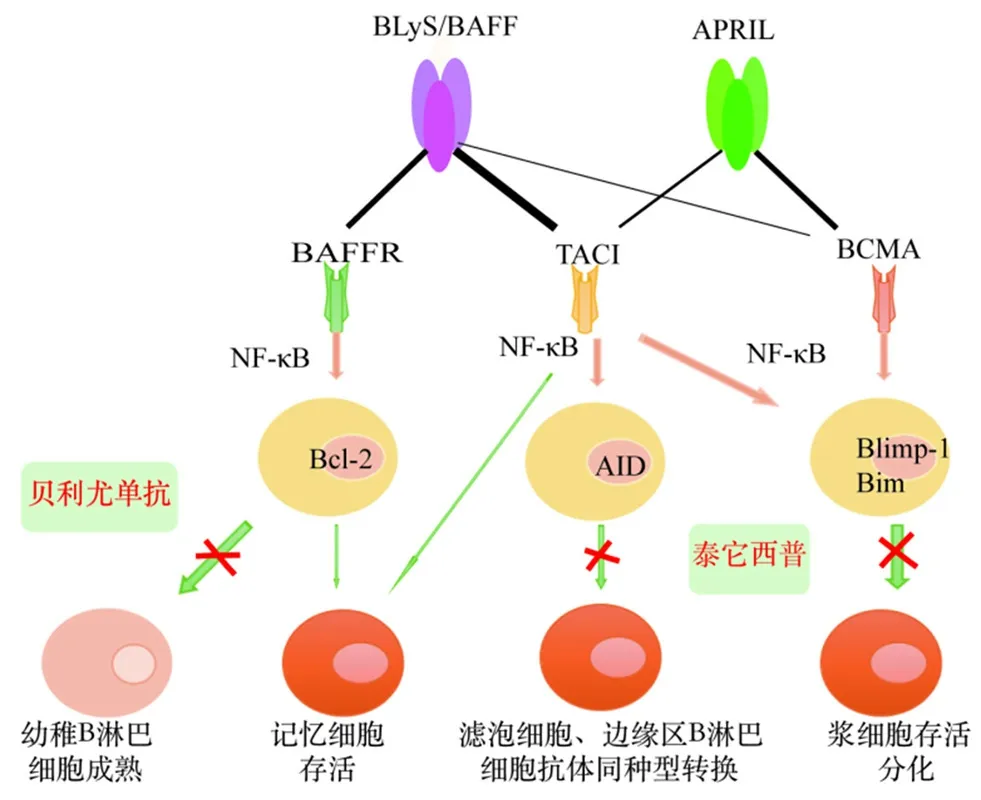
图1 泰它西普及贝利尤单抗靶向B 淋巴细胞治疗SLE 的机制Fig 1 Mechanism of telitacicept and belimumab targeting B lymphocytes in the treatment of SLE
泰它西普于2021年3月在国内上市,它是非传统单抗类的新型融合蛋白生物制剂,由BLyS及APRIL 的共同配体TACI 蛋白基因片段与人体IgG 蛋白的可结晶片段(Fc)融合构成,能够同时阻滞BLyS 及APRIL 与TACI 结合而抑制浆细胞分化和存活、边缘区B 淋巴细胞和滤泡性B 淋巴细胞的抗体同种型转换发挥治疗SLE的作用[13-16,18-19],对BAFFR 特异性影响的幼稚B 淋巴细胞及BCMA 影响的长寿浆细胞作用较小[10,17]。临床用于治疗常规治疗基础上仍有高疾病活动的活动性、自身抗体阳性的成年SLE 患者。临床禁忌证参考贝利尤单抗。
贝利尤单抗是一种重组的完全人源化IgG2λ单克隆抗体,靶向结合BLyS 并抑制BAFFR、TACI 和BCMA 对幼稚B 淋巴细胞、记忆细胞、浆细胞、边缘区B 淋巴细胞和滤泡性B 淋巴细胞的分化、存活和抗体分泌作用[20-21]。鉴于APRIL 仍可与TACI 和BCMA 结合,贝利尤单抗治疗中以幼稚B 淋巴细胞减少最为常见[22]。临床用于治疗5 岁及以上儿童及成年人的活动性、自身抗体阳性的成年SLE 患者及联合免疫抑制剂治疗活动性狼疮的成年患者[23-24]。过敏、合并重度活动性中枢神经系统狼疮、重度活动性狼疮肾炎、获得性免疫缺陷综合征(AIDS)、感染、结核、乙肝、丙肝、低丙种球蛋白血症及器官或细胞移植史患者禁用[23-24]。
2 用法用量
泰它西普和贝利尤单抗在用法、用量、用时和用药频次方面存在明显差异。泰它西普目前仅有皮下注射的给药方式,推荐剂量为每次160 mg[25],每周一次。贝利尤单抗有静脉和皮下注射两种不同给药方式,静脉注射或滴注贝利尤单抗推荐剂量为10 mg·kg-1[26];皮下注射贝利尤单抗推荐剂量为每次200 mg[24];使用频次均为每周一次,皮下用药时间一般为几分钟,静脉用药时间最少1 h[25,27]。
3 药代动力学
中国人群药代动力学临床试验表明,每周皮下注射泰它西普显示一级动力学吸收的二室靶点介导药物代谢动力学模型[28]。在此模型下,泰它西普吸收和转运速率与其剂量成正比,进入人体后以高亲和力与BLyS 紧密结合后转化为结合型泰它西普并通过内化作用消除,消除程度由泰它西普暴露量及其靶点量的相对大小而定。当泰它西普暴露量大于靶点量时,该消除途径达到饱和,表现为清除率随着剂量的增大而减小,药物代谢曲线呈现出非线性特征,反之呈现为线性药动学特征[29-30]。此外,因泰它西普进入人体后与BLyS 结合转化成结合型泰它西普,因此人体内的泰它西普一般描述为总泰它西普、游离型泰它西普和结合型泰它西普三种类型[30]。首次给药后,血清总泰它西普和游离型泰它西普浓度在1~2 d 内达到峰浓度(Cmax),经多次皮下注射后,患者体内药物积蓄,Cmax随之升高[19],达Cmax后呈指数下降,消除半衰期(t1/2)分别为19.8 d 和11.7 d,且Cmax和药时曲线(AUC)变化趋势近似[19,30]。结合型泰它西普形成和消除均较缓慢,皮下注射泰它西普后17~63 d 后才可达Cmax,同时存在蓄积现象,维持7 周后逐渐下降,t1/2为19.4 d,且其t1/2随泰它西普剂量增加而增加[19];但也有研究表明结合型泰它西普在连续4 周每周皮下180 mg 后,第84日测得结合型泰它西普浓度仍大于Cmax的50%[19],此现象提醒临床医师在应用泰它西普治疗SLE 时应特别注意剂量及蓄积效应。此外,研究表明在类风湿关节炎(RA)患者中,泰它西普也表现出与SLE 患者相似的药物代谢动力学特征[18-19]。
贝利尤单抗静脉注射10 mg·kg-1或皮下注射每周200 mg 患者血清药物浓度相当,但皮下注射给药方案血清浓度的波动较小[27]。目前仅有静脉注射用的贝利尤单抗(倍力腾)在中国上市。中国人群的群体药代动力学临床试验表明,静脉用贝利尤单抗是无吸收的线性二室药代动力学模型[31]。在此模型中,贝利尤单抗在输注完成时或完成后不久即可达Cmax(约为221 μg·mL-1),而后向外周组织分布和消除,t1/2约为14.6 d[32];在日本人群中的药代动力学特征与之相近(Cmax222 μg·mL-1、t1/215.7 d)[33],在美国人群中的数据略有不同(Cmax为192 μg·mL-1、t1/2为10.6 d)[34]。皮下注射贝利尤单抗仅有国外研究数据,显示一级动力学吸收的线性二室药代动力学模型,此模型中吸收滞后时间为4.25 h,贝利尤单抗的生物利用度为74%,首次给药达峰时间(tmax)为5.1 d,t1/2为18.7~19.4 d[21,27]。两种药物的具体药代动力学特点对比见表1。
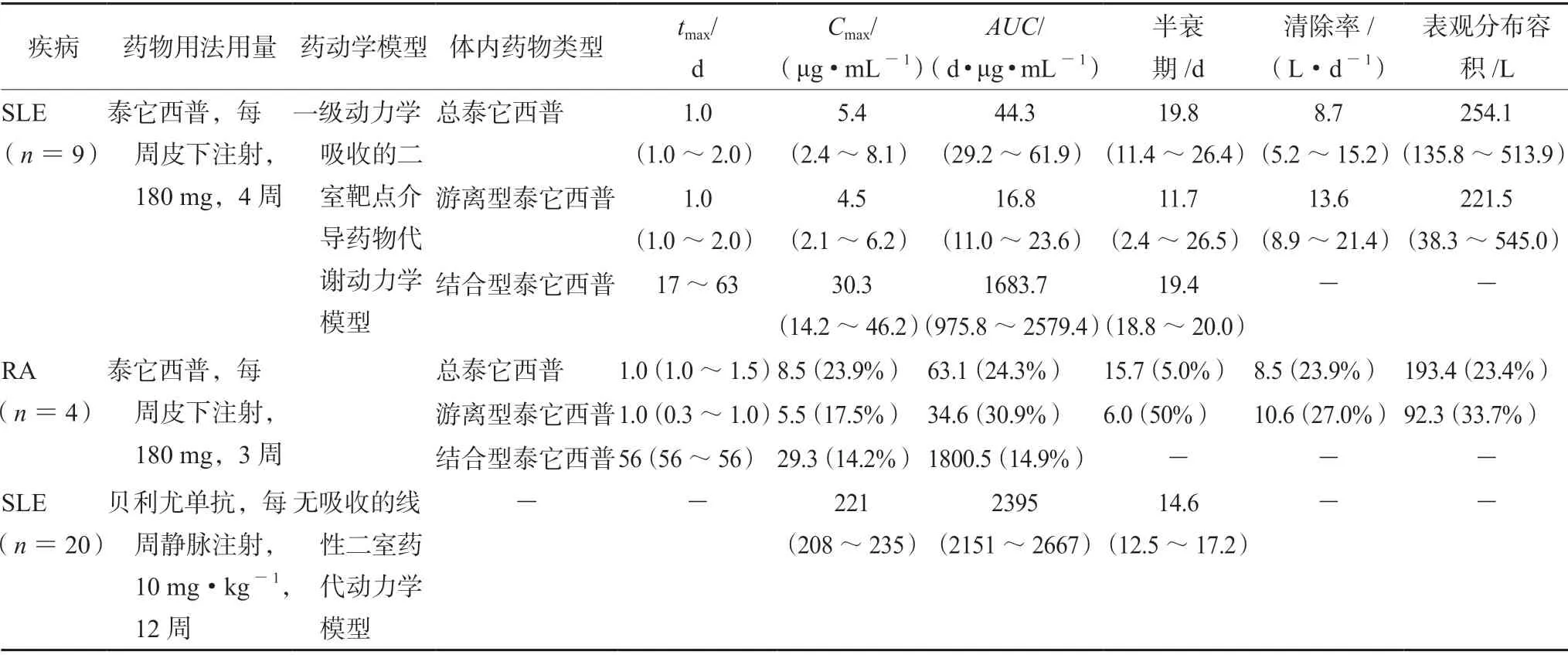
表1 泰它西普与贝利尤单抗药代动力学特点对比Tab 1 Pharmacokinetic characteristics of telitacicept and belimumab
4 有效性和安全性
目前,泰它西普虽尚未有Ⅲ期临床试验结果发布,但泰它西普Ⅰ、Ⅱ期临床试验都显示出对SLE 患者治疗的有效性和安全性。研究人群集中于18~65 岁符合SLE 诊断标准、SELENASLEDAI ≥8 且ANA 和/或抗 dsDNA 抗体阳性、有稳定传统治疗方案的SLE 患者,排除过敏、禁忌证、妊娠及哺乳、入组前3 个月内使用任何靶向B 淋巴细胞生物制剂及入组前1 个月内行血浆置换或注射疫苗的患者;治疗方案为实验组在传统治疗基础上加用泰它西普,对照组在传统治疗基础上加用安慰剂[19,25,35]。在泰它西普Ⅰ期单中心、随机、单盲和安慰剂临床试验中,实验组(n=9)SLE 患者病情稳定,而对照组(n=3)患者病情恶化,具体免疫学表现为实验组患者B淋巴细胞数量及IgM、IgA、IgG 水平降低,补体C3、C4 水平增加[19];安全性方面,大多数不良事件为轻中度,其中实验组咽炎、头痛、疲乏、恶心发生率小于对照组[19][(33.3%vs66.7%)、(22.2%vs66.7%)、(33.3%vs66.7%)、(22.2%vs66.7%)];上呼吸道感染(33.3%vs33.3%)、肌肉骨骼疼痛(33.3%vs33.3%)发生率一致,腰肋骨痛(44.4%vs0%)、带状疱疹(22.2%vs0%)、皮疹(55.6%vs33.3%)等发生率高于对照组[19]。泰它西普Ⅱb 期多中心、随机、双盲、安慰剂临床试验部分实验结果显示,泰它西普80 mg(n=62)、160 mg(n=63)、240 mg(n=62)均观察到了相似的疗效和安全性,实验组以批准的每周皮下注射泰它西普160 mg 治疗方案为例,在48 周时SLE 患者反应指数4(SRI 4)、SELENASLEDAI 评分降低 ≥ 4 分、研究者总体评价(PGA)无进展率均显著高于对照组[(68.3%vs33.9%)、(77.8%vs50%)、(92.1%vs75.8%)][25];实验组和对照组不良事件发生率相近(92.1%vs82.3%),常见不良事件主要是上呼吸道感染和注射部位反应,其中严重不良事件发生率也无显著性差异(15.9%vs16.1%)[25]。此外,国内泰它西普Ⅱb 期单中心临床试验中也观察到了与上述Ⅱb期多中心临床试验相似的疗效与安全性[35],不同的是实验组在上呼吸道感染、带状疱疹、过敏性皮炎发生率高于对照组[(28.6%vs0%)、(28.6%vs0%)、(14.3%vs0%)][35]。值得注意的是泰它西普也可有效降低RA 患者IgM、IgG 和IgA 水平,但其对甲氨蝶蛉或TNF-α抑制剂反应不足的活动性RA 患者无效[18,30],在SLE 人群中暂未发现此种趋势,有待进一步研究确认。
目前贝利尤单抗在临床应用较为成熟,禁忌和慎用人群研究较为明确。在中、日、韩开展的一项多中心随机、双盲、安慰剂Ⅲ期临床试验中,实验组(n=451)在传统治疗基础上加用每周静脉用贝利尤单抗10 mg·kg-1,对照组(n=226)在传统治疗基础上加用安慰剂,实验组52 周时SRI4 反应指数、SLE 患者反应指数7(SRI7)、SELENA-SLEDAI 评分降低 ≥ 4 分均高于对照组[(53.8%vs40.1%)、(32.4%vs23.5%)、(55.7%vs42.2%)][36];糖皮质激素用量也显著低于对照组(P<0.01);实验组与对照组总体不良事件发生率无显著性差异(75.7%vs74.9%),其中实验组上呼吸道感染(13.8%vs16.6%)、鼻咽炎发生率(11.1%vs11.9%),与对照组无显著性差异,且其余不良事件(腹泻、带状疱疹、恶心等)发生率均小于10%,然而严重不良事件发生率实验组低于对照组(12.3%vs18.3%)[36]。两种药物的疗效与安全性对比见表2。
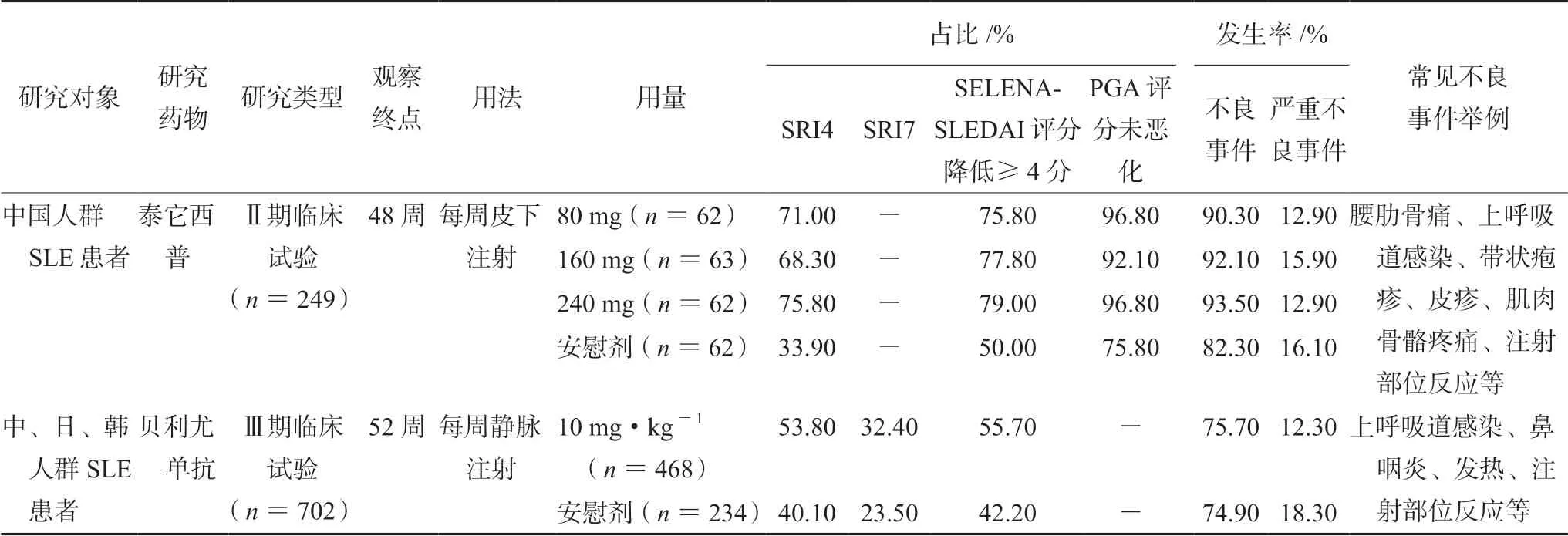
表2 泰它西普与贝利尤单抗疗效与安全性对比Tab 2 Efficacy and safety of telitacicept and belimumab
5 其他
泰它西普及贝利尤单抗在妊娠、哺乳、儿童、老年等人群方面的研究尚不明确。两种药物虽均未开展药物相互作用研究,但也没有证据表明两者与SLE 常用治疗药物糖皮质激素、免疫抑制剂(如羟氯喹、硫唑嘌呤、甲氨蝶呤等)合用时产生药物相互作用[25,37]。
6 结论
从作用机制上看,泰它西普作用于B 淋巴细胞的两个调控因子BLyS 及APRIL,贝利尤单抗仅靶向BLyS 因子。从用法用量对比看,泰它西普皮下注射仅需几分钟,而贝利尤单抗为静脉滴注时间多为1 h 以上。从药代动力学对比看,静脉用贝利尤单抗吸收及消除速度均快,便于剂量调控和停药,而泰它西普Tmax最快也需要1~2 d,连续使用蓄积且因存在结合型泰它西普而消除速度较慢,不利于及时调控药物作用。从药效学对比来看,泰它西普在升高患者SRI4 应答率和降低SELENA-SLEDAI 评分等方面均优于贝利尤单抗。从安全性对比来看,泰它西普和贝利尤单抗的总体不良事件发生率与对照组相比无显著性差异,但泰它西普组中带状疱疹、上呼吸道感染发生率高于对照组,且出现了不同于贝利尤单抗的腰肋骨痛不良事件。
值得注意的是Atacicept 作为首个进入临床试验的靶向BLyS 及APRIL 的生物制剂,其结构与泰它西普相似,区别仅在于泰它西普与Fc 结合的TACI 片段稍长于Atacicept[38-39],该结合方式显著增强TACI 与BLyS、APRIL 的结合力[18]。既往研究表明Atacicept 在降低中、重度SLE 患者复发率方面的作用较显著,在降低轻度SLE 患者复发率方面的作用不明显,甚至会因过度抑制B 淋巴细胞功能而增加不良反应发生风险和复发率[8]。此外AtaciceptⅢ期临床试验疗效与安全性方面数据表明,SLE 患者每周应用Atacicept 150 mg 时,虽能显著降低SLE 患者B 淋巴细胞数量及IgG、IgA、IgM、抗dsDNA 抗体水平、升高补体C3、C4 水平,却因其出现致命性肺部感染及严重的丙种球蛋白血症,导致实验终止[38]。然而有研究表明出现此种现象可能与合用狼疮肾炎首选药物吗替麦考酚酯有关,联合Atacicept 时导致自身感染风险加剧[40-42]。而目前的泰它西普临床试验中未曾提到合用吗替麦考酚酯的相关信息,因此作为相似结构和作用机制的泰它西普在后续临床试验或治疗中可能呈现出相似的治疗效果和不良事件,医师应特别注意。
相比泰它西普,2011年已在国外批准用于治疗SLE 的贝利尤单抗在临床应用已较为成熟[3]。开展的多项大型多中心、随机、双盲、对照的贝利尤单抗Ⅲ期临床试验和上市后临床试验表明[43-45],在美洲、亚洲、欧洲、非洲等人群中应用贝利尤单抗治疗活动性SLE(尤其是血清学活动、疲劳、皮肤关节受累的患者)均可显著降低疾病活动度、预防疾病严重发作、减少糖皮质激素剂量、改善患者疲劳和健康评分,且患者不良反应可耐受。尤其对于非重度活动性的狼疮肾炎患者,贝利尤单抗(联合或不联合吗替麦考酚酯)可显著降低蛋白尿、减少器官损伤[4,46];2019年EULAR 发布的SLE 治疗指南也肯定了贝利尤单抗作为一线治疗后疾病仍持续活动或反复发作或糖皮质激素不能减量至≤7.5 mg·d-1的狼疮肾炎患者的备选治疗药物[47]。然而SLE 患者累及脑部出现神经、精神方面的症状时,应用贝利尤单抗易出现严重不良事件(如进展性多灶性脑白质病、抑郁、自杀)[48],因此应用前需认真权衡。
综上所述,结合泰它西普及贝利尤单抗作用机制、用法用量、药代动力学、有效性和安全性,医师应在充分考虑患者病情严重程度、疾病表现、紧急情况等诸多因素,选择最适药物,保证临床用药安全有效。但泰它西普研究数据有限,且缺乏直接比较两种生物制剂疗效与安全性方面的数据,因此后续应继续开展大型临床试验进一步验证。
