影像学危险因素对儿童腹部神经母细胞瘤手术指导及术后并发症预测价值研究
2022-11-15冶文千周鹏圆王平
冶文千 周鹏圆 王平
神经母细胞瘤(neuroblastoma,NB)是儿童期常见的腹部实体瘤,其好发位置以腹膜后居多,占总原发位置的半数以上,其次为肾上腺、纵隔、盆腔以及外周器官转移,其发病机制尚不清楚[1-2]。国际神经母细胞瘤临床分期(international neuroblastoma staging system,INSS)是神经母细胞瘤临床分期常用标准,但通常为术后评判标准,对于术前指导及并发症预测的应用价值不大[3]。2009年提出影像学定义的危险因子(image-defined risk factors,IDRFs)分期法基于影像学对神经母细胞瘤进行分期,为神经母细胞瘤的术前风险评估及术后并发症预测提供了新的途径[4]。本研究对78例腹部神经母细胞瘤患儿影像学资料进行分析,为儿童腹部神经母细胞瘤的临床诊疗提供参考。
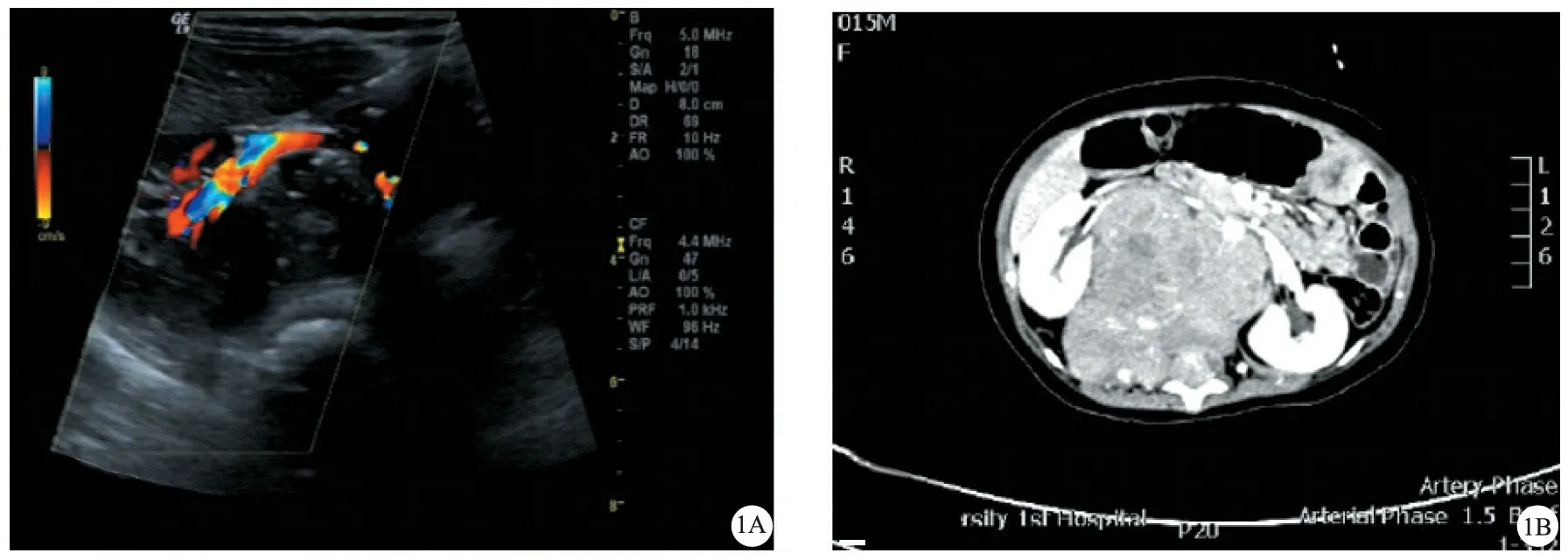
A 超声影像图,可见肿瘤压迫肾门血管、下腔静脉和腹主动脉;B CT平扫图,可见腹主动脉及双肾血管压迫 图1 患儿腹部血管侵袭影像学图
对象与方法
一、对象
2018年1月~2020年2月我院肿瘤外科收治未经化疗且行手术治疗的腹部神经母细胞瘤患儿77例。纳入标准:(1)病理学检查诊断为神经母细胞瘤,均为初次发病,经多学科探讨无需术前行化疗;(2)肿瘤位于腹膜后;(3)患儿术前经综合评估具备手术指征,并可耐受手术治疗;(4)患儿家属知情本研究并签署知情同意书。排除标准:非腹部神经母细胞瘤或合并其他部位神经母细胞瘤;肿瘤破裂或无法未经化疗直接手术;合并遗传代谢病、严重肝肾功能不全、心肺功能异常、免疫系统疾病;入院前接受其他治疗;临床资料不全。
二、方法
1.资料收集:包括入院后超声检查、CT平扫及增强重建、MRI检查、骨髓穿刺、血清NSE检测、基因分型检测。术中失血量、发生实质脏器损伤、血管损伤、神经损伤、乳糜腹等术中并发症情况,以及术后乳糜漏、电解质紊乱、感染、肠梗阻、肠套叠、切口积液、血肿等并发症情况。患儿的手术治疗均由同一诊疗组完成,相关影像学检查由专业医师操作及阅片。
2.IDRFs分期:参照2011修订的IDRFs分期法,根据神经母细胞瘤原发部位及对应侵袭血管及脏器,将神经母细胞瘤分为L1、L2、M及MS四期,并根据神经母细胞瘤与周围血管和器官的关系列出20多种危险因子。局限性神经母细胞瘤为L1期和L2期,其中L1期为肿瘤局限并未侵袭重要血管和脏器;L2期为肿瘤局限但已侵袭周围血管和脏器,L2期包含1个或以上IDRFs;M期为伴有远处转移;MS期为伴有皮肤、骨髓、肝脏转移但小于18个月。由于M期与MS期的神经母细胞瘤患儿治疗形式均以化疗为主而排除出本次研究,纳入研究的78例患儿IDRFs分期均为L1、L2期。对腹部神经母细胞瘤的IDRFs分期法中,侵袭重要血管的判断需要满足以下条件:(1)神经母细胞瘤侵袭肠系膜动脉或其主要分支;(2)神经母细胞瘤侵袭腔静脉、髂静脉,并导致其管腔在影像学上不可见;(3)神经母细胞瘤侵袭单侧或双侧肾蒂。见图1。IDRFs分期法对侵袭重要脏器的判断需要满足以下条件:神经母细胞瘤侵袭膈肌、肾脏、肠系膜、胰十二指肠等脏器;神经母细胞瘤侵袭肝十二指肠韧带、肝门等。见图2。
三、统计学方法
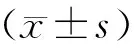
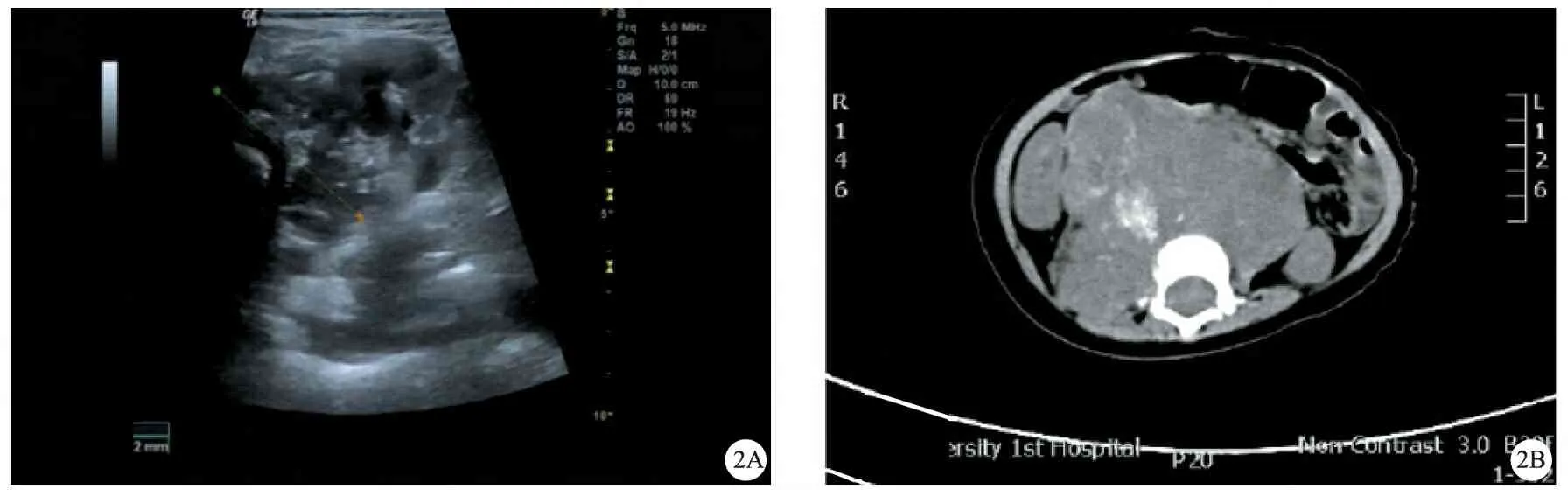
A 超声影像图,可见右侧肾门后方低回声团块;B CT平扫图,可见腹膜后巨大肿块影,内有斑片状钙化密度影
图2 患儿腹部脏器侵袭影像学图
结果
本研究共纳入77例初发腹部神经母细胞瘤患儿,经肿瘤科、放射科等科室联合诊断讨论后诊断为未经诱导化疗下可进行手术治疗,其中男44例,女33例;发病年龄7~106个月,中位年龄为34.7月;体重7.2~31.3 kg,中位体重16.5 kg。按照INSS分期法划分Ⅰ期24例,Ⅱ期41例,Ⅲ期12例。按照IDRFs分期法划分L1期26例,L2期51例。
1.L1与L2期患儿手术方式及手术情况比较:L1期患儿手术完全切除率为80.77%,L2期为49.02%,差异有统计学意义(P<0.05);L1期患儿术中输血3例(11.54%),L2期为20例(39.22%),差异有统计学意义(P<0.05);L2期患儿手术时间长于L1期,差异有统计学意义(P<0.05)。见表1。
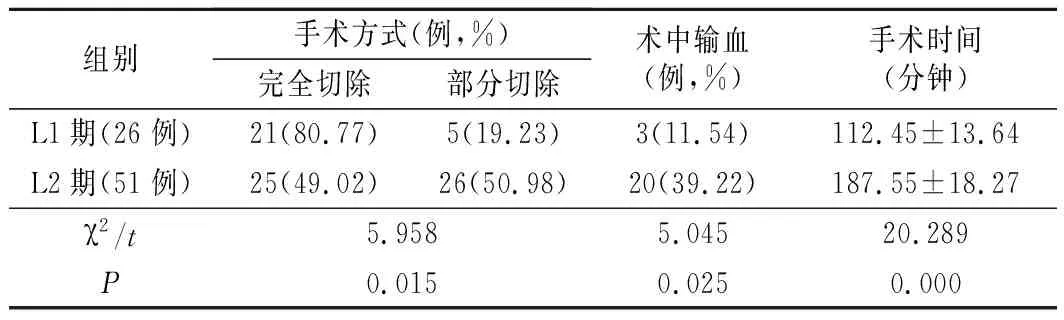
表1 L1与L2期患儿手术方式及手术情况
2.L1期与L2期患儿手术并发症情况:L2期患儿术中脏器损伤、浸润脏器切除、术中出血等术中并发症发生率高于L1期,差异有统计学意义(P<0.05);L1期与L2期患儿术中血管损伤、乳糜腹及其他术中并发症发生率无统计学差异(P>0.05);L2期患儿术中共发生并发症91次,平均频次为1.78次,L1期患儿术中共发生并发症14次,平均频次为0.54次,L2期患儿的术中并发症频次显著高于L1期,差异有统计学意义(P<0.05)。L2期患儿术后切口积液、切口血肿发生率显著高于L1期,差异有统计学意义(P<0.05);L1期与L2期患儿术后乳糜漏、电解质紊乱、感染、肠梗阻、肠套叠及其他术后并发症发生率比较,差异无统计学意义(P>0.05);L2期患儿术后共有并发症86次,平均频次1.69次,L1期患儿术后共有并发症15次,平均频次0.58次,L2期患儿术后并发症频次显著高于L1期,差异有统计学意义(P<0.05)。见表2,表3。
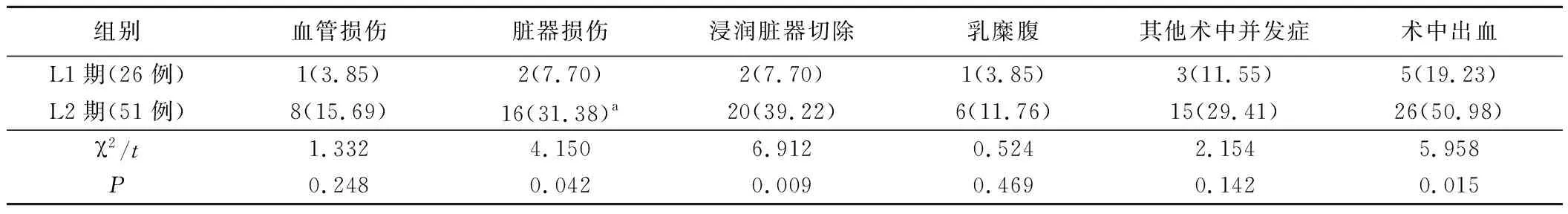
表2 IDRFs分期与术中并发症情况(例,%)
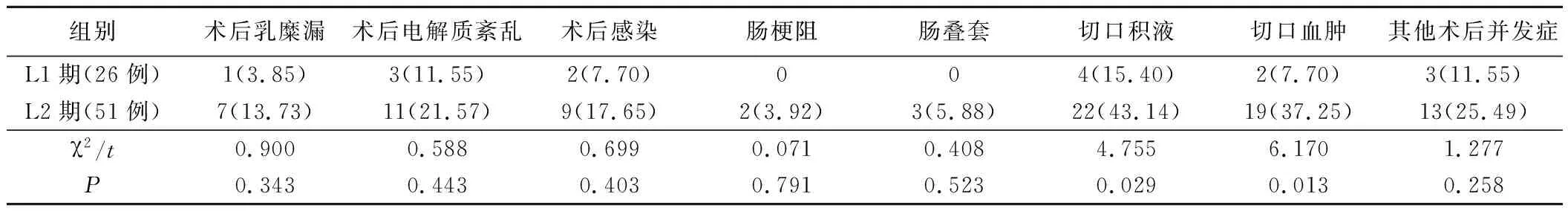
表3 IDRFs分期与术后并发症情况(例,%)
3.IDRFs分期与术后并发症相关性分析:采用Spearman相关性分析显示,IDRFs分期中L1期与术后并发症存在中等相关性(r=0.416,P<0.05),L2期与术后并发症存在强相关性(r=0.711,P<0.05)。
4.IDRFs分期预测术后并发症ROC曲线分析:以IDRFs分期为检验变量,以发生手术并发症为状态变量,ROC曲线分析显示L1期的曲线下面积(Area under the Curve,AUC)为0.702,灵敏度为67.2%,特异度为65.1%;L2期的AUC为0.887,灵敏度为86.2%,特异度为80.3%。见图3。
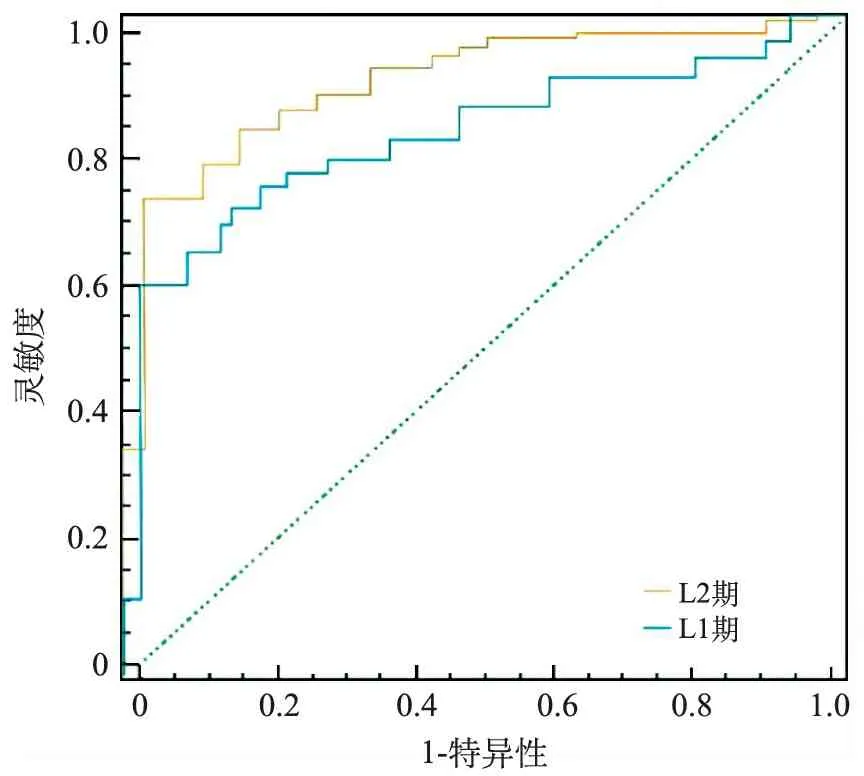
图3 IDRFs分期法预测术后并发症ROC曲线
讨论
神经母细胞瘤是儿童常见恶性肿瘤,其发病率约占儿童肿瘤的7%~10%[5]。外科手术切除是治疗神经母细胞瘤的常用手段,但治疗效果较差[6]。目前,INSS分期仍然是指导儿童腹部神经母细胞瘤治疗方案的重要参考依据,但是INSS分期必须根据术后肿瘤切除程度、淋巴结清扫情况等确定,选择不同术式可能导致INSS分期截然不同,而且无法指导术前风险评估[7]。基于术前影像学筛选神经母细胞瘤对重要脏器、血管压迫浸润情况而进行IDRFs分期,为儿童腹部神经母细胞瘤的术前评估提供新的选择。
Irtan等[8]报道新辅助化疗后IDRFs评估有助于预测神经母细胞瘤切除的彻底性,对指导手术治疗具有重要作用。Avanzini 等[9]提出,术前IDRFs分期能够定义神经母细胞瘤不可切除风险因素,有助于指导术前手术方案的制定。我国于2015年将IDRFs分期法纳入神经母细胞瘤诊疗专家共识[10]。本研究回顾性分析78例腹膜后神经母细胞瘤患儿临床资料,依据IDRFs分期法,M期与MS期患儿由于存在远端转移,临床治疗手段以化疗为主,排除出本次研究。按照IDRFs分期法划分为L1期26例,L2期51例。L1期患儿手术完全切除率显著高于L2期患儿完全切除率;L1期患儿术中输血例数显著少于L2期;L2期患儿手术时间长于L1期。分析认为,IDRFs分数越高,肿瘤对周围脏器浸润、血管压迫和包绕情况越严重,因此,L2期患儿手术难度较L1期更大,手术时间更长,并影响手术切除率及术中输血量。与术中才能对神经母细胞瘤进行分期INSS相比,IDRFs在术前即可对手术难度进行预判,对于神经母细胞瘤手术具有指导价值。
此外,IDRFs分期法较INSS分期法对于神经母细胞瘤的术中与术后并发症提供较强的指导意义[11-13]。本研究发现,L2期患儿术中脏器损伤、浸润脏器切除、术中出血等术中并发症发生率显著高于L1期;L2期患儿术中并发症频次显著高于L1期。此外,在术后并发症方面,L2期患儿术后切口积液、切口血肿发生率显著高于L1期;L2期患儿术后并发症频次显著高于L1期,与文献所报道结果较一致[14-15]。Spearman相关性分析显示,IDRFs分期中L1期与术后并发症存在中等相关性,L2期与术后并发症存在强相关性,与患儿术后并发症情况相符,提示IDRFs分期不同而术后并发症风险不同,L2期术后并发症风险高于L1期。分析认为,IDRFs分期可以用于预判手术风险,而手术风险与术中、术后并发症密切相关,因此通过术前IDRFs分期有助于预测术后并发症情况。原因与之前类似,L2组患儿在发生周围组织黏连以及血管包绕的情况更为突出,若无法做到肿瘤分离,则需要切除部分脏器,导致术中并发症发生率更高,而手术的复杂性和时间长度影响了术后并发症的发生,因此,除手术更加复杂外,L2组发生术中、术后并发症概率均更高。
以IDRFs分期为检验变量,以发生手术并发症为状态变量,ROC曲线分析显示L1期的曲线下面积(AUC)为0.702,灵敏度为67.2%,特异度为65.1%;L2期的AUC为0.887,灵敏度为86.2%,特异度为80.3%,上述结果与文献[16]所报道结果较一致,提示IDRFs分期对预测儿童腹部神经母细胞瘤手术并发症具有重要价值。
综上所述,IDRFs分期法能够客观、简单的指导儿童腹部神经母细胞瘤手术选择,而且能够反映和预测术后并发症发生风险,有助于儿童神经母细胞瘤的临床诊疗。
