合金钙线中铝含量的化学测定方法探究
2022-11-12张小红
张小红
(陕钢集团汉中钢铁有限责任公司,陕西 勉县 724200)
钙线在炼钢过程中可以解决铝镇静钢中难熔夹杂物Al2O3的性态,防止浇注过程中钢水死流,影响钢材性能。铝作为钙线的含杂成分,其含量是衡量钙线的重要指标,需要准确检测。由于钙线中铝含量低,铝作为钙线的含杂成分,是衡量钙线的重要指标,需要准确检测。由于钙线中铝含量w(Al)低于1%,目前大部分实验室的通用方法为原子吸收法,但原子吸收仪价格昂贵,实验室没有原子吸收光谱仪,拟寻求化学分析的办法进行钙线中铝含量的准确测定。通过查找参考文献和各类物料铝的分析方法,经过反复比对,发现只要控制好制样方法,pH值、称样量、移取比够得到准确的分析结果。
1 实验用试剂及设备
盐酸(1+1)、硝酸(1+1)、PAN指示剂(0.1%酒精溶液)、氨水(1+1)、溴甲酚绿指示剂(0.04%酒精溶液)、醋酸(36%)、EDTA标准溶液(0.010 0 mol/L)、硫酸铜标准溶液(0.010 0 mol/L,称取硫酸铜6.249 0 g于400 mL烧杯中,加水溶解后移入1 L容量瓶中,冲洗烧杯数次,稀到刻度,摇匀备用)。分析天平(感量为0.000 1 g)、电热板(功率为2 000 W)。
2 讨论
2.1 制样方法的制定
1)从文献查找制备试样,在无污染、无锈蚀的待测无缝钙线卷上,截取长度为10 mm试样6~8粒,弃去端部试样,将中间试样用密封袋封闭后用于检测。
2)分离出试样中的钙芯并制备待测溶液,称取定量试样置于烧杯中,在向烧杯中加入50~80℃的蒸馏水60~100 mL浸泡试样20~30 min,向烧杯中滴加体积配比为1∶1的浓盐酸(1.19 g/cm3)与蒸馏水混合而成的盐酸溶液,当烧杯中的浸出液由浑浊转变为清亮后停止滴加入盐酸溶液,将钢管外壳从烧杯中取出后用蒸馏水清洗干净,用烘箱将洗净后钢管外壳于100~110℃烘干20~30 min,从烘箱中取出钢管外壳,将钢管外壳冷却至15~25℃后对其称重;将烧杯中钙芯的浸出液转移至250 mL容量瓶,用蒸馏水将容量瓶中钙芯的浸出液定容至250 mL制备成待测溶液;此方法适合钙线芯为颗粒的样品,但分析的钙线芯为实心,溶解时在烧杯中加入50~80℃的蒸馏水60~100 mL浸泡试样20~30 min,溶解速度极慢,只有两端冒气泡,滴加(1+1)盐酸,反应速度加快,但是,盐酸与钙线试样反应的同时,也与钙线外包装管发生少量反应,影响试样质量的定量测定。通过拆除钙线外包装,发现钙线棒外表皮为灰绿色氧化物,使用硬质勺刮蹭,去掉氧化层,迅速截取1 cm长短的钙线样品,进行称量,放入烧杯,加入50~80℃热水,少量加入(1+1)盐酸,控制合适的样品溶解速度,待溶解完成后,将溶解液冷却至室温后,定容到250 mL的容量瓶中,移取25 mL母液与500 mL三角瓶中,加入(1+3)三乙醇胺10 mL摇匀,加入(20%)的氢氧化钾溶液20 mL摇匀,加入3滴钙指试剂摇匀,用0.010 0 mol/L EDTA溶液进行滴定,计算样品钙的百分含量,测定结果与外部结果比见表1。
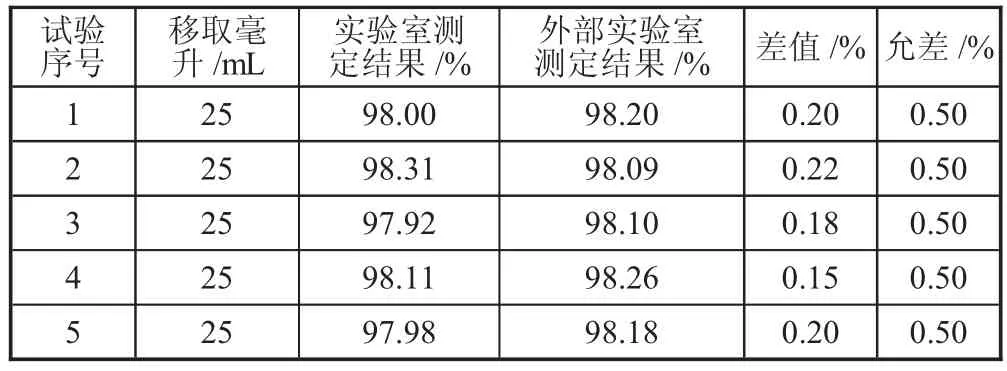
表1 碳线钙分析数据
经过分析与外部权威部门的分析结果的比对,钙线中钙的分析结果与比对结果均能保证在误差范围之内,证实此制样和溶解方法符合分析要求。
3)最终制定制样方法:截取1.0~1.5 cm长度的钙线条,剥离出试样中的钙芯,用刀具迅速刮掉泛灰绿的氧化层,迅速称取试样质量,置于烧杯中,加入50~80℃的蒸馏水60~100 mL,浸泡试样的同时,缓慢逐滴加入1+1的盐酸溶液,当烧杯中的浸出液由浑浊转变为清亮后,立即停止滴加盐酸溶液。将烧杯中钙芯的浸出液转移至250 mL容量瓶,用蒸馏水将容量瓶中钙芯的浸出液定容至刻度线制备成待测溶液,摇匀备用;由于样品的含杂未知,拟通过排除法选择适合钙线中铝的分析方法。
2.2 分析原理
定量移取母液,调节至pH=2.5~3.0左右,加过量的EDTA标准溶液,在加热的情况下将铝络合,其稳定常数KP=16.13。
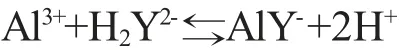
过量的EDTA调至溶液在pH=4.2左右,用硫酸铜标准溶液回滴;
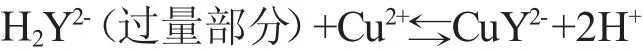
上述二反应产生氢离子,加入冰醋酸进行缓冲,以免反应不完全。
2.3 求得铝的含量
计算公式:
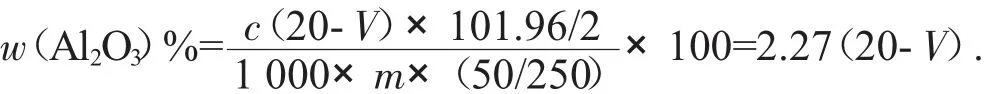
式中:c为EDTA的浓度0.010 0,mol/L;V为硫酸铜滴定的毫升数,mL;m为试样的称样量,精确至0.000 1 g。
2.4 拟采取铝的测定方法(方法一)
吸取上述制备母液25.00 mL于300 mL三角瓶中,加2~4滴溴甲酚绿,用(1+1)盐酸中和至溶液呈黄色,这时加EDTA25.00 mL(视含量而定)后用(1+1)NH3H2O中和呈兰色,再用1 mol/L的盐酸调至黄色并过2~3滴,加缓冲液20 mL,加热煮沸2 min,立即加10滴PAN指示剂,用CuSO4标液滴定至紫红色为终点,根据滴定所消耗的CuSO4标液体积来计算铝的含量。用CuSO4标液反滴定时,3~5滴后试液立即变为酒红色,计算结果见表2。

表2 方法一的分析数据
分析结果与外部原子吸收分析结果偏离太多,说明溶液中的部分离子与溶液中过量的EDTA发生反应,干扰离子未得到充分掩蔽,此法不可取。
2.5 拟采取铝的测定方法(方法二)
吸取母液50.00 mL于300 mL烧杯中,加1 mL硝酸(1+1),加热煮沸,加氢氧化钾溶液(20%)至溶液中出现红棕色氢氧化铁后再过加10 mL,加热煮沸,使沉淀凝聚,用定量滤纸过滤于500 mL锥形瓶,用氢氧化钾溶液(2%)洗涤,向分离沉淀后的溶液中加入10 mL浓盐酸,15.00 mL EDTA标准溶液,6~7滴溴加酚绿指示剂,滴加氨水(1+1)至天兰色刚出现。再加入5 mL冰醋酸,使溶液呈黄色,加热煮沸2 min,然后滴加13滴PAN指示剂,用硫酸铜标准溶液滴至溶液呈现紫红色为终点,分析结果见表3。

表3 方法三分析数据

表3 方法二分析数据
分析结果与外部原子吸收分析结果偏离太多,说明溶液中的部分离子与溶液中过量的EDTA发生反应,干扰离子未得到充分掩蔽,此法不可取。
2.6 拟采取铝的测定方法(方法三)
移取母液50 mL,加入EDTA标液20 mL(按试样铝含量高低可适当加减),加溴甲酚绿指示剂3滴,以氨水调节兰色出现(pH=4.7~5.5),加冰醋酸5 mL于电炉上煮沸1 min,加PAN指示剂5滴,以硫酸铜标液滴至紫红色出现为终点,分析结果见表4。
分析结果与外部原子吸收分析结果均能保证在误差范围之内,平行样之间的误差也能小于误差,说明溶液中的干扰离子得到充分掩蔽,此方法能进行钙线中铝的分析,拟采用此法进行分析。
3 结论
通过以上实验,方法三实验数据的重复性、准确性均满足低含量铝的误差小于0.10%的要求,方法三的方法,EDTA滴定法分析结果与外部原子吸收法分析结果均在允许误差范围内,确定方法三适合钙线中铝的分析。
