内镜下组织黏合剂联合硬化剂注射治疗胃静脉曲张临床研究及随访
2022-11-10张梦茵袁晓琴蔡波尔吴云林
张梦茵,陈 平,袁晓琴,蔡波尔,吴云林
(上海交通大学医学院附属瑞金医院北部院区消化内科,上海 201801)
胃静脉曲张见于5%~33%的门静脉高压症病人。作为临床上门静脉高压症常见的危重并发症之一,其破裂出血后病死率高,抢救难度大,且治疗后因仍有较高的再出血率而成为临床治疗的难点[1]。由此,治疗胃静脉曲张急性出血或预防再次出血具有重大意义。目前临床上常采用的方法涉及生长抑素(商品名思他宁、善宁等)、β受体阻滞剂(如卡维地洛、普萘洛尔等)降低门静脉压力的药物治疗,内镜下食管胃底静脉曲张套扎,硬化剂和(或)联合组织黏合剂以闭塞和消除曲张静脉和预防出血的微创治疗,通过改变血流途径的经颈静脉肝内门体静脉分流术(transjular intrhepatic portosystemic shunt,TIPS)和高选择性阻塞曲张静脉流入道途径的经球囊导管阻塞下逆行闭塞静脉曲张术(balloonoccluded retrograde transvenous obliteration,BRTO)等介入治疗,及外科手术阻断血流和分流血流途径的治疗等[2]。治疗方法较多,但对于胃底静脉曲张的二级预防和治疗措施,欧洲及我国指南推荐内镜下组织黏合剂(如α氰基丙烯酸烷基酯)的应用[3]。笔者既往研究已报道内镜下黏合剂联合硬化剂注射治疗可有效消除结节隆起型孤立性胃静脉曲张(isolated gastric varices,IGV)1 型静脉瘤[4],部分病人取得良好效果。本研究就该技术在因上消化道出血接受胃镜检查证实为胃静脉曲张破裂出血的病人应用内镜下组织黏合剂联合硬化剂注射治疗后的相关结果及随访数据进行分析以期指导临床实践。
资料与方法
一、研究对象
纳入2006年至2015年间在上海交通大学医学院附属瑞金医院总院和北部院区消化内科因上消化道出血接受胃镜检查证实为胃静脉曲张破裂出血并行记录随访的84例病人为研究对象,其中16例内镜治疗前行脾切除术、贲门周围血管离断术、肝移植术。病人平均年龄(60.2±14.4)(29~88)岁。男性45例,女性39例。Child-Pugh分级分别A级27例、B级42例和C级5例。病因如下。①乙型肝炎34例。②其他肝炎17例:乙型肝炎合并丙型肝炎1例,乙型肝炎合并血吸虫病1例,乙型肝炎合并酒精性肝炎1例,丙型肝炎1例;酒精性肝炎4例,酒精性肝炎合并肝癌1例;自身免疫性肝炎3例,自身免疫性肝炎合并血吸虫病1例。③ 其他原因14例:胆汁淤积性5例,肝癌1例,结肠癌肝转移1例,血吸虫病5例,门静脉海绵样变性1例,先天性门静脉狭窄1例,胰源性门静脉高压4例(胰腺癌3例,重症急性胰腺炎1例)。④原因不明19例。排除有内镜下治疗禁忌证的病人:上消化道内镜检查禁忌证(严重的心肺疾患和颈胸段脊柱畸形),处于休克抢救期,肝性脑病处于昏迷期或不能配合检查,目前有严重的咽喉部疾患和大量腹水,严重黄疸等。
二、研究方法
(一)胃静脉曲张分型
本研究采用通用的国际Baveno会议共识分型,分为胃食管静脉曲张型(gastro-esophageal varices,GEV)和IGV。 GEV分两型:① GEV1,是食管静脉曲张的延续,沿胃小弯延伸至胃食管连接处以下2~5 cm;② GEV2型,静脉曲张位于胃底,与食管静脉曲张相连接,常呈结节状或瘤样隆起。IGV分两型:①IGV1型,静脉曲张孤立位于胃底;②IGV2型,异位静脉曲张位于胃体、胃窦、幽门周围、十二指肠等。
(二)静脉曲张的治疗标准[3]
胃曲张静脉根除是内镜治疗结束,治疗区域所形成的溃疡及糜烂完全消失后,内镜下完全看不到静脉曲张,黏膜呈现其基本色泽。胃曲张静脉基本消失是内镜治疗结束后,内镜下仍可见残留的细小曲张静脉。
(三)内镜检查和曲张静脉治疗过程
术前所有病人均签署知情同意书,禁饮、食12 h后行胃镜检查。术前15 min口服利多卡因胶浆和二甲硅油去泡。先行常规胃镜检查,其后观察胃底曲张静脉瘤体形态,通常以静脉瘤体中央为穿刺点或选择存在活动性出血灶或表面见明显红色或白色血栓等近期出血征象的瘤体病灶旁1 cm处。然后根据曲张静脉瘤体大小选择注射剂量,选用一次性体内注射针(商品名Interject,Boston Scientific公司)。穿刺曲张静脉瘤体内抽吸可见回血后,推注入硬化剂(1%聚桂醇注射液)1.5~3.0 mL。随后立即推注组织黏合剂1.5~5.0 mL(康派特医用胶),再推入硬化剂(1%聚桂醇注射液)1.5~2.5 mL以便将注射导管残留黏合剂全部推入曲张静脉内。其后少许注射用水冲洗管腔后拔针。最后用注射针外鞘管局部压迫片刻,确认注射针孔无活动性出血,退针结束治疗。另外,在内镜治疗前24 h和治疗后72 h静脉泵持续静脉推注生长抑素(商品名思他宁)降低门静脉压力。术后2个月持续使用质子泵抑制剂抑酸,使用胃黏膜保护剂促进溃疡愈合,减少出血风险。其后排除禁忌证换用普萘洛尔(商品名心得安)或卡维地洛口服,持续降低门静脉压力行预防性降低消化道出血的可能(剂量根据心率调整,心率≤55次/min停药)。
(四)随访
嘱病人内镜治疗后1~3个月可行胃镜复查。胃镜检查中如仍存在明显曲张静脉,则再次行组织黏合剂联合硬化剂治疗,其后嘱病人每6~12个月行胃镜复查。
三、数据统计
统计分析使用SPSS 16.0软件。计量资料以均数±标准差表示,组间比较采用t检验。计数资料以频数或率表示,组间比较采用卡方检验。P<0.05为差异有统计学意义。
结 果
一、胃静脉曲张内镜分型
84例中,IGV 1型39例(46.4%),GEV 1型 15例(17.9%),GEV 2型 19 例(22.6%),GEV 1 型+GEV 2型10例(11.9%),GEV 2型+IGV 2型1例(1.2%)。
二、内镜治疗
84例共行内镜下组织黏合剂联合硬化剂注射治疗 111 次,平均治疗(1.32±0.68)(1~5)次/例。 其中治疗1次的为64例,治疗2次的为15例,治疗3次的为4例,治疗5次的为1例。组织黏合剂注射平均剂量为(1.97±0.94) mL,硬化剂注射平均剂量(5.41±2.68)mL。111例次中有6例次在术中拔针后喷射性出血,立即出血部位追加注射组织黏合剂和硬化剂后止血成功,治疗后无异位栓塞、感染并发症发生。
三、转归
84例中,治疗后 15 d内 2例(2.4%,2/84)因再出血而死亡,2个月内共6例(7.1%,6/84)因再出血而死亡。内镜下治疗后随访期间有12例后续进行外科手术,手术方式11例涉及脾脏切除和(或)贲门周围血管离断术或分流术和1例肝移植术。外科手术后随访至本研究结束。12例随访期间除其中1例因骨折后全身多器官功能衰竭死亡外,其余11例未再出血,均生存至随访结束。
四、治疗后出血情况比较
内镜治疗后半年内16例有再出血现象,随访半年至1年有2例发生再出血,1~5年有10例再出血,5年后2例发生再出血。截至随访结束期间,有30例治疗后曾出血,42例治疗后未再出血,12例随访期间后续转外科手术。84例平均治疗前出血频率为(0.72±0.54)(0.06~2.50)次/月,远高于治疗后平均出血频率(0.30±0.82)(0~5.00)次/月,差异有统计学意义(P<0.01)。
五、胃静脉曲张消除
48 例在随访(0.1~131)(17.1±27.7)个月中行胃镜复查,另外36例未行胃镜复查。48例中动态随访以6个月为节点,其中24例在内镜治疗后6个月内复查胃镜并记录胃曲张静脉状况。发现胃曲张静脉完全消失2例(8.3%),基本消失16例(66.7%),无明显改善6例(25.0%),加重0例。另外24例在内镜治疗6个月后行复查,发现胃曲张静脉完全消失 11例(45.8%),基本消失 6例(25.0%),无明显改善3例(12.5%),加重 4例(16.7%)。6个月内和6个月后复查胃静脉曲张根除+基本消失率分别为75.0%及 70.8%,差异无统计学意义(P>0.05)。
六、举例
男性,63岁,因反复呕血、黑便半年余就诊,既往有乙型肝炎后肝硬化史。住院后行胃镜检查,随后给予内镜下组织黏合剂联合硬化剂注射 (见图1~4),术前24 h及术后72 h给予生长抑素类药物降低门静脉压力,术后2个月使用质子泵抑制剂抑酸,胃黏膜保护剂促进溃疡愈合。1年半后复查胃底曲张静脉明显消退,至随访结束未再发生出血。

图1 胃底内镜治疗前所见
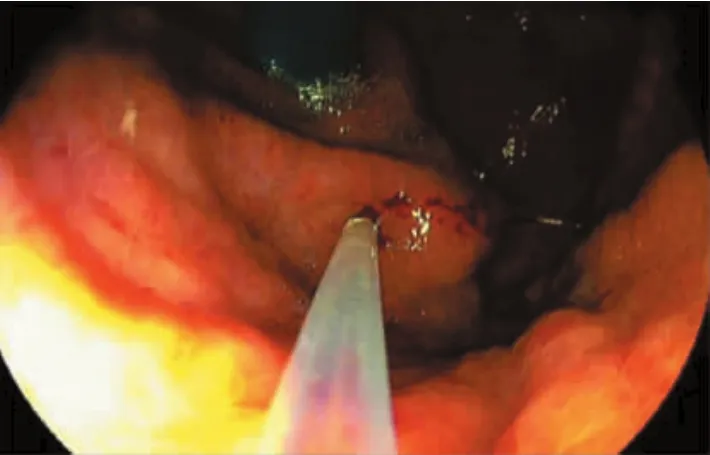
图2 胃底内镜治疗术中所见

图3 胃底内镜治疗术后37 d随访所见

图4 胃底内镜治疗术后1年半随访所见
讨 论
由于门静脉高压性胃静脉曲张破裂较快而大量的出血导致较高的死亡率和较低的抢救成功率,因此成为临床治疗的急诊危重症之一。目前较好的方法就是预防出血。如根据病因、病人的全身状况、Child分级、门静脉高压程度及肝门静脉系统血流动力学状态来选择外科手术治疗[5-6]。缺点是其并发症发生率和死亡率较高,且肝功能Child C级病人多已失去手术机会。介入治疗作为常见的治疗手段如TIPS有效地降低门静脉压力、预防静脉曲张破裂出血的发生,但可致肝性脑病的发生率升高。治疗的有效率使其目前仍作为出血病人的紧急治疗手段和内镜下治疗失败的后续治疗手段。既往常用的三腔二囊管压迫法,多用于基层医院和内镜下治疗手段欠缺的医院应对曲张静脉破裂出血的有效抢救措施之一,并为其他可行的治疗措施争取时间[7]。
目前食管静脉曲张内镜下套扎治疗或硬化剂注射治疗已被广泛使用并取得良好的疗效。如既往在胃曲张静脉瘤体序贯注入碘油-组织黏合剂-碘油的“三明治”法治疗,缺点为可能发生碘过敏。
近年来部分改进的内镜下治疗措施有超声内镜引导下纤维线圈置入联合组织黏合剂或硬化剂注射,有较高的曲张静脉闭塞率和较低的再出血发生率,仍在探索阶段。也有研究采用多部位多点同时圈套结扎胃底曲张静脉治疗以闭塞曲张静脉,取得一定疗效[8]。还有人探索在胃底曲张静脉行金属夹夹闭以阻断血流或减少曲张静脉压力和血流量,再辅助组织黏合剂联合硬化剂注射治疗曲张静脉[9]。此外,目前有研究提出内镜下食管胃底静脉曲张精准治疗术。即根据多普勒超声内镜检查分析曲张静脉中的静脉回流,然后根据曲张静脉的分流特征,在相应的血管内精准注射硬化剂和组织黏合剂进而闭塞曲张静脉,最终消除曲张的食管胃底静脉[10]。
本研究则采用目前常规模式,先行硬化剂注射,再序贯同部位注射组织黏合剂。并对治疗病人的长期随访进行回顾性分析,了解预后情况和疾病转归,为临床干预提供帮助,并为今后不同内镜下干预模式的长期预后比较提供依据。具体的治疗方法主要根据胃曲张静脉瘤体的部位、大小和形态,按步骤有序地通过注射针向曲张静脉瘤体内注入适量的硬化剂和组织黏合剂,后续少量硬化剂和生理盐水冲洗注射针。组织黏合剂在血液中阴离子的作用下快速聚合,从而阻断血流,以达到急诊止血的效果,其后经历数周至数月,固化的黏合剂常规通过注射部位缓慢自行排出,继而排胶处的溃疡面愈合从而消除胃静脉曲张[11]。硬化剂治疗则通过诱导注射血管局部血栓形成,产生炎症和局部纤维化,进而闭塞局部静脉管腔以消除局部静脉曲张[12]。组织黏合剂联合硬化剂治疗后的并发症主要是治疗后2个月内发生再出血的风险,其主要原因与内镜下治疗中所注射的组织黏合剂在后续脱落过程中所形成的胃壁溃疡局部血管尚未闭合有关。因此,术后需住院密切随访观察数日。治疗期间我院常规使用生长抑素类药物降低门静脉压力,使用质子泵抑制剂抑酸,使用胃黏膜保护剂促进溃疡愈合,尽可能减少近期术后并发出血。本研究在使用上述药物的基础上,随访2个月内,如所列举的病例发现内镜下胃底组织排胶现象,并伴有局部溃疡形成。此外,有少数病人在治疗后发生排胶局部溃疡再出血。因此,有必要强化术后的随访和预防治疗。
有研究发现食管胃静脉曲张首次出血病人如无积极的预防措施,1年内再次出血率可达50%~80%,采用内镜下治疗和药物等积极的预防措施可能使再出血的概率降至约30%[13]。本研究随访发现内镜下行组织黏合剂联合硬化剂治疗6个月内及6个月后复查胃静脉曲张根除和基本消失率分别为75.0%及70.8%,可见内镜下组织黏合剂联合硬化剂治疗术可长期有效地消除静脉曲张,并在6个月左右复查及追加治疗即可。且本研究随访显示内镜下治疗术后1年内再发出血率仅为21.4%,但结果仍需大样本的临床数据验证。值得关注的是,结合随访结果发现,虽然内镜治疗术后出血复发率下降,但出血仍是主要死亡原因之一。可能的情况有门静脉高压性胃病的形成或胃底侧支循环的建立如胃底曲张静脉与左肾静脉和下腔静脉间自发形成较粗大的分流通道 (胃-肾和胃-腔分流)等,进而导致内镜下治疗效果欠佳等。但应用内镜下曲张静脉硬化剂或套扎治疗可能使部分病人肝功能评估级别降低至Child评分A级或B级,为后续的手术治疗或介入治疗做准备。本研究发现内镜下治疗术后随访有12例,经外科手术后随访至本研究结束均未再出血。因此,对于部分门静脉高压性食管胃曲张静脉出血病人,必要时应及时行转换治疗,从而改善生活质量。
本研究所列举的病例既往有肝硬化胃底静脉曲张破裂出血史,内镜下行黏合剂联合硬化剂治疗后未再出血,提示胃静脉曲张内镜下组织黏合剂联合硬化剂注射治疗是有效的。
总之,门静脉高压性胃静脉曲张内镜下组织黏合剂联合硬化剂注射治疗可作为过渡治疗方式,改善曲张静脉状态,降低出血风险。但部分病人仍应择期行外科手术或介入治疗,以期较长时间不出血。同时对于该类病人,应作好门静脉高压其他并发症的防治和肝脏功能检测,以期早发现、早治疗,进而提高病人生活质量和远期生存率。
