阻塞性睡眠呼吸暂停低通气综合征与耳鸣的相关性研究
2022-11-10高妍王忠巧黄东海
高妍,王忠巧,黄东海
(1.新疆医科大学第二附属医院 耳鼻咽喉头颈外科,新疆 乌鲁木齐 830063;2.中南大学湘雅医院 耳鼻咽喉头颈外科,湖南 长沙 410008)
阻塞性睡眠呼吸暂停低通气综合征(obstructive sleep apnea hypopnea syndrome,OSAHS)是耳鼻咽喉科常见病,病因多为上呼吸道塌陷或阻塞,可伴有睡眠打鼾、睡眠低氧、睡眠紊乱、嗜睡等,甚至引起多器官损伤。有研究报道,部分OSAHS患者伴有听力障碍[1],有文献报道,OSAHS患者耳鸣发生率是正常人的1.36 倍[2]。耳鸣是很多潜在疾病的病理症状,同时也是很多疾病的并发症。虽然耳蜗病变是导致耳鸣的根本原因,但不同听觉中枢对听力损失的失代偿功能是耳鸣发病的根源[3]。本文探讨了OSAHS伴耳鸣患者的临床特征,希望为其治疗提供方向。
1 对象与方法
1.1 研究对象
2018年1月—2021年6月就诊于新疆医科大学第二附属医院耳鼻咽喉科的OSAHS患者共71例,其中男55例(78.0%),女16 例(22.0%);年龄34~78岁,平均年龄(49.32±11.18)岁,所有患者均由耳鼻咽喉科医师进行详细的病史采集、专科查体、多导睡眠监测(polysomnography,PSG)检查和相关的听力检查。入组标准: 患者符合2011年中华医学会呼吸病学分会睡眠呼吸障碍学组的标准[3];有夜间睡眠打鼾、白天嗜睡等症状,且睡眠呼吸监测结果睡眠呼吸暂停低通气指数(apnea hypopnea index, AHI)≥5次/h的患者。排除标准:能够引起耳鸣及听力下降的其他疾病,如突发性耳聋、中耳炎、听神经瘤、耳硬化症、梅尼埃病、甲状腺功能减退、糖尿病、高血压、自身免疫性疾病等。
1.2 研究方法
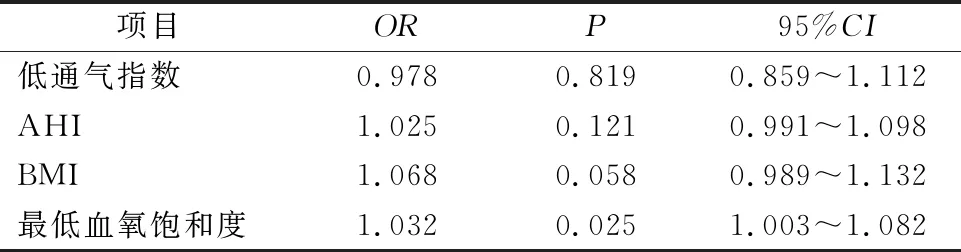
1.2.1 睡眠呼吸监测 采用凯迪泰医学科技有限公司生产的SW-SM2000CB便携式多导睡眠监测仪,检测时间大于6h以上,自动记录数据,后经人工修正。根据AHI监测结果,其中5次/h 1.2.2 纯音测听及声导抗测试 利用纯音测听仪(丹麦瑞声达ORBITER922)检测双耳气导0.25~8 kHz听阈,耳鸣检测仪检测骨导0.25~4 kHz 听阈。声导抗听力计(Madsen-ZODI-AC901)检测声导抗,除外B、C型鼓室曲线患者。听力下降分级,其中轻度:26~40 dB,中度:41~60 dB,重度:61~80 dB,极重度:>80 dB。 在71例OSAHS患者中,轻度14例,中度16例,重度41例。低氧血症严重程度分级:轻度41例、中度18例、重度12例。OSAHS无耳鸣者42例,伴有耳鸣者29例。各组间年龄、血压、AHI、体质指数(bodymass index, BMI)差异具有统计学意义(P<0.01),各组间平均听阈值、最长呼吸暂停时间差异无统计学意义(P>0.05)。具体数据见表1。 表1 OSAHS患者一般资料 (例, 29例伴有耳鸣患者中,其中轻度9例,中度3例,重度17例。各组听阈值以4~8 kHz下降为主。中、重度OSAHS患者听力损失较轻度明显,但差异无统计学意义(P>0.05)。具体数据见表2。 表2 不同程度OSAHS患者听力频率值 在71例OSAHS 患者中,伴有耳鸣的患者29例(40.8%);其中单侧听力下降12 例,双侧听力下降17 例;22例为轻度听力下降,6例为中度听力下降,1例为重度听力下降。轻、中、重度OSAHS 组耳鸣发生率分别为:44.4%(6/14)、58.3%(9/16)、34.1%(14/41),各组在高音调耳鸣中明显,中、重度OSAHS 组听力下降的比例较轻度OSAHS组高,但各组间差异无统计学意义(P>0.05)。具体数据见表3。 表3 不同程度且伴有耳鸣的OSAHS患者不同音调耳鸣情况分析 用多因素Logistic分析低通气指数、AHI、BMI、最低血氧饱和度与OSAHS的关系。结果显示,最低血氧饱和度是OSAHS患者耳鸣发生的独立因素(P=0.025)。具体数据见表4。 表4 耳鸣相关Logistic回归分析 普遍认为,听力损失是耳鸣发生的主要病因。既往研究发现,OSAHS患者容易引起耳鸣,而且高频听力是最容易损伤的波段[4-5],认为OSAHS患者的耳蜗及前庭功能因低氧血症和血氧饱和度降低而受到影响[4,6]。此外,低氧血症引起的炎性反应也是耳鸣、听力损失的病因[7-8]。本研究结果显示,不到50%OSAHS患者存在听力下降(4~8 kHz为主),听力下降幅度与疾病严重程度呈正相关。目前认为耳鸣的发生可能和毛细胞更容易受到缺氧的影响[9],原因是狭窄的耳蜗基底回蜗管中的血供相对较差。此外,耳蜗基底回的抗氧化物较少,抗氧化能力弱[10]。有理论认为,分布耳蜗的动脉不一,位于耳蜗底部的动脉多一些,血管纹也相对厚一些,耗氧量自然也要大,同时自蜗底至蜗顶处,基底膜是由窄逐渐变宽,而Corti器细胞也是逐渐变大,所以蜗底听功能的储备也相对较弱。慢性缺氧对蜗底的影响最严重,因此高音调耳鸣最明显[11]。此外,打鼾引起的噪音也被认为是OSAHS患者耳鸣发生的潜在危险因素[12]。有报道称慢性缺氧导致耳蜗对噪音的敏感度上升。我们的研究中,OSAHS患者的耳鸣伴有听力下降以4~8 kHz为主,所以因打鼾噪音引起OSAHS患者耳鸣的发生,继而出现听力损伤[13-14]。 OSAHS 患者的听力损失是耳鸣发生的病因,但并非所有听力损失患者都存在耳鸣[1,15]。人体听觉中枢对可调控传入的信号。当耳蜗受损后,外周听觉系统接受的信息减少,中枢皮层抑制作用出现问题,导致频率排列错乱,神经元出现异常电活动,从而导致耳鸣[16]。有文献报道,在轻、中度OSAHS 患者中存在隐匿型听力损失,不易被感知[17]。我们发现,部分听力正常OSAHS患者也存在耳鸣,与单纯纯音测听检测不灵敏有关。 轻微听力下降可通过听力的代偿功能产生耳鸣,当代偿功能恢复正常,微小的耳鸣信号会消除[15]。本研究中,OSAHS 患者耳鸣发生率(40.8%)高于正常人10%左右[18]。睡眠障碍、偏头痛及镇静药物均是耳鸣的常见病因等。大脑中的胶质淋巴系统是清除神经毒素的主要方式[19-20]。耳鸣是听觉皮层产生的一种异常电信号,在我们的睡眠过程中,会从中枢网络消除,不被感觉到。睡眠障碍患者这种清除作用出现问题,引起毒素堆积,干扰了大脑正常功能,引起中枢代偿功能障碍[19]。偏头痛干扰了高级对初级听觉皮层的控制,加强初级听觉皮层在听力损失上的代偿作用。过于敏感的大脑也会影响情绪中枢系统,进一步影响中枢的代偿作用,以上都会对耳鸣的出现产生一定的影响[20]。另外,也有证据显示偏头痛和耳鸣有着极为相似的病理机制。解剖学证实,三叉神经系统及听觉系统交叉于蜗核处[16],此神经通路直接参与了外周的非听觉系统对听力下降及耳鸣的代偿作用。偏头痛可以提高三叉神经系统的活性[21]。可以提高听觉中枢对感知声音信号的敏感性,从而诱发耳鸣。而OSAHS患者在睡眠过程中打鼾引发的震动、慢性间歇性缺氧、中途觉醒以及睡眠中断,都是偏头痛的诱因[22]。目前,多数学者认为超重与肥胖是OSAHS的主要发病原因之一,有研究表明在普通人群中,超重、肥胖是耳鸣发生的独立危险因素[23]。本研究观察了不同程度的OSAHS患者BMI存在差异,且BMI与耳鸣发生之间有相关性,这从另外一个角度证明了耳鸣患者与BMI的关系。 此外,最低血氧饱和度与OSAHS患者耳鸣有关,年龄、AHI、平均听阈值、血压等因素与耳鸣无关,这与王琳等[3]的研究结果一致。此次研究的样本量不大,在未来的研究中,我们将继续收集样本,通过进一步完善听力学检查,如听性脑干检查等,继续研究OSAHS的治疗与听力恢复情况的相关性。 总之,OSAHS患者高频听力更易受损,最低氧饱和为OSAHS患者耳鸣的危险因素。1.3 统计学分析
2 结果
2.1 患者一般情况
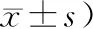
2.2 听力损失
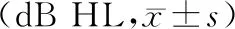
2.3 耳鸣情况

2.4 OSAHS患者伴发慢性耳鸣相关因素的Logistic回归分析
3 讨论
