硫氰酸红霉素精制工艺研究
2022-11-07王晓军白海龙刘万莲李麟基
王晓军 白海龙 刘万莲 李麟基
(宁夏泰益欣生物科技有限公司,宁夏银川 750205)
硫氰酸红霉素(Erythromycin Thiocyanate),别名高力霉素;红霉素硫氰酸盐,外观为白色结晶性粉末,微溶于水,易溶于甲醇、乙醇、丙酮等有机溶剂[1]。红霉素为大环内酯类抗生素药物,红霉素通过与细菌核蛋白体的50S亚基结合,来抑制转肽作用或者信使核糖核酸移位,从而抑制细菌蛋白质的合成,抵抗细菌感染,良好的药用性使得红霉素使用广泛,但同时抗生素污染环境也同样值得注意[2]。
硫氰酸红霉素属大环内酯类抗生素,本品在碱性溶液中抗菌作用较强,但当pH值低于4时,抗菌作用几乎完全消失。分子中含有一个14元内脂环、两分子糖苷及一份子硫氰酸,分子量:793.02结构式如图1所示。
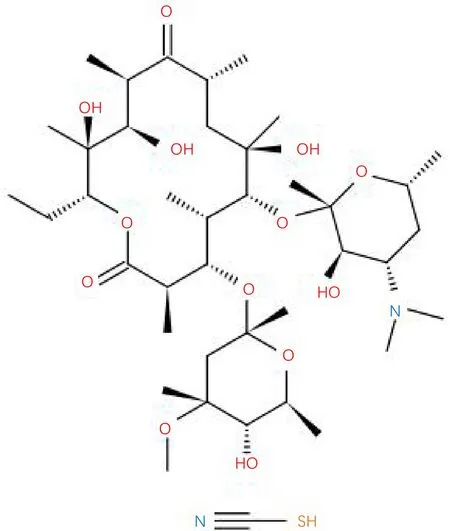
图1 硫氰酸红霉素结构式
大环内酯类化合物已成为临床应用仅次于β-内酰胺类抗生素的第二大类抗感染药物,因为其毒副作用小、安全性高、抗菌活性好和无过敏反应,所以在临床治疗上具有重要的地位。第一代大环内酯类抗生素,是指红霉素及其酯类衍生物,产品包括红霉素、琥乙红霉素、硬脂酸红霉素、红霉素碳酸乙酯、醋硬脂红霉素、乳糖酸红霉素和依托红霉素等[3]。
国外20世纪60~70年代曾报道过,由硫氰酸红霉素可以改善红霉素在水中的溶解度或减少苦味儿改善药物动力学性质,降低毒副作用等,同时又具有红霉素的抗菌活性因而得到应用,我国每年约生产21万吨抗生素,约占世界总量的60%,涉及36种抗生素化合物,其中过半的抗生素被用于养殖业。据报道,养殖业大约90% 的抗生素都是在亚治疗浓度下使用的,其中70%是为了预防疾病,30%是为了促进生长[4]。抗生素药物中约有85%的产品是以固体形式提供的,硫氰酸红霉素便是以固体形式提供的。在晶体药物产品生产中,结晶工序通常是其精制纯化的终端工序,最终决定了药物的质量,也决定了药品的药效与稳定性[5]。同时,结晶收率的提高,对于提高医药产品的总收率与降低成本也起着关键性的作用。因此,结晶不仅是药物生产中的一种分离及提纯手段,更是制备具有医药活性及特定状态固体药物的一种不可缺少的关键步骤。因此,本文研究硫氰酸红霉素制备精制结晶工艺控制及工艺优化。
1.仪器与试剂(见表1和表2)

表1 所用主要试剂列表

表2 所用主要设备仪器列表
2.材料与方法
2.1 材料来源
硫氰酸红霉素粗品由宁夏泰益欣生物科技有限公司提供。
2.2 方法
2.2.1 方法一
加入结晶液体积10%~20%的纯化水,用50%的冰醋酸调节pH至6.5~7.5,流加结晶液体积5%~7%的30%NaSCN溶液。结晶温度控制在42℃~46℃,保温养晶60min~180min(过程检测pH值保持在6.5~7.0)。
2.2.2 方法二
不加水,用50%的冰醋酸调节pH至6.5~7.5,流加结晶液体积的5%~7% 40%NaSCN溶液。结晶温度控制在42℃~46℃,保温养晶60min~180min(过程检测pH值保持在6.5~7.0)。
2.2.3 方法三
利用反应结晶特点,进行梯度分步结晶。
一次结晶:用50%的冰醋酸调节结晶液pH至7.8~8.0,流加结晶液体积3%的30%NaSCN溶液。结晶温度控制在42℃~46℃,保温养晶30min。
二次结晶:进行热过滤,过程保温进行,收集母液进行二次结晶。流加结晶体积2.5%的30%硫氰酸钠,补加结晶液体积10%~20%的纯化水降温结晶,最终降至10℃左右养晶30min进行过滤。
2.3 梯度结晶硫氰酸钠加量筛选
硫氰红霉素为反应结晶,合适量的反应物更能控制结晶成品的质量,因此对梯度结晶,一、二次硫氰酸钠加量进行以下筛选:一次加量分别为2.5%、3.0%、3.5%。二次加量分别为3.0%、2.5%、2.0%。
3.检测要求
色谱条件:用十八烷基硅烷键合硅胶为填充剂;检测波长为215nm,色谱柱:4.6mm×150mm×3.5μm,流速为1.1ml/min,柱温为 40℃。
流动相:0.020mol/L磷酸氢二钾缓冲溶液:乙腈=60:40,量取 0.020mol/L 磷酸氢二钾缓冲溶液 600ml,量取乙腈400ml,用稀磷酸溶液调节pH值为9.60~9.80,混匀脱气,即得。
4.实验结果与分析
4.1 粗品与丙酮比例选择
用运行业现有工艺筛选出最佳粗品与丙酮溶解比例,计算最优溶液效价。取用硫氰酸红霉素粗品,用丙酮溶解,溶解温度控制在38℃~46℃,以硫氰酸红霉素粗品质量:丙酮体积 1:1.2、1:1.5、1:1.8、1:2.1、1:2.4比例进行最优溶剂加量选择;
用饱和盐水洗脱色素及水溶性杂质。加入溶解液体积2.5%的饱和盐水搅拌洗涤10min~15min,洗涤完成后静置10min分离底部水相,重复此步骤3遍后开始结晶,实验结果见表3。
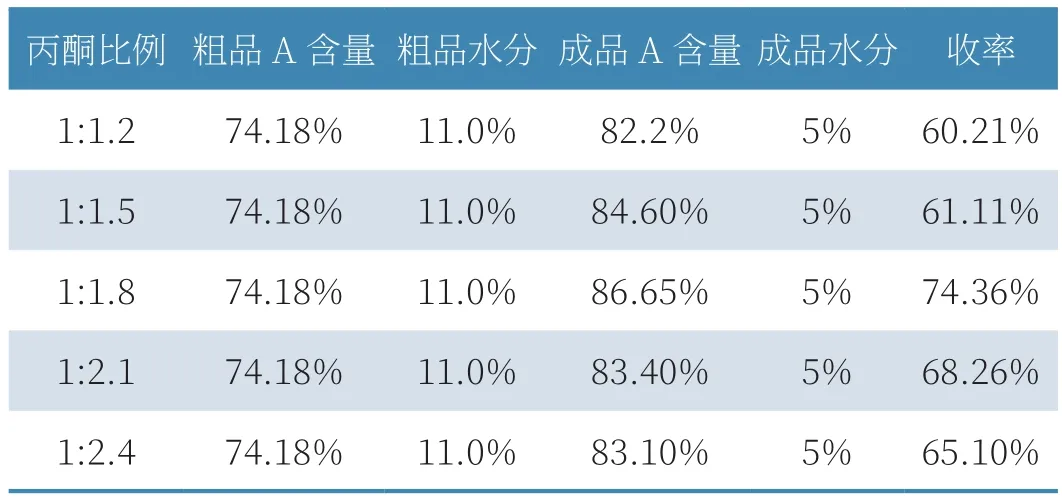
表3 粗品与丙酮比例筛选结果
由表3可知,粗品与丙酮比例从1:1.2增加至1.8时,成品A含量由82.2升高至86.65时又开始下降,粗品量不变在丙酮加量增加时,1:1.8比列下成品质量与收率为最优加量,收率及红霉素A含量最高。
4.2 结晶方法选择
通过3种结晶方法进行结晶对比,检测结果见表4和表5。

表4 结晶方法对比结果
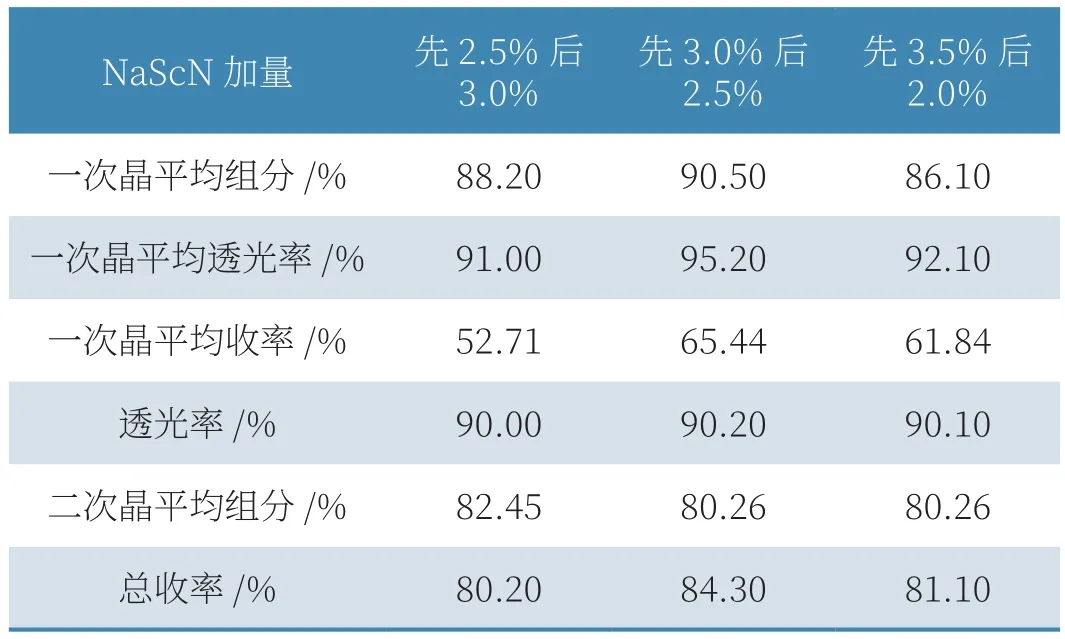
表5 梯度硫氰酸钠加量筛选结果
通过上表数据发现,梯度结晶一次晶组分高达90%,两次结晶平均收率高达80.23%,相较于其他两种方法,梯度结晶制备产品质量及收率更好。
通过表4、表5筛选结果可以看到,反应结晶中反应物加量对梯度结晶一次晶质量有影,通过不同NaScN加量可以看到,先2.5%后3.0%一次晶平均组分为88.2%,总收率80.2%。先3.0%后2.5%一次晶平均组分为90.5%,总收率为84.3%。先3.5%后2.0%一次晶平均组分86.1%,总收率为81.1%,因此最终确定一次结晶硫氰酸钠加量为3.0%,二次结晶硫氰酸钠加量为2.5%为最优加入量。
由图2、图3可知,反溶剂加入结晶体系中(反溶剂为水),溶液中产生的局部过饱和度也越高,系统就会瞬时形成大量的晶核以降低整个体系过饱和度,这样系统的结晶速率会产生较大的波动。结晶系统不能维持一个较稳定的结晶速率,则形成的晶体粒度差异大,粒度分布不均匀,同时容易夹带杂质。大量硫氰酸钠加入同理。

图2 方法一制备成品

图3 方法二制备成品
由图4可知,梯度结晶系统能够维持一个较稳定的结晶速率,符合硫氰酸红霉素结晶条件。晶体晶型相对完整且内部包裹杂质较少,晶体透亮。将红霉素的整个结晶过程分段控制,采用在较高的温度下结晶,然后逐渐添加硫氰酸钠及降温养晶的方法,从而达到图4制备成品晶型。

图4 方法三制备成品
5.结论
运用梯度结晶方法,能够维持一个较稳定的结晶环境,控制硫氰酸酸钠加量从而控制反应结晶速率,形成的晶体粒度差异较小,粒度分布较为均匀,同时不容易在晶体内部夹带杂质,最终获得硫氰酸红霉素成品组分≥90%,整体收率能够达到84.3%左右。
