B2O3含量对SiO2-B2O3-Al2O3-Na2O系陶瓷结合剂结构与性能的影响*
2022-11-04徐三魁徐天兵闫国进陈兆奇吴坦洋
王 照,徐三魁,黄 威,徐天兵,韩 平,闫国进,陈兆奇,吴坦洋
(1.河南工业大学 材料科学与工程学院,郑州 450001)
(2.连云港市沃鑫高新材料有限公司,江苏 连云港222300)
陶瓷结合剂金刚石磨具以其耐热性好、磨削精度高、自锐性好、修整间隔较长等特点,广泛应用于超硬工具精磨、半导体精加工等方面,且使用量连年增加[1-3]。但陶瓷结合剂金刚石砂轮的使用性能很大程度上取决于陶瓷结合剂的性能[4],而陶瓷结合剂的性能主要取决于其玻璃相的成分与浓度,以及玻璃相形成的微观网络结构等[5]。其中,以SiO2-B2O3-Al2O3-Na2O(R2O 为碱金属氧化物)为基础的硼铝硅酸盐陶瓷结合剂具有可调节热膨胀系数、良好的力学性能、与磨料结合性能好等特点[6],成为本领域的研究热点之一。尤其是B2O3的熔融温度低,只有450 ℃,将其引入陶瓷结合剂中,可以极大地降低陶瓷结合剂的烧结温度[7],为陶瓷结合剂的超低温烧结提供了可能。
根据玻璃相形成的网络理论,B2O3和SiO2在熔融状态下不能形成均匀一致的熔体,因为前者为层状结构,后者为架状结构;但在其中加入Na2O 等碱金属氧化物后,Na2O 提供的游离氧促使硼氧三角体[BO3]转变为硼氧四面体[BO4]架状结构,与硅氧四面体[SiO4]共同构成三维立体的空间网络结构,从而增大硅酸盐玻璃的强度[8]。JACKSON 等[9]将硼铝硅酸盐玻璃用于陶瓷结合剂中,发现结合剂热稳定性好、热膨胀系数高等。张小福等[10]研究了高温下陶瓷结合剂对金刚石磨料的浸润性,发现B2O3的加入使浸润性变好,而碱金属氧化物可增加结合剂的高温流动性但并不能改善其浸润性。何峰等[11]在硅酸盐玻璃中添加了不同含量的B2O3,结果表明R2O 提供的游离氧不会无限地使[BO3]转变为[BO4]。张盼等[12]采用X 射线光电子能谱、EDS 能谱、紫外-可见光能谱进一步分析了B2O3对低膨胀硼硅酸盐玻璃结构的影响。
总之,添加B2O3对陶瓷结合剂性能具有重要作用。但目前工业上用的陶瓷结合剂中B2O3含量不高,其摩尔分数普遍在5%~10%,B2O3含量较高的陶瓷结合剂在少量发明专利中有涉及[13-14]并取得了一定的应用效果,但高含量的B2O3引入到基础陶瓷结合剂中的科学研究报道较少,缺少相关理论支持。因此,将B2O3引入到基础陶瓷结合剂中,改变不同比例的B2O3与SiO2含量,使B2O3的摩尔分数最高达到27%,同时碱金属氧化物的摩尔分数高达20%,来系统探究各成分之间的动态反应平衡以及陶瓷结合剂玻璃化后的微观结构与性能,以期得到性能更加优良的超低温烧结的高强度陶瓷结合剂。
1 试验
1.1 玻璃样品和结合剂制备
表1 为试验设计的陶瓷结合剂摩尔分数配方,主要研究B2O3含量对陶瓷结合剂性能的影响。为便于配料以及和国内常用配方形式对比,转换为原料质量分数的配比如表2所示,其样品原料均为分析纯(西陇科学股份有限公司生产)。将表2 中的5 组试样按照不同质量分数准确称量300 g,使用研钵研磨混合均匀后压成小块,分别放入刚玉坩埚中,在高温熔炼炉中升温至1 400 ℃使其熔融,保温2 h 后对熔融玻璃料做如下处理:一部分滴在预热好的石墨板上缓冷,随后在500 ℃下退火2 h随炉冷却,以消除玻璃内部的应力,得到5 组玻璃样品;另一部分倒入去离子水中急冷,再经破碎、球磨、过200 目筛(筛网网孔尺寸为75 μm)得到5 组陶瓷结合剂。得到的玻璃样品及陶瓷结合剂都用1#~5#命名。
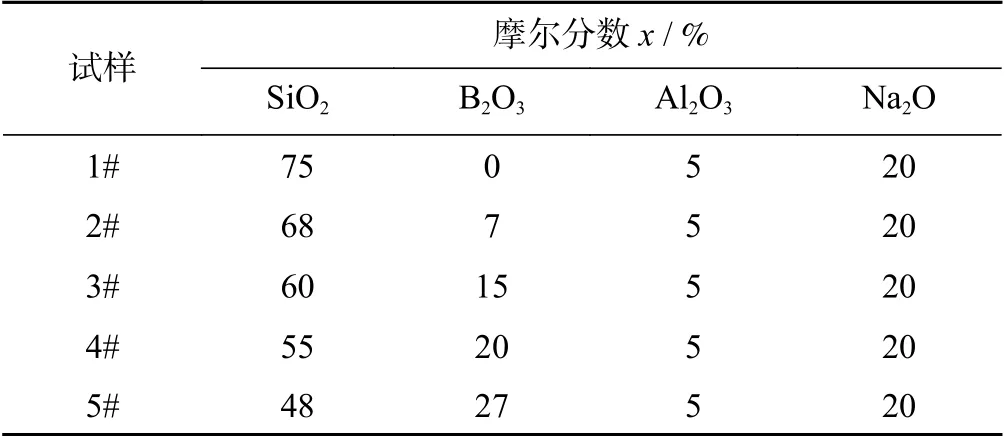
表1 陶瓷结合剂化学组成Tab.1 Chemical compositions of ceramic binder

表2 陶瓷结合剂原料质量分数Tab.2 Mass fractions of ceramic binder raw materials
1.2 陶瓷结合剂样品制备及性能检测
将5 组陶瓷结合剂分别与质量分数为5%的PVA黏结剂混合均匀,冷压成15 mm×15 mm 的圆柱体和5 mm×6 mm×30 mm 的待烧结试样条,在80 ℃时干燥12 h得到5 组结合剂试样。使用岛津IR Prestige-21 红外光谱仪对结合剂试样进行红外光谱测试,其扫描波数范围为400~4 000 cm-1。使用D8 Advance X 射线衍射仪对5 组结合剂试样的物相进行分析。采用标准耐火锥测定5 组结合剂试样的耐火度。采用平面流淌法测定其流动性。采用济南永科WDW-50 微机控制电子多功能试验机用三点弯曲法测定结合剂试样的抗折强度。采用阿基米德排水法精确测量玻璃样品的密度。使用FM-ARS900 显微硬度仪检测5 组玻璃样品的显微硬度。对5 组结合剂试样进行热膨胀系数测试,并采用FEI 公司生产的INSPECT-F50 型扫描电镜观察陶瓷结合剂烧结后的形貌。
2 结果与讨论
2.1 红外光谱分析
红外光谱分析的主要作用是利用吸收谱峰的位置、强度和形状来推测样品的化学键种类、物质的结构与化学组成以及各成分之间的相互作用情况。表3 是硼硅酸盐玻璃常见的结构基团与红外吸收峰的特征振动对应表[15],图1 是5 组结合剂试样的红外吸收图谱。由表3 和图1 可知:1#陶瓷结合剂分别在468,770 和1 040 cm-1出现明显的吸收峰(带),分别对应于Si-O-Si 弯曲振动峰、O-Si-O 伸缩振动峰和Si-O-Si 反对称伸缩振动峰。其中,位于468 cm-1处的Si-O-Si 弯曲振动峰与表3 中的相应峰值460 cm-1稍有差距,这是因为在玻璃态中Si-O-Si 的弯曲振动峰就位于468 cm-1处[11];770 cm-1处的吸收峰为O-Si-O 伸缩振动峰,对应被游离氧断键后形成的非桥氧键。与2#~5#样品相比,1#样品770 cm-1处O-Si-O 伸缩振动峰最为尖锐,强度最高,且2#~5#样品中O-Si-O 伸缩振动峰逐渐减弱。
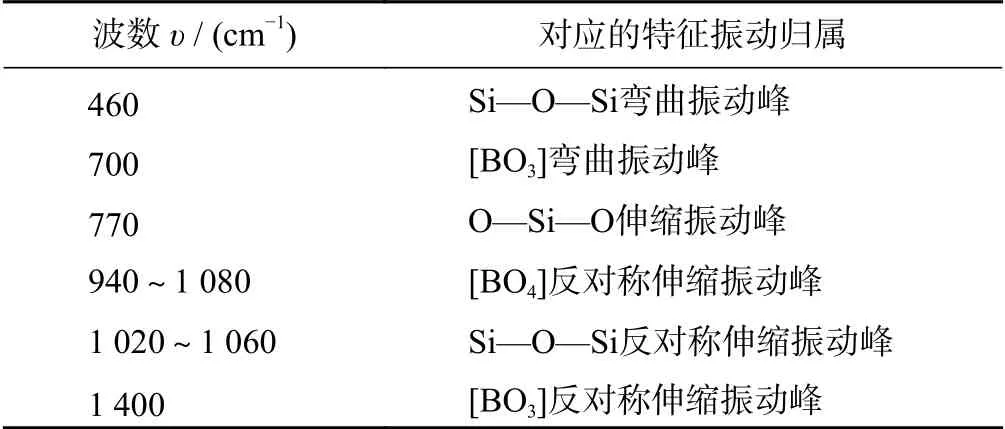
表3 硼硅酸盐玻璃常见的红外吸收光谱特征振动[15]Tab.3 Characteristic vibrations of borosilicate glass infrared absorption spectra[15]

图1 不同B2O3 含量陶瓷结合剂的红外吸收光谱Fig.1 Infrared absorption spectra of ceramic binders with different B2O3 contents
由表3 和图1 还可知:2#~5#样品除了1#样品相应的吸收峰外,随着B2O3添加量的逐渐增加,样品图谱中还在700,1 400 cm-1处出现明显的红外吸收峰,且吸收峰的强度随B2O3添加量的增加而增强,其分别对应[BO3]的弯曲振动峰和反对称伸缩振动峰,这表明玻璃中[BO3]的含量在增加;而出现在1 000 cm-1附近处的吸收峰是Si-O-Si 和[BO4] 反对称伸缩振动峰的合峰。且合峰随B2O3含量增加,2 种峰的相关作用增强,Si-O-Si 反对称伸缩振动减弱,[BO4]反对称伸缩振动增强,其共同作用导致其振动峰向低波数方向偏移[16]。
样品2#~5#与1#对比,其460,770和1 020~1 060 cm-1处的Si-O-Si 2 个吸收峰和O-Si-O 的吸收峰的位置发生了部分移动,且770 cm-1处的O-Si-O 伸缩振动峰逐渐减弱。说明添加的B2O3与原玻璃料中的SiO2等成分间发生了一定的相互作用,B2O3夺取了[SiO4]中的游离氧,导致770 cm-1处的O-Si-O 减少,影响了SiO2的化学成键,而使Si-O-Si 吸收峰移动。可以预见,该相互作用也会影响陶瓷结合剂的理化及使用性能等。
2.2 X 射线衍射分析
图2 是5 组陶瓷结合剂样品的X 射线衍射图谱。从图2 中可知:5 组样品均在15°~30°出现较宽的衍射峰,这是典型的玻璃相衍射峰特征;而在其他位置没有明显的衍射峰,说明样品除玻璃相外没有其他晶体生成。从结构上讲,这种玻璃相能实现结合剂对磨料的良好包覆,有利于陶瓷结合剂与磨料的结合,可提高磨具的强度等性能。

图2 5 组陶瓷结合剂试样的XRD 图谱Fig.2 XRD patterns of 5 groups of ceramic binder samples
2.3 陶瓷结合剂的耐火度和流动性
结合剂的耐火度可决定其烧结温度。不同B2O3摩尔分数的陶瓷结合剂试样耐火度和流动性如图3所示,图3 中的每个值是3 次测量结果的平均值。从图3可以看出:由于B2O3的催熔作用,随着B2O3摩尔分数增加,5 组结合剂试样的耐火度显著降低,且5#陶瓷结合剂的耐火度可低至688 ℃,比1#陶瓷结合剂(未添加B2O3)的耐火度低约127 ℃。根据烧结理论,烧结温度应比耐火度高60~100 ℃。同时,金刚石磨料在温度高于800 ℃时容易氧化,因此要保证金刚石磨具的耐火度低于800 ℃。

图3 不同B2O3 摩尔分数的陶瓷结合剂的耐火度和流动性Fig.3 Refractoriness and fluidity of ceramic binder with different B2O3 mole fractions
流动性是反映结合剂熔体在高温下黏度变化的重要参数。流动性越好,结合剂熔体的黏度越低。结合剂良好的流动性有利于其在磨料颗粒周围分布均匀,且超精密磨削用纳米金刚石磨料更需要流动性良好的结合剂来充分润湿,并保证其有良好的结合性,以避免金刚石磨料团聚而对加工工件造成的划伤、划痕等。在瓷砖衬底700 ℃下烧结2 h 的陶瓷结合剂的流动性如图3所示,5 组陶瓷结合剂试样的高温流动性在97.47%~150.73%,均在陶瓷结合剂正常流动性范围之内(90.00%~280.00%)[17]。同时,1#与2#陶瓷结合剂的流动性低于100.00%,是因为这2 组陶瓷结合剂在700 ℃下发生了固相烧结,坯体紧密收缩所致;随着B2O3摩尔分数的增加,其他结合剂的流动性则显著增加,且与结合剂的耐火度呈相反的变化趋势。其中,5#结合剂的流动性为150.73%,比1#结合剂的高出约50.00%。这是因为B2O3具有较低的熔点(450 ℃),陶瓷结合剂的耐火度随B2O3摩尔分数增加而降低,因而显著降低了结合剂的熔融温度,且降低结合剂熔体的黏度,降低其耐火度。结合剂耐火度越低,结合剂在高温下的流动性越好。
2.4 抗折强度
磨具的耐磨性能直接反映磨具的耐用程度,但其耐磨性能一般不能直接测量,所以用抗折强度来间接衡量磨具的耐磨性。图4 为5 组陶瓷结合剂试样在不同烧结温度下测得的抗折强度曲线。由图4 可以看出:5 组结合剂试样的抗折强度都表现出随烧结温度升高先升高后降低的趋势。在最合适的烧结温度下,5 组陶瓷结合剂试样都出现了抗折强度峰值。这是因为低于最佳烧结温度时,坯体致密度较低,气孔率较高,不易发生固相烧结反应,结合剂各组分间相互作用力弱,导致样条强度不高;烧结温度高于烧结点时,结合剂中液相增加,高温流动性变强,留在结合剂内部的气体无法排出体外,出现过烧发泡现象,使结合剂收缩率降低、强度下降。
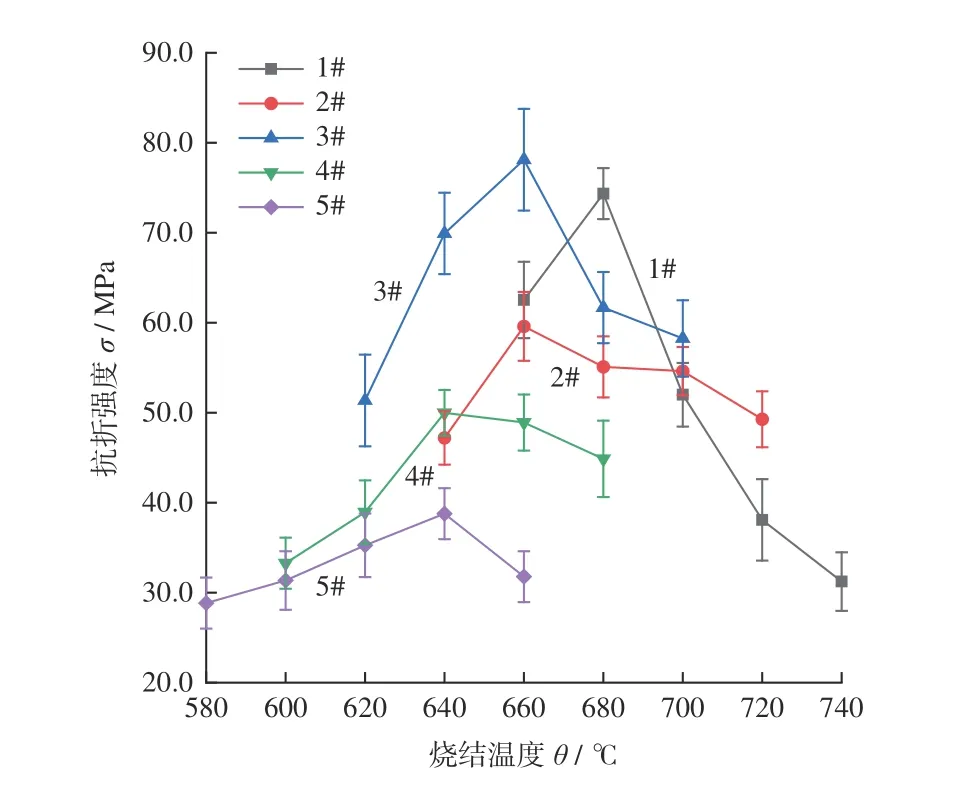
图4 5 组陶瓷结合剂在不同烧结温度下的抗折强度变化Fig.4 Changes of bending strength of five groups of ceramic binders at different sintering temperatures
由于1#陶瓷结合剂为纯铝硅酸盐玻璃,根据玻璃形成理论,SiO2作为主体网络形成体构成了较为稳定的[SiO4]骨架,碱金属氧化物Na2O 作为网络变性体为玻璃体提供游离氧,使Si-O 键断裂,降低玻璃熔融温度,同时与摩尔分数为5%的网络中间体Al2O3结合形成[AlO4]四面体增强玻璃结构。经计算1#陶瓷结合剂试样的氧硅比R值为2.18,结构参数(桥氧)为3.64,这表明1#结合剂大部分为结构稳定的[SiO4]骨架结构,结合力较大,抗折强度较高,最高达到74.34 MPa。而2#~5#结合剂为硼铝硅酸盐玻璃,当B2O3摩尔分数为7%时(2#),B2O3取 代SiO2使[SiO4] 数量减少,且[BO3]数量增加,玻璃结构的聚合程度稍有下降,因而相比于1#陶瓷结合剂的强度有所降低;同时,Na2O 提供的游离氧使得[BO3]变为[BO4]。当B2O3摩尔分数达到15%时(3#),3#的[BO4]含量达到最高,都参与到[SiO4]构成的网络构成骨架中,此时抗折强度最高达到78.11 MPa。相对于3#结合剂试样来说,4#、5#结合剂试样中再加入B2O3后,由于游离氧不足导致[BO3]在体系中占据了较高比例,因而结合剂的抗折强度峰值先升高后降低,出现了“硼反常”特性,这进一步验证了红外光谱分析结果。另外,高含量B2O3的4#和5#结合剂样条依然具有较高的抗折强度,且在不同烧结温度下抗折强度相差不大,因而提高了陶瓷结合剂的烧结范围。
2.5 玻璃样品的密度和硬度
为了得到更好的低温高强耐磨陶瓷结合剂,对玻璃的密度与显微硬度这2 个表征玻璃结构与性能的重要指标进行探究。分别选取上述的1#~5#熔融缓冷的母体玻璃测试其硬度与显微硬度,结果如图5所示。图5中:5 种玻璃的密度与显微硬度都呈现出相同的趋势,且1#~3#玻璃的密度和显微硬度呈逐渐增大的趋势,3#玻璃的最大密度达到2.45 g/cm3,显微硬度最大值达到856 MPa;4#和5#玻璃的密度降低,硬度变小且硬度数值较为接近。

图5 不同B2O3 摩尔分数的玻璃的密度和显微硬度Fig.5 Density and microhardness of glass with different B2O3 mole fractions
随着B2O3的加入,玻璃的网络结构逐渐变得有序化,使玻璃的结构变得致密。由于B-O 的键能高于Si-O 的,[BO4]的体积小于[SiO4]的体积,玻璃网络结构紧密程度提升后,在密度增大的同时表面硬度增加;但4#和5#的B2O3摩尔分数较高,过多的B2O3破坏了玻璃的网络结构,且可能产生了分相,玻璃内部的气孔等缺陷增多,使二者密度及显微硬度降低。4#和5#的显微硬度相差不大而密度差别较大的主要原因,可能是5#样品的总气孔率比4#的总气孔率要高,所以其密度较小;但气孔有大有小,大的气泡对样品的硬度和强度影响大,而微小气孔对其影响较小,因而5#样品中的气孔与4#样品的相比,5#样品中的气孔更小更均匀,因而其显微硬度降低少。因此,要获得硬度较高的玻璃陶瓷结合剂制品,添加的B2O3摩尔分数为15%最好。
2.6 热膨胀系数
陶瓷结合剂的热膨胀系数对陶瓷砂轮的性能有重要影响,为了获得陶瓷结合剂良好的把持力,避免其与磨料界面产生热应力,要求陶瓷结合剂与磨粒之间尽可能有好的热匹配性能[18]。
在650 ℃下烧结2 h 后,5 组陶瓷结合剂试样的热膨胀系数如图6所示。由图6 可知:在650 ℃下烧结的1#、2#、3#、4#和5#陶瓷结合剂的热膨胀系数分别为7.56 × 10-6,5.75 × 10-6,5.62 × 10-6,6.21× 10-6和6.42×10-6/℃,B2O3的加入会极大地降低陶瓷结合剂的热膨胀系数,且随着B2O3添加量的增加,陶瓷结合剂的热膨胀系数呈先减小后缓慢增大的趋势。当B2O3添加的摩尔分数为15%时,3#陶瓷结合剂试样的最低热膨胀系数为5.62 × 10-6/℃,与金刚石的热膨胀系数4.50 ×10-6/℃最匹配。热膨胀系数依赖于不同网络结构的玻璃化键与各组分的化学成分,B2O3加入量对热膨胀系数的影响与Na2O/B2O3比值有关,且硼离子存在于玻璃结构中的[BO3]三角体和[BO4]四面体中。[BO4]能增强玻璃网状结构的致密性,提高玻璃的热稳定性,使其热膨胀系数下降;相反,[BO3]会降低网络结构的致密性,使其热膨胀系数上升。随着B2O3含量的增加,[BO4]浓度首先增加,这有利于热膨胀系数的下降。然而,当B2O3含量增加到一定值时,Na2O 的浓度达到饱和,提供的游离氧不足以生成[BO4],使[BO3]浓度增加,因此玻璃化陶瓷结合剂的热膨胀系数会上升。
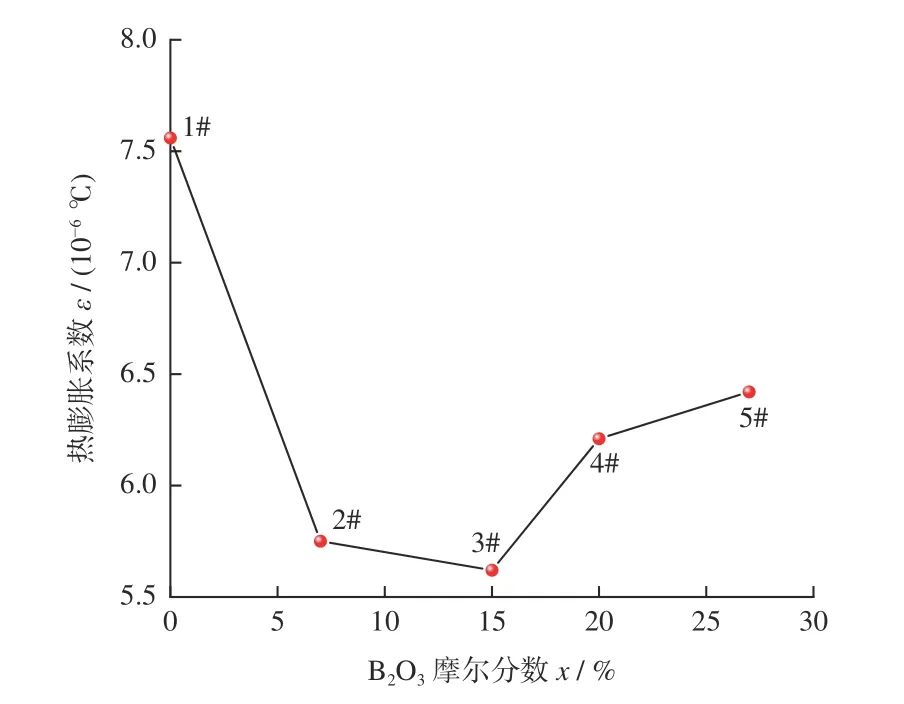
图6 不同B2O3 摩尔分数的陶瓷结合剂的热膨胀系数Fig.6 Thermal expansion coefficients of ceramic binders with different B2O3 mole fractions
2.7 陶瓷结合剂的断口扫描形貌
玻璃粉末的液相烧结是在表面自由能的推动下进行的,随着温度逐渐升高,粉末颗粒发生黏性蠕变传质从而致密化的过程[19]。采用扫描电镜观察B2O3的加入对陶瓷结合剂试样形貌的影响,图7 是1#、3#、5#陶瓷结合剂的扫描电镜形貌,其中的图7a、图7b、图7c 和图7d、图7e、图7f 分别是这3 种结合剂分别放大1 000倍、3 000 倍时的试样形貌。由图7 可以发现:在不加B2O3(1#)、适量B2O3(3#)和过量B2O3(5#)的粉末烧结试样中,气孔的大小和多少也出现了“硼反常”。1#试样气孔较大、气孔率较高,气孔最大尺寸达到15 μm,是液相烧结时未能排尽坯体中的气体产生的,说明只依靠添加R2O(碱金属氧化物)产生的液相烧结并不充分,且不利于磨具力学性能的提高;3#试样的断口形貌为典型的脆性断裂,试样气孔最少、气孔率最低,且大部分是微孔,分布较为均匀。由于在玻璃化熔融过程中排尽了大部分空气,表现出了较高的致密性,产生了如图4、图5所示的高抗折强度和密度等,这有利于增加结合剂对金刚石的把持能力,增加磨具的耐磨性。过量添加B2O3的5#试样由于[BO3]过量且产生分相导致其气孔较多、气孔尺寸较大,并使其致密度下降,气孔率进一步升高,这也与前面样品的密度和抗折强度试验结果相一致。

图7 陶瓷结合剂烧结试样断口扫描形貌Fig.7 SEM fracture morphology of sintered samples of ceramic binders
3 结论
B2O3作为超硬磨具陶瓷结合剂的一种组成成分,对陶瓷结合剂的结构和性能影响较大。通过在SiO2-Al2O3-Na2O 系陶瓷结合剂中加入不同含量的B2O3进行烧结,并对获得的玻璃和陶瓷结合剂烧结试样进行XRD、红外光谱、扫描电镜及各项力学性能分析,得出如下结论:
(1)B2O3的加入使陶瓷结合剂的耐火度和流动性大为改善。加入摩尔分数为27%的B2O3后,陶瓷结合剂的耐火度和流动性可达688 ℃、150.73%。
(2)玻璃试样与陶瓷结合剂粉末烧结体试样的性能都显示出了明显的硼反常特性。随着B2O3添加量增加,陶瓷结合剂的抗折强度先增大后减小,B2O3摩尔分数为15%时的陶瓷结合剂抗折强度最高为78.11 MPa;同时,玻璃样品的密度和硬度呈先增大后减小的趋势。其中,B2O3摩尔分数为15%的玻璃样品显微硬度最高、密度最大,分别为856 MPa 和2.45 g/cm3。
(3)B2O3的加入对降低陶瓷结合剂试样的热膨胀系数起到了关键作用,尤其是B2O3摩尔分数为15%时,陶瓷结合剂试样的热膨胀系数低至5.62× 10-6/℃,与金刚石的热膨胀系数接近。
(4)B2O3摩尔分数为7%~15%时的SiO2-B2O3-Al2O3-Na2O 陶瓷结合剂具有较低的耐火度、良好的流动性和热膨胀系数,有利于与金刚石形成理想的复合结构,同时增加制成的磨具的耐磨性。
