高性能掺硼金刚石电极的研究进展
2022-11-04李莲莲陈冠钦
李莲莲,陈冠钦
(1.国家知识产权局,北京 100088)
(2.同方威视技术股份有限公司,北京100084)
随着现代经济和社会的快速发展,各行业的污水排放量日益增加,污染物成分也越来越复杂[1],对人体健康和生态环境都产生了巨大的破坏。如何处理这些污水,成了全人类共同面对的巨大挑战。目前,常用的污水处理方式包括物理法、化学法以及生化法。但传统处理方法在面对污染物成分复杂、污染物浓度高以及具有生物毒性的污水时,往往无法对污水进行有效的降解处理。同时,传统的污水处理方法还面临处理周期长、设备投资大以及引入其他污染物等问题。
电化学高级氧化工艺(electrochemical advanced oxidation processes,EAOP)[2]作为一种新型污水处理工艺,由于其具有所需设备简单、操作容易、控制方便、适用范围广、无需添加化学试剂等优点被视为一种极具应用潜力的污水处理工艺。电化学高级氧化工艺的核心在于阳极材料。常用的阳极材料包括石墨电极[3]、金属电极(Cu、Pb 等)、金属氧化物电极(MnO2、RuO2、NiO 等)[4]以及掺硼金刚石(boron doped diamond,BDD)电极。其中,BDD 电极具有电化学势窗宽、背景电流小、介电常数低、可逆性好、空穴迁移率高等特点,在污水处理中具有广阔的应用前景,成为近年来的研究热点。
BDD 是金刚石中一部分碳原子被硼原子取代的金刚石材料。因金刚石本征电阻可达到1016Ω·cm,是一种性能优良的绝缘材料。当硼原子掺杂进入金刚石中,金刚石从绝缘体转变为半导体。这是由于硼原子进入金刚石晶格后产生空穴载流子,使之成为空穴型半导体或P 型半导体。随着硼掺杂浓度的增加,金刚石中的空穴浓度随之增加,载流子浓度增加,导电性能提升。但当金刚石中的硼原子浓度过高时,则会破坏金刚石的结构,导致金刚石的导电性能大幅降低。
在通电条件下,BDD 表面会将水中的有机物直接或者间接地氧化成无毒无害的无机物[5-7]。图1 为BDD污水处理的原理示意图。直接氧化法是指有机污染物吸附在阳极表面,在阳极高电势的作用下失去电子,从而被氧化为CO2、H2O 等物质。间接氧化法则是指阳极电极与水反应产生具有强氧化作用的羟基自由基(·OH)活性基团,羟基自由基与有机污染物间发生氧化还原反应,最终将有机污染物氧化为CO2、H2O 等物质。因此,提高BDD 电极污水处理效率的主要方法便是增加BDD 电极的比表面积[8]。随着BDD 电极的比表面积增加,有机污染物在电极表面的吸附位点增加,从而增加羟基自由基的产量,降解效率提高。构建三维或多孔结构是增加BDD 电极比表面积的有效途径之一[9]。此外,通过在电极表面沉积具有高析氧过电位的材料[10]以及构建特殊的异质结等表面修饰处理也可以改善BDD 电极的电化学性能,提高有机污染物的降解效率。
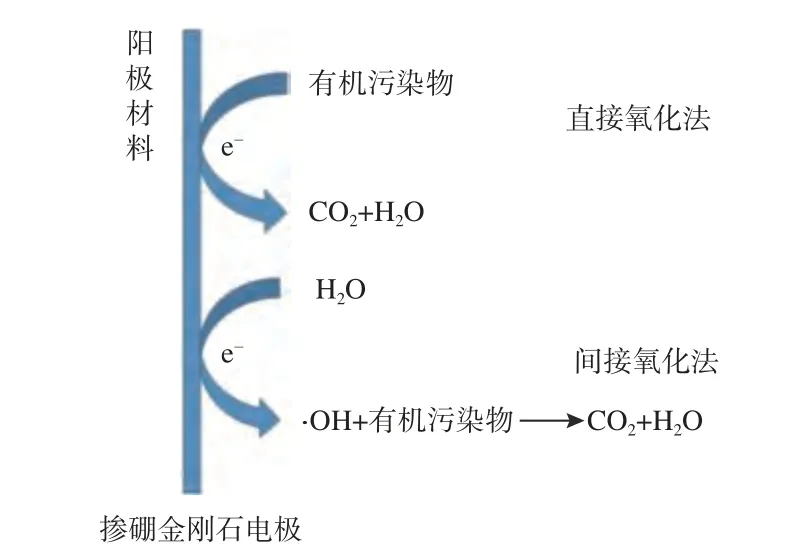
图1 掺硼金刚石污水处理原理图Fig.1 Schematic diagram of boron doped diamond sewage treatment
目前,关于BDD 电极在污水处理领域应用的研究很多,但其工业化应用仍存在巨大的挑战。因此,介绍BDD 的制备方法,对比分析不同制备方法的优缺点,探讨BDD 电极在污水处理中的工业化应用前景[11-12]。
1 掺硼金刚石电极的制备方法
1.1 高温高压法
高温高压法(high temperature high pressure,HPHT)是一种常用的人造金刚石合成方法。将石墨碳源以及触媒按比例进行混合后,经过高温高压处理即可得到金刚石。在此基础上,通过对石墨碳源和触媒合金进行渗硼处理或是直接将硼粉与石墨碳源以及触媒进行机械混合的方式,即可制备出BDD 粉体。SHAKHOV等[13]将纳米金刚石、季戊四醇以及无定形硼粉作为原料,在7 GPa、1 230 ℃的条件下,保温10 s 制备得到纳米BDD 粉体。DUBROVINSKAIA 等[14]将B13C2和石墨作为原料在20 GPa、2 426 ℃和无金属触媒参与的条件下,成功制备出BDD 块体。ZHANG 等[15]使用BDD 微粉,以Al-B-C 作为烧结助剂,在1 450 ℃、5 GPa 的条件下,成功制备出BDD 块体电极,并对亚甲基蓝模拟的印染污水进行了电化学降解试验,脱色效果高达97%,表现出了优异的降解性能。然而,使用高温高压法制备BDD 时,金刚石颗粒通常需要在金属溶剂的环境下析出,导致所制备得到的金刚石往往以微粉的形式存在,需进一步烧结成形才能作为电极材料使用。因此,关于高温高压法制备BDD 电极的报道相对较少。
1.2 化学气相沉积法
化学气相沉积法(chemical vapor deposition,CVD)是将CH4和H2转变为含碳基团以及原子态氢,使其在基底材料上经过多次的吸附、解析等过程最终形成金刚石薄膜。在使用化学气相沉积制备金刚石膜的过程中,将气态硼源作为原料气体中或是在原料气体中引入挥发性的液态、固态硼源,从而实现硼元素的直接掺杂,直接在基底上形成BDD 薄膜。化学气相沉积法所制备得到的BDD 膜性能稳定,硼原子的掺杂浓度可控。同时,化学气相沉积技术所制备得到的BDD 膜可直接作为膜电极使用。ZHU 等[16]采用CVD 法制备得到BDD 膜电极,对纺织污水进行降解,结果表明经过3 h的降解处理,污水的颜色去除率可到100%。
常见的化学气相沉积法包括热丝化学气相沉积法
(hot filament chemical vapor deposition technology,HFCVD)以及微波等离子体化学气相沉积法(microwave plasma chemical vapor deposition,MPCVD)。HFCVD 是在惰性气体的保护作用下,通过加热灯丝,在高温灯丝的作用下,促使CH4和H2转变为含碳基团以及原子态氢,同时以辛硼烷或乙硼烷等气态硼化物作为硼源,最终在基底材料上得到BDD 膜。但由于气态硼源往往具有毒性,可以通过采用硼酸三甲酯、硼酸三乙酯等液态硼源或三氧化二硼、单质硼等固态硼源进行替代。HFCVD 具有操作方便、设备简单等优点,适用于大尺寸BDD 膜电极的制备。但是由于灯丝温度较高,基底材料所处的温度场分布不均匀,靠近灯丝的位置温度更高,沉积速度更快,而远离灯丝的位置温度较低,沉积速度较慢,最终制备得到的膜电极厚度不均。此外,采用的灯丝材料受热分解会使BDD 膜受到污染。而MPCVD 则是通过微波能量将气体原料激发为等离子体,从而沉积在基底材料上形成BDD 膜。采用MPCVD 制备得到的BDD 膜纯度高,性能优异。但是MPCVD 设备价格高昂,导致其所制备的BDD 膜电极成本也相对较高,MPCVD 多用于实验室合成BDD 电极。
因CVD 法制备得到的BDD 膜电极需要沉积在基底材料上,基底材料的选择同样会影响BDD 膜电极的性能。在选取基底材料时,选取热膨胀系数与金刚石相近的材料可以避免沉积后的金刚石膜出现龟裂或剥离等现象。此外,基底材料表面应能形成碳化物。表面碳化物的形成能够提高金刚石膜与基底材料之间的结合力,确保膜电极在使用时不会脱落,延长其使用寿命。常用的基底材料包括Ti、Ta、Si 等材料,Ti、Ta、Si 都可以与碳反应生成碳化物。Ti、Ta、Si 材料的热膨胀系数以及其碳化物的热膨胀系数如表1所示[17]。Si 具有与金刚石最为接近的热膨胀系数,但是由于Si基底不导电,以单晶Si 为基底材料会使BDD 膜电极的导电性受到影响。同时,Si 是典型的脆性材料,以其作为基底会导致BDD 膜电极具有较差的力学性能。Ta作为金属材料,具有导电性好和强度高等特点,但Ta的价格昂贵,限制了其作为基底材料的应用。金属Ti是比强度(强度与密度的比值)最高的材料,其密度仅为4.5 g/cm³。以Ti 为基底的BDD 膜电极,不仅导电性能好,同时具有优异的力学性能以及轻质化等特点[18],此外,金属Ti 价格也低于Ta 的。因此,对于BDD 膜电极而言,金属Ti 是最具应用前景的基底材料。

表1 常用基底材料及其热膨胀系数[17]Tab.1 Common base material and its coefficient of thermal expansion[17]
CVD 法是目前最为常用的制备BDD 电极的方法。关于CVD 法制备BDD 膜电极的研究也相对成熟。但目前CVD 法制备BDD 膜电极仍面临生产效率低、设备成本高等问题。同时,BDD 电极的稳定性和可靠性也同样重要。良好的制备工艺能够保证BDD 膜电极在使用时不会出现剥离失效等现象,提高电极的稳定性与可靠性。因此,探究更为优化的BDD 膜电极生产工艺,降低电极生产成本,将有助于促进BDD 膜电极的商业化应用。
2 高比表面积的掺硼金刚石电极的制备
现有的2D-BDD 电极具有活性面积小、表面利用率低、传质速率低等缺点,限制了其降解效率,难以发挥BDD 高效化处理的优势,而制备具有高比表面积的BDD 电极可以有效解决这一问题。目前,提高比表面积的途径有2 种:一种是自下而上的设计方式,即通过改变基底材料形貌来获取具有特殊结构的电极材料,典型的有模板法;另一种则是自上而下的修饰方式,即通过对样品进行表面处理的方式,使得电极材料具有特殊形貌,从而达到提高比表面积的目的,以期提高电极的整体电化学性能,典型的有表面刻蚀法。
2.1 模板法
模板法是选用具有特定形貌的基底材料,利用基底材料的表面形貌,制备具有高反应活性面积的BDD电极材料的方法。模板法的关键问题在于选择合适的基底材料。MEI 等[19]使用泡沫钛为基底材料,制备出了具有连通大孔径的三维掺硼金刚石(three dimensional boron doped diamond,3D-BDD)电极,不同倍数下3D-BDD 电极内部结构SEM 图像,如图2所示。

图2 不同放大倍数的3D-BDD 电极内部结构SEM 图像[19]Fig.2 The SEM images of internal pores at different magnifications of 3D-BDD electrode [19]
与相同尺寸的平板电极相比,3D-BDD 电极的反应活性面积提升了20 倍,对活性蓝(reactive blue 19)的降解效率提高了350 倍。SUO 等[20]将孔隙率为80%的泡沫镍作为基底,制备出了具有大孔径、高孔隙率的BDD泡沫电极材料,结果发现:随着比表面积的增加,起始电位和极限扩散电流密度均得到增加,并且BDD 的氧还原活性与比表面积大小成正比。HE 等[21]使用网状钛金属为基底材料,制备出了网状BDD 电极,发现:更高的表面积、传质速率和疏水表面赋予BDD 电极优异的电化学氧化能力。选择具有连通大孔径的泡沫金属或是网状金属材料作为基底材料,不但能够提高电极材料的反应活性面积,而且连通孔径的结构会对水体的流动产生一定的影响。当含有污染物的水体流经电极的孔洞时,羟基自由基与污水进行充分反应。与二维平板电极相比,具有三维孔径结构的电极极大地改善了羟基自由基的利用率。但是,这些研究者均使用金属作为基底材料,根据CHAPLIN 等[22]的研究,金属材料与BDD 薄膜的热膨胀系数差距较大,会导致基底材料与薄膜分离,进而导致复合电极材料失效,所以匹配的热膨胀系数和比表面积较大的基底材料是进一步开发自下而上的BDD 电极制备方法的关键所在。
为解决这一问题,PETRÁK 等[23]通过旋涂法制备SiO2纤维基底,并在其表面沉积BDD,制备出了多孔BDD 电极。图3 为旋涂法的流程,流程如下:(1)在硅基片基底上旋涂纳米金刚石颗粒作为种子层;(2)使用MPCVD 反应器沉积BDD 薄膜;(3)由2种旋涂方式制备得到模板(图3a 展示了在介质中旋涂纤维来制备SiO2纤维基底,图3b 则展示了以糊剂刮刀涂覆来制备SiO2纤维基底);(4)在模板上沉积BDD;(5)通过HF 去除SiO2纤维,增加表面积。
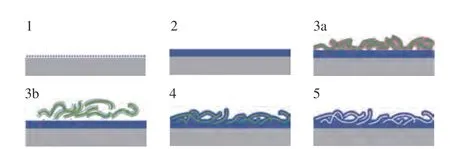
图3 基于旋涂法的多孔BDD 合成的策略[23]Fig.3 Strategy of porous BDD synthesis by spin-coating method[23]
相比于选区具有特定形貌的基底材料,旋涂法简单有效,易于操作,极大地降低了基底材料的制备难度和制备成本。而且,SiO2纤维基底与BDD 的热膨胀系数较为接近,可以有效避免由于热膨胀系数不一致而导致的膜电极与基底材料之间的分离,为3D-BDD 电极材料的大规模商业化应用提供了一种全新的思路。但是,相对于金属基底的BDD 材料,使用SiO2纤维基底制备的BDD 复合电极材料的导电率和机械稳定性较低。
除了选用具有特定相貌的基底材料外,研究者们还通过改变基底材料的形貌,实现了对BDD 电极材料的形貌设计。LEE 等[24]采用金属催化硅刻蚀工艺和静电纳米金刚石播种法,在硅基底上构建纳米线形貌,从而制备出了BDD 纳米线电极,如图4所示。具有纳米线结构的电极材料的反应活性面积提高了3 倍,由此生成大量的羟基自由基,对甲醛和苯酚的降解效率得到大幅提高。同时,其团队还以氧化钨纳米棒为基底,制备出了具有中空结构的BDD 纳米棒电极材料[25],反应活性面积达到相同尺寸平板电极的15 倍。

图4 BDD 纳米线电极的制备工艺示意图[24]Fig.4 Schematic of fabrication process for B-doped diamond nanowire electrode[24]
图5 为BDG/BDD 和BDG/NBDD/TiO2电极的制备示意图。YAN 等[26]通过电化学阳极氧化法在Ti 基底上制备TiO2纳米管阵列,以此作为基底材料,得到纳米晶BDD 电极,并在电极表面负载硼掺杂石墨烯(boron doped graphene,BDG),从而制备出了BDG/NBDD/TiO2纳米阵列电极材料。在保证其电学性能的前提下,BDG/NBDD/TiO2复合电极表面离子迁移速率得到提高,其电化学性能也得到了显著改善。

图5 BDG/BDD 和BDG/NBDD/TiO2 电极的制备示意图[26]Fig.5 Schematic illustration of fabrication of the BDG/BDD and BDG/NBDD/TiO2 electrode[26]
与传统的平板电极相比,模板法增大了BDD 电极的反应活性面积。随着反应活性面积的增大,BDD 电极能够产生的羟基自由基也随之增多,提高了电极的降解效率。同时,根据实际需求,可以选择合适尺寸和形状的模板材料,也可以对模板材料进行相应的结构设计,这为具有特殊结构的BDD 电极材料的制备提供了一种行之有效的解决方案。然而,出于成本、使用寿命、机械稳定性、导电性等各种原因,合适的基底材料仍是BDD 电极的规模化应用的制约因素之一。
2.2 表面刻蚀
表面刻蚀也是一种增大BDD 电极比表面积的方法。常见的刻蚀方法包括氢气等离子体刻蚀和高温刻蚀。在BDD 表面,LI 等[27]采用磁控溅射在BDD 表面溅射一层金属镍(Ni)。金属Ni 具有极高的碳溶解度,能够促进金刚石表面C 原子与H2之间发生反应,生成CH4。利用金属Ni 作为催化剂,采用H2/Ar 混合气体对BDD/Ta 的表面进行刻蚀,制备出了具有多孔结构的BDD 膜电极,增大了电极的反应活性面积,通过电芬顿法实现了对亚甲基蓝的快速降解。图6 为制备多孔BDD/Ta 薄膜的示意图[27],图7 为不同刻蚀时间下Ni/BDD 薄膜的SEM 图像[27]。在800 ℃的温度下,MIAO等[28]基于硼金刚石的热失重原则制备了Si/BDD 电极,结果发现:其电化学活性反应面积增大至初始的3.9 倍,对盐酸四环素的降解效率提升至初始的1.73 倍,TOC移除率增加至1.74 倍。
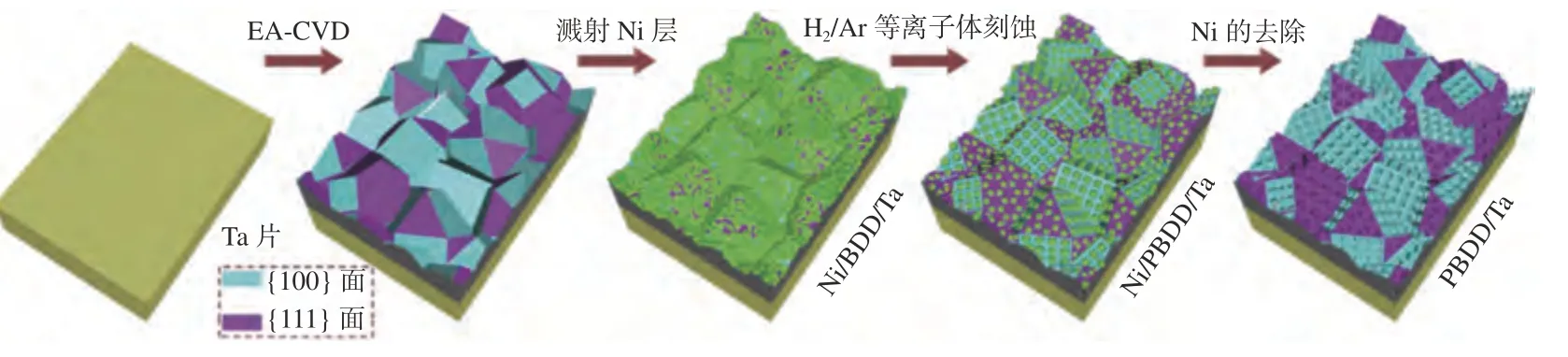
图6 制备多孔BDD/Ta 薄膜的示意图[27]Fig.6 Schematic diagram depicting the preparation of a porous BDD/Ta films[27]

图7 不同刻蚀时间下Ni/BDD 薄膜的SEM 图像[27]Fig.7 SEM images of Ni/BDD films with different etching times[27]
3 表面修饰处理制备掺硼金刚石电极
除了通过增大BDD 电极的比表面积外,研究人员还通过对电极材料进行表面修饰来提高电极的电化学氧化能力。常用的方法主要包括2 种:(1)通过在BDD 膜电极表面负载过渡金属氧化物的方式构建复合电极。常用的过渡金属氧化物包括PdO2、SnO2、MnO2等。这类金属氧化物具有析氧过电位高、催化活性较强等特点。在通电时,BDD 与过渡金属氧化物均会产生羟基自由基,从而实现降解效率的提升。但过渡金属氧化物的引入会造成复合电极导电性降低,造成一部分电流损耗。(2)通过在BDD 电极表面构建p-n结结构来提高电极性能。通常以BDD 膜电极作为p型半导体,TiO2作为n 型半导体材料。由于TiO2还具有光催化特性,TiO2/BDD 复合电极往往具有光电协同特性,能够更好地对污水实现降解。
ZHUO 等[29]将PdO2和SnO2前驱体溶液涂覆在BDD 电极表面,制备出了纳米SnO2修饰的BDD 复合电极材料,以及纳米PbO2修饰的BDD 复合电极。图8为BDD 复合电极的SEM 图[29]。如图8所示:将F 原子引入SnO2晶格中,可有效减小SnO2粒径,与BDD 电极相比,BDD/SnO2-F 的析氧过电位增加了0.13 V。同时,在氯化聚氟醚磺酸盐(F-53B)的降解实验中,BDD/SnO2-F 电极的降解速率比BDD 电极的提高了15.07%,明显提升了降解效率。

图8 BDD 复合电极的SEM 图[29]Fig.8 SEM of BDD composite electrode[29]
席耀辉等[30]通过水热法在BDD 表面负载棒状纳米TiO2,制备出了具有p-n 结效应的复合电极。图9为n-TiO2/p-BDD 异质结和光生载流子的转移过程的示意能带图[30],其中:vac 表示真空度,χ表示电子亲和势,EF表示费米能级,VB 表示价带,CB 表示导带,h 为普朗克常量,v为光的频率。从图9 中可以看出:在紫外光的照射下,TiO2半导体可以产生光生载流子(电子和空穴),p-BDD 导带中的电子向n-TiO2导带中转移,n-TiO2价带中的空穴向p-BDD 价带转移,在空间电荷区内部的静电势有利于光生载流子的分离,从而使电子-空穴复合率显著降低,而与电子、空穴相关的氧化还原反应过程会持续发生,促进有机污染物在电极表面的高效降解。另外,金刚石和TiO2的禁带宽度分别达到5.47 eV 和0.50 eV,电子亲和势分别达到3.2~3.4 eV 和4.3 eV。在n-TiO2/p-BDD异质结结构中,基底材料禁带宽度大,电子亲和势小的特性可以促进电子从p-BDD 的导带向n-TiO2导带运动,进而提高TiO2的光催化活性。同时,使用TiO2/BDD 复合电极对亚甲基蓝模拟的染料污水进行了降解试验,在通电和光照作用下,30 min 即可达到100%的降解效果。与BDD 电极相比,降解效率提高20%。

图9 n-TiO2/p-BDD 异质结和光生载流子的转移过程的示意能带图[30]Fig.9 Schematic band diagram of n-TiO2/p-BDD heterojunction and the transfer processes of photo generated carriers[30]
在TiO2/BDD 复合电极的基础上,马玉祥[10]借鉴光催化领域重用的电子传输Z 型机制,构建TiO2/Au/BDD体系,其电子转移方式如图10所示。在TiO2/Au/BDD复合电极中,Au 作为电子传输媒介,使得TiO2与BDD之间的接触电阻大大降低,形成欧姆接触。TiO2的导带(CB)中的电子(e-)通过Au 层可以直接与BDD的价带(VB)中的空穴(h+)复合。TiO2/Au/BDD 的这种三元结构有利于TiO2和BDD 内部的e-、h+分离和传输,减少内部载流子的复合机会。BDD 内CB 上的e-和TiO2内VB 上的h+被更多地保留下来,用于氧化还原反应中,从而电极的催化性能得到极大提高。因此,与其他电极相比,TiO2/Au/BDD-30 电极具有更好的催化效果。在对垃圾渗滤液的处理试验中,90 min 内,可使垃圾滤液的化学需氧量(chemical oxygen demand,COD)值下降46.61%。
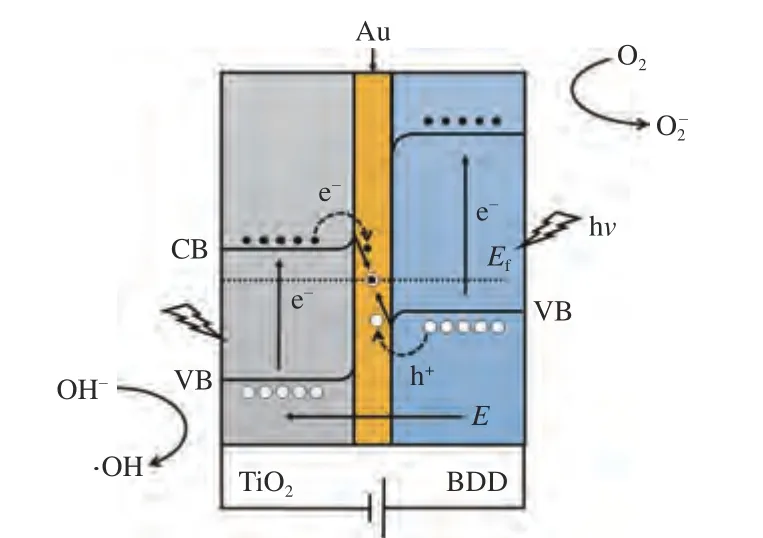
图10 TiO2/Au/BDD 电极Z 型机制载流子传输示意图[10]Fig.10 The carrier transport diagram of TiO2/Au/BDD electrode Z-scheme mechanism[10]
使用表面修饰的方法改进BDD 电极的电催化性能,需要重点考虑表面修饰材料与BDD 电极之间的结合强度,在提高BDD 与复合材料的电子转移速率的同时,保证在污水处理过程中复合材料不存在失效的风险。相比于使用PdO2和SnO2等析氧过电位高的材料,TiO2与BDD 的复合会降低复合电极的电化学势窗和析氧过电位,p-n 异质结的形成会进一步提高体系的反应速率,同时使复合电极拥有光催化氧化的能力。
4 总结与展望
BDD 电极作为一种新型的污水处理电极,具有极为广阔的应用前景。然而,BDD 电极的实际应用需要建立在具有低成本、良好稳定性等的BDD 电极的制备的基础之上。关于BDD 电极的制备和开发,可以从以下几方面进行:
(1)化学气相沉积法作为当前制备高比表面积的BDD 电极的主要制备方法,仍存在工艺成本高,生产效率低等缺点。因此,需要进一步研究和优化高比表面积的BDD 的合成条件,探寻更佳的工艺设计。此外,随着制备工艺的进步,也需要积极探寻其他制备方法和基底材料的可能性。
(2)探究BDD 复合电极中电子传输机制,依据p-n结构、Z 型电子传输机制等理论设计更优的BDD 复合电极结构,对BDD 的表面进行更有效的修饰改性。此外,通过在电极表面负载具有光催化性能的其他物质,制备具有光电协同催化作用的复合电极,同样也是极具前景的研究方向。
(3)开发BDD 电极与生物法、物理法、化学法等方式的联用处理方法。针对不同污水处理的应用场景,采用定制的方式设计BDD 电极材料,均衡成本与效率之间关系,使BDD 电极满足工业化大规模应用条件。
