纳武利尤单抗相关肾脏毒性反应文献病例分析
2022-11-03夏小玉迟成丽王永振
夏小玉,迟成丽,王永振
0 引言
纳武利尤单抗(Nivolumab,Nivo)是一种抗程序性细胞死亡-1(Programmed cell death 1,PD-1)抗体,可作用于多种恶性肿瘤的免疫检查点抑制剂(Immune check point inhibitors,ICIs)。其独有的副作用即免疫相关不良事件(Immune-related adverse events,irAEs)可影响任何器官或系统,包括肾脏[1]。本文检索国内外Nivo肾脏毒性反应的相关病例报道,梳理其发生特点及处置方案,为临床识别、降低该不良反应(Adverse drug reaction,ADR)的发生风险及安全用药提供参考。
1 资料与方法
1.1 资料来源 收集中国知网、维普、万方和PubMed数据库中相关病例报道,截至2021年11月。英文检索以“nivolumab”、“kidney injury”、“nephrotoxicity”、“renal disorder”等为关键词组合,中文以“纳武利尤单抗”、“不良反应”、“肾损伤”、“肾毒性”、“肾炎”等为关键词进行组合检索。纳入标准:①文献类型为病例报告;②肾脏毒性反应诊断明确,且被判定与Nivo相关;③患者基本信息、临床表现、实验室检查及治疗与转归等资料相对完整;④中文及英文语种发表。排除标准:①综述、临床试验等非病例报道类文献;②重复发表文献。
1.2 方法 利用Excel统计患者性别、年龄、原发疾病、Nivo用药情况、是否合并应用质子泵抑制剂(Proton pump inhibitor,PPI)/非甾体抗炎药(Nonsteroidal anti-inflammatory drug,NSAID)、肾毒性发生时间、临床表现、实验室检查、治疗与转归等信息。
2 结果
2.1 文献收集和患者一般资料 共纳入42篇文献,均为外文文献;患者53例,男35例(66%),女18例(34%),年龄19~79岁,中位年龄68岁。原患疾病以肺癌(19例,36%)与恶性黑色素瘤(19例,36%)为主。大多数患者的基线肾功能正常,血清肌酐中位数为0.91 mg/dl(0.5~1.66 mg/dl)。28例(53%)患者有同时应用PPI/NSAID用药史。既往有高血压病史14例,慢性肾脏疾病史5例。见表1。

表1 患者基本情况
2.2 用药情况 Nivo 单药治疗者39例,其中33例用药频率为1次/2周,2例为1次/3周,4例用药频次不详。Nivo联合伊匹单抗(Ipilimumab,Ipi)治疗者9例,6例用药频率为1次/3周,2例为1次/2周,1例为4次/3周。Ipi/Ipi+Nivo与Nivo序贯治疗4例,其中先Ipi+Nivo 2次,后Nivo治疗1例,用药频次为先1次/3周后1次/2周;先Ipi+Nivo 1次,2个月后Nivo治疗1例,单药治疗时用药频次为1次/2周;Ipi停用8周后开始Nivo治疗1例,用药频次为1次/2周;先Ipi 3个月,停用4个月后Nivo治疗1例,其用药频次不详。Nivo联合贝伐珠单抗治疗者1例,用药频率为1次/2周。Nivo单次剂量为0.1~10 mg/kg或170~480 mg。
2.3 发生时间和临床表现 发生时间最短为用药后4 d,最长为用药后24个月,中位发生时间为用药后3.5个月。临床表现以急性肾损伤(Acute kidney injury,AKI)49例(92%)为主,其次为肾病综合征(Nephrotic syndrome,NS)。见表1。
2.4 肾脏毒性反应发生情况
2.4.1 实验室检查 患者血清肌酐(Serum creatinine,SCr)均升高,中位SCr峰值为3.48 mg/dl。40例(75%)患者进行了尿常规检测,最常见为蛋白尿(27例,51%),其次为脓尿(16例,30%),进行尿培养结果多为阴性(15/16)。见表2。
2.4.2 诊断/活检结果 急性肾小管间质性肾炎(Acute tubulointerstitial nephritis,ATIN)是肾脏毒性反应最为常见的病理表现,其次为肾小球病变。诊断/活检证实,66%(35/53)的患者有ATIN表现,其中单纯ATIN 29例,3例同时伴随急性肾小管损伤(Acute tubular injury,ATI),3例同时伴随肾小球病变。11%(6/53)出现ATI,其中单纯ATI 1例,ATIN+ATI 3例,2例同时伴随肾小球病变。经活检证实38%(20/53)出现肾小球病变,其中单纯肾小球病变15例,5例同时伴随肾小管病变。常见的肾小球病变类型为肾血管炎(8/20)和免疫球蛋白A(Immunoglobulin A,IgA)肾病(6/20)。见表2。
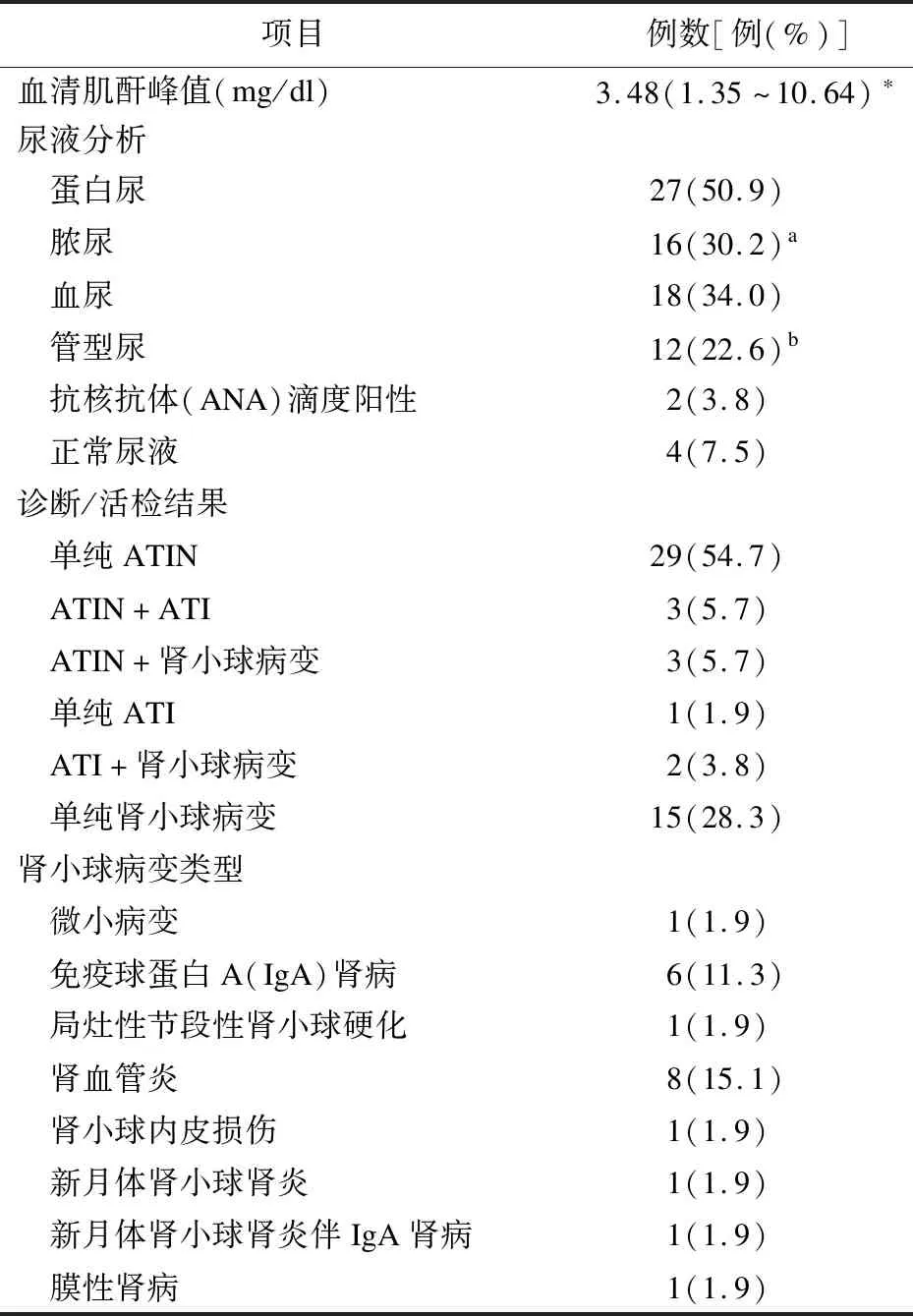
表2 患者肾脏毒性反应临床特征
2.4.3 治疗和转归 发生ADR后,除1例外,大多数患者(52例,98%)均停止Nivo治疗。8例(15%)患者仅停用Nivo治疗,45例(85%)最初接受糖皮质激素(Glucocorticoid,GC)治疗,其中1例继续Nivo+GC治疗,44例停用Nivo+GC治疗。16例患者对GC反应不敏感,最终患者接受GC+利尿剂治疗1例,GC+免疫抑制剂治疗6例,GC+血液透析治疗6例,GC+免疫抑制剂+血液透析治疗3例,即共有9例患者还同时使用霉酚酸酯(Mycophenolate mofetil,MMF)和(或)利妥昔单抗及抗肿瘤坏死因子α(TNF-α)进行免疫抑制剂治疗,9例患者接受血液透析治疗。经治疗肾功能好转或治愈51例(96%),肾功能稳定但无改善1例(2%),预后不详1例(2%),其中肾功能稳定但无改善的患者选择的治疗方案是停用Nivo+GC+利尿剂。3例(6%)患者进展为终末期肾病,需要长期血液透析治疗。10例(19%)患者重启ICIs治疗,其中8例再次给予Nivo治疗,2例患者给予帕博利珠单抗治疗,4例再次出现肾脏ADR(40%)。见表3。

表3 患者肾脏毒性反应的治疗及预后
3 讨论
3.1 Nivo肾脏毒性反应的发生率 ICIs相关肾脏irAEs中,AKI最为常见[1]。3 695例接受ICIs治疗患者的Ⅱ期和Ⅲ期临床试验显示,AKI的总发生率为2.2%,Ipi+Nivo联合治疗组、Nivo单药治疗组AKI发生率分别为4.9%、1.9%[2]。Ipi和Nivo序贯给药也使肾脏毒性增加至5.1%[3]。现有数据可能低估了由于误诊或报告不足而导致的实际发病率[4],肾脏irAEs可能比既往报道中更常见。
本研究结果中,53例发生Nivo相关肾脏irAEs患者中,单用者占74%(39/53),联合(序贯)应用Nivo治疗者占26%(14/53),单药发生率高于联用(序贯),考虑与纳入本研究中联用(序贯)治疗的例数较少、ADR个案报道也较少有关。
3.2 Nivo肾脏毒性反应与患者性别和年龄的关系及发生时间 一项回顾性研究发现,1 444例ICIs肾脏ADR报告中,男性、65岁以上人群更多见[5]。肾脏ADR中位发生时间约为14周[6],其可以在治疗后的任何时间发生,从第一次给药后数天到最后一次给药后的10周以上[7]。本研究结果显示,患者中位年龄68岁,男与女性别比为1.94∶1;肾脏ADR最早发生于首次用药后4 d,最晚出现于用药后2年,中位发生时间为用药后3.5个月,与上述研究结果基本一致。男性多于女性,这可能与男性中某些皮肤癌患病率增加有关[8]。因此,男性且年龄约为68岁的患者在Nivo用药3.5个月内应加强监测。
3.3 Nivo肾脏毒性反应的影响因素 Ipi是细胞毒性T淋巴细胞相关抗原4(Cytotoxic T lymphocyte-associated antigen-4,CTLA-4)检查点抑制剂。低基线估计肾小球滤过率(Estimated glomerular filtration rate,eGFR)、伴随PPI的使用和联合抗CTLA-4和抗PD-1/其配体PD-L1药物免疫治疗已被Cortazar等确认为ICIs相关AKI的独立危险因素[7]。1 016例应用ICIs的患者中,使用PPI是AKI持续48 h或更长时间的强危险因素[9],其他与ATIN相关的药物,如NSAID等也可能导致ICIs相关ATIN[7,10]。回顾性研究也表明,其他irAEs的发展和既往高血压诊断与AKI风险增加有关[11]。
本文研究显示,53例ADR患者中28例(53%)患者有同时应用PPI/NSAID用药史,既往有高血压病史14例(26%),慢性肾脏疾病史5例(9%),联合(序贯)应用Nivo和Ipi者13例(25%),支持了先前的研究成果。纳入研究的28例患者有同时应用PPI/NSAID用药史,但在Nivo治疗前,患者接受PPI/NSAID治疗期间未出现包括肾损伤在内的重大不良事件。根据国家药物不良反应监测中心“药物与不良反应关联的5标准”判断,肾脏毒性的出现与Nivo的应用有时间关联性,符合该类药物已知的ADR类型,且不能用患者病情进展来解释。停用Nivo并经GC等治疗后,患者多数好转,故判定该肾脏毒性与Nivo相关性大,与PPI/NSAID不太可能是因果关系,但Nivo与PPI/NSAID联用后出现AKI的可能性更大。根据Shirali等[12]的研究,停用PPI/NSAID药物后,患者的ICIs相关AKI有所改善。故建议在临床应用过程中,对这类高危患者应加强肾功能监测,患者应实施健康的饮食和体育活动,必要时应通过药物控制高血压,Nivo治疗前谨慎联用PPI/NSAID,Nivo治疗中应降低药物肾损伤的叠加风险,停用或减少PPI/NSAID,对防治该肾脏毒性ADR有益。
3.4 Nivo肾脏毒性反应的机制 Nivo免疫相关肾脏毒性反应的机制尚不明确,目前认为其发病机制可能是正常组织对T 细胞耐受下降,NSAID、PPI及ICIs增加特异性T细胞活化以及自身抗体产生等[13]。
3.5 Nivo肾脏毒性反应的临床特点及诊断 ICIs所致肾脏毒性的组织病理学特征以ATIN最为常见,但也可能伴有肾小球损伤,有越来越多的病理类型被发现[6]。美国安德森癌症中心回顾性分析了16例ICIs相关AKI患者,14例存在ATIN,9例同时伴有肾小球疾病,包括免疫性肾小球肾炎、IgA肾病、膜性肾病和血栓形成性微血管病等类型[14]。另一项研究也发现,25例接受了肾活检的ICIs相关AKI患者中,ATIN为主要诊断,其他病理表现为IgA肾病、血管炎、ATI及高血压相关改变[15]。多中心研究发现,ICIs相关AKI患者除SCr升高,71%的患者有蛋白尿,约50%的患者有无菌性脓尿和白细胞管型尿,40%的患者有血尿[7]。本研究结果也证实,Nivo所致肾脏毒性反应患者SCr升高,有亚肾病蛋白尿、无菌性脓尿及高倍视野显微镜下可见血尿,与既往研究基本相符。此外,也可出现正常尿液分析,提示尿液分析正常并不能排除肾脏毒性ADR,还应把尿常规及尿沉渣、24 h尿蛋白和SCr相结合作为初筛最重要的指标[13]。因此,临床上要加强患者用药教育,由于Nivo致肾脏毒性ADR的潜伏期较分散,建议在Nivo治疗时,每个周期都应进行监测,在基线和治疗后应进行肾功能评估和尿液分析,在治疗过程中及时进行数据比较,如发现SCr升高,尿常规和尿液分析中出现白细胞或红细胞升高,伴蛋白尿,且尿培养阴性,提示患者可能出现AKI,这有助于早期发现、诊治肾脏毒性ADR。
肾脏活检是诊断ICIs相关肾脏毒性反应的金标准,但美国临床肿瘤学协会和国家综合癌症网络指南建议:如果无法确定AKI的另一种原因,临床医生应直接进行GC治疗,而不需要肾活检,除非存在中/重度危及生命的肾脏irAEs[16-17]。我国也建议在鉴别诊断困难时才考虑肾活检[18]。本研究显示,正电子发射断层显像显示在肾皮质18F-脱氧葡萄糖摄取增加,对确认ICIs诱导的ATIN可能是一个有价值的辅助试验[19]。此外,Isik等[20]研究表明,ICIs诱导AKI患者血清C反应蛋白和尿视黄醇结合蛋白/尿肌酐水平高于非ICIs诱导的AKI患者,提示这两个生物标志物可能有助于鉴别ICIs和引起AKI的其他原因。
3.6 Nivo肾脏毒性反应的治疗与再挑战 ICIs相关肾脏毒性反应的治疗以停止Nivo治疗为主,GC为一线药物,MMF、英夫利西单抗、抗肿瘤坏死因子α抑制剂等为第二线治疗,必要时透析治疗为第三线治疗[18]。本研究中,除2例患者(1例继续Nivo+GC,1例选择停用Nivo+GC+利尿剂)外,治疗方案与指南推荐的治疗方案相符。大多数患者经及时干预,肾功能多数可部分甚至完全恢复[13]。AKI不恢复是死亡率增加的标志[7]。故AKI出现时,早期GC的启动是至关重要的。Cortazar等[7]研究138例与ICIs相关的AKI患者,119例使用GC,87%的患者部分或完全康复。本研究中,85%的患者应用GC,96%的患者经治疗肾功能好转或治愈,与上述文献结果相一致。Lee等[21]研究证实,ICIs所致AKI患者经3周强的松治疗并停用其他与ATIN相关的药物(PPI、NSAID等)后,肾功能恢复良好,与接受强的松治疗时间较长(4~6周)的历史对照组相比,差异有统计学意义。因此,及时停用PPI、NSAID等与ATIN相关的药物很重要,如不能停用PPI,可将PPI转换为H2受体阻滞剂[4,19]。越来越多的证据表明,ICIs诱导肾脏毒性反应康复的患者中,ICIs可重启,肾脏毒性反应复发的比例约为25%[10,22]。31例患者再次应用ICIs,39%的患者再次应用同时接受GC治疗,23%再次应用患者出现复发性AKI,早期AKI发作与再次应用之间的潜伏期较短[7]。本研究中,有19%(10/53)的患者重启ICIs治疗,60%(6/10)再次应用成功,40%(4/10)出现肾脏毒性反应复发。故一旦再次应用ICIs,需要密切监测,及时进行干预。在再次应用ICIs时应避免选择ICIs联用方案,并避免PPI的使用[6]。在少数复发或持续性AKI的患者中,英夫利西单抗是一种可能的治疗方案。10例复发性ICIs诱导的AKI患者中,80%的患者在接受英夫利西单抗治疗后取得了持久的完全或部分缓解[23]。
总之,Nivo应用中存在肾脏毒性ADR发生风险,建议临床应知晓、警惕该ADR,加强用药监测,特别是对男性老年患者(低eGFR)、联合使用PPI及Ipi的患者,谨防肾脏毒性ADR的发生。如果确诊,患者应立即停用Nivo,及时开启GC治疗。
