妊娠晚期孕妇生殖道B族链球菌感染对并发胎膜早破与新生儿感染、围生结局影响
2022-11-02王婷婷薛飞扬刘春花
王婷婷 薛飞扬 綦 萍 刘春花
青岛市胶州中心医院(266300)
B族链球菌(GBS)通常情况下可定植于泌尿生殖道、下消化道、上呼吸道等处,并具有条件致病性。孕妇妊娠过程因生理改变会影响生殖道微生态环境,增加GBS感染风险。相关统计表明[1],10%~30%孕妇会感染GBS,其中40%~70%产妇分娩时会感染新生儿,感染GBS新生儿中5%可致死亡。可见,孕妇感染GBS不仅影响妊娠结局,也会增加新生儿不良预后风险。胎膜早破是妊娠晚期常见并发症,其中未足月胎膜早破风险最大,发生率为2%~4%,可导致早产、孕妇及胎儿感染、新生儿死亡等不良妊娠结局[2]。既往研究表明[3],生殖道感染是胎膜早破的危险因素,但生殖道GBS感染与并发胎膜早破是否存在关联尚缺少循证医学证据。此外,目前关于妊娠晚期孕妇生殖道GBS并发胎膜早破对新生儿感染及妊娠结局的研究鲜有报道。鉴于此,本研究分析了胎膜早破孕妇与无胎膜早破孕妇生殖道GBS感染、新生儿感染及围生结局,为临床防治提供参考依据。
1 资料与方法
1.1 临床资料
经院伦理委员会批准,选取2019年1月—2020年6月本院产科收治的单胎妊娠晚期孕妇824例为研究对象,其中胎膜早破孕妇400例为观察组,无胎膜早破孕妇424例为对照组。纳入标准:①单胎活体妊娠,在本院规律产前检查,孕周>35周;②符合胎膜早破临床诊断标准[4];③患者签署知情同意书。排除标准:①严重肝肾功能不全、心肺功能异常、感染性疾病、妊娠期糖尿病、妊娠期高血压、精神疾病等;①合并生殖道其他细菌感染、阴道炎症、性传播疾病等;③近期服用抗生素药物或影响本研究结果的药物;④依从性差,无法配合完成本研究等。
1.2 检测方法
产前检查孕35~42周时采集孕妇生殖道分泌物标本,新生儿出生后采集鼻咽拭子标本。将采集标本接种于无乳链球菌增菌肉汤中,35℃恒温增菌18~24h,转种于5%哥伦比亚绵羊血琼脂平板和无乳链球菌显色平板,35℃孵育18~24h,观察菌落特征,挑选典型菌落与GBS显色平板菌落分纯培养。最后采用全自动微生物分析仪(TEK 2 Compact型,法国梅里埃公司)进行细菌鉴定。
1.3 观察指标
①比较两组孕妇生殖道GBS感染情况;两组分娩新生儿感染GBS情况;②比较观察组GBS阳性孕妇不同胎膜早破时间、不同产程者分娩新生儿感染情况;③分析两组围生结局。
1.4 统计学方法
2 结果
2.1 一般情况
观察组年龄(29.5±6.8)岁(21-39岁),体质指数(BMI)(26.6±2.6)kg/m2,产次(0.9±0.3)次;对照组年龄(30.16±7.03)岁(20~40岁),BMI(26.8±2.7)kg/m2,产次(0.9±0.4)次。两组基线资料无差异(P>0.05)。
2.2 GBS感染情况
观察组GBS检出率(31.5%,126/400)高于对照组(10.4%,44/424)(χ2=56.082,P=0.000);观察组分娩新生儿GBS感染率(19.0%,76/400)高于对照组(5.2%,22/424)(χ2=37.468,P=0.000)。
2.3 观察组GBS阳性孕妇新生儿感染情况
观察组GBS阳性孕妇126例中,胎膜早破时间≤24h有87例,其分娩新生儿GBS感染率为51.7%(45/87);胎膜早破时间>24h有39例,其分娩新生儿GBS感染率为79.5%(31/39)。产程时间≤24h有92例,其分娩新生儿GBS感染率为50.0%(46/92);产程时间>24h有34例孕妇,其分娩新生儿GBS感染率为88.2%(30/34),不同胎膜早破时间、不同产程时间孕妇分娩的新生儿GBS感染率均有差异(P<0.05)。
2.4 围生结局情况
观察组发生宫内感染、产褥感染、胎儿窘迫、早产、羊水污染等不良妊娠结局高于对照组,其分娩新生儿发生窒息、肺炎、低体重等不良新生儿结局高于对照组(P<0.05);两组孕妇分娩新生儿败血症、黄疸等不良新生儿结局发生率无差异(P>0.05)。见表1。
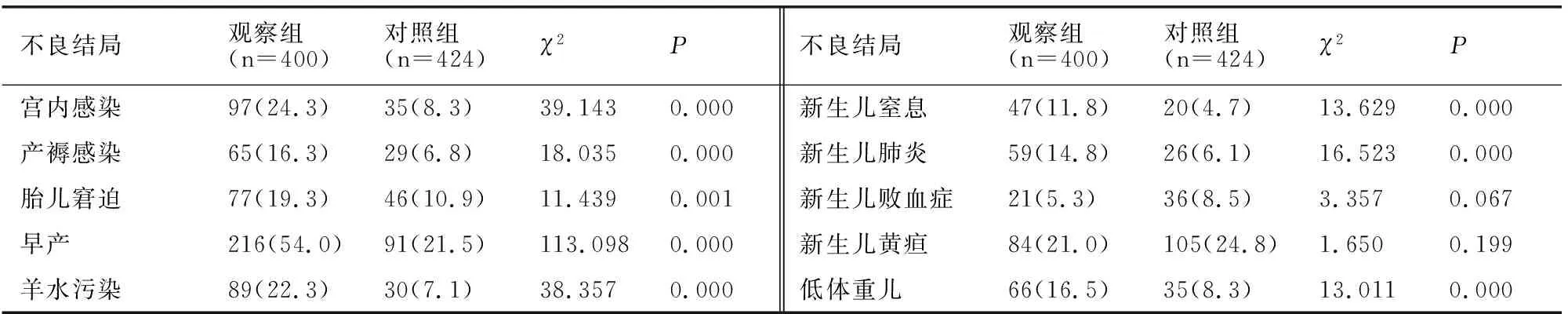
表1 两组孕妇及新生儿不良结局情况比较[例(%)]
3 讨论
大量临床研究已证实GBS是围生期感染的常见病原体,阳性检出率与地域、种族相关[6]。陈小丽[7]、方寅飞[8]等报道国内孕妇GBS阳性检出率在10%~30%。本研究检出率为10.4%,与相关报道较一致。
胎膜早破是妊娠期晚期常见并发症之一。既往研究表明[9],导致胎膜早破的原因包括生殖道感染、医源性创伤、胎膜发育异常等,其中生殖道感染是胎膜早破的重要危险因素。无乳链球菌属于β类溶血性链球菌,对绒毛膜的亲嗜性较好,长期生殖道内定植的GBS可在特定条件下通过产生磷酸酯酶A2而水解细胞膜,从而上行感染至胎膜,造成胎膜早破[10]。本研究中有胎膜早破的观察组GBS检出率高于无胎膜早破的对照组,且略高于文献[11]所报道结果。可能与入组样本筛查方式、时间及地区限制有关。提示,妊娠晚期孕妇生殖道GBS感染与胎膜早破存在密切关联。
由于GBS具有垂直感染风险,因此新生儿感染GBS是常见不良结局。临床报道30%~70%的GBS阳性孕妇分娩过程中可导致新生儿感染[12-13]。此外,有研究证实胎膜早破会导致宫内感染、羊水污染,从而增加新生儿GBS感染风险。本研究结果显示,有胎膜早破孕妇分娩新生儿GBS感染率高于无胎膜早破孕妇分娩的新生儿,提示妊娠晚期孕妇生殖道GBS阳性并发胎膜早破将增加新生儿感染GBS概率。比较126例GBS阳性孕妇分娩结果显示,胎膜早破时间>24h、产程时间>24h均将增加分娩新生儿感染GBS风险。与文献[14]报道结果较一致。分析认为:对于GBS孕妇而言,垂直传播风险较大,而胎膜早破时间、产程时间过长均会增加垂直传播几率,从而导致新生儿感染GBS概率大大提高。因此,对出现胎膜早破孕妇及时采取必要措施,缩短胎膜早破及产程时间有助于降低新生儿垂直感染GBS风险。
本研究结果,有胎膜早破孕妇发生宫内感染、产褥感染、胎儿窘迫、早产、羊水污染等不良妊娠结局概率高于无胎膜早破孕妇,且孕妇分娩新生儿不良新生儿结局概率高于对照组。提示妊娠晚期孕妇生殖道GBS感染并发胎膜早破将增加不良妊娠结局风险,同时也会导致不良新生儿结局。GBS上行感染至宫内胎膜,炎性细胞不断侵入胎膜使其张力减少,从而导致胎膜早破。此外,通过胎膜进入宫腔内的病原菌不仅直接导致羊水污染,也会造成持续的宫内感染,影响胎儿正常生长发育[15]。由此可见,妊娠晚期孕妇生殖道GBS感染不仅与胎膜早破密切相关,同时也会增加不良妊娠结局和新生儿不良预后风险。
综上所述,妊娠晚期孕妇生殖道GBS感染与胎膜早破存在密切关联,会增加新生儿感染及不良妊娠结局风险,临床上应加以重视并早期干预及治疗。
