肠梗阻手术联合肠内营养对十二指肠先天性梗阻新生儿肠功能和营养状态的影响*
2022-11-02肖田刘俊罗艳梅向旋杨星海
肖田,刘俊,罗艳梅,向旋,杨星海
(湖北省妇幼保健院 小儿外科,湖北 武汉 430070)
先天性十二指肠梗阻属于先天性消化道畸形中最常见的类型,是新生儿常见外科急腹症[1]。手术是治疗先天性十二指肠梗阻的唯一方法,目的在于通过手术解除梗阻,重建与生理结构相符的消化道[2-3]。然而有研究显示,肠梗阻手术后禁食易导致机体肠绒毛萎缩,肠上皮细胞凋亡,增加肠上皮细胞与机体蛋白连接,加大细菌移位风险[4]。有效的营养支持可改善危重症、消化道疾病患儿自然病程,降低并发症风险,临床常用营养支持方案包括胃肠外营养、肠内营养[5]。术中经鼻留置空肠营养管可直接经空肠进行早期肠内营养,逐步应用于新生儿上消化道畸形的营养支持中。本研究通过与肠外营养支持比较,阐述经鼻留置空肠营养管肠内营养支持在十二指肠先天性梗阻新生儿肠梗阻手术中的应用效果,现报道如下。
1 资料与方法
1.1 一般资料
选取2018年11月—2021年12月湖北省妇幼保健院收治的十二指肠先天性梗阻新生儿103 例。将患儿分为观察组和对照组,分别有52 例和51 例。观察组中男性31 例,女性21 例;自然分娩22 例,剖宫产30 例;早产16 例,足月36 例;胎龄32~42 周,平均(38.06±1.17)周;出生体重1 696~4 417 g,平均(3 001.88±310.95)g;手术日龄1~5 d,平均(2.64±0.72)d;疾病类型:先天性肠旋转不良28 例,十二指肠闭锁或狭窄12 例,环状胰腺8 例,混合病例4 例。对照组中男性30 例,女性21 例;自然分娩23 例,剖宫产28 例;早产15 例,足月36 例,胎龄33~42 周,平均(38.18±1.28)周;出生体重1 642~4 387 g,平均(3 014.55±301.80)g;手术日龄1~5 d,平均(2.59±0.69)d;疾病类型:先天性肠旋转不良28 例,十二指肠闭锁或狭窄13 例,环状胰腺7 例,混合病例3 例。纳入标准:①先天性十二指肠梗阻新生儿,接受腹腔镜下肠梗阻手术治疗;②术前相关检查完备,腹平片及上消化道碘造影确诊为十二指肠梗阻,胃十二指肠超声明确病因;③经医院伦理委员会批准,患儿家属均知情同意。排除标准:①合并其他严重先天畸形,如复杂先心病、呼吸、神经系统畸形等;②合并先天性遗传代谢性疾病;③合并肿瘤疾病、结核等,术前进行过腹部手术者;④合并严重心肺功能异常;⑤出现休克或/和多器官功能衰竭者;⑥染色体结构或数目存在异常;⑦宫内生长迟缓或过速。两组患儿一般资料比较,差异无统计学意义(P>0.05)。
1.2 方法
1.2.1 手术方法两组患儿均接受腹腔镜下肠梗阻手术,采用三孔法,脐缘左下方做5 mm 切口,置3 mm套管作为目镜通道,左上腹、右中腹取3 mm 切口,置3 mm 套管为操作通道。通过探查结果选择手术方式:①先天性肠旋转不良行腹腔镜下Ladd's 术:抓钳提着肠系膜由左往右侧逆时针复位,至系膜展平,无扭转情况,显露回盲部、升结肠旁侧腹膜。从十二指肠球部向下游离韧带:回盲部与右侧后腹膜间对十二指肠形成压迫的Ladd's 韧带、对十二指肠与近端空肠形成束缚的腹膜索带、致肠系膜根部缩窄的黏连索带,将十二指肠、近端空肠拉直,系膜根部展平。将十二指肠、空肠置于脊柱右侧,结肠置左侧腹腔。②十二指肠狭窄患儿采用十二指肠隔膜纵切横缝手术:充分游离十二指肠梗阻的远近端,分别悬吊,纵向切开肠壁,寻及隔膜并用电钩切除,横向连续缝合肠壁。③环状胰腺患儿采用腹腔镜下十二指肠菱形吻合术:采用腹腔镜下,缝针由左右腋前线肋缘穿刺入腹,缝于梗阻近端扩张肠管前壁,腹壁穿出,腹壁外悬吊十二指肠梗阻近端,固定。近端横形剪开,远端纵向剪开,止血,置入吸痰管至远端,探查梗阻。5-0 可吸收线连续交锁全层内翻缝合后壁、外翻缝合前壁,菱形吻合。④十二指肠隔膜患儿行腹腔镜下切除术:同②方法悬吊十二指肠梗阻近端,梗阻点近远端纵向剪开,挤压胆囊,观察胆汁流出位置确定十二指肠乳头,避开乳头,切除隔膜。5-0 可吸收缝线连续交锁外翻缝合肠壁。对于多发畸形者采取上述联合术式。
1.2.2 营养支持对照组给予肠外营养支持,术后给予静脉营养液支持,胃肠功能恢复后,采用经口喂养。若经口喂养能量不能满足生理需求则根据实际情况继续予以静脉营养支持,喂养达460 J/kg时,停止静脉营养给予。观察组采用经鼻留置空肠营养管肠内营养支持,术中吻合前经鼻置入营养管,置入后间歇泵注葡萄糖,5 mL/次,30 min/次,间隔8 h泵注1 次。试喂过程中患儿无呕吐、腹胀现象后根据实际耐受情况给予深度水解奶粉,输注量:奶量10~15 mL/(kg·d),持续0.5~1.0 h,间隔6 h/次。持续输注≥3 d 后,若无喂养不耐受,酌情加大奶量,当1 h 内奶量输注达460 J/kg 时,同对照组给予常规肠外营养。
1.3 观察指标
1.3.1 术后肠功能恢复情况比较两组首次排便时间、完全肠内营养时间、喂养达到40 mL/3 h 时间、住院时间。
1.3.2 体格检查情况分别于术前及术后7 d 进行体格检查,体重测量使用婴儿电子台秤;身高采用新生儿专用身长测量尺;头围采用新生儿专用头围测量尺,经枕骨粗隆、双侧眉弓最高点绕头1 周。
1.3.3 血液指标于术前及术后7 d 取患儿股静脉血6 mL,其中3 mL 在常温条件下3 000r/min 离心15 min,取血清。营养指标:血清前白蛋白(Prealbumin,PA)、总蛋白(total protein,TP)、白蛋白(Albumin,ALB)采用速率散射免疫比浊法检测,试剂盒购自上海臻科生物科技。生长调节指标:生长激素(growth hormone,GH)检测采用化学发光免疫分析法,胰岛素样生长因子结合蛋白3(insulin-like growth factorbinding protein 3,IGFBP-3)、胰岛素样生长因子-1(insulin-like growth factor 1,IGF-1)检测采用放射免疫分析法,试剂盒购自武汉默沙克生物科技。炎症指标:血清白细胞介素6(Interleukin- 6,IL-6)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、C 反应蛋白(C-reactive protein,CRP)检测采用酶联免疫吸附试验,试剂盒购自上海臻科生物科技。免疫指标:采用美国贝克曼公司的Cyto FLEX 流式细胞分析仪及其相应配套溶血剂检测CD4+和CD8+,计算CD4+/CD8+。
1.3.4 术后并发症比较两组术后切口感染、呼吸道感染、腹泻、粘连性肠梗阻、呕吐、胆汁淤积发生情况。
1.4 统计学方法
数据分析采用SPSS 22.0 统计软件。计数资料以率(%)表示,比较用χ2检验,计量资料以均数±标准差(±s)表示,比较用t检验。P<0.05 为差异有统计学意义。
2 结果
2.1 手术情况
观察组患儿腹腔镜探查除确定术前超声、消化道造影检查诊断的病因外,先天性肠旋转不良28 例中合并空肠闭锁4 例;环状胰腺8 例中合并肠旋转不良2 例,幽门异位胰腺、空肠闭锁1 例;十二指肠闭锁或狭窄12 例中合并肠扭转不良3 例,除1 例肠扭转局限肠坏死中转开腹行肠切除吻合手术外,其余51 例均在腹腔镜下完成手术,且术中无并发症,手术时间77~259 min,平均(159.75±37.81)min。对照组术前超声、消化道造影诊断病因外,先天性肠旋转不良28 例中合并空肠闭锁3 例;环状胰腺7 例中合并肠旋转不良1 例,幽门异位胰腺、空肠闭锁1 例;十二指肠闭锁或狭窄13 例中合并肠扭转不良4 例,除1 例患儿转开腹手术外,其余均在腹腔镜下完成手术,且术中无并发症,手术时间81~242 min,平均(161.04±35.90)min。
2.2 两组术后肠功能恢复情况比较
两组术后首次排便时间、完全肠内营养时间、喂养达到40 mL/3 h 时间、住院时间比较,差异有统计学意义(P<0.05),观察组短于对照组。见表1。
表1 两组术后肠功能恢复情况比较 (±s)

表1 两组术后肠功能恢复情况比较 (±s)
组别观察组对照组t 值P 值n 52 51术后首次排便时间/h 50.25±8.28 59.73±9.47 5.412 0.000完全肠内营养时间/d 10.49±1.50 14.96±1.94 13.097 0.000喂养达到40 mL/3 h时间/d 16.40±2.06 20.38±2.71 8.401 0.000住院时间/d 19.05±3.09 22.81±4.28 5.119 0.000
2.3 两组手术前后体重、身高、头围的差值比较
两组手术前后体重、身高、头围的差值比较,差异无统计学意义(P>0.05)。见表2。
表2 两组手术前后体重、身高、头围的差值比较 (±s)

表2 两组手术前后体重、身高、头围的差值比较 (±s)
组别观察组对照组t 值P 值n 52 51体重/g 53.70±12.92 49.74±11.55 1.639 0.104身高/cm 0.64±0.14 0.63±0.17 0.326 0.745头围/cm 0.67±0.16 0.64±0.18 0.894 0.373
2.4 两组手术前后营养指标的差值比较
两组手术前后血清PA、ALB、TP 的差值比较,差异有统计学意义(P<0.05),观察组高于对照组。见表3。
表3 两组手术前后血液营养指标的差值比较 (±s)
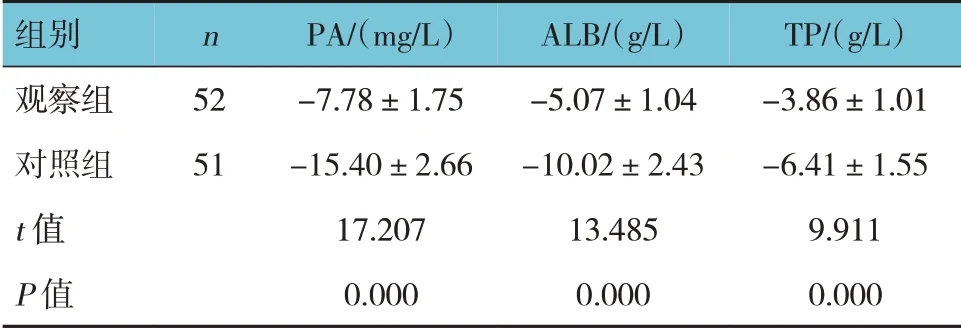
表3 两组手术前后血液营养指标的差值比较 (±s)
组别观察组对照组t 值P 值n 52 51 PA/(mg/L)-7.78±1.75-15.40±2.66 17.207 0.000 ALB/(g/L)-5.07±1.04-10.02±2.43 13.485 0.000 TP/(g/L)-3.86±1.01-6.41±1.55 9.911 0.000
2.5 两组手术前后生长调节指标的差值比较
两组手术前后血清GH、IGFBP-3 的差值比较,差异无统计学意义(P>0.05)。两组手术前后IGF-1的差值比较,差异有统计学意义(P<0.05),观察组高于对照组。见表4。
表4 两组手术前后生长调节指标的差值比较 (±s)
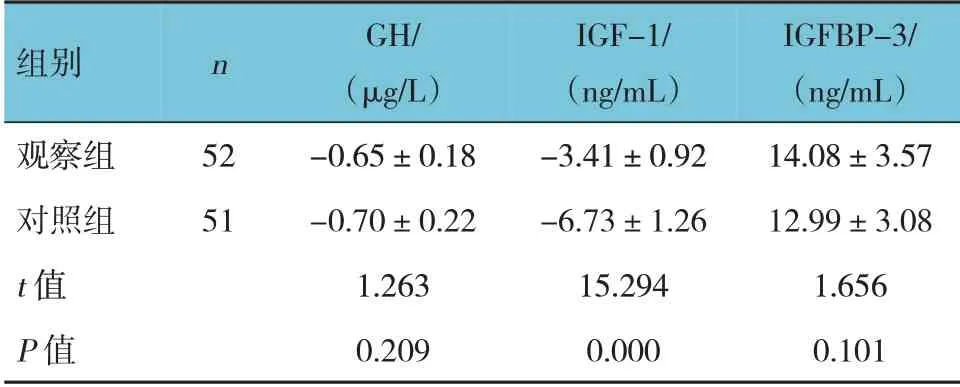
表4 两组手术前后生长调节指标的差值比较 (±s)
组别n观察组对照组t 值P 值52 51 GH/(μg/L)-0.65±0.18-0.70±0.22 1.263 0.209 IGF-1/(ng/mL)-3.41±0.92-6.73±1.26 15.294 0.000 IGFBP-3/(ng/mL)14.08±3.57 12.99±3.08 1.656 0.101
2.6 两组手术前后炎症指标与免疫功能指标的差值比较
两组手术前后TNF-α、IL-6、CRP 的差值比较,差异有统计学意义(P<0.05),观察组低于对照组。两组手术前后CD4+、CD4+/CD8+的差值比较,差异有统计学意义(P<0.05),观察组高于对照组。两组手术前后CD8+的差值比较,差异无统计学意义(P>0.05)。见表5。
表5 两组手术前后炎症指标与免疫功能指标的差值比较 (±s)
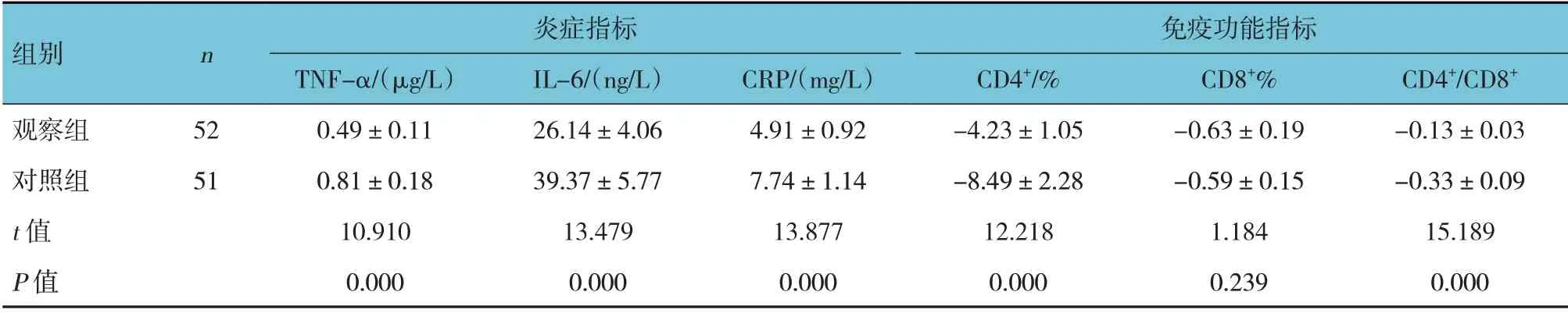
表5 两组手术前后炎症指标与免疫功能指标的差值比较 (±s)
组别n 炎症指标免疫功能指标IL-6/(ng/L)26.14±4.06 39.37±5.77 13.479 0.000观察组对照组t 值P 值52 51 TNF-α/(μg/L)0.49±0.11 0.81±0.18 10.910 0.000 CRP/(mg/L)4.91±0.92 7.74±1.14 13.877 0.000 CD4+/%-4.23±1.05-8.49±2.28 12.218 0.000 CD8+%-0.63±0.19-0.59±0.15 1.184 0.239 CD4+/CD8+-0.13±0.03-0.33±0.09 15.189 0.000
2.7 两组术后并发症情况比较
观察组术后并发症总发生率为15.38%,对照组为33.33%,经χ2检验,差异有统计学意义(χ2=4.513,P=0.034),观察组低于对照组。见表6。

表6 两组术后并发症情况比较 例
3 讨论
先天性十二指肠梗阻多于新生儿期急性或亚急性起病。该疾病确诊后应尽快予以早期手术治疗,否则易引发严重水电解质紊乱、营养障碍,甚至导致肠扭转坏死、严重内环境紊乱等威胁患儿生命安全,早期明确诊断并予以手术干预对改善患儿预后具有重要意义[6-7]。
随着外科技术以及新生儿围术期管理水平提高,腹腔镜手术被逐步应用于新生儿先天性十二指肠梗阻的诊治,患儿术后存活率得到明显提高[8]。相关实践证明,先天性十二指肠梗阻患儿围术期的营养支持对于细胞代谢保证、组织和器官结构及功能完整性、机体免疫维持以及伤口愈合等均具有重要价值[9]。一方面作为一种创伤刺激,手术可导致机体应激,进入快速分解代谢的状态,影响术后组织修复、伤口愈合;另一方面梗阻近端肠管长期处于被动、继发性扩张,肠管较为肥厚且动力差,导致患儿术后胃肠功能的恢复较为迟缓,肠道慢性功能性梗阻增大患儿经口喂养难度,食物在近端扩张胃肠潴留,不能正常进入下游肠管后被消化吸收,需通过长期全静脉营养来维持生命,由此可能增加感染、胆汁淤积、水电解质酸碱平衡紊乱等发生风险。同时,长期禁食将导致肠绒毛萎缩,使得肠上皮细胞增殖减少,增加肠黏膜通透性,细菌移位,甚至引起全身炎症性反应综合征[10]。经鼻留置空肠营养管肠内营养支持是一种为危重症患者提供营养的重要方式,并发症风险低、营养吸收有效、操作简单,符合机体生理,能维持肠道黏膜结构、功能完整,降低肠道细菌易位发生风险[11]。本研究对先天性十二指肠梗阻新生儿实施手术联合经鼻留置空肠营养管肠内营养支持,取得了良好疗效。
本研究中观察组患儿的肠功能恢复优于对照组,采用经鼻留置空肠营养管进行早期肠内营养支持,由等渗葡萄糖向低渗透压深度水解配方逐步过渡,依照患儿耐受情况逐步增加肠内营养量与速度,更符合生理状态,刺激肠道消化液的分泌,维持肠黏膜结构的稳定,促进肠蠕动,加速肠道功能恢复[12]。本研究中两组手术前后体重、身长、头围的差值比较无差异,这可能是由于本研究仅对比术前与术后7 d 体格指标差异,研究时间较短。营养状态对新生儿生长与发育具有重要影响,进一步比较两组营养指标差异,结果显示,观察组手术前后ALB、PA、TP 的差值高于对照组,说明经鼻留置空肠营养管肠内营养支持有利于减少术后体内蛋白质缺失,改善蛋白质负平衡。先天性十二指肠梗阻术后恢复过程中,营养需求较大,营养不足易使新生儿生长停滞,对体格、神经、免疫等发育产生不良影响。相关研究显示新生儿出生后1 周每天至少需摄入335~377 J/kg 热量才可保持和宫内相近生长水平[13]。
GH、IGF-1、IGFBP-3 及其受体构成的GH/IGF-1轴是人体生长调节重要机制。GH/IGF-1 轴调节机体合成及分解,促进细胞DNA、RNA、蛋白质合成,促进细胞增殖[13]。本研究中观察组手术前后血清IGF-1 的差值高于对照组,提示经鼻留置空肠营养管肠内营养支持可尽早为先天性十二指肠梗阻手术患儿提供能量与蛋白质,促进IGF-1 分泌,有利于患儿生长发育。YU 等[14]研究结果显示早期肠内营养可通过保护肠黏膜屏障,减少炎性介质释放,改善机体免疫功能。T 淋巴细胞水平反映机体当前免疫状态,本研究中观察组手术前后CD4+、CD4+/CD8+的差值高于对照组,胃肠道生态平衡与炎症反应关系密切,一方面,肠道正常菌群通过免疫球蛋白调节平衡细胞因子释放,有效控制炎症反应;另一方面肠道菌群失调时导致的局部炎症反应加速肠黏膜损害,增加肠通透性,使得有害物质进入到机体血液中,加重炎症反应。本研究中经鼻留置空肠营养管肠内营养支持为患儿尽早提供必要营养物质,促进肠道蠕动,逐渐恢复机体免疫反应性,促进T 细胞增殖,增强机体免疫,提高免疫功能。LI 等[15]报道肠内营养支持可促进胆汁从肠道排出,减少呕吐、胆汁淤积等静脉营养并发症风险。本研究结果显示,观察组术后并发症总发生率低于对照组,提示经鼻留置空肠营养管肠内营养有较高的临床安全性。
综上所述,肠梗阻术后经鼻留置空肠营养管肠内营养支持可有效改善十二指肠先天性梗阻新生儿营养状态,促进IGF-1 合成分泌,减轻术后炎症反应,提高免疫功能,降低术后并发症风险。本研究的不足之处在于样本量不足,缺乏术后中长期随访资料,可能导致结果存在偏倚,且未对不同类型先天性十二指肠梗阻患儿术后恢复情况进行对比,后续需行多中心、大样本研究作进一步验证。
