营养素缓解婴幼儿食物过敏的研究现状
2022-10-24鄢宇婷黄美佳陈红兵高金燕
鄢宇婷,马 鑫,黄美佳,陈红兵,高金燕,李 欣*
(1 南昌大学 食品科学与技术国家重点实验室 南昌 330047 2 南昌大学食品学院 南昌 330047 3 南昌大学中德联合研究院 南昌 330047)
1 婴幼儿食物过敏
食物过敏是指当反复暴露于特定食物中时,机体产生不良特异性免疫反应的现象[1]。90%以上食物过敏反应是由八大类食物引起的,包括牛奶、鸡蛋、花生、大豆、小麦、坚果、鱼和水生贝壳类动物[2]。对婴幼儿而言,最常见的食物致敏原为鸡蛋,其次是牛奶、虾和鱼[3]。美国一项调查研究[4]估计10.8%的人对食物过敏,而婴幼儿食物过敏患病率比成年人更高。日本调查显示:在婴儿中食物过敏患病率为5%~10%,幼儿患病率为13%[5]。2010年,我国三城市大样本研究表明0~1 岁婴儿食物过敏患病率为3.8%~6.4%[6]。2013年中国居民营养与健康监测项目数据显示2 至3 岁幼儿患食物过敏病率在4.37%[7]。2017年中国儿童食物过敏问卷调查中,儿童食物过敏发生率为5.83%[8]。
食物过敏是一种免疫疾病,是免疫失调和正常口服耐受性丧失的结果[9]。食物过敏的免疫机制均为对摄入的抗原产生的反应: 一是速发型过敏反应,主要为IgE 介导的过敏反应,特异性IgE 抗体与肥大细胞和嗜碱性粒细胞结合,触发介质的释放,导致迅速的生理反应[10]。二是迟发型过敏反应,迟发型过敏性炎症过程主要局限于肠道,是食物蛋白诱导的直肠结肠炎、小肠结肠炎和嗜酸性食管炎综合征的基础[11]。婴幼儿免疫系统发育不完善,相较成人来说,更易发生食物过敏。
食物过敏症状主要有皮肤、胃肠道和呼吸道症状。对于婴幼儿来说皮肤症状多为急性荨麻疹、特应性皮炎及血管性水肿;胃肠道症状为腹泻、呕吐、便秘,严重患者可能存在便血或者休克,非IgE介导过敏患者可能患有嗜酸性食管炎、结肠炎;呼吸道症状有过敏性鼻炎、结膜炎、哮喘等[11-12]。
2 营养素与婴幼儿食物过敏的关系
婴幼儿在生命最初几个月的生长和发育高度依赖膳食中的蛋白质[13]。而膳食中的蛋白质又常常是食物过敏原。其次营养是婴幼儿维持正常生长发育的基本保障,营养摄入不但会影响婴幼儿的生长发育,更会导致一些疾病的易感性,其中就包括食物过敏。这就让营养素与婴幼儿食物过敏之间的关系密不可分。目前有许多研究探究了婴幼儿食物过敏的营养素干预作用。
婴幼儿过敏的营养素干预最先被关注的是维生素D 营养干预,早在2007年,Camargo 等[14]首次报道了发达国家治疗食物过敏的主要方法——肾上腺素自动注射针在美国存在着纬度梯度,日照较少的北方地区处方使用率比南方高出4 倍,而紫外线能促进维生素D 的合成,这个报道引发了对维生素D 干预效果的广泛研究,由此食物过敏的营养素干预逐渐走入人们的视野,如今研究较多的也是对婴幼儿的维生素和脂肪酸营养干预效果。一个基于沙特阿拉伯人群的哮喘研究中显示:过敏患者饮食中摄入定量膳食纤维、维生素E、镁、钙、钠和钾均明显少于正常人群[15],这也提示了营养素干预和免疫类疾病有一定的关联性。
不仅仅是婴幼儿本身的营养素摄入,母亲的营养素摄入可能也会影响到后代食物过敏的发展。母亲营养素干预在生命早期1 000 d 时效果比较显著,这是指从怀孕开始到2 岁这一时期,是一个人最重要的发育时期,必须把握好生命早期1 000 d 的营养摄入。越来越多的证据表明,生命早期营养素摄入可以影响婴幼儿胃肠道健康,包括胃肠道中的微生物群[16]。在食物过敏发展方面,表现在怀孕和母乳喂养时期母亲饮食对婴幼儿食物过敏的影响。
3 不同营养素缓解食物过敏的作用
正如上文所说,营养素与婴幼儿食物过敏之间有密不可分的关系。婴幼儿食物过敏根据干预的物质可以分为维生素、微量元素、脂肪酸和膳食纤维等;根据干预对象可以分为对婴幼儿的营养素干预和对母亲的营养素干预。下面内容是关于婴幼儿和母亲在生命早期1 000 d 的营养素摄入对婴幼儿食物过敏影响。
3.1 维生素
维生素在免疫系统中起着重要作用。有研究表明,维生素及其代谢产物能够通过影响固有免疫应答和适应性免疫应答,发挥重要调节作用。其中,效果最显著的是作为重要抗氧化剂的脂溶性维生素A、D 和E[17]。
3.1.1 维生素A 维生素A 是一种重要的脂溶性维生素,人体的主要摄取途径可分为:从植物中获取的维生素A 前体——类胡萝卜素以及从动物中摄取的视黄醇。维生素A 在上皮细胞分化和肠道黏膜免疫系统发育中起着至关重要的作用[18]。维生素A 缺乏会损害胃肠道黏膜的上皮屏障,在小鼠模型中补充维生素A 可抑制干扰素-γ 和白细胞介素-4 的分泌,减少Th1 细胞数量并起到保护黏膜的作用[19]。在过敏性疾病方面研究中,视黄酸即维生素A 的活性代谢物已被发现可以抑制小鼠外周血单个核细胞中IgE 的产生[20],维生素A 可能通过TGF-β 介导的机制促进T 细胞向调节性T细胞转化[21-22]。也有证据表明,维生素A 在血液中的循环形式——视黄醇水平升高与IgE 介导的致敏风险增高有关[23]。上述证据均表明维生素A 在免疫系统发育中发挥着作用,在食物过敏中可能也扮演着重要的角色。但迄今为止,还没有关于维生素A 干扰食物过敏试验的相关研究报道,也没有在生命早期1 000 d 母亲摄入维生素A 干扰食物过敏的相关研究报道。
维生素A 缺乏(VAD)是世界卫生组织确认的四大营养缺乏症之一,如今婴幼儿缺乏维生素A的现象非常普遍,所以许多婴儿在早期便会补充维生素A。值得注意的是更提倡用脂溶性形式如花生油补充维生素A,研究表明在婴幼儿中由于水溶液的条件下维生素A 和D 吸收性更差,增加了患过敏性疾病的几率[24]。此外,也有文献报道花生油中含有ω-3 和ω-6 脂肪酸,可以减少自身免疫性疾病和预防过敏。由于市面上脂溶性维生素补充制剂大多同时补充维生素A 和维生素D,使用这些制剂补充时应明确维生素A 和维生素D可能具有拮抗作用,补充含有这两种维生素的制剂(例如鱼肝油)与补充纯维生素A 或纯维生素D的表现可能不同[25]。缓解过敏的机理和最佳的剂量还未见深入研究。
3.1.2 维生素D 维生素D 干预食物过敏的研究较多。近几年随着食物过敏患病率的增加,出现了许多假说,如双重过敏原暴露假说、维生素D 假说和卫生假说等。维生素D 影响食物过敏的机制有许多不同的解释:从基因层面上来说,维生素D 代谢相关的基因可能与过敏性疾病的发生有关。下游靶基因通常在启动子区域含有维生素D 反应元件,维生素D 进入靶细胞并与核膜上的维生素D受体(VDR)结合。在细胞核中,它与维甲酸X 受体(RXR)形成异源二聚体,并与靶基因启动子区域的维生素D 反应元件(VDRE)结合,进而调节代谢反应,如图1所示[26]。目前已发现几个与食物过敏相关的基因,包括编码细胞因子TNF-a、IFN-c、IL-10 以及抗原受体蛋白HLA-DRB1 和HLADQA1 的基因[27]。Oraei 等[28]的动物实验从小鼠脾细胞中分离CD4(+) T 细胞,采用real-time PCR技术对FOXP3、IL-10 和转化生长因子-β (TGFβ1)基因的表达进行相对定量,结果显示维生素D参与甲基化过程,诱导FOXP3 相关基因的表达,并可能诱导Treg 细胞因子的表达,从而缓解食物过敏。

图1 维生素D 在核内调节机制[26]Fig.1 Mechanism of vitamin D regulation in the nucleus[26]
从免疫细胞层面上来说: 维生素D 影响着关键免疫细胞的发育和功能,包括T 细胞、树突状细胞和调节性T 细胞[29-31]。已有研究发现维生素D能抑制Th2 免疫反应[32],同时维生素D3的代谢物25(OH)D3能够抑制IgE 介导的肥大细胞激活[33];试验数据表明1,25(OH)2D 会阻碍未成熟树突状细胞的成熟[34];血清25-OHD 水平与IL-10 水平呈正相关[35],然而其确切免疫机制尚未确定。近期Meeland 等[36]的研究也表明增加阳光照射或补充维生素D 可以增加婴幼儿体内Treg 细胞数,从而促进免疫耐受。
有许多研究结果显示维生素D 缺乏的婴幼儿更易食物过敏;最有代表性的有患上食物过敏的婴儿更可能出生于秋冬季[37],高纬度地区及日光照射少的地区婴幼儿食物过敏更加常见[14,38-39]。这些证据都表明维生素D 缺乏与食物过敏有一定的相关性,也存在更为直接的研究——美国的全民健康和营养调查和澳大利亚研究结果均显示维生素D 缺乏的儿童比维生素D 充足的儿童更易过敏[40-41]。台湾一队列研究表明:儿童血清维生素D缺乏与特异性IgE 水平成反比,可能增加儿童早期过敏(包括鼻炎和哮喘)的易感性[42]。
与之相反,有研究结果显示维生素D 过量也会引起食物过敏患病率增加。一项比较有针对性的队列研究显示维生素D 补充可能不会降低3 个月大时婴儿湿疹的严重程度,但可能会增加2 岁以后食物过敏的风险[43]。Rosendahl 等[44]最近的研究结果显示: 高剂量维生素D 补充剂在生命的第一年不能预防过敏、过敏性疾病或喘息。相比之下,随机补充维生素D 的婴儿患牛奶过敏的风险增加,高脐带血维生素D 状态的婴儿过敏敏感的风险增加,表明高浓度维生素D 可能产生不良影响。
基于上述两种结论,自然就有学者提出介于两者之间的研究结论-“u 型”假说,该假说认为体内维生素D 水平过高或过低均会影响食物过敏患病率。最早为该假说提供证据的是2003年研究,结果表明25(OH)D 可能在全身水平促进TH2 免疫偏斜,同时在局部/器官水平促进抗炎作用,而当体内25(OH)D 水平不同时,这些作用也不同[45]。Mullins 等[46]在澳大利亚进行的调查研究表明新生儿25 (OH)D 水平在75~99.9 nmol/L 之间时花生过敏风险较低。高于这个范围时过敏并没有减少,而低于50 nmol/L 水平与过敏无显著关系。到目前为止,还没有评估婴儿时期补充维生素D 以预防食物过敏的完整随机对照试验,但是可以推断出婴幼儿体内维生素D 水平与食物过敏必定存在关联。
生命早期1 000 d 母亲摄入维生素D 与后代食物过敏关系的研究结果并不单一。有研究表明,孕妇和母乳喂养的妇女补充维生素D 可能对儿童早期的食物过敏没有影响[47]。而Helene 等[48]的研究认为母亲补充维生素D,尤其在产前补充维生素D 至体内25(OH)D 水平大于30 ng/mL,能减少后代患哮喘/复发性喘息的概率。Shi 等[49]的近期研究也得出了相同的结论。母亲体内和脐带血25(OH)D3水平与儿童在头两年内食物过敏的风险呈正相关[50]。也有研究认为孕期维生素D 的补充方式也与后代过敏反应相关: 孕期使用维生素D补充剂增加后代患牛乳过敏的风险,而当孕妇从食物中摄入维生素D 可降低患牛乳过敏的风险[51]。但这些研究大多都是根据问卷调查得出维生素D 补充剂量,存在不准确,有主观性等问题,需要进一步通过试验验证。母亲摄入维生素D 的剂量和形式对婴幼儿食物过敏的影响和具体机理还需要进一步研究。
3.1.3 维生素E 食物中的维生素E 是4 种生育酚(α-,β-,γ-,和δ-生育酚)和4 种生育三烯醇(α-,β-,γ-,和δ-生育三烯醇)的集合。这些物质均具有抗氧化活性,但不能相互转化,只有α-生育酚才能满足人体对维生素E 的需求[52]。其主要膳食来源是植物油,良好来源是坚果。维生素E 通过影响细胞膜的稳定性和通透性、二十烷类化合物的产生、抑制中性粒细胞的迁移和抑制IgE 的产生来调节细胞的功能[53]。
膳食中维生素E 的摄入已被证明与较低的血清IgE 浓度有关,对未成熟T 细胞的分化也起着重要作用[54]。α-生育酚在免疫细胞中的免疫调节机制如图2[55]所示,对免疫细胞的特异性作用为维生素E 的免疫调节机制提供了有价值的证据,这表明其可能与过敏性疾病有关,但对食物过敏是否有干预作用还并不明确,需要更多的研究证明。
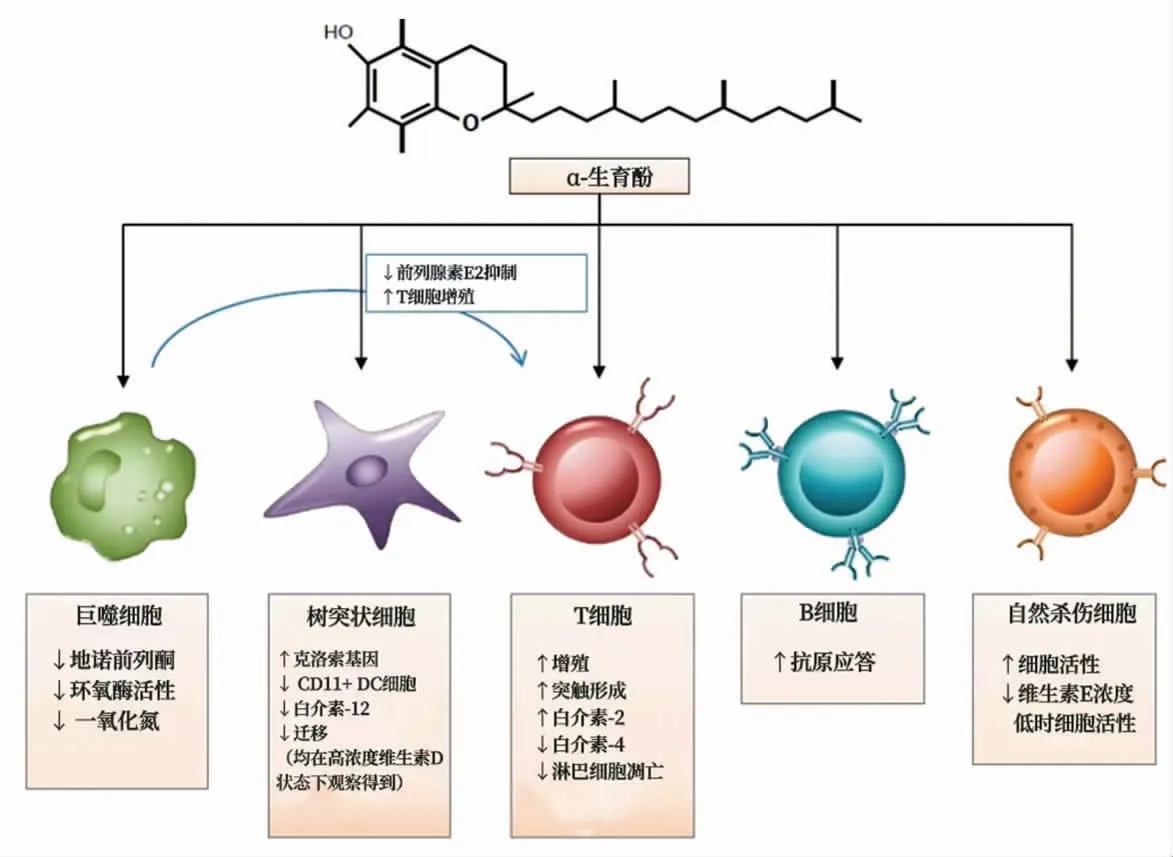
图2 α-生育酚在免疫细胞中的调节机制[55]Fig.2 Regulatory mechanism of α-tocopherol in immune cells[55]
3.1.4 维生素B B 族维生素属于水溶性维生素,包括维生素B1(thiamine,硫胺素)、维生素B2(riboflavin,核黄素)、维生素B3(niacin,烟酸)、维生素B5(pantothenic acid,泛酸)、维生素B6(pyridoxine,吡哆醇)、维生素B7(biotin,生物素)、维生素B9(folate,叶酸)和维生素B12(cobalamin,钴胺素)。叶酸对新生儿神经发育有着重要作用,也可能与食物过敏有潜在联系;B 族的其它维生素未见相关报道。早在1991年,就有研究证明在孕前和怀孕初期补充叶酸可以显著降低新生儿神经管缺陷的风险[56]。但其是否与食物过敏存在联系的研究结果还没有准确的答案,迄今有针对小鼠的试验结果也有针对婴幼儿的分析结果。
Hollingsworth 等[57]的小鼠模型表明,饲喂甲基供体(包括叶酸)饮食的母鼠幼崽的OVA 激发导致了气道反应性升高、嗜酸性粒细胞和IL-13 变多,血清总IgE 水平升高,CD4+/CD8+细胞比例升高并产生IL-4,这在人体内是Th2 偏倚的典型特征,增加了过敏性疾病的严重程度,这表明在孕期补充叶酸可能是新生儿患呼吸系统疾病甚至是过敏性疾病的危险因素。该项研究所用小鼠为单一品种,试验结果可能会受到叶酸剂量等因素的影响。
叶酸干扰婴幼儿的研究结果并不一致,Veeranki 等[58]的流行病学调查发现与未额外补充叶酸妇女所生的孩子相比,仅怀孕初期3 个月或怀孕期一直补充叶酸的妇女所生婴儿患哮喘的相对几率增加,而在怀孕3 个月后补充叶酸妇女所生的孩子并不存在与哮喘的相关性。也有针对牛乳过敏"高风险"婴幼儿的研究认为母亲怀孕期间叶酸的摄入与后代患牛乳过敏的风险增加有关,尤其在母亲本身患有过敏性疾病的这类人群中[51]。Mcgowan 等[59]针对叶酸形式的研究则认为孕期未代谢叶酸(UMFA)水平较高的婴儿由于在子宫内暴露于合成叶酸,出生时更可能患上食物过敏。Håberg 等[60]对2000年至2005年出生的32 077 名婴幼儿进行分析,结果表明在怀孕期间服用叶酸补充剂的母亲,其后代在18 个月前喘息和下呼吸道感染的风险略有增加,这个研究得到了与上述小鼠模型一致的结论: 孕期孕产妇饮食中的甲基供体可能会影响婴幼儿的呼吸健康[57,60]。
有研究显示了相反的结果:Crider 等[61]的荟萃分析表明孕妇在孕前至怀孕前3 个月服用叶酸补充剂(与不服用叶酸相比)与儿童哮喘之间不存在关联。叶酸作为《中国居民膳食指南》提倡的备孕和怀孕女性都应补充的营养素,其在胎儿生长发育中的作用是毋庸置疑的,但补充叶酸是否会增加婴幼儿食物过敏的风险,怀孕前3 个月补充是不是和食物过敏发展有关,是否由于剂量和补充方式而导致上述结果的差异,需进一步细化干扰方案来探讨。
3.1.5 维生素C 维生素C 又称为抗坏血酸,是一种高效的抗氧化剂,它能提供电子,从而保护重要的生物分子(蛋白质、脂类、碳水化合物和核酸)免受细胞代谢过程中产生的氧化剂损害[62]。体外研究表明,维生素C 可促进淋巴细胞孵育增殖,在未成熟T 细胞的发育分化和成熟中有重要作用[63]。维生素C 在免疫系统中发挥作用可能预示着它对食物过敏有一些干预作用,但具体机制和干预结果还未见相关研究报道。
3.2 微量元素
根据矿物质在人体内的含量可以分为微量元素和常量元素,微量元素指在人体中含量低于0.01%~0.005%的元素,主要包括铁、碘、锌、硒、氟、铜、钴、镉、锆、铷、锗和稀土元素等。微量元素多是抗氧化剂或体内代谢酶的辅因子,能够对机体免疫系统进行调节。目前主要有锌、硒、铁元素对食物过敏的相关报道。
3.2.1 锌 锌是包括超氧化物歧化酶(SOD)在内的许多酶的辅助因子,在维持机体氧化-抗氧化平衡中起着重要作用[64]。Barbara 等[65]的研究表明食物过敏的婴幼儿与其他正常婴幼儿相比,其体内硒和锌的值明显较低,谷胱甘肽过氧化物酶和超氧化物歧化酶含量也同样降低,停止摄入过敏食物6 个月后升高。Yosuke 等[66]发现特应性皮炎病史的儿童血清锌水平低,血清特异性IgE 水平明显高于无过敏症状的儿童。这项研究没有在结果中指明研究对象和研究方法,只有一个简单结论,但为我们探索锌和食物过敏相关性研究提供了新思路。
3.2.2 硒 硒是谷胱甘肽过氧化物酶的辅因子,可以通过诱导谷胱甘肽过氧化物酶或其它抗氧化酶的产生来减少氧化应激[67],从而减轻炎症反应的严重程度[68],但它们在过敏反应中的作用尚不清楚。Podlecka 等[69]提出两种可能的影响机制:母体或新生儿硒水平的降低可能通过促进辅助性T细胞向2 型辅助性T 细胞分化而导致婴幼儿喘息;另一种可能的机制是基于低硒浓度可能促进病毒感染。
根据Arthur 等[70]的研究,如果母亲的血清硒水平在80 mg/L 左右,则被认为是平台期,血浆或红细胞谷胱甘肽过氧化物酶活性不会进一步升高。与之对应,Iwona 等[71]的分析发现患有特应性皮炎的婴儿脐带血浆中谷胱甘肽过氧化物酶的活性明显低于无该症状的婴儿。适量的低硒摄入会降低过敏性气道炎症的易感性[72],微量营养素硒通过其免疫学效应影响机体免疫反应水平,过量的硒更易诱发过度的变态反应,从而导致更严重的皮炎症状[73]。Sakazaki 等[74]认为严重的缺乏硒会导致免疫缺陷。轻度的硒缺乏可加重过敏,而膳食中补充硒代蛋氨酸可消除过敏。近期研究也表明补充适量硒能下调炎症因子IL-6,IL-1β 和TNF-α 的表达,抑制肠道的炎症反应[75]。
从流行病学的观点来看,过敏性疾病与饮食中硒等营养物质的改变密切相关。一项针对新西兰儿童的调查表明硒能够通过抗氧化作用阻止哮喘发展[76]。也有一些研究表明硒与过敏性疾病之间不存在相关性[69,77],但Podlecka 等[69]的这项研究缺乏对婴儿血浆硒浓度的进一步评估,也没有母亲在怀孕期间硒摄入量的信息,结果并不准确。再加上这些研究是在不同的人群中进行的,结果可能会受到年龄、社会经济地位和居住地等因素的影响,流行病学的研究调查结果十分模糊。
3.2.3 铁 配方乳粉铁含量在过去的几十年里增长至原来的20 倍[78],婴儿铁摄入量稳步增加[79-80]。在小鼠模型中补铁可显著抑制气道嗜酸性粒细胞增多,而全身铁灌注可显著抑制过敏原诱导的气道嗜酸性粒细胞增多和高反应性[81]。研究表明,铁螯合剂可显著降低2 型辅助性T 细胞(Th2)介导的自身免疫大鼠模型的血清IgE 水平[82]。此外,乳铁蛋白作为一种天然的铁螯合剂,其在小鼠模型中能够缓解试验性过敏症状[83]。这都表明铁代谢和过敏性疾病的发展之间因果关系,有待进一步的探究。
3.3 脂肪酸
脂肪酸可以根据碳氢链是否饱和分为饱和脂肪酸和不饱和脂肪酸。多不饱和脂肪酸(PUFAs)是所有细胞膜中均存在的磷脂的重要组成部分,磷脂及其组成的PUFAs 通过影响膜的“流动性”[84]以及促进特定的蛋白-脂质和蛋白-蛋白相互作用而发挥作用,以调节细胞信号转导、基因表达和细胞功能[85]。同时PUFAs 通过这种膜介导的作用,可以调节免疫细胞的功能[86],并可能影响过敏性疾病的发展和表现[87]。这些脂肪酸的衍生物作为二十烷类化合物的前体和类似介质发挥作用,因此可以影响炎症过程,在过敏性炎症中发挥作用。在西方饮食中,PUFAs 占膳食中脂肪酸摄入的5%~20%。PUFAs 主要有两个家族——ω-6 家族和ω-3 家族。在大多数饮食中,ω-6 PUFAs 的摄入量超过ω-3 PUFAs,其中亚油酸和α-亚麻酸分别是最简单和最丰富的ω-6 和ω-3 不饱和脂肪酸代表[88]。亚油酸大量存在于许多植物油中,包括玉米油、葵花籽油和大豆油,以及由这些油制成的产品如人造黄油中。α-亚麻酸存在于绿色植物组织及一些常见的植物油中,如今与食物过敏相关性研究较多的是多不饱和脂肪酸(PUFAs)尤其是长链ω-3 多不饱和脂肪酸,如二十碳五烯酸(EPA)和二十二碳六烯酸(DHA)。在整个生命过程中尤其是怀孕至婴儿分娩时期,ω-3 脂肪酸都是必需脂肪酸[89]。在产妇饮食中补充ω-3 脂肪酸对婴儿视网膜和大脑的正常发育至关重要[90]。
长链ω-3 PUFAs 存在于海鲜,特别是油性鱼类中,它能抑制花生四烯酸与细胞膜结合,最终抑制花生四烯酸代谢为二十烷类化合物。但PUFAs与过敏相关性的具体研究结论差异性很大。Miles等[91]提出,早期饮食摄入ω-3 PUFAs 可能影响免疫系统和免疫细胞功能,起到预防婴幼儿过敏的作用。临床观察发现6月龄时对食物过敏的婴儿其母亲的初乳中总ω-3 脂肪酸、二十二碳五烯酸(EPA)和二十二碳六烯酸(DHA)较高[92],为ω-3脂肪酸在过敏性疾病中可能的有害影响提供了证据,因为,最早发现脂肪酸与食物过敏相关性的研究是Bolte 等[93]的研究,他们发现食用大量人造黄油的男孩比不食用人造黄油的男孩更容易发生过敏和过敏性鼻炎,而女孩中并没有这种趋势。也有研究表明患有特应性皮炎或其它过敏性疾病的澳大利亚学龄儿童的黄油摄入量更高[94],在患有过敏性疾病的婴儿母乳中亚油酸含量更高[95]。后来随着“鱼油中不饱和脂肪酸含量高”这一认知的逐渐普及,相关研究开始转向鱼类摄入量。Hamazaki等[96]的研究表明在鱼类高摄取量国家(>227 g 或2 份/周的鱼类),食用鱼类或食用ω-3 PUFA 对过敏有好处,但也可能由于鱼类中含有的环境污染物而增加过敏风险。这些研究说明饮食中摄入PUFAs 与过敏性的疾病有密切联系。因此有研究者建议,婴幼儿在4 至6 个月大时添加辅食时,无需延迟食用高过敏性食物,如鱼。而油性鱼类来源的ω-3 长链多不饱和脂肪酸,如二十二碳六烯酸(DHA)和二十碳五烯酸(EPA),已被建议通过抗炎作用降低过敏性疾病的风险[97]。而对于总脂肪酸组成和膳食中ω-3 及ω-6 脂肪酸的比例和具体脂肪酸对免疫系统的潜在影响,仍需要进一步研究阐明。
妊娠期和哺乳期妇女服用的鱼油补充剂可能会轻微减少易患食物过敏婴幼儿的过敏症状。有少量证据表明,孕妇摄入更多鱼类,尤其是脂肪含量高的鱼类,与后代在婴儿期和儿童期患过敏性疾病的风险较低相关[98],Palmer 等[99]的试验证明怀孕时补充鱼油的孕妇,其新生儿过敏性湿疹和鸡蛋过敏率显著降低。但其它研究却没有这种趋势。Chen 等[100]的研究表明婴儿时期摄入鱼类与患湿疹风险较低相关,而母亲在怀孕期间摄入鱼类与其后代婴儿患湿疹风险无明显关联。另有一项针对早产儿的试验结果表明母亲和婴儿服用金枪鱼油(高DHA)对过敏反应无缓解效果[101]。生命早期1 000 d 补充鱼油或摄入鱼类对婴幼儿过敏干预作用还不明确。
除了鱼油可以补充脂肪酸,也有研究针对补充长链多不饱和脂肪酸(LCPUFA)与过敏的关系,但结论也并不明确。一项纵向研究表明,孕期补充二十二碳六烯酸和二十碳五烯酸可增加母乳中LCPUFA 的浓度[102],这表明孕期补充LCPUFA 是能够对婴幼儿发挥作用的,Prescott 等[103]的研究更加深入,认为孕妇的饮食中若摄入足量的ω-3 长链多不饱和脂肪酸(LCPUFA)能对新生儿过敏起到预防作用。但也有研究不支持这个观点,Palmer等[104]的研究表明在妊娠期间补充ω-3 LCPUFA在婴幼儿3 岁前没有显著减少IgE 相关过敏性疾病。虽然这些研究结论不一致,但还没有研究显示孕期补充脂肪酸对食物过敏发展存在不利影响,因此可以提倡母亲在生命早期1 000 d 额外补充不饱和脂肪酸。但其具体剂量和方案可进一步深入探索。
3.4 膳食纤维
饮食干预可能通过调节肠道微生物群的组成来改变过敏性疾病的风险[105]。而膳食纤维能够影响肠道微生物群[106],在此背景下,已在小鼠模型中证明,膳食纤维摄入可通过增强Treg 细胞的数量和功能,显著抑制气道过敏性疾病的诱导,膳食纤维摄入量低会增加过敏性疾病的发生概率[107]。对于婴幼儿来说,膳食纤维多在固体食物如谷物、蔬菜等的添加中摄入。但针对膳食纤维和食物过敏相关性的研究很少,膳食纤维对食物过敏的影响机制也仍需继续探究。
4 营养素缓解食物过敏的干预方案
婴幼儿的饮食是分阶段的,从母乳喂养至补充喂养,再到后期的膳食结构,都会影响婴幼儿的营养素补充和免疫系统的发育。
4.1 补充喂养
补充喂养是指当母乳满足不了婴幼儿的营养需求时,添加补充(固体)食物以满足婴幼儿的营养需求。从20世纪70年代开始,许多欧洲国家建议引入固体食物。2003年,世界卫生组织建议纯母乳喂养至26 周,再添加固体食物并继续母乳喂养至两岁。而在美国和澳大利亚,建议在4 到6 个月开始引入固体食物[108]。许多研究阐明了补充喂养的时间和过敏之间的联系[109-112];针对不同食物的研究表明,延迟引入牛奶产品可能会增加湿疹患病风险,推迟引入其它食物与2 岁时患过敏性疾病风险增加有关[113]。针对过敏风险较高的婴幼儿研究表明: 过敏风险较高的婴幼儿在3~4 个月摄入固体食物会增加发生过敏性疾病的风险[114]。针对不同喂养条件的研究表明: 在引入固体食物的同时进行母乳喂养,会缓解过敏反应的发生[115]。这些研究可能受到不同人群、种族或母乳喂养方式的影响,但都表明延迟或提前补充喂养可能会增加婴幼儿食物过敏的患病率,我国更提倡上文所说的世界卫生组织建议喂养方法,即纯母乳喂养至26 周再添加固体食物进行混合喂养。
4.2 饮食多样性
1984年发表的过敏预防策略表明预防过敏就应该在妊娠时便尽量减少对过敏原的接触,而花生、鱼这种比较容易引起过敏的食物应该在1~3 岁时引入[116]。但后来研究发现通过主动接触过敏原蛋白产生免疫耐受是解决过敏新途径[117],过敏原回避策略也因此受到质疑[118]。Venter 等[119]长达10年的队列研究表明,在婴儿6月龄前每增加1 种食物,10 岁前发生食物过敏的几率就会降低10.8%;在1 岁前每多接触1 种食物抗原,10 岁前食物过敏的可能性显著降低33.2%。Tsuang 等[120]报道了1 岁前的饮食多样性和4~6 岁食物过敏之间呈反比。Hua 等[121]的研究表明,增加婴儿期对食物过敏源(包括水果、鸡蛋、鱼、贝类和花生)的接触,可减低婴儿IgE 过敏的风险。此外,来自英国出生队列的数据表明: 不易发生食物过敏的婴儿在2 岁时饮食结构中水果、蔬菜较多,工业化食品较少[122],这个结果提示婴幼儿食物过敏与工业化生产食品可能存在潜在相关性,对食物过敏的干预方案提供了新的思路。这些研究均表明了饮食多样性能减少食物过敏的风险,毫无疑问,在婴幼儿饮食结构中保证饮食多样性对食物过敏有着积极作用。
5 结语
如今食物过敏受到广泛关注,而婴幼儿膳食结构单一,消化系统和免疫系统发育不够完善,发生食物过敏概率高。本综述针对维生素、脂肪酸、微量元素等营养素,分别阐述婴幼儿饮食和生命早期1 000 d 母亲饮食中这些营养素与婴幼儿食物过敏的相互作用。从有效性、作用机理、部分干预研究结果等方面概述了这些营养素在食物过敏发展方面可能起到的作用。
婴幼儿食物过敏的唯一应对方法就是严格避免摄入该食物,但对于婴幼儿来说严格避免某类食物的摄入会影响其生长发育,若婴幼儿食物过敏能通过某种营养素的干预作用得到一定的缓解,对这些婴幼儿的生活质量和健康状况都会有大量益处。
【本文得到澳优乳业(中国)有限公司基金资助。项目名称:维生素D 对婴幼儿牛乳过敏的免疫营养干预作用研究(AU-YJY-B-LX-20-024)】
