抗中性粒细胞胞浆抗体相关性血管炎患者肾损伤预测模型的构建与验证
2022-10-24张梦珂叶力夏提阿德力别克李静
张梦珂 叶力夏提·阿德力别克 李静
抗中性粒细胞胞浆抗体(ANCA)相关性血管炎(AAV)是一组累及全身中小血管的自身免疫性疾病,可累及全身多个脏器[1-2],其主要病理特征表现为血管壁的破坏。近年来,关于AAV的研究越来越多,其诊断治疗均已取得很大进步,但是依然给患者带来了较大危害。AAV最常见且严重的并发症是急性肾损伤(AKI),可导致慢性肾脏病(CKD)、终末期肾功能衰竭(ESRD)甚至死亡[3]。早期诊断或识别AAV肾损伤并及时治疗能有效降低患者肾脏损伤程度,延长其生存时间。本文回顾性收集216例AAV患者的临床资料,分析可能导致肾脏损伤的因素,并且绘制列线图通过相关因素预测AAV患者走向透析或者死亡的概率。
对象与方法
1.对象:回顾性纳入我院2010年1月~2017年12月确诊为AAV的患者216例。纳入标准:(1)符合2012年美国北卡罗莱纳州教堂山会议定义的AAV分类诊断标准[4]及1990年美国风湿学会(ACR)制订的关于AAV的诊断标准[5];(2)血清ANCA检测阳性。排除标准:(1)原发性肾脏损伤或继发于其他疾病的肾脏损伤;(2)继发性血管炎。将216例患者随机分为建模组(142例)和验证组(74例)。本研究经我院伦理委员会审核批准。
2.方法
(1)一般临床资料及实验室检查结果收集:收集患者的一般临床资料及实验室检查结果[血肌酐(Cr)、血红蛋白(Hb)、红细胞沉降率(ESR)、PLT计数、血清K+、尿蛋白(PRO)、尿素氮(BUN)、补体C3、补体C4、D-二聚体、C反应蛋白(CRP)、促甲状腺激素(TSH)]。估算的肾小球滤过率(eGFR)采用慢性肾病流行病学合作研究(CKD-EPI)公式计算。CKD分期标准按照1999年美国肾脏病基金会肾脏病预后质量倡议工作组(KDOQI)提出的CKD定义及分期标准。
(2)随访情况:采用电话随访的方式,随访起点为患者就诊的时间,随访终点为2018年1月或患者死亡。统计患者随访期间透析或死亡的情况。

结 果
1.两组患者的一般临床资料和实验室检查结果比较:建模组及验证组未走向终点事件的患者分别为97例和44例,结局为终点事件的患者分别为45例和30例。两组患者一般临床资料和实验室检查结果比较差异均无统计学意义(P>0.05)。见表1。
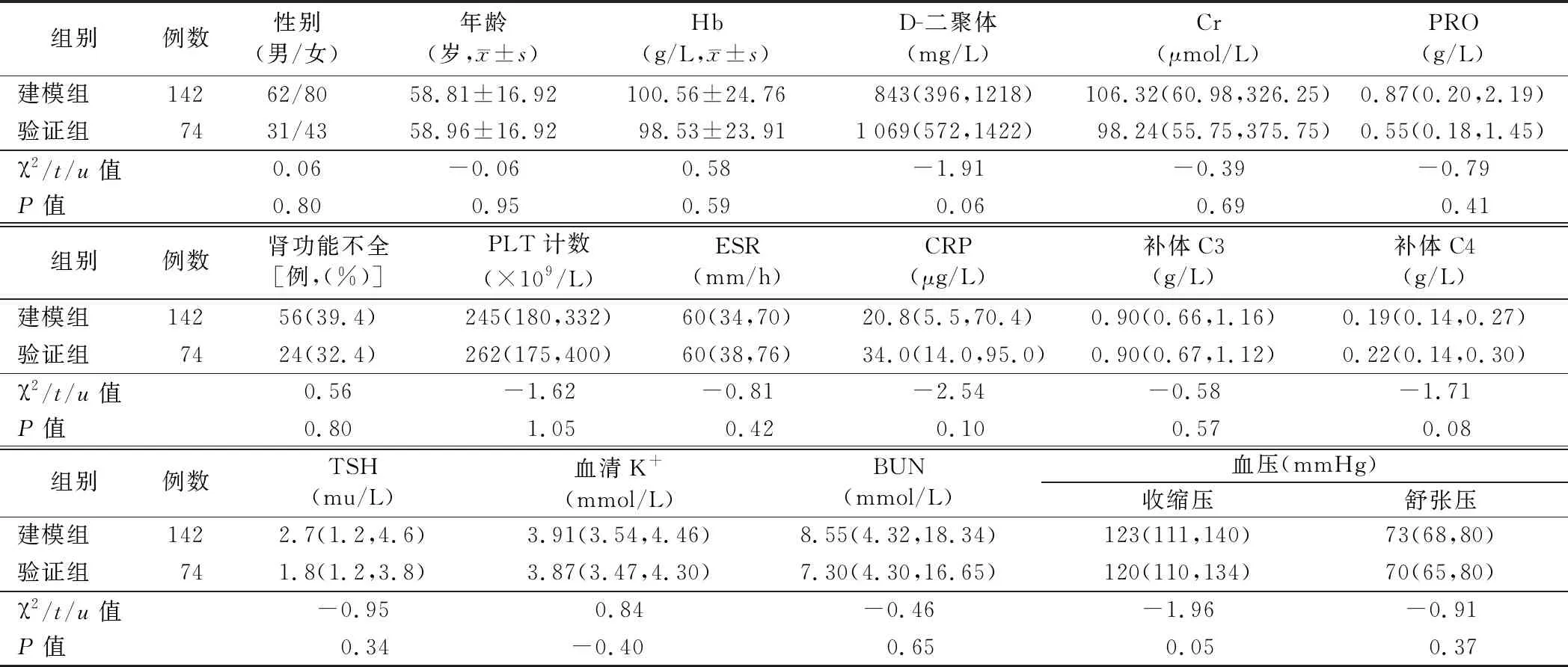
表1 两组患者一般临床资料和实验室检查结果比较[M(P25,P75)]
2.影响AAV患者肾损伤的单因素、多因素logistic回归分析结果:单因素logistic回归分析结果显示,Hb、收缩压、舒张压、CRP、补体C3、血清K+、BUN、Cr、肾功能不全均是AAV患者肾损伤影响因素(P<0.05)。见表2。将单因素分析结果纳入多因素logistic回归35分析模型,血清K+为连续性变量;起病时的肾功能、补体C3为二分类变量;CKD 1期和CKD 2期定义为肾功能正常,CKD3期及以上定义为肾功能不全;C3<0.79 g/L定义为低水平的C3,C3≥0.79 g/L定义为正常水平的C3。结果显示血清K+升高、补体C3水平降低、肾功能不全是AAV患者肾损伤的独立危险因素(P<0.05)。见表3。
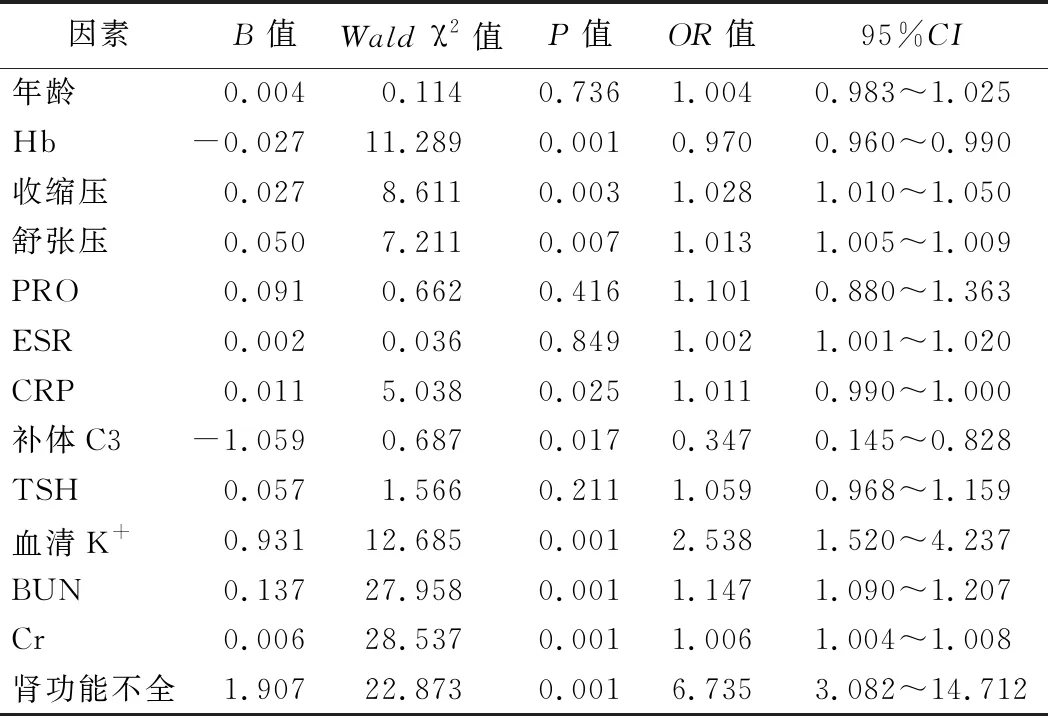
表2 影响AAV患者肾损伤的单因素logistic回归分析结果
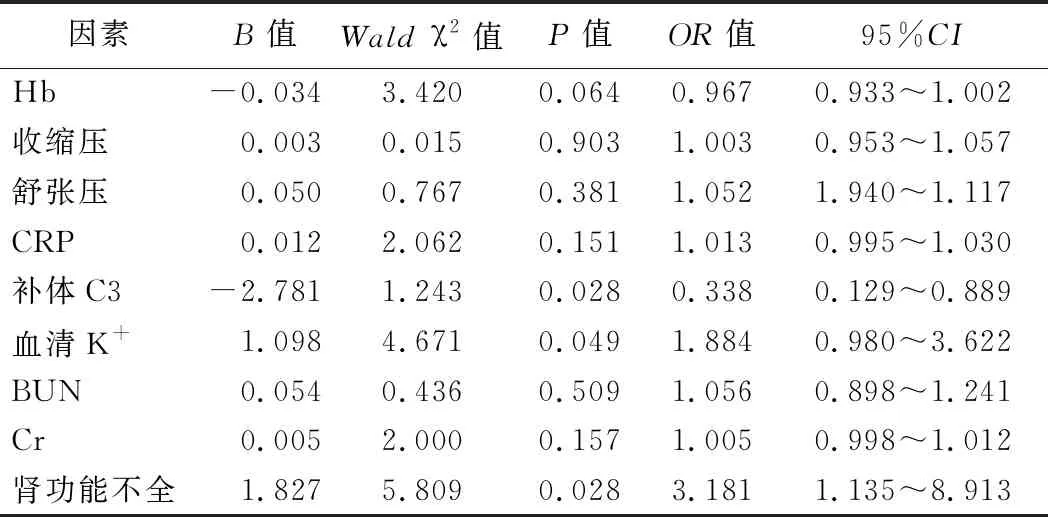
表3 影响AAV患者肾损伤的多因素logistic回归分析结果
3.预测AVA患者肾脏透析或死亡概率的列线图:根据预测模型构建AAV患者发生透析或死亡概率的列线图,在图中将对应指标的分值相加,最终得到的数值对应相应概率。如某患者补体C3低于正常水平(33分),血清K+浓度为4 mmol/L(30分),患者存在肾功能不全(36分),则该患者的总分为99分,可预测其发生透析或者死亡的概率为53%。见图1。

图1 预测AVA患者肾脏透析或死亡概率的列线图
4.对模型的评价和验证:建模组[0.768(95%CI0.740~0.789)]和验证组[0.730(95%CI0.720~0.745)]的ROC曲线下面积(AUC)均大于0.7,表明该模型对AVA患者是否进展为终点事件具有较好的区分作用。见图2、3。DCA曲线结果表明,当预测概率介于0.2~0.7时,诊断患者发生终点事件比“全部诊断”或“全部不诊断”使患者获益更多。
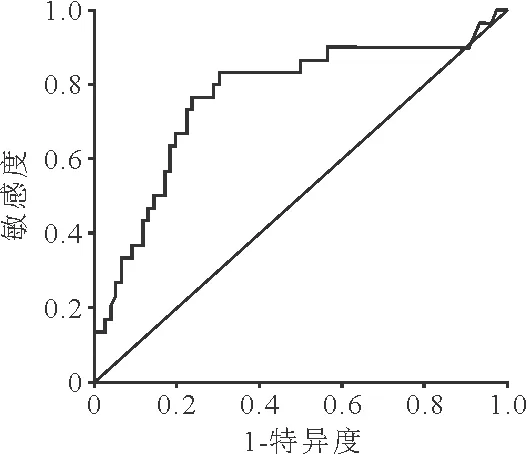
图2 建模组的ROC曲线

图3 验证组的ROC曲线
讨 论
AAV患者最常见的并发症是肾脏损害,肾功能进行性恶化是其常见的表现,往往会进展为终末期肾病(ESKD),甚至死亡。目前国内外大部分研究集中在AAV患者肾脏损伤的相关影响因素上,如起病时肾功能情况、补体C3、血清K+、Cr、Hb水平及年龄等,这些因素均会影响AAV患者肾脏预后[6-7]。但是对相关预测模型研究较少,导致不能量化肾脏损伤的概率。因此本研究通过回顾性分析,收集临床已有数据进行分析,绘制列线图,并进行内部验证。
本研究综合考虑了统计学意义和实际意义,选择了3个预测指标,分别是起病时的肾功能情况、血清K+及补体C3。既往文献指出起病时肾功能情况是影响患者预后的因素,当肾脏损伤时,促红细胞生成素(EPO)分泌减少,因此易发生低Hb血症[8]。目前许多研究已经确定了Hb降低与死亡率之间的关系,低Hb血症是AAV患者发生ESRD的独立危险因素[9]。本研究通过单因素和多因素logistic回归分析,结果表明血清K+升高是AAV患者肾损伤的独立危险因素,可用于预测肾脏功能的预后。临床上已有研究显示住院患者死亡风险与血清K+浓度有着十分密切的关系,尤其是CKD和糖尿病患者[10]。这可能与AAV患者电解质紊乱有关。AAV患者肾、肺功能受损,机体维持内环境稳态的能力下降,同时也会造成其营养不良。因此,AAV患者易发生电解质紊乱。这提示在AAV的治疗中,应密切关注K+指标,监测AAV电解质水平变化,及时纠正电解质紊乱,改善患者预后。近年来,越来越多的研究表明补体替代激活途径(ACP)在AAV患者中的重要作用[11]。同时也有研究证明,补体C3水平降低与AAV患者肾脏损伤及预后有着密切联系[12],低C3水平往往与较低的肾脏存活率、较高的患者死亡率显著相关。因此,补体C3水平低可作为AAV患者肾损伤的独立危险因素。
目前,国内关于AAV的研究主要集中于肾损伤的影响因素[13],通过AAV患者肾损伤的相关因素构建logistic回归模型,仅以公式表达,在临床上较难推广。本研究根据回归方程作出列线图,可量化每个指标对于结局的影响,具有良好的区分度和一致性。DCA曲线可得出患者在一定概率范围内被诊断为终点事件时的获益情况。因此,该列线图具有一定的临床适用性。
但本研究仍然存在一定局限性:(1)该研究为回顾性研究,在样本的选择以及数据收集等方面都可能存在误差;(2)该研究为单中心研究,相较多中心研究说服力差,未来可在不同的地区和医院再次进行外部验证;(3)本研究中未收集肾穿刺活检报告,因此未对AAV患者从病理类型上分层分析。
综上所述,基于起病时的肾功能状态、血清K+、补体C3做出的列线图能够很好的预测AAV患者肾脏预后的情况,未来应该在多中心进行外部验证,以期提高模型的说服力,及早应用于临床,指导个体化治疗。
