Mfolfox6方案联合西妥昔单抗和辛伐他汀治疗K-Ras突变结直肠癌疗效及对预后的影响
2022-10-21王敬东张庆尧
王敬东,张庆尧
(大连大学附属新华医院,辽宁 大连116021)
作为临床上常见的恶性肿瘤之一,结直肠癌(Colorectal cancer,CRC)的发病率不仅随社会发展呈逐年上升趋势,其病死率也位居恶性肿瘤的第四位[1-2]。发病初期,患者临床症状并不明显,等到临床确诊时肿瘤往往已经发生转移,病情较为严重,严重时会发展成为转移性结直肠癌(Metastatic colorectal cancer,mCRC),此时已经不能通过手术方式进行治疗,临床上通常会采用化疗方式或者靶向药物进行治疗[3-4]。有文献报道称,对于mCRC患者而言,K-Ras基因发生突变的几率较高,容易使得肿瘤细胞发生增殖和转移[5-6]。近年来,随着医学技术的不断发展以及医学药物的研发,临床对于mCRC患者的治疗有了新的给药模式、化疗药物以及治疗方案,临床疗效取得了很大程度的进步[7-8]。本文主要是对K-Ras突变结直肠癌患者采用Mfolfox6方案联合西妥昔单抗和辛伐他汀进行治疗的临床疗效,并对患者治疗后生存时长的相关危险因素进行分析,以便提高临床疗效。
1 资料与方法
1.1 一般资料 将2018年5月至2021年5月接受诊疗的128例K-Ras突变的结直肠癌患者作为本次研究对象,并按照随机数表法分为观察组和对照组(各64例)。观察组男36例,女28例,年龄30~69岁,平均(51.44±6.71)岁,左半结肠39例,右半结肠25例,中高分化40例,低分化24例,腹膜转移9例,无腹膜转移55例;对照组男34例,女30例,年龄33~62岁,平均(51.94±5.53)岁,左半结肠36例,右半结肠28例,中高分化39例,低分化25例,腹膜转移8例,无腹膜转移56例。两组患者的一般资料比较差异无统计学意义(均P>0.05),具有可比性,见表1。本研究经医院医学伦理委员会审批通过。病例纳入标准:①患者经临床诊断及影像学检查确诊为K-Ras突变结直肠癌[9];②患者临床资料完整且自愿配合本次研究;③患者及其家属对本研究知情同意;④所有研究对象预期生存时间均大于3个月。排除标准:①存在恶性肿瘤、脑部疾病或其他严重心血管疾病患者;②理解、沟通能力差或意识障碍患者;③妊娠期或哺乳期妇女;④对本研究使用药物过敏患者;⑤患有严重心、肝、肾等脏器疾病患者;⑥严重干扰本研究患者;⑦未能完成随访患者。

表1 两组患者一般资料比较
1.2 治疗方法
1.2.1 对照组:患者给予Mfolfox6方案联合西妥昔单抗进行治疗。治疗第1天采用静脉滴注的方式将85 mg/m2的奥沙利铂(国药准字H20000337)于2 h内注入患者体内,同时将400 mg/m2亚叶酸钙(国药准字H20080718)静脉滴注至患者体内,再静脉注射5-氟尿嘧啶(国药准字H31020593)400 mg/m2,之后持续注射5-氟尿嘧啶共46 h,用量不超过2400 mg/m2,治疗每隔2 d重复一次。西妥昔单抗(注册证号:S20130004)首次于2 h内静脉滴注400 mg/m2,后续每次与1 h内静脉滴注250 mg/m2,治疗每周1次。
1.2.2 观察组:在Mfolfox6方案联合西妥昔单抗治疗的基础上口服辛伐他汀(国药准字H20093943),每次10 mg,夜间服用,并根据患者自身胆固醇水平对辛伐他汀用量进行适量调整。所有患者治疗均持续两个月,并进行定期随访。
1.3 观察指标
1.3.1 采用实体瘤临床疗效评价标准(RECIST)对两组患者的临床疗效进行评估[10]:将患者病灶完全消失判定为完全缓解(CR);患者经治疗后病灶最大直径减少30%以上判定为部分缓解(PR);患者病灶增大不超过25%,缩小低于50%判定为病情稳定(SD);患者病灶增加大于25%,或者恶化出现新病灶判定为病情进展(PD);临床有效率=(CR+PR+SD)/总例数×100%。
1.3.2 不良反应:记录并比较两组患者治疗过程中恶心呕吐、皮疹、腹泻、血小板减少、白细胞下降、感觉神经毒性等不良反应的发生情况。
1.3.3 随访:根据定期随访情况,比较两组患者治疗后2年内的总体生存率。分析患者治疗后生存时长的相关危险因素。

2 结 果
2.1 两组患者临床疗效比较 与对照组患者相比,观察组患者CR、SD例数较多,PR、PD例数较少,总体临床疗效有显著提高,组间比较差异具有统计学意义(均P<0.05),见表2。

表2 两组患者临床疗效比较[例(%)]
2.2 两组患者不良反应发生情况比较 观察组患者治疗过程中不良反应发生率为25.00%,明显低于对照组患者(42.19%),组间比较差异具有统计学意义(P<0.05),见表3。
2.3 两组患者2年内生存情况比较 与对照组相比,观察组治疗后1年、治疗后2年生存患者均有明显升高,且组间比较差异有统计学意义(均P<0.05),见表4。
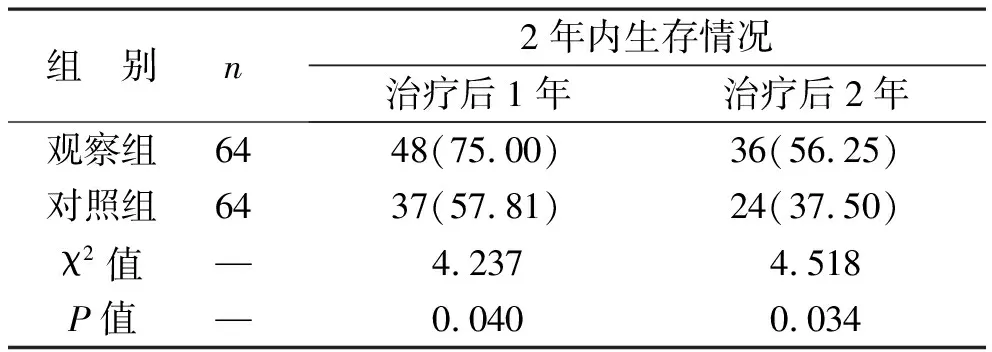
表4 两组患者2年内生存情况比较[例(%)]
2.4 患者治疗后生存时间影响因素分析 单因素分析结果显示,患者的平均生存时间与年龄、性别无显著相关性(均P>0.05),与病理分级、腹膜转移以及治疗方案有显著相关性(均P<0.05),见表5;多因素Logistic分析结果显示,病理分级与腹膜转移是患者治疗后平均生存时间的危险因素,见表6。
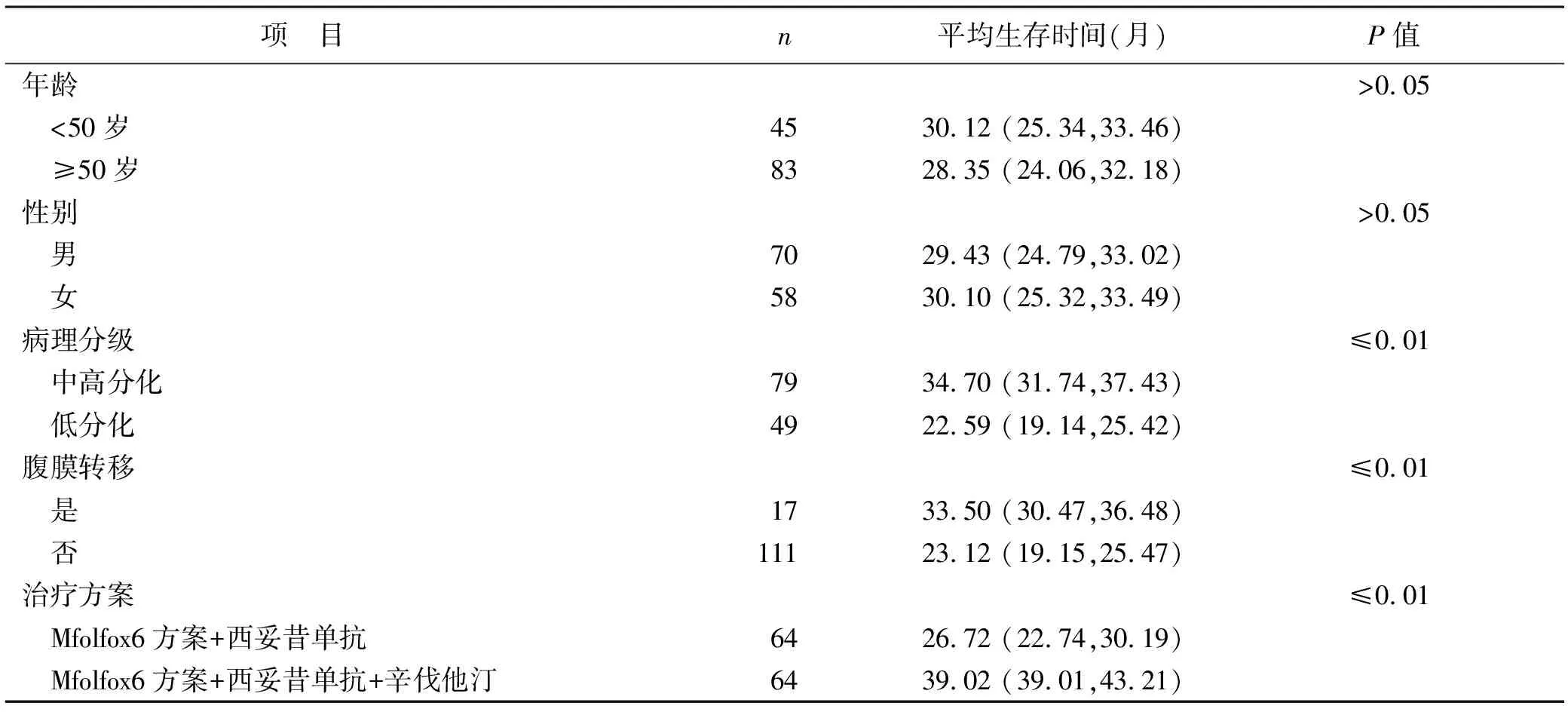
表5 两组研究对象各影响因素分析[M(P25,P75)]
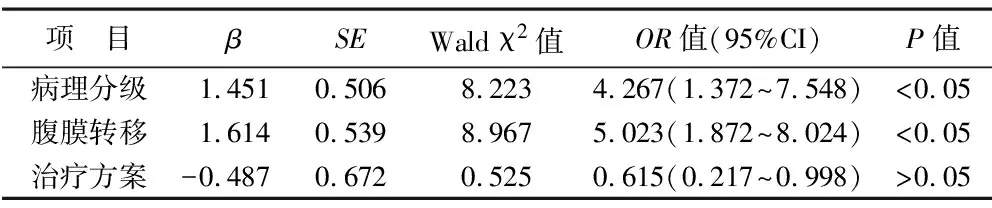
表6 患者平均预后生存时间的多因素分析
3 讨 论
CRC在全球恶性肿瘤中的发病率紧随肺癌和胃癌之后,作为临床常见的胃肠道恶性肿瘤,发病早期并无特异性症状,患者往往容易忽视,确诊时病情已经极其严重,对患者的生活及工作造成极大威胁[11-12]。临床上治疗晚期结直肠癌的标准化方案为Mfolfox6方案,方案中的药物主要包括奥沙利铂和5-氟尿嘧啶[13]。奥沙利铂作为一种新型的铂类抗癌药物,主要是通过抑制DNA的复制和转录来阻止肿瘤细胞增殖分化;5-氟尿嘧啶则是通过抑制胸苷酸合酶的活性使得肿瘤细胞停留在S期,从而达到抗肿瘤的作用[14]。
CRC中常见的致癌基因主要是K-Ras基因,K-Ras基因主要作用只控制细胞增殖分化,其也是EGFR信号通路中的关键基因,通过编码Ras蛋白,EGFR信号能够被传递到丝裂原活化蛋白激酶(MAPKs),进而参与调控细胞生长、增殖、分化以及血管生成[15]。西妥昔单抗属于一种分子靶向肿瘤药物,其能够对EGFR起到靶向作用,通过竞争性结合EGFR,进而阻断信号传递、抑制细胞增殖分化,达到抗肿瘤的疗效[16-17]。患者由于K-Ras基因突变,但体内Ras蛋白与EGFR信号通路仍处于激活状态,此时西妥昔单抗治疗对肿瘤细胞的生长并不能够起到抑制作用,临床疗效不佳[18]。辛伐他汀作为一种还原抑制剂,临床治疗中常用于降血脂,相关研究显示,其可以提高K-Ras基因CRC细胞对西妥昔单抗的敏感性,进而抑制细胞增殖分化,此外,其还能够抑制细胞固有生长途径,联合西妥昔单抗对患者进行治疗能够促进细胞凋亡,具有更为理想的临床疗效[19-20]。本研究结果显示,与Mfolfox6方案+西妥昔单抗治疗组相比,Mfolfox6方案+西妥昔单抗+辛伐他汀治疗组CR、SD例数增多,PD例数明显降低,不良反应发生率也有显著降低,提示辅以辛伐他汀治疗能够显著提高临床疗效,降低不良反应的发生风险。推测原因是辛伐他汀能够逆转K-Ras基因突变的CRC患者对西妥昔单抗的耐药性,而且辛伐他汀与西妥昔单抗同时治疗能够抑制肿瘤细胞的增殖分化,使得肿瘤细胞的侵袭能力下降,凋亡速度加快。加用辛伐他汀组患者治疗后2年的生存率有明显升高,说明加用辛伐他汀能够提高患者对西妥昔单抗的敏感性,延缓肿瘤的进一步发展,推测可能是与辛伐他汀诱导的凋亡相关蛋白的表达有关。研究发现,患者治疗后平均生存时间与患者病理分级、有无腹膜转移以及治疗方案显著相关,其中病理分级、腹膜转移是影响患者生存的危险因素,腹膜转移是导致结肠癌患者死亡的主要原因,且转移程度越高,患者生存时间越短。加用辛伐他汀不会直接影响患者生存时间,但一定程度上能够延长生存时间,有利于患者预后。
综上所述,对于K-Ras突变的结直肠癌患者而言,采用Mfolfox6方案+西妥昔单抗+辛伐他汀治疗方案能够显著提高临床疗效,明显降低患者治疗过程中的不良反应发生率,患者治疗后的生存率也有明显提高,延长了患者的生存时间,具有很好的临床应用价值。研究还发现患者病理状况以及是否存在腹膜转移也是影响患者预后的主要因素。
