基于药物治疗管理的门诊癌痛患者全程化疼痛管理模式的效果评价
2022-10-20高培培许晶晶龚婧如陆惠平
高培培 许晶晶 龚婧如 陆惠平△
(1上海市浦东医院-复旦大学附属浦东医院药剂科 上海 201399;2上海健康医学院药学院 上海 201318)
世界卫生组织国家癌症研究机构发布的2020年全球最新癌症负担数据显示:中国新发癌症人数和死亡人数均位居全球第一,癌症的治疗成为了医疗卫生问题中的重点和难点,切实提高癌症患者的生存质量是目前国内亟待解决的医疗问题[1]。疼痛是恶性肿瘤患者十分常见的症状,癌症疼痛(以下简称“癌痛”)的治疗面临十分严峻的形势,新发癌症中约25%的患者伴有不同程度的疼痛,晚期癌症患者疼痛发生率高达60%~80%,其中1/3的患者为重度疼痛[2]。癌痛得不到缓解,严重影响着患者的生活质量,导致患者情绪低落,进而出现焦虑及抑郁等心理疾患,同时疼痛还直接或间接抑制机体免疫功能进而促进肿瘤进展,给患者及其家庭带来巨大的精神和心理负担[3]。因此,癌痛的规范化治疗是癌症治疗的重要环节之一,规范、有效的药物治疗能够缓解80%以上癌症患者的癌痛症状[4]。
“癌痛规范化治疗示范病房”创建活动的开展使临床药师服务于住院癌痛患者,对住院患者的规范化管理相对到位[5-7]。由于癌痛患者需门诊就诊并长期口服用药,门诊癌痛的规范化管理是全程管理的重要环节,是衔接住院管理与居家管理的“桥梁”,门诊癌痛规范化管理缺失是癌痛患者控制不佳的主要原因[8-10]。国外有研究将药物治疗管理(medication therapy management,MTM)模式应用于门诊癌痛患者,并进行了相关探索,证实由药师主导的药物治疗管理模式可显著改善癌痛患者的临床、人文及经济指标[11-13]。我国目前药物治疗管理服务的发展正处于探索起步阶段,还未形成标准化模式。上海市浦东医院临床药师通过药学门诊,运用MTM,为门诊癌痛患者提供全程化管理,建立了基于MTM的门诊癌痛药学服务模式,旨在为规范门诊癌痛患者用药及MTM服务模式的标准化提供参考。
资料和方法
临床资料收集2021年1—12月在上海市浦东医院门诊接受强阿片类药物镇痛治疗并建立门诊癌痛专用病历本的成人癌痛患者。采用随机数字表法进行分组,将符合纳入标准的80名癌痛患者,随机分为干预组(n=40)与对照组(n=40),共41名男性和39名女性,年龄为28~80岁。纳入标准:(1)年龄≥18周岁且≤80周岁;(2)经细胞学或病理学确诊为恶性肿瘤,并伴有中重度癌痛的患者;(3)ECOG评分<4分,预期生存期≥6个月;(4)能进行有效的语言沟通。排除标准:(1)年龄<18周岁或>80周岁;(2)ECOG评分>4分,预期生存期<3个月;(3)有认知障碍,不能进行自主疼痛评估的患者;(4)有沟通障碍,不能进行有效语言交流的患者;(5)存在严重脏器功能不全(肝肾等)的患者。本研究经上海市浦东医院伦理委员会批准(伦理批号QWJWXM-09),所有患者均签署书面知情同意书。
干预措施运用门诊癌痛MTM管理系统,两组患者均在药学干预前(d0)完成入组调查评估,包括一般情况调查表、疼痛和疼痛影响评估以及服药依从性评估作为基线数据。
对照组接受常规的医护告知,调剂药师的基本用药告知,临床药师不对其进行全程化药物治疗管理。
干预组患者接受除常规医护告知、调剂药师的基本用药告知外,临床药师在药学门诊为患者提供全程化的药物治疗管理服务,主要包括:(1)通过门诊癌痛MTM管理系统,患者每次就诊都为其建立电子MTM用药档案,分别从所服用药物的适应证、有效性、安全性、依从性四方面分析患者目前用药是否存在药物治疗相关问题(drug-related problems,DRPs),针对存在的问题对患者或主诊医师提出合理化的用药建议;(2)对每位就诊患者进行疼痛评估和不良反应监测;(3)对每位就诊患者进行5 min用药教育和癌痛及癌痛药物相关宣教,发放服药提醒智能药盒;(4)建立癌痛药物咨询微信平台,实时在线回复患者在家所遇到的疼痛问题及定期发布癌痛知识宣教;(5)对患者进行每周1次电话回访调查;(6)约定患者每15日门诊复诊干预。
药物治疗管理服务不是一次性地为患者提供用药咨询,而是需要对患者的长期药物治疗提供监护,通过跟踪随访,与患者建立持续稳定的服务关系,可以持续为患者的药物治疗和生活方式全方位地提供科学规范的指导,保证患者持续获益的终极目标。因此一个完整的药物治疗管理服务流程至少需要患者2次来院就诊,也就是需要4周的时间。为了更好地服务患者,同时为了提高试验结果的可靠性,在参考大量文献研究的基础上,我们将本研究的干预时间设计为8周,即持续8周后(d56)对两组进行第2次调查评估,再次评估患者疼痛控制情况、疼痛影响评估和服药依从性等。
观察指标
主要观察指标 (1)疼痛评分:采用数字分级法(numerical rating scale,NRS),用0~10代表不同程度的疼痛,0为无痛,1~3为轻度疼痛,4~6为中度疼痛,7~10为重度疼痛[2]。让患者选出最能代表自身疼痛程度的数字,观察两组患者干预前(d0)、干预后56天(d56),过去24 h内最剧烈的疼痛程度、平均疼痛程度的NRS评分。(2)疼痛影响评分:采用“简明疼痛评估量表(Brief Pain Inventory,BPI)”对癌性疼痛进行疼痛影响评估,疼痛对患者的影响包括7项:过去24 h内对日常生活、日常工作、情绪、睡眠、行走能力、与他人关系、生活乐趣,用0~10代表疼痛影响程度,0代表无影响,10代表完全影响[2]。观察两组患者d0、d56的疼痛影响程度。(3)不良反应发生率:观察两组患者用药期间的不良反应发生情况。
次要观察指标 (1)服药依从性评分:采用Morisky(Morisky Medication Adherence Scale-8,MMAS-8)用药依从性问卷中文版[14]对癌痛患者进行依从性评价,该问卷满分为8分,8分为依从性良好,6~7分为中等,<6分为差,观察两组患者d0和d56的服药依从性。(2)生存质量评分(ECOG评分):采用美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)推荐的体力状况评分标准(Zubrod-ECOG-WHO,简称ECOG评分法),将患者的活动状态分为0~5分共6级,正常活动为0分;症状轻,生活自在,能从事轻体力活动为1分;能耐受肿瘤的症状,生活自理,但白天卧床时间不超过50%为2分;肿瘤的症状严重,白天卧床或坐轮椅时间超过50%,但还能起床站立,仅部分生活自理,评分为3分;病重卧床不起为4分;患者死亡,评分为5分。ECOG评分越低,患者的体力状况越好,生存质量越高[15]。观察两组患者d0和d56的ECOG评分。
统计学方法采用SPSS 25.0统计软件分析,计量资料以表示,并采用t检验分析;计数资料以例数或率表示,并采用χ2检验分析。P<0.05为差异有统计学意义。
结 果
一般情况采用χ2检验对80例患者的性别、年龄、肿瘤类型、婚姻状况、文化程度、ECOG评分等一般资料进行分析,结果显示两组患者的一般资料和临床资料均衡,基线具有可比性(表1)。
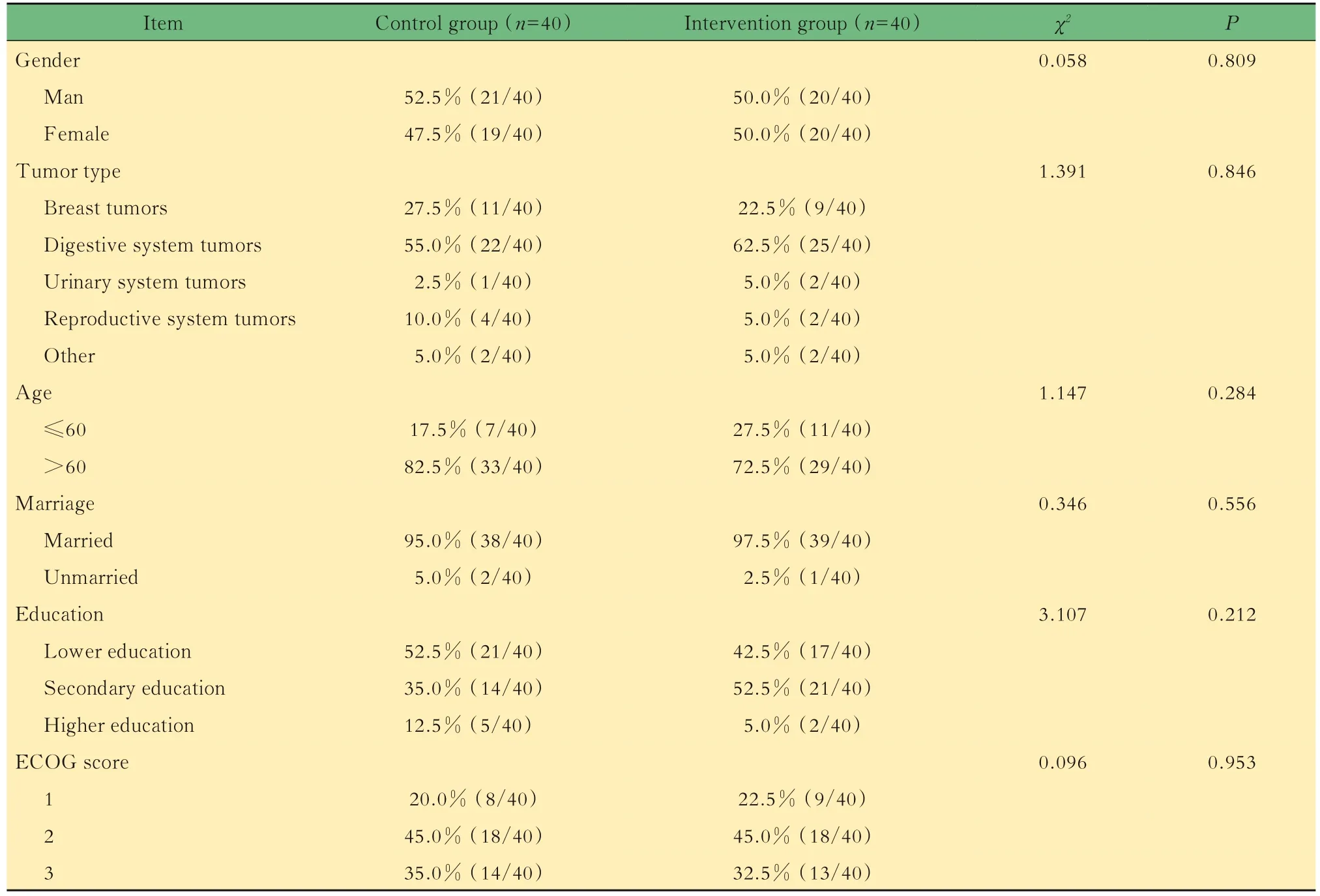
表1 两组患者一般资料和临床资料比较Tab 1 Comparison of general and clinical information of patients between the two groups
干预组患者药物治疗管理开展情况本研究通过对干预组40例患者实施药物治疗管理,共发现了83个药物治疗相关问题(DRPs),人均2.08个,主要问题集中在药物治疗的安全性、有效性和依从性三方面,其中药物不良反应32例(38.55%)、依从性差18例(21.69%)、给药剂量不足17例(20.48%)、无效药物治疗4例(4.82%)。临床药师通过提出用药建议,以及对患者进行宣教和随访,解决了65个药物相关问题,问题采纳率高达78.31%,涉及适应证和有效性的药物相关问题全部得到解决,依从性问题解决了77.78%,不良反应问题解决了56.25%(表2)。
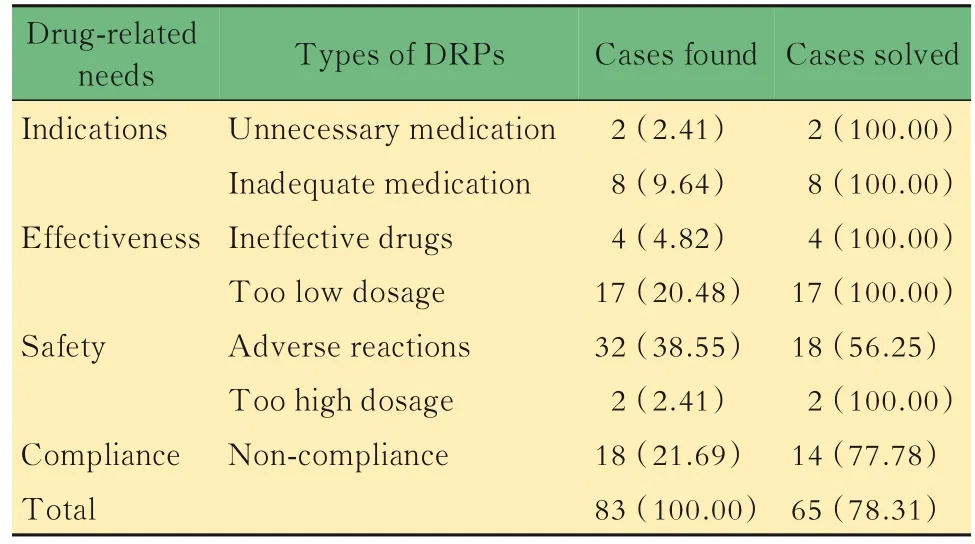
表2 干预组药物相关问题分布及解决情况Tab 2 Distribution and resolution of DRPs in the intervention group [n(%)]
患者疼痛评分的比较对所有80例患者的疼痛评分进行总体分析,发现入组评估24 h内最严重疼痛评分为5.76±1.37,中位数为6,平均疼痛评分为4.20±1.31,中位数为4。将两组(n=40)的疼痛评分采用配对t检验。与干预前相比,两组的24 h内最严重疼痛和平均疼痛均显著减轻(P<0.001,表3)。
表3 两组患者各组干预前后NRS评分比较Tab 3 Comparison of NRS score before and after intervention individually in control and intervention group ()
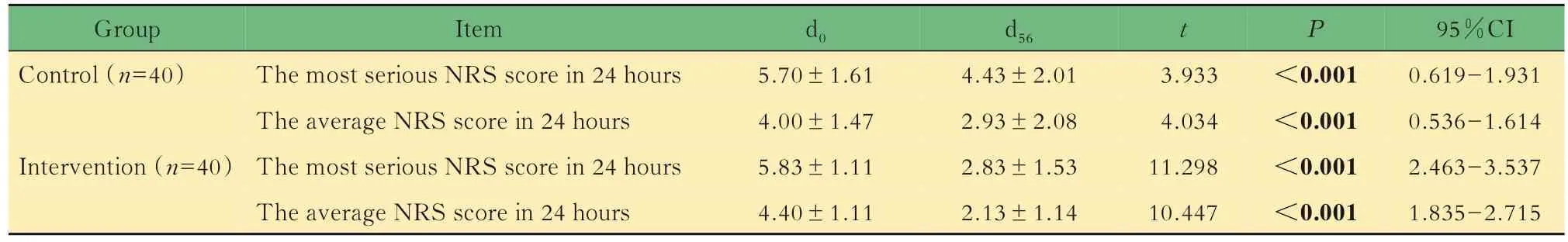
表3 两组患者各组干预前后NRS评分比较Tab 3 Comparison of NRS score before and after intervention individually in control and intervention group ()
Group Control(n=40)Intervention(n=40)Item The most serious NRS score in 24 hours The average NRS score in 24 hours The most serious NRS score in 24 hours The average NRS score in 24 hours d0 5.70±1.61 4.00±1.47 5.83±1.11 4.40±1.11 d56 4.43±2.01 2.93±2.08 2.83±1.53 2.13±1.14 t 3.933 4.034 11.298 10.447 P<0.001<0.001<0.001<0.001 95%CI 0.619-1.931 0.536-1.614 2.463-3.537 1.835-2.715
采用独立样本t检验分析比较对照组和干预组的疼痛评分,干预前(d0),两组之间的最严重疼痛和平均疼痛没有显著差异,基线具有可比性。干预后(d56),两组最严重疼痛评分差异有统计学意义(P<0.001),平均疼痛评分差异有统计学意义(P<0.05)。干预组的最严重疼痛评分和平均疼痛评分均显著低于对照组,疼痛治疗效果改善更显著(表4)。
表4 两组患者干预前后NRS评分比较Tab 4 Comparison of NRS score between 2 groups before and after intervention ()
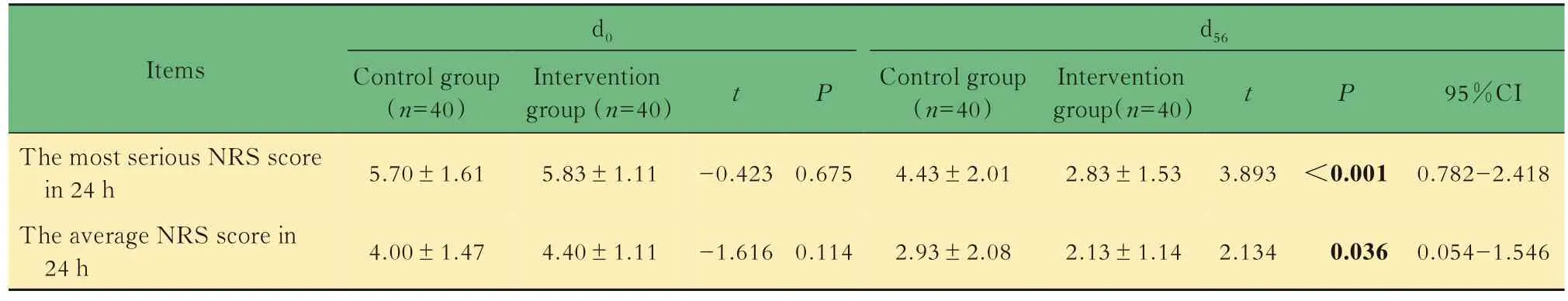
表4 两组患者干预前后NRS评分比较Tab 4 Comparison of NRS score between 2 groups before and after intervention ()
Items The most serious NRS score in 24 h The average NRS score in 24 h d0 Control group(n=40)5.70±1.61 4.00±1.47 Intervention group(n=40)5.83±1.11 4.40±1.11 t-0.423-1.616 P 0.675 0.114 d56 Control group(n=40)4.43±2.01 2.93±2.08 Intervention group(n=40)2.83±1.53 2.13±1.14 t 3.893 2.134 P<0.001 0.036 95%CI 0.782-2.418 0.054-1.546
患者疼痛影响评分的比较分析80例患者入组时的疼痛影响评分,其中疼痛对日常生活、情绪、行走能力和日常工作的影响得分较高,中位数均为7;疼痛对与他人关系、睡眠、兴趣的影响的评分中位数均为6。采用配对t检验分析干预前后两组疼痛对患者的影响评分,干预后两组的各项疼痛影响评分均改善显著(P<0.001,表5)。
表5 两组患者各组干预前后疼痛影响评分比较Tab 5 Comparison of pain effect score before and after intervention individually in control and intervention group()
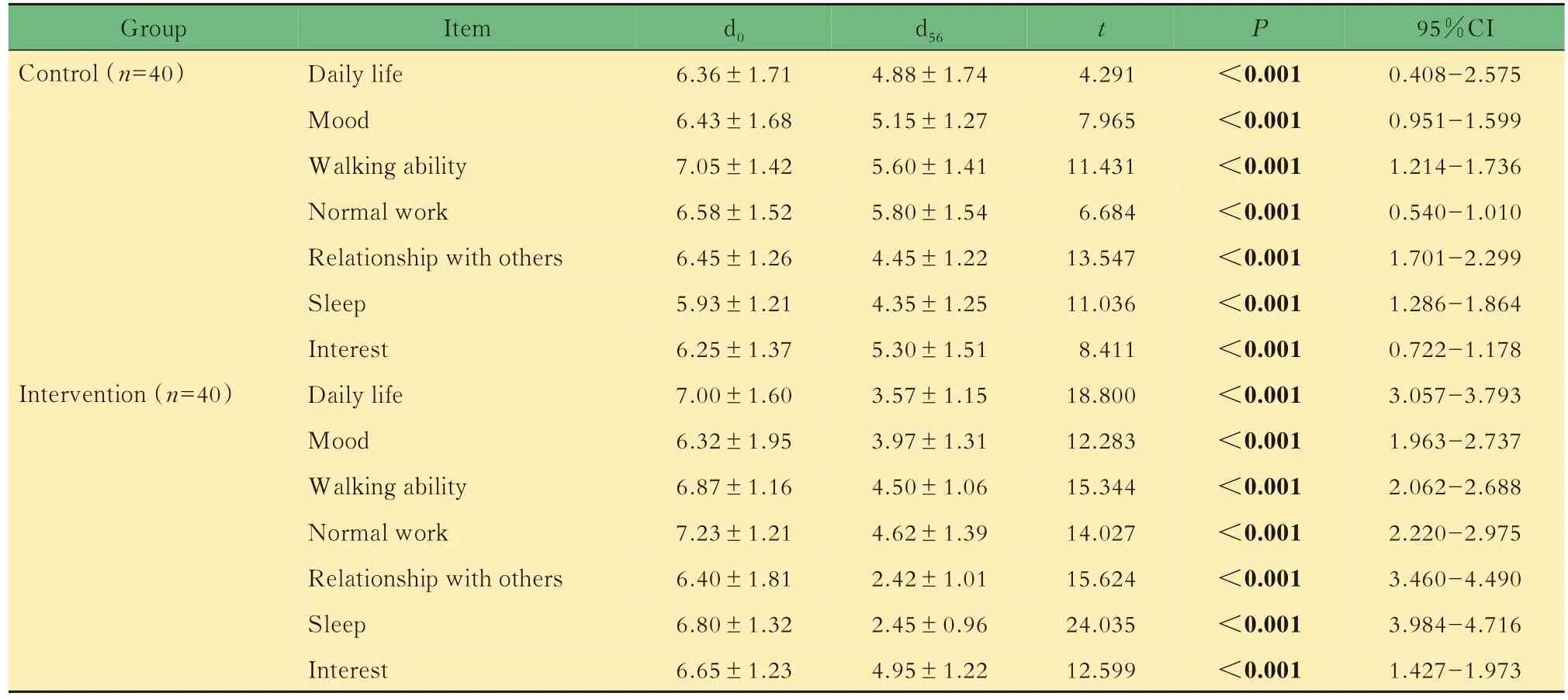
表5 两组患者各组干预前后疼痛影响评分比较Tab 5 Comparison of pain effect score before and after intervention individually in control and intervention group()
Group Control(n=40)Intervention(n=40)Item Daily life Mood Walking ability Normal work Relationship with others Sleep Interest Daily life Mood Walking ability Normal work Relationship with others Sleep Interest d0 6.36±1.71 6.43±1.68 7.05±1.42 6.58±1.52 6.45±1.26 5.93±1.21 6.25±1.37 7.00±1.60 6.32±1.95 6.87±1.16 7.23±1.21 6.40±1.81 6.80±1.32 6.65±1.23 d56 4.88±1.74 5.15±1.27 5.60±1.41 5.80±1.54 4.45±1.22 4.35±1.25 5.30±1.51 3.57±1.15 3.97±1.31 4.50±1.06 4.62±1.39 2.42±1.01 2.45±0.96 4.95±1.22 t 4.291 7.965 11.431 6.684 13.547 11.036 8.411 18.800 12.283 15.344 14.027 15.624 24.035 12.599 P<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001<0.001 95%CI 0.408-2.575 0.951-1.599 1.214-1.736 0.540-1.010 1.701-2.299 1.286-1.864 0.722-1.178 3.057-3.793 1.963-2.737 2.062-2.688 2.220-2.975 3.460-4.490 3.984-4.716 1.427-1.973
采用独立样本t检验分析比较对照组和干预组的疼痛影响评分,结果显示干预前(d0),两组之间的7项疼痛影响评分没有显著差异,基线可比。干预后(d56),干预组和对照组在疼痛对生活兴趣的影响方面没有差异;疼痛对日常生活、情绪、行走能力、正常工作、他人关系和睡眠的影响差异有统计学意义(P<0.05),干预组的疼痛改善更显著(表6)。
表6 两组患者干预前后疼痛影响评分比较Tab 6 Comparison of pain effect score between 2 groups before and after intervention ()
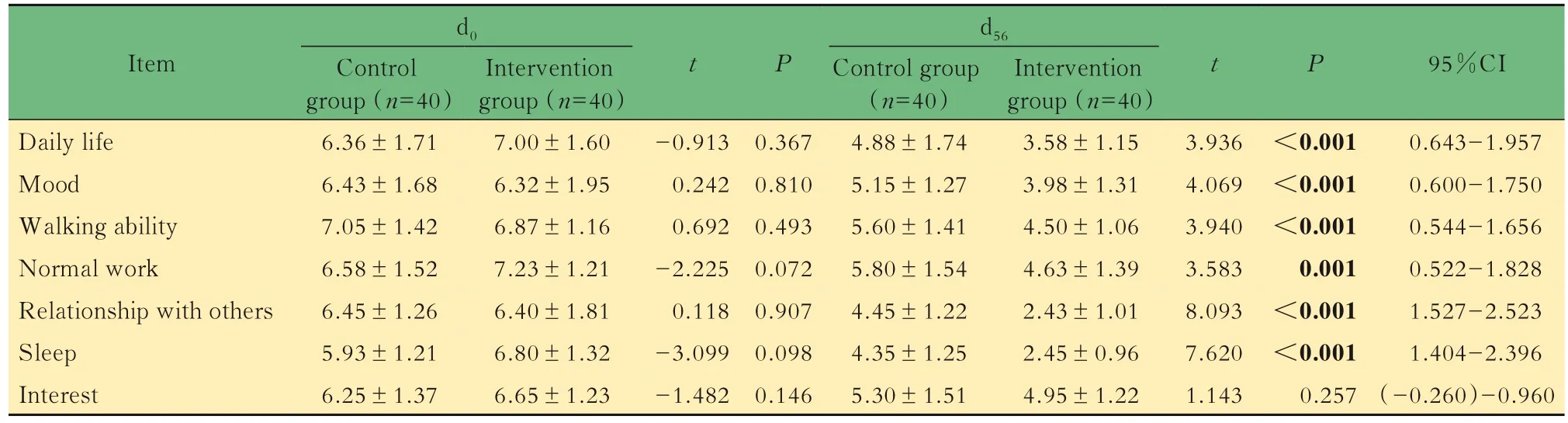
表6 两组患者干预前后疼痛影响评分比较Tab 6 Comparison of pain effect score between 2 groups before and after intervention ()
Item Daily life Mood Walking ability Normal work Relationship with others Sleep Interest d0 Control group(n=40)6.36±1.71 6.43±1.68 7.05±1.42 6.58±1.52 6.45±1.26 5.93±1.21 6.25±1.37 Intervention group(n=40)7.00±1.60 6.32±1.95 6.87±1.16 7.23±1.21 6.40±1.81 6.80±1.32 6.65±1.23 t-0.913 0.242 0.692-2.225 0.118-3.099-1.482 P 0.367 0.810 0.493 0.072 0.907 0.098 0.146 d56 Control group(n=40)4.88±1.74 5.15±1.27 5.60±1.41 5.80±1.54 4.45±1.22 4.35±1.25 5.30±1.51 Intervention group(n=40)3.58±1.15 3.98±1.31 4.50±1.06 4.63±1.39 2.43±1.01 2.45±0.96 4.95±1.22 t 3.936 4.069 3.940 3.583 8.093 7.620 1.143 P<0.001<0.001<0.001 0.001<0.001<0.001 0.257 95%CI 0.643-1.957 0.600-1.750 0.544-1.656 0.522-1.828 1.527-2.523 1.404-2.396(-0.260)-0.960
患者药物不良反应发生率的比较比较两组的总体不良反应发生率,发现干预组的不良反应发生率明显低于对照组,差异有统计学意义(35.0%vs.67.5%,P<0.05)。两组患者最常见的不良反应为便秘,其次为恶心、呕吐。
患者服药依从性的比较比较两组的服药依从性,发现对照组干预前(d0)服药依从性评分为5.90±0.25,干预后(d56)的服药依从性评分为6.08±1.19,差异无统计学意义(P=0.055);干预组干预前(d0)服药依从性评分为5.93±1.38,干预后(d56)的服药依从性评分为7.75±0.48,干预组通过药物治疗管理及用药宣教,服药依从性明显提高,差异有统计学意义(P<0.001)。
患者ECOG评分的比较比较两组的ECOG评分,对照组 干预前(d0)的ECOG评分为2.85±0.36,干预后(d56)的ECOG评分为2.73±0.45,差异无统计学意义(P=0.058);干预组干预前(d0)的ECOG评分为2.83±0.38,干预后(d56)的ECOG评分为1.83±0.71,干预组的患者生存质量明显提高,ECOG评分显著降低,差异有统计学意义(P<0.001)。
讨 论
肿瘤康复与姑息治疗首要解决的问题就是控制癌痛,2015年中国癌症统计数据显示,全国仍有约70%的癌痛患者未能接受有效的镇痛治疗[16]。有50%以上癌痛患者用药过程存在药物相关问题(DRPs)[8],癌痛患者服药依从性不佳、缺乏疾病及药物宣教、门诊随访体系不健全以及担心阿片类药物成瘾性是癌痛患者疼痛控制不佳的主要原因[17]。
药物治疗管理(MTM)指具备药学专业技术优势的药师对患者提供用药教育、咨询指导等一系列专业化服务,从而提高用药依从性、预防用药错误,最终达到实现患者进行自我管理,提高用药治疗效果的目的[18]。有研究显示,临床药师运用药物治疗管理,为高血压、糖尿病等慢病患者进行药物治疗管理,以解决患者的药物相关问题,可显著提高治疗效果、改善依从性、降低药物治疗安全性和经济费用[19]。
本次研究的结果显示,临床药师通过药学门诊,运用药物治疗管理为门诊癌痛患者提供全程化的药学服务,可显著改善门诊癌痛患者的疼痛治疗效果;改善疼痛对患者日常生活、情绪、行走能力、日常工作、与他人关系、睡眠等六方面产生的影响;降低药物不良反应发生率;提高患者的服药依从性,改善患者的生存质量。我们的研究证明了该药学服务模式在门诊癌痛患者规范化管理中的应用价值。在门诊癌痛患者的MTM方面,国内外研究者也都进行了积极的探索,证明MTM在癌痛规范化治疗中的应用,可以使癌痛患者的止痛治疗效果得到提升,提高患者用药依从性,降低药物相关不良反应发生率,提高患者生存质量和满意度等[11-13,20]。所有的研究都是基于MTM,围绕MTM的五大核心要素即信息收集、分析评估、计划制定、计划执行以及跟踪随访展开,这5个步骤形成一个完整的闭环,确保临床药师可以以患者为中心对患者的用药进行全方位、全时段、全领域的综合管理。但具体的工作模式、流程、工作职责、工作任务等方面还是存在一些差异。本研究通过独立的药学门诊开展MTM服务,同时运用信息化创建了门诊癌痛MTM管理系统,避免了纸质记录患者信息的繁琐,管理患者更加高效便捷,同时创建了患者微信群,实现线上和线下全方位、全时段互动,可以更好地服务患者,同时药学门诊和肿瘤内科临床医师的门诊同时段进行,药物相关问题和医师讨论沟通更加顺畅。
在对癌痛患者进行MTM中,药物相关问题最突出的就是癌痛治疗的有效性、药物不良反应和患者的依从性,其中药物不良反应和患者的依从性又直接影响治疗的有效性,因此临床药师需要特别关注患者的不良反应和依从性。通过药师的宣教和随访,患者的不良反应和依从性不佳得到改善,但仍有部分患者的不良反应改善并不明显,这可能与强阿片类药物本身的药物特点有关,其最常见且不可耐受的不良反应就是便秘,恶心、呕吐等其他的不良反应一般会随着服药时间的延长而逐渐减轻,作为临床药师要加强对患者或照看者进行宣教,当患者出现不良反应时给予生活或用药建议等人文关怀措施,也能在一定程度上改善患者的生活质量和治疗效果。
本次研究也有不足之处:(1)病例数量较少;(2)属于单中心研究,患者来源较单一。(3)部分患者或家属的依从性较差,合理用药意识缺乏。
综上所述,基于MTM的门诊癌痛患者全程化疼痛管理模式的效果评价,明确了该模式可显著改善门诊癌痛患者疼痛治疗效果,降低不良反应发生率、提高服药依从性、改善生存质量,为探索门诊癌痛规范化管理及药学服务模式提供了理论依据和方法学参考。
作者贡献声明高培培 数据收集、统计和分析,论文构思、撰写和修订。许晶晶 数据统计、分析、整理和保存。龚婧如 研究可行性分析,论文撰写指导。陆惠平 论文构思,研究监督和指导。
利益冲突声明所有作者均声明不存在利益冲突。
