微/纳米钼酸盐结构在锂离子电池负极材料中的应用
2022-10-20梁晨楠
梁晨楠,袁 松,吴 竹
应用研究
微/纳米钼酸盐结构在锂离子电池负极材料中的应用
梁晨楠1,袁 松2,吴 竹3
(武汉船用电力推进装置研究所,武汉 430064)
本文系统地总结了基于相关材料的金属钼酸盐的合成方法,如:水热法、共沉淀法、声化学法、燃烧法、溶胶-凝胶法和固态法。随后,对电极材料的设计和优化进行了详细的讨论和金属钼酸盐作为电极材料的电化学性能的证据。最后对开发高性能下一代锂离子电池做出了结论和展望。
钼酸盐 电化学储能 电极材料
0 引言
地球上的钼资源丰富。中国在世界上的比例最大,占已知储量的44%。美国紧随其后,占28%,智利排在第三位,占13%,这三个国家拥有大部分的钼资源。除了这三个国家,化学元素钼在加拿大的储量占了5%。俄罗斯和亚美尼亚的比例相同(2%)。其他国家共享剩余的1%的钼资源。金属钼酸盐化合物可作为无机缓蚀剂,金属缓蚀剂,用于腐蚀试验和光催化应用。
近年来,金属钼酸盐化合物MMoO4(M=Co、Zn、Mn、Fe、Ni等)已被证明是各领域的重要材料,引起了研究人员的浓厚兴趣[1]。通过利用不同金属钼酸盐组分之间的协同效应,成功地合成了含有多种金属钼酸盐化合物的纳米复合材料[2]。目前,已采用一系列实用的合成方法来合成特定的钼酸盐化合物,如:水/溶剂热法;共沉淀方法;声化学的方法;燃烧方法;溶胶-凝胶方法;固态的方法[3]。近年来,水/溶剂热法被广泛研究合成钼酸盐金属化合物。
金属钼酸盐晶体结构稳定,氧化还原性能好,物理化学性能优异,电导率高,是储能领域研究的热点之一[4]。此外,金属钼酸盐也可以提供许多其他优点,如:提供直流电路;缩短离子扩散距离;降低充放电时间;增加电解质-电极接触面积;适应容量的扩张和对环境友好。此外,锂离子电池(LIBs)作为全球便携式电子设备的首选技术已经产生了越来越大的影响[5]。因此,金属钼酸盐纳米技术的探索和应用对于提高锂离子电池的能量密度具有重要意义[6]。
本文系统地总结了基于相关材料的金属钼酸盐的合成方法,对电极材料的设计和优化进行了详细的讨论,展望了开发高性能下一代高性能锂离子电池的前景。
1 合成方法
1.1 水/溶剂热法
水热法的特点是在密封的反应釜中,水作为溶剂在高温高压下进行化学反应[7]。其原理主要是溶解再结晶过程。水热法具有以下优点:1)水热法受中温液相控制,能耗较低,适用性强;2)在水热反应中,通过调节反应温度、反应物浓度、反应时间、pH等因素,可以有效控制反应和晶体生长特性,从而得到理想的晶体结构和可控粒子的产物大小;3)产品无需热处理即可在热液条件下结晶,减少了颗粒的团聚和杂质的引入。水热法是开发高质量金属钼酸盐化合物的有效方法,许多纳米结构用水热法制备,将在以下部分更详细地描述这些方法。
例如,Sakthikumar等人通过SnCl2与Na2MoO4在十六烷基溴化铵(CTAB)胶束介质中持续搅拌反应制备了Sn(MoO4)2纳米材料[8]。首先,60 mL 0.1 M Na2MoO4和0.434 g CTAB混合在一起,然后连续搅拌30分钟左右。接下来,逐滴添加60毫升SnCl2乙醇溶液,60°C下搅拌约120分钟。然后,在高压反应釜中120°C加热10h。之后进行冷却,清洗,离心,80°C烘干,500°C煅烧。此外,当CTAB浓度较高时,合成产物颗粒的主要形态为针状Sn(MoO4)2。水热法制备Sn(MoO4)2纳米材料方法如图1所示:

图1 水热法制备Sn(MoO4)2纳米材料
此外,溶剂热法因其生产规模大、工艺简单、成本低、可扩展性好、分散性好等优点,也被广泛应用于合成钼酸盐金属化合物。然而,金属钼酸盐化合物的生长取向和晶体结构难以通过此方法控制。
1.2 共沉淀法
共同沉淀的方法包含一个或多个离子,通过添加沉淀剂(如OH−,CO32−,等等)水解形成不溶性的氢氧化物,氧化物或其他盐沉淀,原溶液中的阴离子冲走,其次是热分解或脱水,获得所需的氧化物粉末。
例如,Ramezani等人使用了一种共沉淀法合成了ZnMoO4纳米结构[9]。Zn(NO3)2·6H2O和(NH4)6Mo7O24·4H2O被用作前驱体。首先,在20 mL蒸馏水中搅拌并溶解(NH4)6Mo7O24·4H2O。之后,7mg Zn(NO3)2·6H2O和十二烷基硫酸钠混合在一起作为表面活性剂,并在蒸馏水中溶解,不断搅拌。随后,溶液冷却,将产品收集、清洗和干燥。在图2中清楚地展示了ZnMoO4纳米结构的形成方案。

图2 ZnMoO4纳米结构的形成方案
共沉淀法是一种简单的操作方法,对设备的要求很低,容易制备大量的产物,而且不容易吸收杂质。但缺点是制备颗粒的尺寸很难控制,粒度分布和表面性能不一致。要获得具有良好形态的纳米材料是非常困难的。
1.3 溶胶凝胶法
采用溶胶-凝胶法合成有机-无机杂化材料或无机纳米材料。溶胶-凝胶法包括凝胶化胶体溶液的凝胶和液相中其他胶体溶液的凝胶。在溶胶-凝胶过程中,将水与无机盐或金属盐混合制备的溶胶形成胶体悬浮液,通过聚合和/或水解反应,使液体溶胶通过三维网络转化成凝胶。
Pechini用溶胶-凝胶法成功合成了LiFe(MoO4)2[10]。首先,在10℃下,MoO3溶解于NH3·H2O和过氧化氢混合溶液。然后,Fe(C2O4)·2H2O溶解在硝酸溶液。随后,上面的两种溶液混合在一起,搅拌一定时间,然后加入一定量柠檬酸,保持溶液温度为60°C,确保外观像金属配合物溶液。之后,加入乙二醇,温度维持在90°C。金属、柠檬酸和乙二醇保持适当的化学计量比,得到凝胶。300℃下干燥和分解,然后通过煅烧将其转化为粉末。
2 锂离子电池
随着能源需求的增加,可再生能源的储存在开发更强大的电池中扮演着重要的角色。最近,锂离子电池的性能优于其他系统。锂离子电池由于其优异的电化学性能、低成本、环保、高能量密度和设计灵活性而引起了人们的广泛关注。过渡金属钼酸盐逐渐被认为是锂离子电池商业石墨负极的替代品,因为金属钼酸盐具有很好的氧化能力,因此金属钼酸盐化合物作为锂离子电池电极材料受到了广泛的关注。
2.1 单金属钼酸盐
FeMoO4作为一种重要的金属钼酸盐化合物,在LIBs电极材料中的应用得到了广泛的研究。此外,FeMoO4理论容量高,为992.3 mA h/g,并且Fe3+和Mo6+可转移9个电子。FeMoO4可作为一种有效的储锂负极材料,显示出更好的应用前景。
采用简单的水热法对单斜FeMoO4纳米棒进行了合理的设计和合成[11]。FeMoO4纳米棒的生长机理如图3d所示:首先形成FeMoO4核和H2MoO4。之后,FeMoO4颗粒合并成纳米棒,H2MoO4分解成MoO42−和H+的同时,MoO42−与Fe2+反应以形成FeMoO4颗粒。最后,FeMoO4纳米棒逐渐变长。样品的场分离扫描电镜(FE-SEM)图像显示纳米棒的长度可达几微米,如图3a所示。样品的透射电镜(TEM)图像显示FeMoO4棒,宽度仅50~150 nm,如图3b所示。
用恒电流充放电(GCD)曲线测定了FeMoO4纳米棒的电化学性质。虽然有很高的理论容量,但是容量迅速衰减,从1134年(第二圈)衰减到451mAh/g(第50圈),如图3c所示。由于电极表面出现了稳定的SEI膜,材料结构发生不可逆破坏,导致锂离子界面储存不可逆,容量迅速下降。随着电容逐渐增加,直到在第500次循环达到1265 mA h g-1。第500圈后,虽然容量逐渐减少,但第1000圈容量仍持续为1110mAh g-1。此外,在此期间,库仑效率从70%提高到99%,这是由于50个循环后SEI膜逐渐稳定。
结果表明,FeMoO4纳米棒的晶体生长与纳米片有关。此外,FeMoO4纳米棒具有较高的比容量和导电能力,使其成为锂离子电池的潜在负极材料。FeMoO4纳米棒具有良好的形貌和良好的电化学性能,可提供高比容量,促进导电能力,增加循环稳定性,这归因于其形貌和其结构特征。
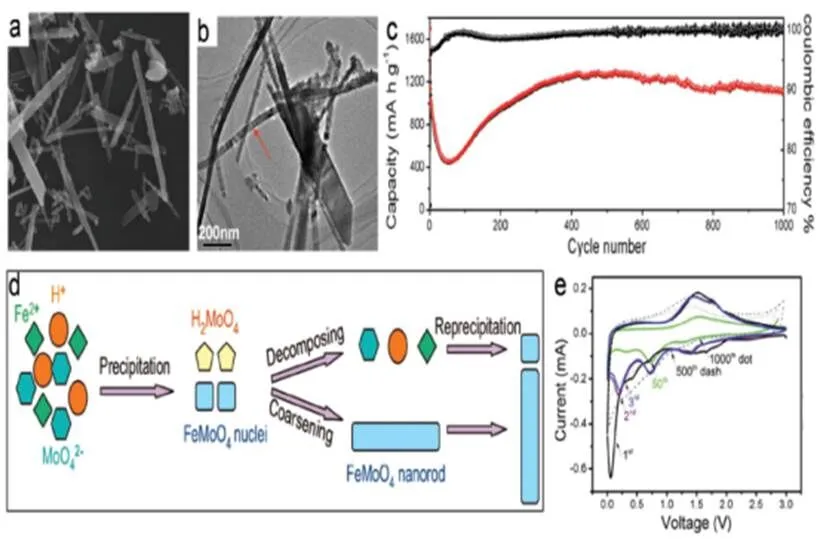
图3 FeMoO4的SEM,TEM,循环性能,生长机理和CV曲线
2.2 二元金属钼酸盐
用固体法制备了多晶形貌的LiFe(MoO4)2纳米材料[12]。将合适化学计量比的Li2CO3、Fe2O3和MoO3混合在一起,并根据其GCD和CV曲线作为LIBs的电极材料进行检测。如图4所示,在第1次放电反应中,可以明显地找到2个在2.57 V和1.74 V左右的平台,分别对应Fe3+、Mo6+到Fe2+、Mo4+的还原反应。在第一圈放电曲线中,比容量达到771 mAh/g。在低电压下,放电曲线变得光滑。之后,在2.57 V和1.74 V附近的平台逐渐消失,表明结构转变不完全。
除这些效果外,第2圈放电容量显示出1034mAh/g的更高的容量。与LiFe(MoO4)2的理论容量相对应。比较第2圈和第1圈的放电曲线,第2圈放电的高容量归因于不可逆转的电化学反应。在图4a的插入中显示了LiFe(MoO4)2的循环性能和库伦效率。在第1个循环中,放电比容量逐渐减少,稳定在580mAh/g。
LiFe(MoO4)2的CV曲线如图4b所示,在第1圈中,两个明显减少峰值在2.60 V和1.74 V之间,是因为从Fe3+到Fe2+和Mo6+到Mo4+的初始还原反应。在扫描电压逐渐下降的情况下,也可以观察到0.76V和0.26V的两个减少峰值,这可以归因于铁和钼的减少和SEI膜分层。在阳极扫描曲线中,由于从Fe到Fe3+和Mo到Mo6+的氧化反应,在1.45 V左右出现了可逆氧化峰值。
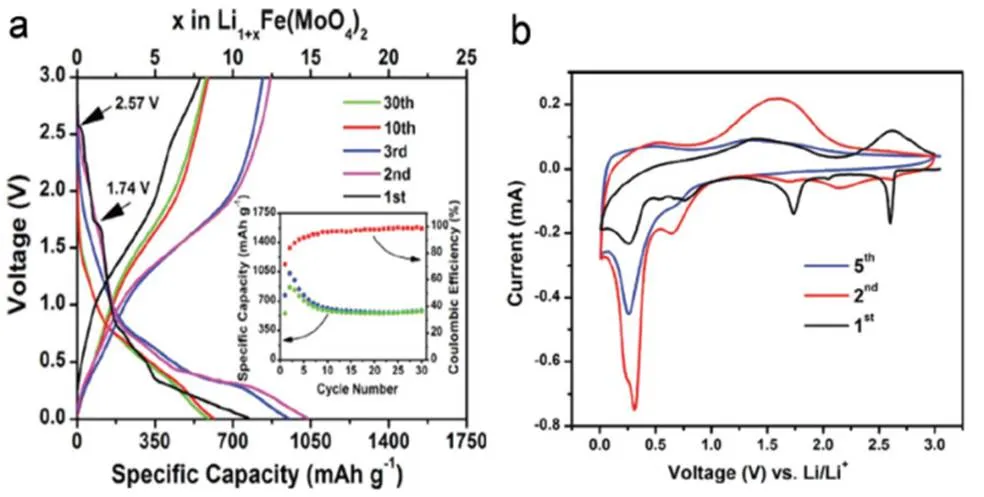
图4 多晶形貌LiFe(MoO4)2纳米材料的GCD和CV曲线
LiFe(MoO4)2纳米材料在电流密度为56mA/g时,其比容量为1034 mAh/g。此外,由于多电子反应性质,LiFe(MoO4)2纳米材料具有良好的性能,为将来的应用提供了环境。
2.3 石墨烯-金属钼酸盐
二维的碳原子单层石墨烯因其比表面积大、理论容量高、电化学性能好而被广泛研究作为负极材料。为了提高容量,研究人员合成了一系列过渡金属氧化物/石墨烯复合材料。与裸碳材料相比,这些复合材料具有很好的稳定性和较高的容量[32]。这种现象是由于高导电性石墨烯与具有高锂离子存储能力的过渡金属氧化物之间的协同化学耦合作用造成的。
采用水热法制备了掺杂在还原氧化石墨烯(CoMoO4NP/rGO)上的CoMoO4纳米粒子[13]。CoMoO4NP/rGO纳米复合材料的制备过程如图5a所示。一开始,合适化学计量比的Co(NO3)2·6H2O和H2MoO4通过搅拌与蒸馏水一起溶解。为了促进[Co(NH3)6]MoO4的形成,在上述溶液中添加了大量NH3·H2O。最后,[Co(NH3)6]MoO4分散在GO悬浮液中。由于氧化石墨烯表面的官能团和缺陷,超声处理后的氧化石墨烯表面吸附了Co3+和Mo6+。
SEM显示了CoMoO4NP/rGO的形貌和晶体结构特征,如图5b所示。多孔结构表明支架是由石墨烯片堆叠而成。然而,纳米颗粒不易通过SEM图像观察到,CoMoO4晶格的高倍TEM图像如图5c所示。很明显,这些微小的CoMoO4纳米颗粒嵌入到石墨烯表面而没有团聚,这导致了混合的CoMoO4NP/rGO纳米片的形成。
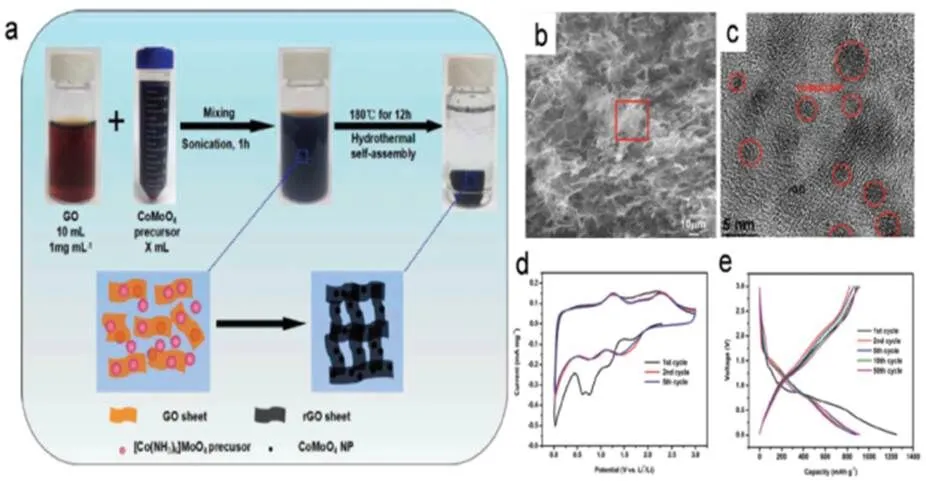
图5 CoMoO4 NP/rGO纳米复合材料的合成方法,SEM,CV和GCD曲线
由于CoMoO4NP/rGO纳米复合材料具有多层多孔结构和较高的表面积,使其具有较高的电化学性能、较好的循环稳定性和较短的锂离子扩散距离。基于这些结构细节,CoMoO4NP/rGO纳米复合材料作为锂离子电池的负极材料有很大的前景。
3 总结和展望
毫无疑问,对金属钼酸盐电极结构、电化学性能及其电荷存储机制的基本了解,是钼酸金属相关研究的重要组成部分。此外,还需要进一步研究电子、离子在活性电极材料和电解质传递中的行为。在大多数情况下,需要使用纳米大小的颗粒而不是散装材料,原因如下:
1)小尺寸的材料可以减少锂离子插入/提取过程中的物理压力。
2)高表面区域允许电解液和电极之间的接触面积增大,从而改善反应动力学。
3)纳米材料可以显著缩短锂离子扩散路径的长度。
因为钼酸的氧化性比其他阴离子基团要弱得多,而且它们的毒性很低,因此钼酸是一种强阳极氧化抑制剂。在水溶液中,钼是非氧化性或弱氧化抑制剂,这是钼在对环境的潜在污染中的微小优势。缺点是它们的缓蚀作用在某些组合中是很差的,目前的价格比较昂贵;单独使用时,所需的数量太大而不经济。因此,进一步的设计更简单的合成方法来增加材料的有效表面积,进一步减少电极材料的电阻仍然是主要的挑战。
[1] 李溪. 石墨烯基膜钼酸镍的制备与锂电性能的研究. [D]. 西安: 西北大学, 2018.
[2] Chen C J, Peng L F, Li Y J, et al. Granadilla-inspired structure design for conversion/alloy-reaction electrode with integrated lithium storage behaviors[J]. ACS Appl. Mater. Interfaces, 2017, 9: 15470-14576.
[3] 陈亚平. 高性能柔性钼酸盐复合纳米线电极的制备及其电化学性能的研究. [D]. 哈尔滨:哈尔滨工程大学, 2015.
[4] Chu S, Majumdar A. Opportunities and challenges for a sustainable energy future[J]. Nature, 2012, 488: 294-303.
[5] Cuan J, Zhou Y, Zhang J, et al. Multiple anionic transition-metal oxycarbide for better lithium storage and facilitated multielectron reactions[J]. ACS Nano, 2019, 13: 11665-11675.
[6] Guo YG, Hu JS, Wan LJ. Nanostructured materials for electrochemical energy conversion and storage devices, Adv. Mater.[J], 2008, 20: 2878-2887.
[7] 喻嘉. 基于过渡金属氧化物的微纳多级复合材料的设计制备及储锂性能研究. [D]. 北京: 中国科学院程工程研究所, 2018.
[8] Xiao Y, Hwang JY, Sun YK. Micro-intertexture carbon-free iron sulfides as advanced high tap density anodes for rechargeable batteries. ACS Appl. Mater. Interfaces[J], 2017, 9: 39416-39424.
[9] Zhu YP, Zhong YJ, Chen G, et al. A hierarchicalZn2Mo3O8nanodots-porous carbon composite as a superior anode for lithium-ion batteries, Chem. Commun[J]., 2016, 52: 9402-9405.
[10] Chen N, Yao Y, Wang DX, et al. LiFe(MoO4)2asa novel anode material for lithium-ion batteries, ACS Appl. Mater. Interfaces[J], 2014, 6: 10661-10666.
[11] Ju ZC, Zhang E, Zhao YL, et al. One-pot hydrothermal synthesis of FeMoO4 nanocubes as an anode material for lithium-ion batteries withexcellent electrochemical performance. Small[J], 2015, 11: 4753-4761.
[12] Wang JX, Zhang GB, Liu ZM, et al. Li3V(MoO4)3as a novel electrode material with good lithium storage properties and improved initial coulombic efficiency, Nano Energy[J], 2018, 44: 272-278.
[13] Yang T, Zhang HN, Luo YZ, et al. Enhanced electrochemical performance of CoMoO4nanorods/reduced graphene oxide as anode material for lithium-ion batteries, Electrochim. Acta[J], 2015, 158: 327-332.
Fabrication of metal Molybdate Micro/Nanomaterials for electrochemical energy storage
Liang Chennan1, Yuan Song2, Wu Zhu3
(Wuhan Institute of Marine Electric Propulsion, Wuhan 430064, China)
TM612
A
1003-4862(2020)10-0040-04
2011-09-09
梁晨楠(1994-),男,助理工程师。研究方向:锂离子电池电极材料。
