仑伐替尼和卡瑞利珠单抗联合TACE术治疗晚期或不可切除肝细胞癌临床疗效
2022-10-19朱方魏娟赵慧慧蒋文朱传东
朱方,魏娟,赵慧慧,蒋文,朱传东
(南京中医药大学附属南京医院/南京市第二医院/南京市肿瘤医院 肿瘤科,江苏 南京 210003)
全球每年有大约一半的肝癌新发和死亡病例发生在我国,肝癌在我国的发病率和死亡率分别占实体恶性肿瘤的第四位和第二位[1- 2],病理类型主要包括肝细胞癌(hepatocellular carcinoma,HCC)和胆管细胞癌,其中HCC占70%~85%[2],是临床治疗的难点。肝癌常发生在既往慢性肝炎、肝硬化、酒精性肝硬化等基础上[3]。因症状隐匿,大部分患者确诊时已到晚期,失去手术机会。对化疗的不敏感导致在过去的几十年间HCC一直缺乏高效的治疗手段[4]。多激酶抑制剂索拉非尼是肝癌治疗的划时代的靶向药物,将肝癌的总生存时间(overall survival,OS)延长了3个月[5- 6],从2008年获批以来一直是晚期HCC的唯一的靶向治疗选择,直到近年随着新的靶向药物仑伐替尼和免疫检查点抑制剂的出现,给晚期肝癌或不可切除肝癌患者带来更多的选择[7]。依据REFLECT Ⅲ期临床试验,仑伐替尼具有比索拉非尼出色的客观缓解率(overall response rate,ORR)、疾病进展时间(time- to- progress,TTP),仑伐替尼获FDA批准用于HCC一线治疗。免疫治疗包括PD- 1抑制剂在多项临床试验(包括CheckMate- 040、KEYNOTE- 224、KEYNOTE- 224)中已证实对HCC的临床效果,已获准用于HCC的二线治疗。近来免疫治疗联合靶向治疗是恶性肿瘤研究领域的热点,也是不可切除HCC治疗的方向和突破点。依据KEYNOTE- 524临床试验,仑伐替尼联合帕博利珠单抗已获FDA批准用于晚期HCC一线治疗[8- 10]。纳武单抗联合仑伐替尼一线治疗晚期HCC的Ib期临床研究结果更优于帕博利珠单抗联合仑伐替尼[11]。CSCO指南推荐PD- 1单抗用于晚期HCC的一线及二线治疗。肝动脉化疗栓塞术(transhepatic arteerial chemotherapy and embolizatio- n,TACE)主要通过化疗药物联合微粒、微球栓塞肿瘤的供血动脉,阻断肿瘤的血供,从而引起肿瘤组织的缺血坏死。已经有研究表明,索拉非尼与TACE联合可获得更长的生存期,而TACE联合仑伐替尼和PD- 1抑制剂的研究仍较少,是否有优势仍是困惑临床医生的课题。受到PD- 1抑制剂联合仑伐替尼前期临床试验的鼓舞,也鉴于相关临床研究数据较少,尚缺乏一线治疗的Ⅲ期临床试验结果,更缺乏联合TACE的相关研究数据,本研究回顾性分析我院一线使用国产PD- 1抑制剂卡瑞利珠单抗和仑伐替尼联合或不联合TACE治疗晚期或不可切除HCC的临床数据,探讨相关疗效及安全性,为临床HCC的治疗提供参考依据。
1 资料与方法
1.1 一般资料
回顾性分析2019年1月至2021年6月南京市第二医院接受仑伐替尼和卡瑞利珠单抗联合(LPT组,44例)或不联合(LP组,28例)TACE治疗的72例晚期或不可切除肝细胞癌患者的临床资料,患者经病理组织学明确诊断,或综合病史、影像学检查、AFP结果而临床诊断,既往未接受其他抗肿瘤治疗,肝功能Child- Pugh分级为A或B,两组患者的临床特征见表1。所有患者均未行PD- L1检测,所有患者治疗前均签署免疫治疗同意书及靶向治疗同意书。
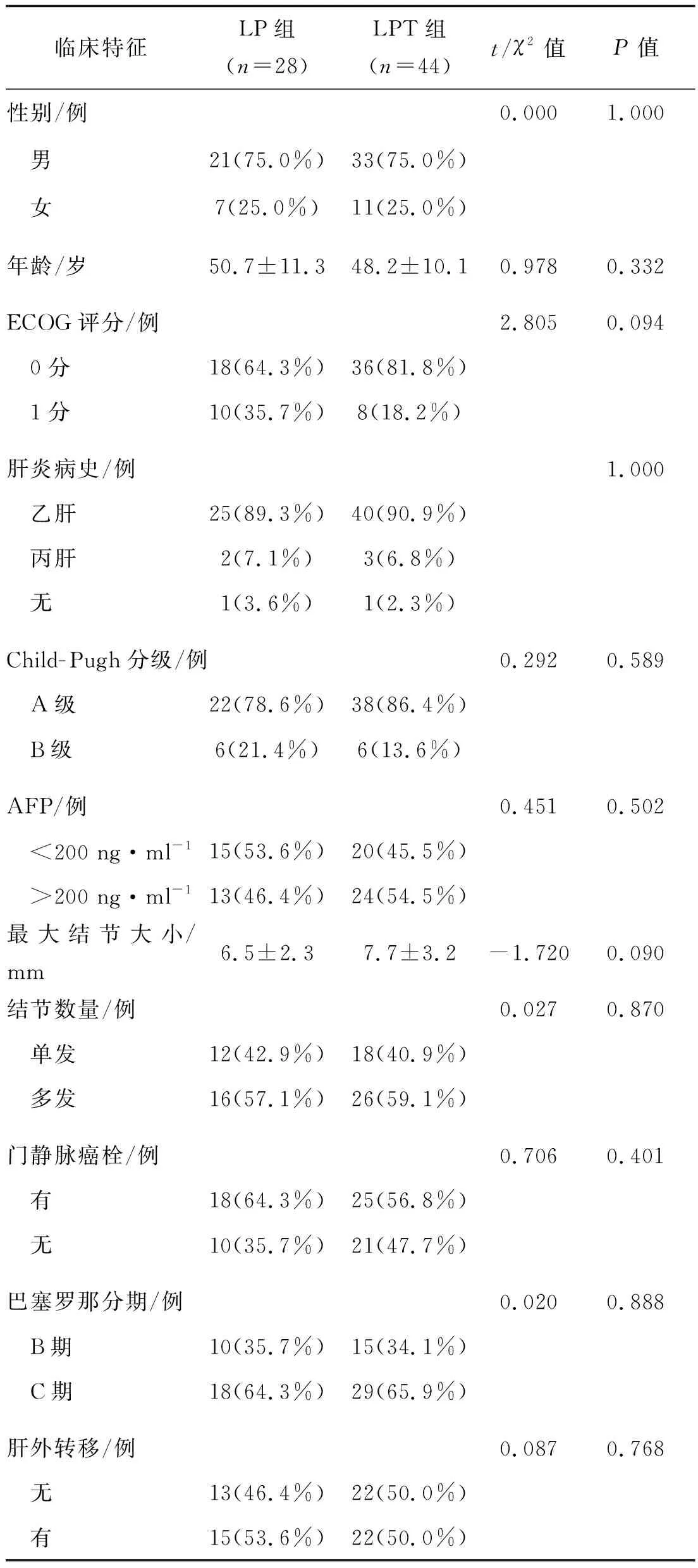
表1 两组患者临床特征的比较
1.2 治疗方法
1.2.1 LPT组 卡瑞利珠单抗200 mg静脉滴注,每3周1次;仑伐替尼(体重>60 kg 12 mg,体重<60 kg 8 mg )口服,1次·d-1。TACE:介入科行洛铂20 mg及微粒、微球灌注栓塞化疗,1个月行1次,最多不超过3次;患者在首次TACE术后1周内开始仑伐替尼及PD- 1治疗。免疫治疗至少2周期,仑伐替尼至少治疗42 d,TACE治疗至少1次。
1.2.2 LP组 卡瑞利珠单抗200 mg静脉滴注,每3周1次;仑伐替尼(体重> 60 kg 12 mg,体重<60 kg 8 mg )口服,1次·d-1。
两组患者每个周期治疗前均例行检查血常规、肝肾功能、电解质、凝血功能、甲状腺功能、心肌酶谱、心电图、心脏彩超,每2周期行1次胸腹部增强CT评估疗效。
1.3 疗效评估
治疗期间每2周期复查胸腹部增强CT或MRI评估病情及效果,参照mRECIST标准[12]评估肝内病灶,参照RECIST1.1标准[13]评估肝外转移病灶。治疗效果包括完全缓解(complete response,CR)、部分缓解(partial response,RR)、疾病稳定(stable disease,SD)、疾病进展(progressive disease,PD)。客观缓解率(objective response rate,ORR)为CR率和PR率之和,疾病控制率(disease control rate,DCR)为CR、PR、SD率之和。疾病进展时间(time to progression,TTP)为治疗开始到进展或死亡的时间间隔,总生存时间(overall survival,OS)为治疗开始到癌症相关的死亡时间间隔。观察患者治疗期间不良反应,依据CTCAE标准评价,分为0至4级[14]。
1.4 随访
随访截至2021年6月30日,以门诊复查或住院的形式随访相关实验室指标,中位随访时间为18个月,随访率100%。
1.5 统计学处理
采用SPSS 28.0软件进行统计学分析,服从正态分布的计量资料采用均数±标准差表示, 两组间均数比较采用独立样本t检验,计数资料用频数(百分比)表示,两组比较采用χ2检验。采用Kaplan- meier法对生存资料进行描述,并采用Log- rank检验和Cox回归对生存曲线进行比较。P<0.05为差异有统计学意义,所有检验均为双侧检验。
2 结 果
2.1 两组疗效的比较
LPT组的ORR为40.9%,高于LP组(17.9%,P=0.041),LPT组DCR为79.5%,高于LP组(53.6%,P=0.020)。见表2。

表2 两组疗效的比较
2.2 两组生存情况的比较
中位随访时间为11.5个月。LPT组3、6、12个月的生存率别为97.7%、88.0%和75.7%,LP组分别为89.0%、63.5%和20.2%。LPT组中位OS为15.7个月,平均OS为13.60个月,LP组中位OS为9.7个月,平均OS为9.20个月,两组OS比较差异有统计学意义(P=0.005,HR=0.36,95%CI0.17~0.76)。LPT组3、6、12个月的无进展率分别为92.9%、80.3%和50.9%, LP组分别为85.1%、57.8%和16.8%。LPT组中位TTP为13.00个月,平均TTP为12.14个月,LP组中位TTP为8.6个月,平均TTP为8.42个月,两组TTP比较差异有统计学意义(P=0.016,HR=0.43,95%CI0.22~0.87)。两组生存曲线见图1。
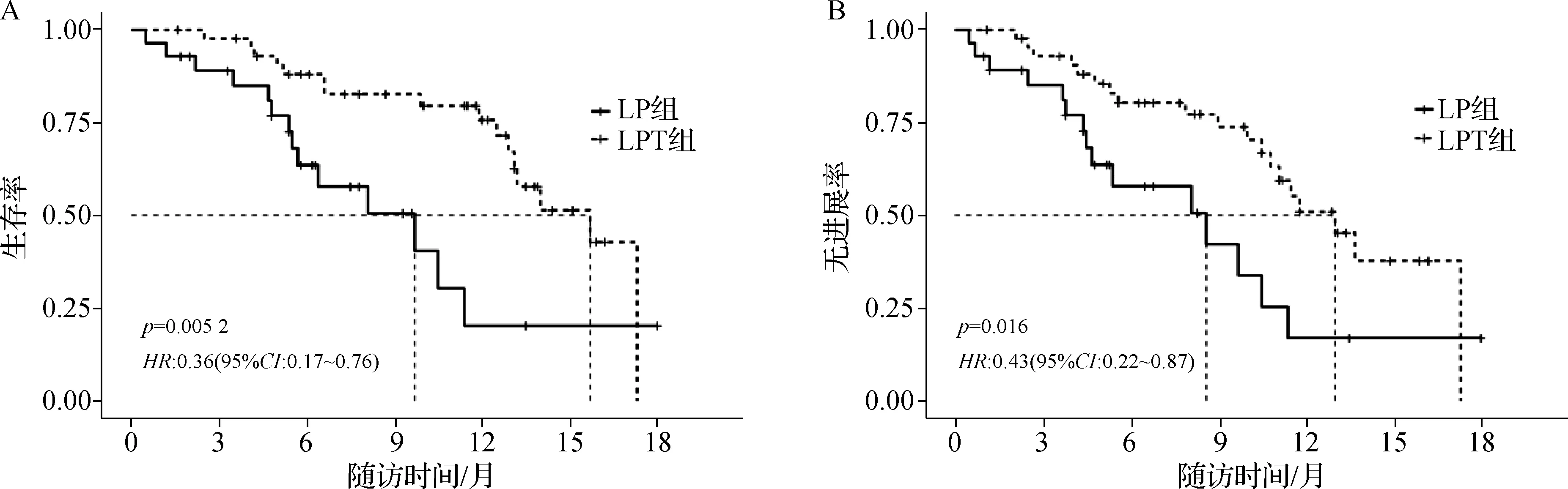
A.OS曲线;B.TTP曲线图1 LPT组和LP组患者的OS曲线及TTP曲线
2.3 两组不良反应发生情况
72例患者均发生了不同程度的不良反应,但均为轻中度和可控的。LPT组不良反应发生率为发热40.9%、疼痛27.3%、疲乏20.5%、高血压6.8%、食欲下降18.2%、腹泻11.4%、皮疹9.1%、尿蛋白4.5%、甲状腺功能减退2.3%、手足综合征6.8%、肝功能损害43.2%、血小板减少6.8%。LP组不良反应发生率为发热14.3%、疼痛10.7%、疲乏17.9%、高血压7.1%、食欲下降7.1%、腹泻10.7%、皮疹7.1%、尿蛋白3.6%、甲状腺功能减退3.6%、手足综合征7.1%、肝功能损害14.32%、血小板减少3.6%。两组除发热(χ2=5.716,P=0.017)和肝功能损害(χ2=6.572,P=0.010)以外,其他不良反应的发生率差异无统计学意义(P>0.05)。两组共有8例患者发生3级不良反应,其中4例为3级疲乏,予仑伐替尼减量至8 mg后好转,4例为3级高血压,予钙通道拮抗剂口服后降至正常,继续原方案治疗;无4级不良反应发生。无患者因不良反应中断治疗。
3 讨 论
HCC在我国发病率高,恶性程度高,很多患者发现时已失去手术机会,而肝癌对化疗不敏感,治疗手段以前主要以化疗栓塞、消融等方法为主,而随着对肝癌发病机制的深入研究,靶向治疗和PD- 1免疫治疗对晚期肝癌的治疗发挥着越来越重要的作用,尤以仑伐替尼联合PD- 1抑制剂的组合成为治疗晚期或不可切除HCC的全身治疗“黄金组合”方案之一。临床实践中,局部治疗联合全身治疗因可以增加肿瘤的局部控制率而被广泛应用。既往研究[15]表明,索拉非尼联合TACE对比索拉非尼单药可提高OS达87.5%,延长6.24个月,提示TACE联合靶向治疗有生存获益,然而相关研究却很少。我们的回顾性研究提示晚期肝癌中,联合TACE与仑伐替尼、卡瑞利珠单抗可以获得更好的TTP及OS。
仑伐替尼是除索拉非尼外的另一种口服小分子多激酶抑制剂,可选择性抑制VEGFR1- 3、FGFR1- 4、PDGFR2、FGF和RET等靶点抑制肿瘤血管的生成和生长。REFLECT试验是一项Ⅲ期随机、多中心、开放、非劣效临床试验,比较仑伐替尼和索拉非尼在不可切除肝癌患者一线治疗中的疗效,共纳入954例患者,结果显示OS分别为13.6、12.3个月,PFS分别为8.9、3.7个月[7]。2018年FDA批准仑伐替尼作为第二个用于晚期HCC一线治疗的靶向药物。但遗憾的是,在OS方面未有统计学优势。
CheckMate- 040研究[16]提示PD- 1抗体Nivolumab在晚期肝癌二线治疗中ORR为20%,DCR为58%,OS 15.1个月,2017年已被FDA批准第一个用于晚期肝癌的二线治疗。受此鼓舞,CheckMate- 459研究[11]比较了Nivolumab和仑伐替尼一线治疗晚期肝癌的OS,分别为16.4、14.7个月,ORR分别为15%、7%。这些研究奠定了PD- 1抑制剂用于晚期肝癌治疗的地位,但是纳武价格昂贵,国内人群选择较为困难,针对这一窘境,国产的PD- 1抑制剂的研发和临床试验,得到了令人鼓舞的结果。
理论上,多靶点酪氨酸激酶抑制剂TKIs通过阻断肿瘤血管的生成和生长而起到抗肿瘤作用,而其暴露可增加炎症细胞浸润[17- 18],此外,TKIs的耐药与免疫抑制微环境有关,通过增加T- reg细胞活性和PD- L1过表达维持,两者有协同增效作用[19- 21],这些理论基础引起了研究者们对PD- L1联合TKIs治疗的期待。Keynote- 524(Ib期)研究了pembrolizumab联合仑伐替尼的剂量限制毒性,PFS为9.3个月,OS为22.0个月[22]。鉴于该结果,2019年7月FDA授予该联合药物突破性治疗称号。一项Ⅲ期开放性临床试验LEAP- 002,研究了PD- 1联合仑伐替尼对比仑伐替尼单药一线治疗晚期HCC的临床疗效,期待结果的发布[23]。本研究中,LP组的TTP和OS数据均小于Keynote- 524相关数据,可能与本研究中患者分期相对较晚、肿瘤平均直径较大及门脉癌栓比例高有关。
TACE是指南唯一推荐中晚期肝癌的局部治疗方法,对晚期或不可切除HCC有较高的局部控制率,且绝大部分患者安全可耐受。TACE联合靶向及免疫治疗,不同作用机制联合,起到了“1+1+1>3”的近期及长期疗效。本研究中,与LP组相比,LPT组获得了更高的ORR、DCR,而且不良反应可耐受。
综上所述,仑伐替尼联合卡瑞利珠单抗及TACE显示了更好的近期及远期疗效,不良反应可耐受,但本研究也存在病例数较少、为回顾性分析、分析过程中可能存在统计偏倚等局限性,后续将会进一步扩大病例数,争取推动多中心随机对照试验,获得更可信的临床数据。
