HPLC法测定氯地松乳膏中氯霉素含量及其稳定性研究
2022-10-15赵柳娅印杰张建中翁静艳
赵柳娅 印杰 张建中 翁静艳
(复旦大学附属中山医院药剂科 上海 200032)
氯地松乳膏为复旦大学附属中山医院自制制剂,以氯霉素和醋酸地塞米松为主药成分,辅料为轻质液状石蜡、甘油、白凡士林、单硬脂酸甘油酯等[1],临床上主要用于神经性皮炎、接触性皮炎、慢性湿疹、局限性瘙痒症等证,效果良好。氯地松乳膏中含氯霉素1%和醋酸地塞米松0.025%,氯霉素对革兰阳性菌、革兰阴性菌和厌氧菌均具抗菌作用[2],制剂质量标准中仅要求测定氯霉素的含量,方法为紫外分光光度计一阶导数法,其影响因素较多;《中华人民共和国药典》(简称《中国药典》)(2020年版二部)收载的氯霉素及其制剂的含量测定方法均为高效液相色谱(high performance liquid chromatography, HPLC)法,该法具有重复性好、灵敏度高等优点[3-4]。已有文献报道氯霉素化学性质不稳定,在生产和储存过程中易水解,从而影响抗菌活性[5],并且存贮和使用过程中遇到温度升高可能会导致氯地松乳膏成分的改变,从而影响其使用安全,因此,氯地松乳膏的说明书指出保存条件为遮光、密闭保存。为确保制剂的安全、有效,本文参考《中国药典》(2020年版二部)氯霉素含量测定方法及相关文献方法[6-8],考察氯霉素受存储条件的影响情况,为氯地松乳膏存储条件提供合理化建议,保证产品在有效期内的稳定性。
1 材料与方法
1.1 仪器
Aglient 1260型高效液相色谱仪(安捷伦科技有限公司);BS124S型电子天平(北京赛多利斯仪器系统有限公司);超声波清洗仪(必能信超声有限公司);水浴锅(上海精宏实验设备有限公司);药品稳定性试验箱(立德泰勀科学仪器有限公司);LRH-150生化培养箱(上海一恒科技有限公司);MJ-150-Ⅰ霉菌培养箱(上海一恒科技有限公司);冰箱(博西家用电器中国有限公司);DJ-Ⅱ型均质器(上海炳隆机电设备有限公司);Milliflex Plus微生物过滤系统(美国默克集团)。
1.2 试药
试药氯地松乳膏(批号:L-061901、L-031901、L-012701、L-030601、L-030602、L-030603,复旦大学附属中山医院制剂室);氯霉素对照品(中国食品药品检定研究院,纯度99.4%);氯霉素二醇物对照品(中国食品药品检定研究院,纯度99.5%);甲醇(美国天地有限公司)为色谱纯,其余试剂为分析纯;磷酸(永华化学科技有限公司);三乙胺(永华化学科技有限公司);1-庚烷磺酸钠(永华化学科技有限公司);磷酸二氢钾(上海凌峰化学试剂有限公司);乙醇(上海凌峰化学试剂有限公司);水为纯化水;胰酪大豆胨琼脂培养基(上海中科昆虫生物技术开发有限公司);胰酪大豆胨液体培养基(上海中科昆虫生物技术开发有限公司);沙氏葡萄糖琼脂培养基(上海中科昆虫生物技术开发有限公司);甘露醇氯化钠琼脂培养基(上海盛思生化科技有限公司);溴化十六烷基三甲铵琼脂培养基(上海中科昆虫生物技术开发有限公司);pH 7.0无菌氯化钠-蛋白胨缓冲液(上海盛思生化科技有限公司)。
菌种金黄色葡萄球菌、枯草芽胞杆菌、白色假丝酵母、黑曲霉、铜绿假单胞菌,来源均为中国药品生物制品检定所。
1.3 方法
1.3.1 色谱条件与系统适应性试验
色谱柱:Aglient 5TC-C18(250 mm×4.6 mm,5 μm);流动相:0.01 mol/L 1-庚烷磺酸钠缓冲溶液(取磷酸二氢钾6.8 g,用0.01 mol/L 1-庚烷磺酸钠溶液溶解并稀释至1 000 mL,再加三乙胺5 mL,用磷酸调pH至2.5)-甲醇(68∶32,V/V);检测波长:277 nm;流速:1.0 mL/min ;柱温 25 ℃ ;进样量 :10 μL。
1.3.2 溶液的制备
1)对照品溶液的制备 精密称取氯霉素对照品10.28 mg,置于100 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得浓度为102.98 μg/mL的氯霉素对照品溶液;精密称取氯霉素二醇物对照品10.50 mg,置于10 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,取上述溶液1 mL置100 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀即得浓度为10.45 μg/mL的氯霉素二醇物对照品溶液。
2)供试品溶液的制备 精密称取氯地松乳膏 0.5 g,置于50 mL量瓶中,加甲醇适量超声30 min,放至室温,加甲醇稀释至刻度,摇匀,过滤,作为供试品溶液。
3)阴性样品溶液 按处方配制缺少氯霉素的阴性样品,并按上述供试品溶液的制备的操作配制阴性样品溶液。
2 结果
2.1 专属性试验
分别吸取溶剂、阴性样品溶液、对照品溶液、供试品溶液,按1.3.1项下的色谱条件测定,记录色谱图(图1)。由图1可知,制剂中存在的杂质不干扰氯霉素的测定。

图1 HPLC图
2.2 线性关系考察
精密称取氯霉素对照品25.9 mg,置于20 mL量瓶中,加甲醇溶解并稀释到刻度,摇匀,作为氯霉素对照品贮备液。精密量取上述氯霉素对照品贮备液适量并用甲醇稀释制得浓度分别为5.149、10.298、20.596、102.98、205.96、514.89 μg/mL的系列溶液,按1.3.1项下色谱条件进样。以氯霉素峰面积为纵坐标(y),质量浓度为横坐标(x),进行线性回归,得回归方程y=1 759.284 3x+7.778 8(r=1.000 0)。结果表明,氯霉素检测质量浓度在5.15~514.89 μg/mL范围内与峰面积积分值呈良好的线性关系。
2.3 精密度试验
取对照品溶液适量,按1.3.1项下色谱条件连续进样6次,测定。结果显示,氯霉素峰面积的RSD=0.74%,说明仪器的精密度良好。
2.4 稳定性试验
取供试品溶液适量,于室温下放置,按1.3.1项下色谱条件,分别于0、2、4、10、16、22、24 h时进样测定。结果显示,氯霉素峰面积的RSD=0.64%,表明供试品溶液在24 h内质量基本稳定。
2.5 重复性试验
取样品适量,共6份,按1.3.2项下的方法制备供试品溶液,按1.3.1项下色谱条件进样测定。结果显示,RSD=1.8%,表明本方法的重复性较好。
2.6 加样回收率试验
精密称取氯地松乳膏空白基质0.5 g,按已知量的80%、100%、120% 3个浓度加入氯霉素对照品。按供试品溶液的制备方法分别处理低中高浓度各3份样品共9份,按1.3.1项下色谱条件进样测定,计算回收率(表1)。
2.7 样品含量测定
取3批氯地松乳膏,按1.3.2项下的方法制备供试品溶液,平行制备2份,按1.3.1项下色谱条件进样测定,以峰面积计算氯霉素的含量(表2)。

表2 氯地松乳膏样品中氯霉素含量测定
2.8 制剂稳定性试验
2.8.1 性状
肉眼观察医院制剂氯地松乳膏0、1、2、3、6、9、12个月的外观性状。结果氯地松乳膏在12个月内外观无明显变化。
2.8.2 加速稳定性试验
根据原料药物与制剂稳定性试验指导原则[9],结合医院制剂的特殊性,将氯地松乳膏样品(L-061901、L-031901、L-012701)按现有包装在温度(30±2)℃,RH(65%±5%)条件下放置,分别于第0、1、2、3、6个月取样,按稳定性重点考察项目进行检测,检验结果见表3。结果表明,按稳定性重点考察项目进行检查,各检测项目与0个月数据比较,氯地松乳膏中氯霉素含量下降较明显且超出规定范围。
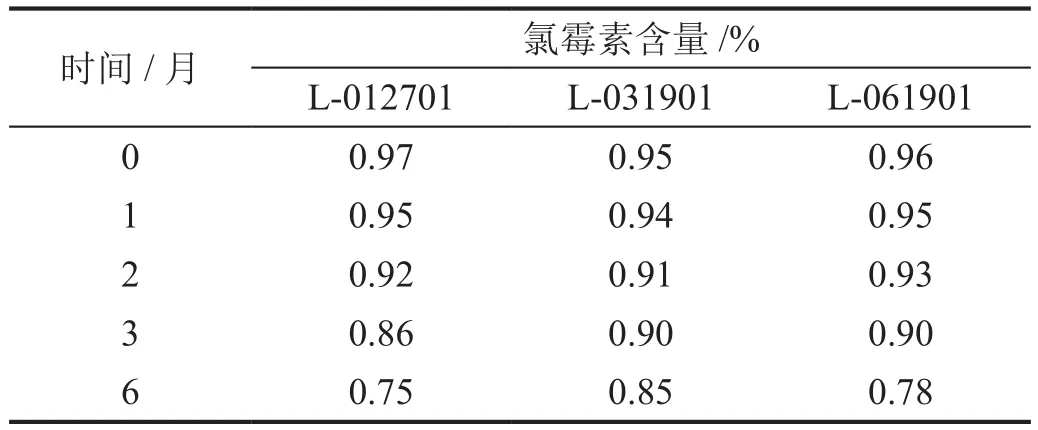
表3 不同批号氯地松乳膏加速稳定性试验
2.9 长期稳定性试验
根据原料药物与制剂稳定性试验指导原则[9],结合医院制剂的特殊性,将氯地松乳膏样品(L-061901、L-031901、L-012701)按现有包装在温度(5±3)℃冷处贮存条件下放置,分别于第0、3、6、9、12个月取样,按稳定性重点考察项目进行检测,检验结果见表4。结果表明,按稳定性重点考察项目进行检查,各检测项目与0个月据比较无显著性变化,均符合规定。

表4 不同批号氯地松乳膏长期稳定性试验
2.10 微生物限度检查
按《中国药典》(2020年版四部)通则1105、1106、1107的非无菌产品微生物限度检查法进行[9],于0、3、6、9、12个月分别检查供试品中需氧菌、霉菌和酵母菌、金黄色葡萄球菌和铜绿假单胞菌,结果均符合规定。
3 讨论
本试验参考《中国药典》(2020年版二部)中的氯霉素含量测定方法,借助HPLC法建立了一种操作简便、结果准确、专属性强、重复性好的分析方法,为氯地松乳膏中氯霉素含量测定提供了理论依据。我院制剂氯地松乳膏质量标准中含量测定的方法是紫外分光光度计一阶导数法,由于一阶导数法干扰因素较多,准确度不高,现改为高效液相色谱法测定其含量。本方法简便、灵敏、准确、重现性好、专属性强,适用于本品的含量测定,为该制剂的质量标准提高提供了参考。
外观性状检查表明,氯地松乳膏在12个月观察期内无明显变化,因为它是油包水型乳膏剂,失水不明显;但加速试验和长期试验表明,本制剂对贮藏温度较为敏感,在常温下不稳定,其有效分成的含量有一定的变化。文献报道,氯霉素易水解生产氯霉素二醇物,氯霉素的分解产物氯霉素二醇物随温度升高和放置时间的延长,其含量也随之升高;在冷处贮存氯地松乳膏相对稳定[9]。氯地松乳膏原贮藏条件为遮光、密闭保存,现建议修改为遮光、密闭、在冷处贮存。同时,建议对氯地松乳膏的配制工艺进行改进,如添加辅料吐温80增加氯霉素的稳定性[10]、对氯霉素进行环糊精包合[11]等方法进一步提高其质量稳定性。
综上所述,本研究以制剂性状、氯地松乳膏中氯霉素的含量变化、微生物限度等项目为指标,考察了氯地松乳膏的稳定性,为制剂质量标准提高、有效期的确定及贮存条件的改进提供了参考依据。
