供水镀锌钢管腐蚀机理与监测技术研究现状
2022-10-13黄明风马湘蒙
黄明风,魏 群,马湘蒙
(广西大学 资源环境与材料学院,南宁 530004)
随着居民生活水平不断提高,饮用水水质标准和供水管网的安全运行受到了广泛的关注。《2020年城乡建设统计年鉴》公布的数据显示,我国城镇供水管网系统总长度约1.0×106km。管网系统的问题和风险主要表现为管道腐蚀导致的水质恶化、管道漏失以及管道爆裂等现象[1]。供水管材主要为金属管、塑料管和复合管三大类,其中以金属管道为主,约为85%。供水管网中塑料管因成本低和腐蚀性低逐渐替代金属管道,但由于工作温度、工作压力以及质量稳定度等影响,其实际应用存在较大局限性。以聚氯乙烯管(polyvinyl chloride,PVC)为例,虽然便于安装,且具有良好的抗腐蚀能力,但由于其刚性和耐高温能力较差,在管道阀门突然关闭或者打开时,管道内水流对阀门及管壁压力急剧变化的“水锤效应”易造成PVC管道破裂,因此,塑料材质管道多应用于冷水管道[2]。随着材料科学的逐渐深入发展,由金属与塑料材料相结合而成的复合型管道应用范围也随之扩大。铝塑复合材料因具有良好的耐腐蚀性能、化学稳定性、水力性能以及机械性能等优势引起了关注。除此之外,国家对铝塑复合材料相关技术进行了产业扶持和技术引进,但铝塑复合材料存在耐高温性差、管径小、相关产品生产与监管尚不完善等问题,因此,塑料复合管的发展受到了限制[3]。
镀锌钢管具有良好的强度、刚度、抗冲击能力以及杂质含量低等优势,其普遍应用在供水管网入户管道的铺设。但其长期使用所产生的管道腐蚀会引起重金属的释放,从而危害饮用水安全,造成较大的经济损失。研究数据表明,每年美国饮用水系统因腐蚀产生的直接成本约为两千亿人民币;每年我国供水系统由于腐蚀造成的损失约为两百亿人民币[4-5]。供水管道长期与水体反应形成腐蚀垢层,增加了输水能耗,腐蚀垢层脱落进入水体,引起水质恶化。同时,水体中的余氯和溶解氧等氧化剂的消耗会使水体浊度及游离重金属离子含量增加,而微生物在内壁上的积累使得管网腐蚀加剧[6-8],对人体健康产生了潜在的威胁。因此,这也对镀锌钢管的防腐工作带来巨大的挑战。目前主要的防腐途径是通过改变管道的水体环境、进行电化学保护或对管道表面涂层改性。
国内外对入户式镀锌钢管的使用情况不尽相同。波兰和美国室内镀锌钢管使用占比分别为53%和56.6%[9],国外对镀锌管材腐蚀特征和形成机制有着较为深刻的理解[10-13]。我国目前使用镀锌钢管作为供水管材占比达到60%以上[14],而近几年针对我国水质变化对镀锌钢管腐蚀影响的调查研究甚少。因此,本文深入探讨和总结镀锌钢管在我国供水系统中的腐蚀情况,主要包括以下三个方面:1)阐明供水管网中镀锌钢管腐蚀机理以及影响镀锌钢管腐蚀的因素;2)对现有腐蚀监测技术进行比较分析;3)对比目前常用的多种防腐措施,提出针对镀锌钢管的新型防腐技术。
1 镀锌钢管腐蚀机理
镀锌钢管腐蚀是管材与电解质水溶液相互作用,引起物理化学反应,导致水质恶化[15-16]。镀锌钢管腐蚀的机理研究有助于预测管道腐蚀趋势,达到控制管材腐蚀恶化和减缓管道腐蚀速率的目的。镀锌钢管在供水管网中主要发生物理腐蚀、电化学腐蚀和微生物腐蚀(见表1),它们具有不同的机理。以下分别讨论镀锌钢管在不同腐蚀机理下的腐蚀速率、腐蚀垢形成和管道金属释放,为镀锌钢管在我国供水体系的防护工作提供理论依据。

表1 镀锌钢管腐蚀机理分类Table 1 Classification of corrosion mechanism of galvanized steel pipe
1.1 物理腐蚀
物理腐蚀主要是指镀锌钢管受到温度、作用力、水流流速等物理因素的影响引起的腐蚀。目前国内外关于镀锌钢管的物理腐蚀研究包括:环境温度、水力停留时间、水流速度以及其他水力因素。
1.1.1 环境温度
我国幅员辽阔,不同地区气候差异大。不同的环境温度对供水管道腐蚀影响程度不同。一方面,常温下管道受到的合应力σ0处于稳定状态;温度降低使管道收缩,产生温度应力σT,此时管壁受到的应力增大为合应力σ0与温度应力σT总和,过大的应力可能使管道发生破裂[17]。另一方面,温度的升高或降低会改变管道与水的固液界面处腐蚀反应的化学平衡、电化学反应速率及腐蚀垢层的溶解度,影响腐蚀产物的形成、相关离子扩散速率及腐蚀垢上微生物的生长情况。通过12周的烧杯实验,研究了温度对低铅镀锌钢试件腐蚀速率和金属释放量的研究,发现水温对腐蚀速率、总铁和可溶性锌以及痕量重金属的释放有重要影响。当碱度为70 mg/L、温度为36℃时低铅镀锌钢腐蚀速率高达0.12 mm/a,这比4℃和20℃条件下的腐蚀速率快3~6倍,并且水体中的铅(Pb)、镉(Cd)含量显著增加[18]。因此,在一定程度上升高温度会使镀锌钢管受到的腐蚀速率增加。
1.1.2 水力停留时间
镀锌钢管的腐蚀速率受到居民用水频率的影响。研究结果表明,居民使用自来水的频率较为集中,使用时间主要在6:00—9:00,11:00—13:00,17:00—23:00这三个时间段[19]。在用水高峰之后,出现长时间的水力停留。镀锌钢管的腐蚀情况受到停滞或流动两种不同水力状态的影响。通常长时间水力停滞会加剧金属管道在电解质中的腐蚀。高玖藜[20]对供水管道中水体总铁浓度和浊度指标进行监测,结果表明,随着停滞时间增加至72~96 h时铁释放速率达到每小时35 mg/L。金属释放增加会刺激管道持续腐蚀。对于管道水力特性而言,停滞是终端出水的一种特殊情况。在停滞情况下,腐蚀电位刚开始会明显下降,随着时间延长逐渐趋于稳定状态。这使得金属供水管道中金属释放量增加以及促进细菌生长[21-22]。
1.1.3 水流速度
水的流速越大,一方面造成水的剪切力越大,使供水镀锌钢管腐蚀垢受到的冲刷和扰动越严重;另一方面溶解氧和余氯在高流速的水流中会加快扩散,使得管道的电化学腐蚀加剧。郭浩等[23]通过结合电化学测试装置、循环管路、水质更新系统以及流动腐蚀模拟监测系统,探究水体流动状态下流速与腐蚀速率关系。研究结果表明,流速从0 m/s增加至0.5 m/s时,腐蚀速率增加约0.07 mm/a,流速的增加带来更多作为氧化剂的溶解氧,从而加剧溶解氧与金属管道发生氧化还原反应,腐蚀速率也因此而加快。Liang等[24]通过研究流速对供水管道腐蚀速率的影响,发现腐蚀速率随水速的增加而增加。流速为1 L/d、10 L/d和20 L/d时,腐蚀速率分别为0.12 mm/a、0.17 mm/a和0.23 mm/a。
1.1.4 其他水力因素
除了环境温度、水力停留时间和水流速度这三个目前研究得比较多的方面外,还存在一些影响管道腐蚀的其他物理因素。例如,经过一定的时间,供水管道腐蚀垢适应了同一个水流方向,生长逐渐稳定,但当水流方向改变时,腐蚀垢会受到剪切力冲击,突然改变原有的稳定状态,造成腐蚀垢中的金属释放到水体中,引起水体污染。例如,谭浩强等[22]采用循环式管道模拟装置,研究水力条件变化对镀锌钢管铁释放的影响。结果表明,改变水流方向,在1 h内水体中铁的浓度增加了0.42 mg/L。
镀锌钢管受不同铺设方式和铺设位置的物理冲击时,管道将呈现不同的腐蚀结果。实验室研究通过比较管材前后的重量变化来反映腐蚀情况。近年来,随着电化学方法的不断发展,Otero等[25]通过极化电阻法,研究了镀锌钢管不同铺设方式的管道腐蚀程度,并结合水质分析,发现水平放置的镀锌钢管所受的水力冲击比垂直放置的大13%,从而导致水平放置的管道腐蚀程度增加18%,这一结果与传统重量法测得的结果相吻合。
1.2 电化学腐蚀
镀锌钢管的电化学腐蚀是指在电解质水溶液中通过电化学反应引起的腐蚀。这些电化学反应过程可以用如下阳极和阴极反应方程描述:

新镀锌钢管刚投入使用时,管道表面主要以锌作为阳极失去电子,反应见式(1),电子从阳极区流向阴极区。而水体中的氧化剂如氢、氧、氯等元素作为阴极能够到达镀锌钢管与水接触的固-液相界面,发生电子反应见式(3)—式(5)。当镀锌层逐渐被氧化剥离管道表面,裸露出钢管基体,会导致管道内的金属铁存在进一步被腐蚀的风险[式(2)]。
阳极区的金属不断电离而形成腐蚀垢层或释放可溶性金属离子,这些金属离子进一步发生水解反应,形成腐蚀结垢,腐蚀结垢在水流的不断冲刷下进入水体影响水质。如,常见的“黄水”“红水”现象是由于溶出的Fe2+会进一步生成铁锈,化学式如下:

研究发现,影响镀锌钢管电化学腐蚀的水质参数主要包括pH、余氯、不同阴阳离子(Cl-、S O42-、HCO3-、Fe2+、Ca2+、Mg2+、Mn2+等) 以及溶解氧(DO)等的浓度。
1.2.1 pH
pH直接影响镀锌钢管所处水体的酸碱环境,进而影响电化学腐蚀中的析氢腐蚀[见式(3)]或吸氧腐蚀[见式(4)][26-27]。pH对供水管道的腐蚀影响显著。pH对镀锌钢管腐蚀的影响可以通过金属释放量的变化情况来表示。在低pH条件下发生析氢腐蚀,新镀锌钢管的镀锌层逐渐减少,使镀锌钢管基体暴露在水体中,使得管道里的Zn2+、Fe2+释放,导致水质恶化。
低pH(4.6~5.6,即低碱度值)的水体对镀锌钢管内表面同样具有腐蚀性,研究发现pH为5.3的酸性水体可使镀锌钢管的腐蚀速率增加0.05 cm/a[28]。相反,在弱碱性的水体中,镀锌钢管镀锌层中的Zn2+溶解在管道表面形成一层致密的保护膜Zn(OH)2,抑制管道的进一步腐蚀。同样,在碱性水体中存在稳定的碳酸盐(如CaCO3)容易沉淀在镀锌钢管管道内表面,也能够形成保护膜抑制腐蚀,减少镀锌钢管可溶性金属的释放及“黄水”或“红水”的出现。利用电感耦合等离子体分析仪及电化学测试技术,对腐蚀速率进行五次重复性测量取平均值和标准偏差。结果表明,对于初始腐蚀速率而言,在pH值为8.5的弱碱度水中,CaCO3含量具有明显的缓蚀效果。当pH增加到10.5时,腐蚀速率明显降低至原来的三分之一[29]。除金属铁外,存在其他可溶性金属的释放。如Zhang等[30]在pH为6、7、8三个不同条件下测试供水管道中Mn2+的释放量,待Mn2+释放量达到平衡时,随着pH升高Mn2+浓度从671 μg/L逐渐减少至336 μg/L。pH升高使Mn2+释放量减少,从而降低镀锌钢管腐蚀程度。
pH不仅对管道腐蚀程度产生影响,且对腐蚀垢的形成产生一定的影响。研究水质变化与管垢形成的关系时,发现增大pH有利于管垢保持稳定;另外通过结合电化学阻抗谱(electrochemical impedance spectroscopy,EIS)测试研究不同pH在腐蚀稳定期对腐蚀垢生长的影响。结果表明,管道内外腐蚀垢层的等效电阻(Ri和Ro)与pH有非线性关系,在pH为6.5~7.0时腐蚀速率较高,使内外腐蚀垢层的等效电阻降低11.5~33 Ω/cm2;而pH为7.5~8.5时内外腐蚀垢层的等效电阻增加到68.3~98.2 Ω/cm2。这是由于碱性条件下更容易形成碳酸钙沉淀,覆盖于腐蚀垢的内外层[26]。
以上实验结果表明,调节pH使水体偏酸性或偏碱性时对镀锌钢管的腐蚀情况和腐蚀垢生长都有影响。从《生活饮用水卫生标准》(GB 5749—2022)可知,供水管网水pH为6.5~8.5的水体,对镀锌钢管腐蚀影响较小,至今镀锌钢管仍作为饮用水供水管材。
1.2.2 余氯
根据国家规定,供水管网末梢出水时余氯浓度不得低于0.05 mg/L。因此,在水厂消毒工序中,需添加适量的消毒剂来保证供水管道中余氯的浓度。余氯是由次氯酸盐或氯气分子组成,主要分为游离氯、含氨化合物或胺类化合物[31]。不同的余氯化合物对管道腐蚀产物的影响不同。例如,Li等[32]的研究表明,使用氯消毒的水体中,镀锌钢管腐蚀产物的晶体结垢较为疏松;而使用氯胺消毒的管道中,腐蚀产物的晶体结构更加紧密,并且氯胺消毒可以使硝酸盐还原菌还原速率加快。当加氯量达到水厂出水标准时,饮用安全才能有保障。但余氯浓度过高,供水管道易发生腐蚀现象以及潜在的消毒副产物会对人体造成毒害作用。因此,余氯浓度在饮用水中的限值及其监测技术得到广泛关注[33]。余氯在供水管网中的腐蚀机理主要包括:余氯与镀锌钢管中的金属发生电化学反应,刺激金属溶解于水中,改变腐蚀垢原本的晶体结构,使镀锌钢管内表面与其他物质接触的概率变大,导致腐蚀速度加快;余氯会抑制镀锌钢管内微生物生长,弱化微生物在管道腐蚀过程的作用,使微生物从供水管体脱落进入水体。研究不同余氯浓度对新旧镀锌钢管的影响时,发现余氯的消耗量、动力学特征、反应对象以及金属溶出情况呈现出两种完全不同的结果。当新镀锌钢管的加氯量为4 mg/L时,镀锌层中的锌离子溶出量高达0.76 mg/L;而在旧镀锌钢管中余氯的消耗传质(由于浓度不均匀引起的质量转移)为一级动力学过程,反应物的浓度和反应速率随时间呈指数级下降,加氯量为4 mg/L时,金属溶出主要以铁为主,但铁离子溶出量并不多,仅为约0.1 mg/L,因为此时余氯主要与生物膜进行反应[34]。另外,余氯不仅能够促进腐蚀垢的形成,余氯的消耗量也会受到腐蚀垢的影响。例如,Zhang等[35]通过X射线荧光光谱仪表征、间歇式反应以及余氯一级动力学反应的研究,发现镀锌钢管中的铁腐蚀水垢消耗了78%~96%的余氯并将其转化为亚氯酸盐。
因此,在镀锌钢管腐蚀过程中,余氯的作用复杂多样,在不同的条件下呈现出不同的现象。关于余氯的研究主要聚焦在余氯含量及余氯与其他因素相结合对镀锌钢管的影响,而对余氯用量的调节技术和维持技术的研究缺乏系统性。为减缓镀锌钢管受余氯的影响,针对这方面的技术问题值得深入研究、探讨并完善,使其在实际生活中得到推广。
1.2.3 溶解氧
溶解氧作为镀锌钢管腐蚀的主要电子受体,在阴极参与反应。溶解氧消耗速度可以反映出腐蚀速度。新投入使用的镀锌钢管内壁未有腐蚀垢形成,此时溶解氧能够到达镀锌钢管内表面与电解水相接处的固液界面,发生电化学反应。镀锌层逐渐被腐蚀,使管材基体暴露于水体中,导致溶解氧能够与管材基体反应。随着腐蚀不断进行,管道内壁发生沉淀、氧化还原等反应,形成腐蚀垢,在水力冲刷下或者溶解等情况下可能向镀锌钢管的水体中释放金属。比如,Fe是镀锌钢管管材基体的主要金属元素,管材基体的暴露加快了腐蚀产物Fe2+氧化成Fe3+的速率,导致镀锌钢管腐蚀速率增加。但是,随着反应的进行,水管中的溶解氧浓度增加至7~9 mg/L时,水体中铁的含量反而下降,低于0.2 mg/L。一方面,主要是因为越来越多腐蚀垢在管壁上沉积,逐渐形成一层钝化膜,阻止水中的溶解氧与金属管壁的接触,并且溶解氧含量逐渐减少,降低了镀锌钢管腐蚀的速率。另一方面,过高浓度的溶解氧可以使腐蚀电流钝化。腐蚀电流钝化后金属供水管道会从腐蚀状态转变为钝化状态,供水管道的腐蚀强度会明显降低[36]。
以上的研究表明,镀锌钢管中的金属释放受到溶解氧的影响。但也有研究表明,在无氧的情况下,管道腐蚀的情况仍然发生[37]。这说明对溶解氧的浓度控制并不能绝对地抑制管道腐蚀的发生,需要对不同条件下的腐蚀情况进行区分说明。
1.2.4 阴阳离子
水中的Cl-和SO42-是引起铁管局部腐蚀的主要离子[38-39]。随着Cl-浓度增加,水体电导率增加,降低了腐蚀电流的电阻,加快了腐蚀反应的进行,导致水体中总锌和总铁含量增加;Cl-也会取代钝化膜中金属相互连接的氢键,破坏钝化膜,生成溶解态金属离子,恶化水质。SO42-能够与腐蚀垢中的FeOOH发生反应,取代FeOOH中的氢键,最终生成(FeO)2SO4等可溶解盐,加快铁离子的释放,使管道腐蚀恶化。米子龙等[40]通过实验室管段模拟反应器,调节SO42-浓度,研究其对腐蚀垢中金属释放的影响。结果表明,当SO42-浓度从50 mg/L增加至180 mg/L时,铁的释放量增加至2.5 mg/L,说明两者之间有很好的相关性。
此外,阴阳离子间相互影响也会进一步加速镀锌钢管的腐蚀。Tian等[41]通过模拟夜间水在镀锌钢管中的停止情况,探究实际管垢中阴阳离子释放对人体健康风险的影响。结果表明,SO42-的存在使Fe2+和Mn2+释放更多,并且Mn2+的释放会增加Ca2+的释放,从而加剧人体健康风险。SO42-浓度影响Mn2+释放,Mn2+释放会影响Ca2+释放,这三者形成递进影响关系。其中,关于Ca2+共存或共沉淀的研究比前两者的研究少,且人体摄入多少管垢中释放的Ca2+将对健康造成影响,目前并未明确指出,这可以作为今后深入研究的一个方向。
1.3 微生物腐蚀
由于SO42-的离子半径是Cl-的8倍,因此,SO42-的迁移性和腐蚀性比Cl-差。但SO42-浓度的增加易生成硫酸盐还原菌。在存在硫酸盐还原菌的情况下,腐蚀机理为:
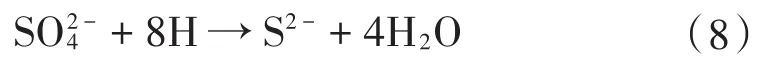

硫酸盐还原功会将SO42-还原成 S2-[式(8)],进一步与镀锌层中的锌离子反应生成硫化锌腐蚀产物[见式(9)],使阴阳极发生去极化现象[42]。除硫酸盐还原菌外,供水系统还存在其他细菌,例如铁细菌、黏液异养菌群、硝酸盐氧化(还原)菌等微生物,它们会与镀锌钢管中锌铁离子直接反应,产生微生物诱导腐蚀,最常见的是铁细菌和硫酸盐氧化(还原)菌诱导腐蚀[43-44]。硫酸盐还原菌通过自身代谢作用将水中的硫酸盐转化成具有严重腐蚀性的硫化氢,导致供水管道发生局部腐蚀至穿孔现象。此外,还发现供水管道中的微生物可以依靠通过电子转移形成的氧生存,微生物将电子传递给管道中的金属发生还原反应。硫酸盐还原菌这一系列反应可以应用于生物修复,去除水体中有机氯等有机物污染。镀锌钢管的服务年限越长、生物膜活菌数越多,导致管网腐蚀严重程度增加,而供水管网中生物膜活细菌通过成块脱落进入水中影响水质,所以水质和镀锌钢管管壁上生物膜之间也存在一定关系[45]。
但也有发现胞外聚合物对铸铁的腐蚀有抑制作用,这些物质可以形成保护膜并延缓氧的阴极还原,进而能够减缓管道中消毒剂如NaClO和ClO2对供水管道的腐蚀[46-47]。因此,微生物腐蚀具有两重性:在消毒剂含量低的情况下,微生物会对镀锌钢管进行腐蚀,反之则会降低镀锌钢管受消毒剂的腐蚀影响。
2 腐蚀垢理化特性分析与腐蚀监测技术
对于镀锌钢管腐蚀及腐蚀垢的理化特性,主要从其腐蚀结垢的结构和组成材料进行静态表征分析;针对不同场景应用腐蚀监测技术,既能反馈当前已有腐蚀情况,又能预测管道未来腐蚀趋势,可提前采取有效预防措施,减少腐蚀带来的损失,延长镀锌钢管使用寿命(见表2)。

表2 腐蚀垢理化特性分析与腐蚀监测技术Table 2 Corrosion scale physical and chemical characteristics analysis and corrosion monitoring technology
2.1 材料表征方法
应用材料分析方法(见表3),主要使用扫描电镜(scanning electron microscope,SEM)、X射线荧光光谱仪(X-ray fluorescence spectrometer,XRF)、X射线单晶衍射仪(X-ray single crystal diffractometer,XRD)、X射线光电子能谱仪(X-ray photoelectron spectroscopy,XPS),对镀锌钢管腐蚀结垢的微观形态、化学组成、晶体结构和化合物构成进行研究[48]。实验表明,镀锌钢管管垢松散易脱落,外层为红褐色凹凸细碎颗粒物,内层多为黑色松散固体;腐蚀结垢的主要化学成分是含铁化合物,内层主要以无定形态化合价存在,而外层主要是晶体Fe2O3。

表3 镀锌钢管腐蚀垢物理化学特征分析Table 3 Physical and chemical characteristics of corrosion scale of galvanized steel pipe
2.2 物理监测技术
目前,物理监测技术不断发展,为有效监测控制供水管道腐蚀,避免管道泄漏及水体流失提供了新的技术手段。常用的物理监测技术主要有遗传算法(genetic algorithms,GAs)技术、独立计算区域技术(district metering area,DMA)以及在线监测技术等。GAs是通过基于线性理论方法的稳态网络水力分析模型来估算供水管道中水体的渗漏率,但该方法尚缺乏实质性数据支撑。DMA是通过分析供水管道夜间流量来推断出最小和最大漏损率,但很难迅速、及时、准确地了解DMA运行状况,对大城市规模化管网难以实现大面积监测。基于智能化技术的在线监测技术,可以高效率监测异常状况,但往往依赖于历史数据,缺乏对管网的实地实时分析,造成结果偏差大[49-51]。因此,在物理腐蚀监测方面需要进一步优化以上技术,比如,监测镀锌钢管内外压力、管道埋设深度或高度、更换管道过程中的震动等物理条件对镀锌钢管腐蚀速率的影响。
2.3 腐蚀监测技术
镀锌钢管腐蚀监测手段可以有效地分析腐蚀速率,测量管道剩余壁厚,掌握局部腐蚀情况,有利于研究腐蚀的发生发展过程及其工艺参数与腐蚀过程之间的关联性,为鉴定腐蚀成因和进一步控制腐蚀提供科学的技术依据,在实际生活中得到广泛应用[52-53]。腐蚀监测技术主要分为离线监测和在线监测两种。传统的通过测量管道腐蚀前后重量变化的失重法能够较为真实地反映出腐蚀情况,但是该法监测周期长,测得的结果只能表示一段时间内的平均腐蚀速率,无法及时地反映设备在某一点的腐蚀速率。
2.3.1 电化学监测技术
镀锌钢管在腐蚀过程中因其表面形态变化而形成不同腐蚀产物,影响其电化学性能。电化学分析方法中的极化曲线(polarization curve,PC)和EIS是较为常用的分析方法,其中PC是反映实验过程中电极电势与电流密度两者关系的曲线,EIS则是对电极施加一个扰动的电信号可以得到相应的电极腐蚀数据,二者能够快速地响应,所得信息可靠性高,是最常用的方法。通过在样品浸入液中测量腐蚀电位,计算或推导出镀锌管道的电极电位和腐蚀速率等参数。Su等[54]使用极化曲线和EIS研究了NaClO对水体中碳钢腐蚀的影响。结果表明,NaClO可以影响阳极和阴极反应,而根据ESI结果快速推断出腐蚀过程中产生了腐蚀垢,从而知道NaClO和ClO2改变了水体中供水管上的电子传递途径和腐蚀产物。而由铁氧化细菌引起的低溶解氧浓度会导致腐蚀电势产生并增加电子传递阻力。通常,电化学分析方法可在受控条件下(例如某些浓度的离子或细菌)连续测量钢铁材料的电化学性能[55-57]。
El-Mahdy等[58]通过EIS对不同干湿条件下镀锌钢板(镀层厚度:3 μm)的腐蚀电流密度和腐蚀电位进行了监测。研究表明,在含氯离子的循环湿-干环境中,随着循环次数的增加,镀锌钢管的腐蚀速率迅速下降,电化学阻抗随着循环次数的增加而增大,最高可达-0.85~-0.80 V。同时也可利用EIS估计红锈出现的时间,红锈出现时间表明腐蚀的开始以及涂层材料的腐蚀速率。
因此,PC和EIS等方法可以识别单个因素对腐蚀结垢电化学性能的影响。然而,在实际情况下,难以控制实验条件对腐蚀垢形成的复杂性,特别是在长期使用过程中。
2.3.2 化学稳定性技术
化学稳定性技术主要是防止镀锌钢管内的腐蚀与腐蚀垢对管道的危害,对碳酸盐系统、铁离子、镁离子等稳定性进行分析。主要对水质稳定性进行判定,提供一系列判定指标。其中朗格利尔饱和指数(langelier saturation index,LSI)和拉森指数(larson ratio,LR)是目前最常用的化学稳定指标,主要用于定性判断水体腐蚀或管垢形成趋势及程度。LSI是通过不同的碳酸钙饱和状态,从而判断腐蚀介质导致管道发生腐蚀的趋势,叫碳酸溶解平衡理论,LSI与pH有关:LSI=pHa-pHs,pHa为供水管网中实际水的pH,而pHs指水与碳酸盐系统处于平衡状态下的pH,当LSI小于零时,说明pHa小于pHs,也即碳酸钙处于未饱和状态,金属继续发生腐蚀使碳酸钙逐渐饱和形成腐蚀垢。研究发现随着水体中pH变大LSI也增大,当LSI大于0时,水体中有腐蚀垢产生,LSI值为零时水质最稳定。拉森指数(LR)被定义为:LR=([Cl-]+2[SO42-])/[HCO3-],通过氯离子、硫酸根离子浓度以及碳酸氢根离子判断水体中总溶解性固体含量、离子强度、离子迁移速率等推测腐蚀速率。因此,通过应用LSI与LR值可以判断镀锌钢管的腐蚀速率[59]。张雅君等[60]通过模拟真实管网水力条件,研究拉森指数对碳钢腐蚀的影响,结果表明,LR=4.00时管道腐蚀速率最大,LR不断升高造成Fe的释放速率增大、管段表面生成的碳酸钙的量不断减少,在镀锌钢管中腐蚀产物主要有α-FeOOH、Fe2O3、Fe3O4;随着腐蚀不断发生,腐蚀产物最终将以α-FeOOH、Fe3O4这两种成分稳定存在,作为一层保护膜,从而抑制镀锌钢管进一步腐蚀。
LSI与LR值只能定性地分析水体腐蚀或管垢形成趋势,另一种稳定性指标——碳酸钙沉淀势(calcium carbonate precipitation potential,CCPP),它是用以表示碳酸钙在水中的沉淀量或溶解量,因此可以有效地评估腐蚀垢与腐蚀情况[61]。当0<CCPP≤4时,水质较为稳定,基本不结垢或者微结垢;至4<CCPP≤10时,轻微结垢;当10<CCPP≤15时,管道内出现较严重结垢;当CCPP>15时,水质极不稳定,出现严重结垢。而在-5<CCPP≤0时,腐蚀性质较为轻微;当-10<CCPP≤-5时,为中度腐蚀;当CCPP≤-10时,则为严重的腐蚀。CCPP与铁的释放速率存在一定的相关性,通过调节化学试剂的量来探究供水管道铁释放的影响,结果表明,增加Ca(OH)2的量,导致CCPP、钙离子浓度增加,减缓供水管网中铁的释放速度[62]。
2.4 管道腐蚀监测技术的发展及其趋势
PC和EIS等一系列的电化学法所测得的腐蚀速率为均匀速度,无法提供局部腐蚀信息。如今,将电化学法与传感器、计算机相结合,直接测量镀锌钢管腐蚀部位情况,进而计算出相应的腐蚀速率,该方法在国内外逐渐受到欢迎。比如,美国西南研究所研发的耦合多极矩阵传感器,可以有效测量局部腐蚀速率;德国的ZAHNER,荷兰的EcoChemie等公司使用的恒电位仪、频响分析仪以及我国的弱极化法、恒电量法、电阻探针,这些腐蚀监测设备具有便携式和智能化的优势[63-65]。随着人工神经网络的发展,灰色模型(grey model,GM)和埋地水管结构完整性监测(Structural integrity monitoring,SIM)系统也开始应用于管道腐蚀的监测。通过建立测量参数的函数关系模型,利用灰色模型对腐蚀速率进行有效预测,可以提高预测的精度。在函数模型中分别采用标准GM和经验关系式改进背景值,考虑初始点影响、灰色模型和back propagation神经网络相结合,输入节点数为测试时间、溶解氧、pH、温度、流速等影响因素;通过模型计算即可输出腐蚀速率[66]。谷小红等[67]研究埋地镀锌管道泄漏信号波传播方程,分析现场实验采集的泄漏信号,得出泄漏信号一般处于低频(1 000 Hz以下)的结论。同时推导出了在低频下沿管道传输的衰减方程,证明泄漏信号可以被声信号传感器检测。另外,SIM系统相较于GM的优点在于只需要管道当前的信息,而不需要太多的其他信息,就可以得出最终预测的信息,判断管道何时发生腐蚀泄漏。这些检测方法不仅缩短了监测时间,而且降低了外界因素对测试结果的干扰,值得推广使用。
3 总结与建议
老化的供水管网会造成大量的水体流失、财产损失以及水体污染。传统的修复、复原和更换办法虽然有效,但是费用昂贵、耗时长及对供水管道管理技术要求高,带来了巨大的挑战。因此,提出以下几点建议:
(1)镀锌钢管在供水金属管材中占主导地位,在长期运行过程中,会发生腐蚀现象和形成腐蚀垢。为了更好改善水质,减少管材因素对水质的影响,可逐步对供水管网进行替换或做好防护措施,使镀锌钢管经济效益达到最大。
(2)对水质高度重视,从水力因素、水质因数、管材本身进行分析,结合腐蚀机理,尤其是电化学腐蚀机理及影响因素,避免水质的二次恶化,从而控制管网水质稳定性。
(3)关于镀锌钢管防护工作,首先,以供水管道常用材质为金属这一出发点出发,应该采用耐腐蚀金属材料进行替换;其次,提高出厂水水质,杜绝二次污染的发生;再次,采用电化学技术,使金属处于本身难以腐蚀的电位区;最后,在管道表面涂覆防腐材料,使管道与周围环境隔开,防止与电解质接触,提高镀锌钢管使用率。
