UPLC-FLR测定长效人红细胞生长刺激素中唾液酸含量
2022-10-12吕素娟刘作龙王玉营王惠琰王云飞
吕素娟,刘作龙,王玉营,王惠琰,王云飞
(山东丰金生物医药有限公司,山东 烟台 264000)
Darbepoetin alfa(商品名 Aranesp)是Amgen公司于2001年上市的多糖基化位点修饰的长效人红细胞生长刺激素,用于治疗慢性肾功能衰竭、癌症放疗化疗及骨髓衰竭患者的贫血[1-3],该产品于2021年于国内上市。本研究使用的苏州康聚生物科技有限公司研制的与Aranesp具有相同氨基酸序列的重组人新型红细胞生长刺激素(处于临床试验阶段),将促红细胞生成素(erythropoietin,EPO)一级结构中的5个氨基酸进行定点突变,在57位和115位改变得到的2个天冬酰胺成为新的N-连接糖基化位点,N糖基化位点由3个增加到5个,从而使其体内半衰期比EPO延长了3倍[4]。因为其糖基化的高丰度和不均一性会影响体内活性[5-7],不均一性主要由糖链末端唾液酸引起,常见的唾液酸主要有两种:N-乙酰神经氨酸(Neu5Ac)和N-羟乙酰神经氨酸(Neu5Gc)。人类缺乏胞苷酸N-乙酰神经氨酸羟化酶基,因此不能合成Neu5Gc,但大多数哺乳动物细胞能进行Neu5Gc修饰,而外源性Neu5Gc及其复合物被机体吸收并沉积在细胞表面,诱导体内产生抗Neu5Gc抗体,进而诱导机体产生慢性炎症最终导致肿瘤的发生和发展[8-9]。因此,唾液酸化(主要为Neu5Ac)程度的高低直接影响药物体内半衰期和药物安全性,是重要的质控指标[4,10-11]。
《中国药典》2020年版三部中人促红素唾液酸含量测定为通则3102,使用酸水解后的唾液酸与间苯二酚反应生成有色化合物,使用有机酸萃取后,测定含量。该方法操作过程使用较多有机溶剂,对环境及人员健康影响较大,且步骤繁琐,结果重现性、耐用性较差,只能测定总唾液酸值,不能区分唾液酸种类[12]。本研究中长效人红细胞生长刺激素与柱前荧光衍生试剂4,5-亚甲二氧基-1,2-苯二胺盐酸盐(DMB)[13-15],在酸性条件下生成DMB衍生物,该衍生物经373 nm激发光激发后,在448 nm能产生可辨识可定量的较强荧光信号,从而对样品中Neu5AC和Neu5Gc进行定性和定量。
1 仪器与试药
1.1 仪器
ACQUITY UPLC超高效液相色谱仪-FLR荧光检测器(Waters);XPR105十万分之一电子天平(梅特勒-托利多);UV2700紫外可见分光光度计(岛津);ThermoMixer C恒温混匀仪(Eppendorf);色谱柱Acclaim RSLC 120 C18(2.2 μm,2.1 mm ×100 mm)(Thermo)。
1.2 试药
N-乙酰神经氨酸(色谱纯,TCI);N-羟乙酰神经氨酸(色谱纯,TCI);甲醇(色谱纯,Fisher Chemical);乙腈(色谱纯,Fisher Chemical);冰乙酸(Sigma);2-巯基乙醇(Sigma);连二亚硫酸钠(Sigma);4,5-亚甲二氧基-1,2-苯二胺盐酸盐(DMB,Sigma);实验用水为Milli Q超纯水;长效人红细胞生长刺激素原液(山东丰金生物医药有限公司)。
2 方法与结果
2.1 溶液配制
2.1.1 DMB标记衍生试剂 取15 ml离心管,加入1.5 ml超纯水、172 μl冰乙酸、112 μl 2-巯基乙醇,涡旋混匀;然后加入4.9 mg连二亚硫酸钠(配制前称于称量纸中),涡旋溶解(此时溶液可能变浑浊);最后加入3.5 mg DMB试剂(配制前称于称量纸中)和200 μl超纯水,涡旋混匀,现用现配。
2.1.2 Neu5Ac标准液(STD)(10 mmol/L) 准确称取Neu5Ac干粉15.5 mg置入5 ml量瓶,超纯水溶解并定容,配制成10 mmol/L Neu5Ac STD。
2.1.3 Neu5Gc标准液(STD)(10 mmol/L) 准确称取Neu5Gc干粉16.3 mg置入5 ml量瓶,超纯水溶解并定容,配制成10 mmol/L Neu5Gc STD。取20 μl Neu5Gc STD(10 mmol/L)逐级稀释至0.1 mmol/L Neu5Gc STD,终体积500 μl 以上。
2.1.4 唾液酸混合标准液:各取100 μl Neu5Ac STD(10 mmol/L)和100 μl Neu5Gc STD(0.1 mmol/L),加800 μl超纯水,涡旋混匀后,再将混合溶液稀释5倍,取200 μl,加800 μl超纯水,涡旋混匀,为标准溶液(200 pmol/μl Neu5Ac STD和2 pmol/μl Neu5Gc STD),现用现配。
2.1.5 标准曲线按照表1稀释。
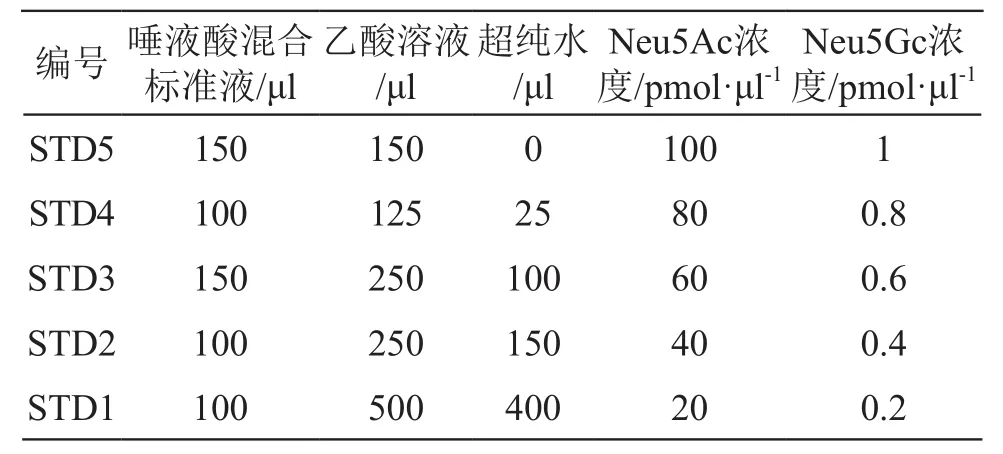
表1 标准曲线稀释表
2.2 样品前处理
2.2.1 样品水解 将长效人红细胞生长刺激素原液稀释至0.1 mg/ml,取50 μl稀释至0.1 mg/ml的待测样品置入1.5 ml离心管,加入50 μl 4 mol/L乙酸溶液,混合均匀后置于恒温混匀仪中,80 ℃保温2.5 h。
2.2.2 样品和标准品标记衍生 在100 μl水解后的样品和100 μl标准品溶液中加入100 μl DMB标记试剂,混匀后置于恒温混匀仪中,50 ℃保温3 h。
2.2.3 中止 在通风橱中移取50 μl标记完成的样品及标准品分别加至装有950 μl超纯水的2 ml离心管中,混匀后,用于色谱分析。
2.3 色谱条件
流速0.45 ml/min;压力上限10000 psi;柱温45 ℃;样品室温度6 ℃;荧光检测器激发波长373 nm、发射波长448 nm;进样体积10 μl;运行时间13 min;流动相(甲醇:乙腈:超纯水=7:9:84)。用流动相平衡超高效液相色谱仪,以流动相为空白,重复进样3次至基线平稳,标准品及样品进样10 μl,运行时间13 min,记录色谱图。
以水解体系中唾液酸标准品的浓度为横坐标,对应的峰面积为纵坐标,绘制标准曲线,计算样品(0.05 mg/ml)水解体系中的唾液酸浓度(pmol/μl)。
2.4 方法验证
2.4.1 专属性 分别使用2.1.2和2.1.3项唾液酸标准液配制60 pmol/μl Neu5Ac STD、0.6 pmol/μl Neu5Gc STD,各取50 μl,同时使用超纯水、STD3(混合标准液)各50 μl,经2.2项处理后进样,色谱图见图1,可见超纯水及空白在Neu5Ac和Neu5Gc峰处无干扰峰,单Neu5Ac STD及单Neu5Gc STD各主峰出峰与STD3混合标准工作液出峰时间相同,证明该方法具有专属性。

图1 唾液酸专属性色谱图
2.4.2 线性与范围 以唾液酸峰面积为纵坐标,唾液酸标准品的浓度为横坐标,得到Neu5Ac标准曲线方程为:y=2.53×106x+2.96×106,r2=0.9989,表明标准品浓度范围20~100 pmol/μl内,线性关系良好;Neu5Gc标准曲线方程为:y=2.52×106x+1.32×104,r2=0.9991,表明标准品浓度范围0.2~1.0 pmol/μl内,线性关系良好。Neu5Ac和Neu5Gc标准溶液的色谱图见图2。

图2 唾液酸标准曲线色谱图
2.4.3 准确度 取长效人红细胞生长刺激素原液分别与STD5(2:8,高)混合,与STD3(5:5,中)混合,与STD1(2:8,低)混合,按步骤处理,各制备3份,每份检测3次,考察回收率,Neu5Ac回收率为89.6 %~95.1 %,RSD为2.5 %,见表2。Neu5Gc回收率为90.9 %~97.4 %,RSD为2.9 %,见表3,表明本法准确度较好。

表2 Neu5Ac回收率试验结果

表3 Neu5Gc回收率试验结果
2.4.4 重复性 使用1批长效人红细胞生长刺激素原液制备6份样品,重复测定6次,Neu5Ac含量RSD为0.3 %,Neu5Gc含量RSD为0.1 %,证明该方法的重复性较好,见表4。
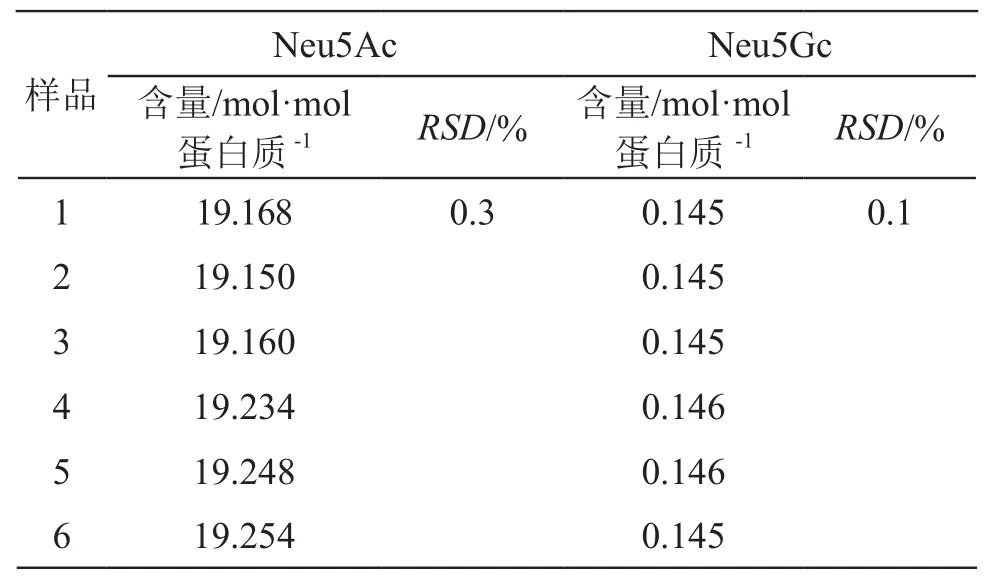
表4 唾液酸重复性试验结果
2.4.5 溶液稳定性 将进行重复性检测的长效人红细胞生长刺激素原液存放12 h后,再次进行检测,计算测定结果相对首次检测结果的回收率,Neu5Ac含量回收率范围为99.0 %~100 %,回收率RSD为0.1 %,Neu5Gc含量回收率范围为97.0 %~100 %,回收率RSD为0.8 %,证明该方法样品溶液稳定性较好,见表5。
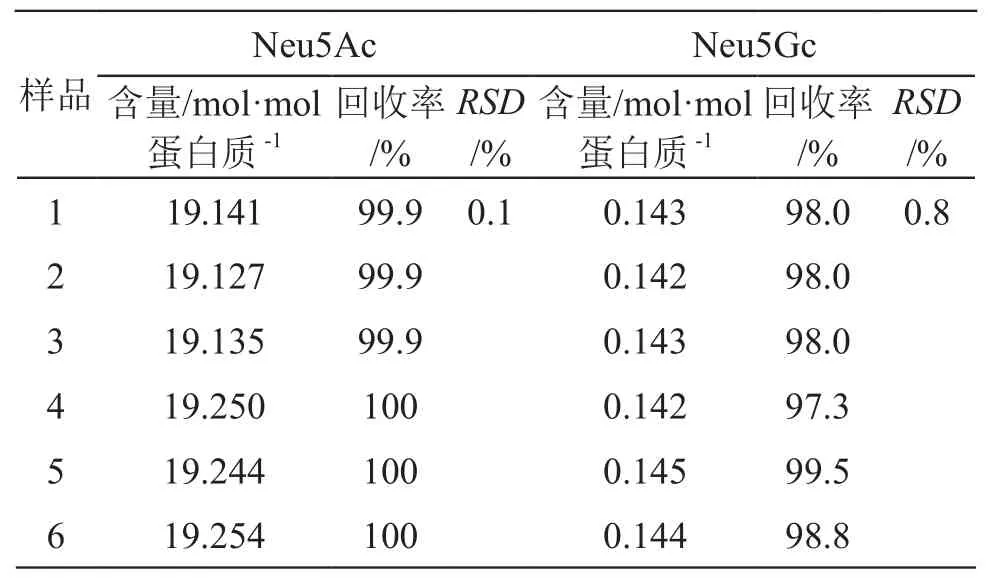
表5 唾液酸稳定性试验结果
2.5 长效人红细胞生长刺激素原液唾液酸含量的测定
取5批长效人红细胞生长刺激素原液,按要求进行样品处理,使用DMB衍生进行唾液酸含量检测,结果见表6,各批次满足质量标准每1 mol蛋白唾液酸含量应不低于18.0 mol,并在理论最大唾液酸修饰含量22.0 mol范围内。
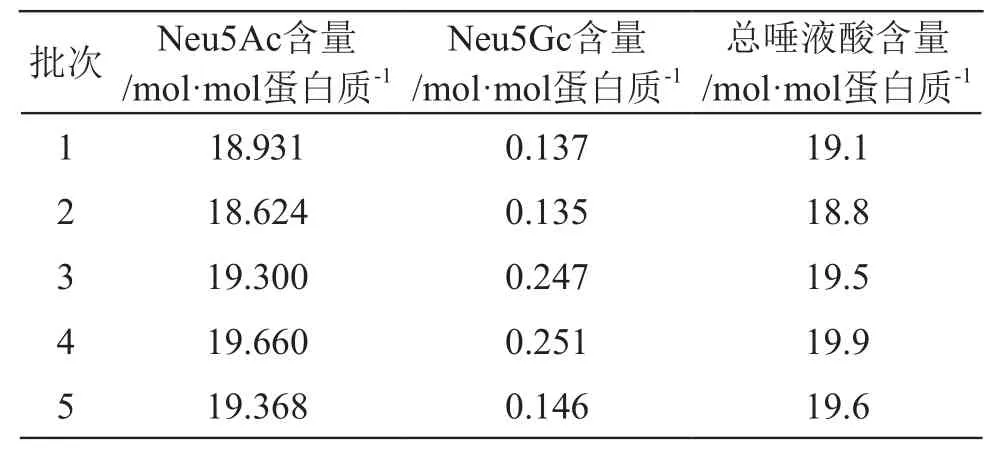
表6 长效人红细胞生长刺激素原液唾液酸含量测定结果
3 讨论
本研究将长效人红细胞生长刺激素原液酸水解后,使用DMB试剂衍生,然后使用超高效液相色谱-荧光检测器进行唾液酸Neu5Ac和Neu5Gc含量检测,该方法使用外标法定量,经过专属性、重复性、准确度、线性与范围、溶液稳定性验证,证明该方法具有较强的实用性,相比于中国药典间苯二酚法,规避了繁琐的样品前处理以及有机溶剂的危害,并能够区分唾液酸Neu5Ac和Neu5Gc两种类型修饰,可用于长效人红细胞生长刺激素原液唾液酸含量的分析。
