恩替卡韦与替诺福韦酯治疗高病毒载量慢性乙型肝炎患者的临床效果分析
2022-10-12王辉
王辉
黑龙江省大庆市油田总医院全科,黑龙江大庆 163000
近年来,乙型肝炎发病率在人们不断改变的饮食结构与生活方式作用下日益提升[1]。由于我国具有较大的人口基数,因此乙型肝炎患者数量也多[2]。乙型肝炎指乙型肝炎病毒检测阳性,缺乏明确的发病日期或病情在6 个月以上[3],慢性肝炎是其临床表现,乏力、恶心、肝区疼痛等是其主要症状,乙型肝炎病毒感染是其诱发因素[4],通常情况下伴肝硬化、肝源性糖尿病等并发症,将不便带给了患者生活,对患者健康造成了严重威胁,对患者生活质量造成了不良影响[5],由于需要隔离患者,因此也将心理创伤带给了患者[6]。本研究统计分析了2011 年2月—2021 年2 月黑龙江省大庆市油田总医院高病毒载量慢性乙型肝炎患者60 例的临床资料,观察了高病毒载量慢性乙型肝炎患者治疗中替诺福韦酯与恩替卡韦的临床效果。
1 资料与方法
1.1 一般资料
回顾性选取本院高病毒载量慢性乙型肝炎患者60 例,依据用药方法分为替诺福韦酯组、恩替卡韦组两组。替诺福韦酯组30 例患者年龄33~69 岁,平均(66.23±10.52)岁;女性 16 例,男性 14 例;在体质量方面,52~62 kg 17 例,63~73 kg 13 例;在乙型肝炎家族史方面,有6 例,无24 例;在既往史方面,吸烟史19 例,饮酒史11 例。恩替卡韦组30 例患者年龄34~70 岁,平均(66.69±10.85)岁;女性15 例,男性15 例;在体质量方面,52~62 kg 18 例,63~73 kg 12例;在乙型肝炎家族史方面,有7 例,无23 例;在既往史方面,吸烟史18 例,饮酒史12 例。两组患者的一般资料比较差异无统计学意义(P>0.05)。本研究通过医院医学伦理委员会批准,患者均知情同意。
1.2 纳入与排除标准
纳入标准:①均符合慢性乙型肝炎的诊断标准[7];②HBV DNA 定量均在 106IU/mL 及以上;③均未接受过抗病毒治疗。排除标准:①有肝硬化或肝癌;②合并药物性肝损伤、非酒精性脂肪性肝炎、全身系统性疾病等对肝脏造成累及;③接受过干扰素、免疫抑制剂治疗。
1.3 方法
1.3.1 恩替卡韦组 让患者口服0.5 mg 恩替卡韦(国药准字 H20052237),1 次/d,24 周为 1 个疗程,共治疗2 个疗程。
1.3.2 替诺福韦酯组 让患者口服300 mg 替诺福韦酯(国药准字H20173092),1 次/d,24 周为1 个疗程,共治疗2 个疗程。
1.4 观察指标
随访1 年。①实验室指标。采用CAP/CTM 对HBV DNA 进行测定,采用全自动生化分析仪(迈瑞BS800)对谷草转氨酶(AST)、谷丙转氨酶(ALT)、总胆红素(TBIL)水平进行测定;②ALT 复常情况。ALT 正常范围值为0~40 U/L[8];③生物化学应答情况。应答标准为ALT 恢复正常[9];④病毒学应答情况。应答标准为乙型肝炎病毒载量(HBV DNA)在500 IU/mL 以下[10];⑤满意度。自制满意度调查问卷,总分 0~3 分,0 分、1 分、2 分、3 分分别评定为不满意、一般、较满意、很满意。满意度=(较满意例数+很满意例数)/总例数×100.00%。
1.5 评定标准
依 据 HBV DNA,<1×103IU/mL 为 有 效 ,≥1×103IU/mL 为无效[11]。
1.6 统计方法
采用SPSS 20.0 统计学软件分析数据,符合正态分布的计量资料用()表示,行t检验,计数资料用[n(%)]表示,行 χ2检验,P<0.05 为差异有统计学意义。
2 结果
2.1 两组实验室指标比较
用药前,两组患者的血清HBV DNA、AST、ALT、TBIL 水平之间的差异无统计学意义(P>0.05);用药后,两组患者的血清 HBV DNA、AST、ALT、TBIL 水平均低于用药前,差异有统计学意义(P<0.05),替诺福韦酯组患者的血清HBV DNA、AST、ALT、TBIL 水平均低于恩替卡韦组,差异有统计学意义(P<0.05),见表1。
表1 两组实验室指标比较()

表1 两组实验室指标比较()
组别替诺福韦酯组(n=30)恩替卡韦组(n=30)t 值P 值HBV DNA(IU/mL)用药前3437.11±9.08 3438.10±9.86 0.405 0.687 AST(U/L)用药后22.66±3.90 28.20±3.77 5.594<0.001用药后1321.30±9.80 2087.05±9.46 307.921<0.001用药前41.10±6.94 41.06±6.80 0.023 0.982

续表1
2.2 两组ALT 复常情况比较
替诺福韦酯组患者的6 个月、1 年ALT 复常率均高于恩替卡韦组,差异有统计学意义(P<0.05),但两组患者的1 个月、3 个月ALT 复常率之间的差异无统计学意义(P>0.05),见表2。
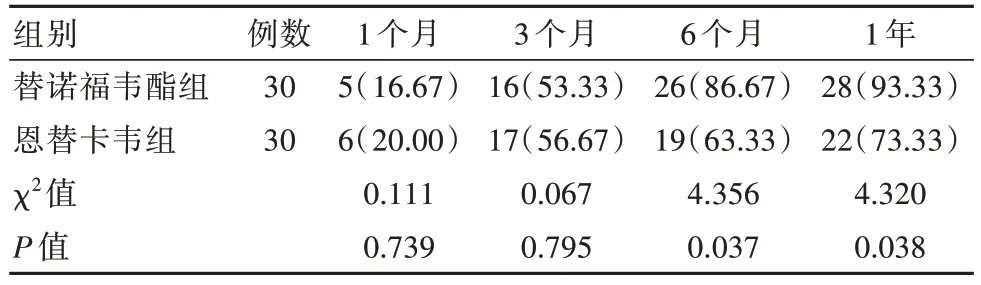
表2 两组ALT 复常情况比较[n(%)]
2.3 两组生物化学应答、病毒学应答情况比较
替诺福韦酯组患者的生物化学应答率、病毒学应答率86.67%(26/30)、93.33%(28/30)均高于恩替卡韦组56.67%(17/30)、60.00%(18/30),差异有统计学意义(P<0.05),见表3。
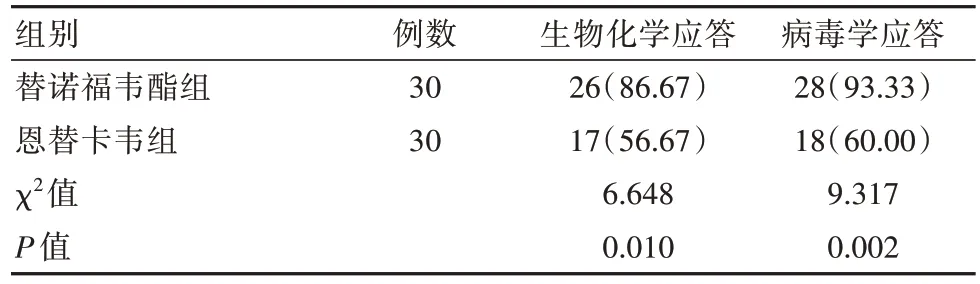
表3 两组生物化学应答、病毒学应答情况比较[n(%)]
2.4 两组临床疗效比较
替诺福韦酯组患者的有效率93.33%(28/30)高于恩替卡韦组66.67%(20/30),差异有统计学意义(χ2=6.667,P<0.05),见表4。

表4 两组临床疗效比较[n(%)]
2.5 两组满意度比较
替诺福韦酯组患者的满意度96.67%(29/30)高于恩替卡韦组73.33%(22/30),差异有统计学意义(χ2=4.706,P<0.05),见表5。
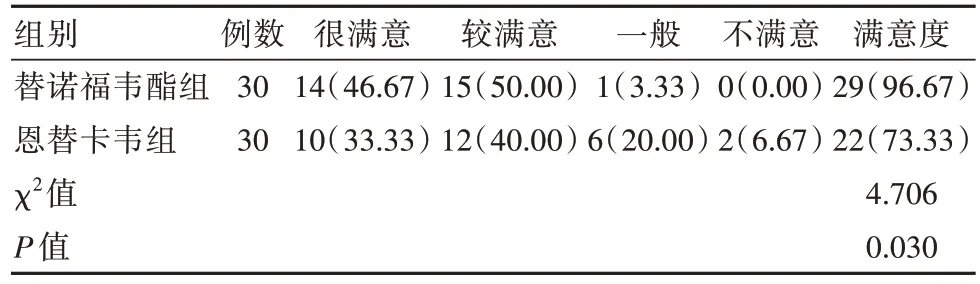
表5 两组满意度比较[n(%)]
3 讨论
慢性乙型肝炎患者的汇管区炎症显著,主要为淋巴细胞浸润,汇管区会在炎症细胞聚集的情况下扩大,促进肝炎的发生[12]。界面肝炎、汇管区炎症是乙型肝炎的特殊性病变[13]。在全球范围内,乙型肝炎病毒感染均是一个严重卫生问题,慢性感染可能引发肝硬化、肝细胞癌等严重并发症[14]。要想将并发症发生率及死亡率降低,关键是要早期诊断与治疗慢性乙型肝炎[15]。治疗目标为对HBV 赋值进行最大限度地长期抑制,使肝功能衰竭、肝细胞癌等并发症的发生延缓及减少[16]。本研究结果表明,用药前,两组患者的血清HBV DNA、AST、ALT、TBIL 水平之间的差异无统计学意义(P>0.05);用药后,两组患者的血清 HBV DNA、AST、ALT、TBIL 水平均低于用药前(P<0.05),替诺福韦酯组患者的血清HBV DNA、AST、ALT、TBIL 水平均低于恩替卡韦组(P<0.05)。替诺福韦酯组患者的6 个月、1 年ALT复常率均高于恩替卡韦组(P<0.05),但两组患者的1 个月、3 个月ALT 复常率之间的差异无统计学意义(P>0.05),原因为恩替卡韦能够对乙肝病毒多聚酶进行抑制,通过磷酸化向三磷酸盐转化,具有活性,能够对病毒多聚酶活性进行抑制,和三磷酸脱氧鸟嘌呤核苷(HBV 多聚酶的天然底物),其中病毒多聚酶的三种活性为HBV 多聚酶启动、前基因组mRNA 逆转录负链形成[17-18]。替诺福韦能够对病毒进行有效抑制,具有潜在抗HIV-1 活性,能够对病毒聚合酶进行有效抑制,通过竞争结合天然脱氧底物,通过将DNA 插入将DNA 链终止,对多种病毒进行抑制[19]。
有研究表明,在高病毒载量慢性乙型肝炎患者的治疗中,替诺福韦酯能够将临床疗效提升(74.00%→94.00%),将HBV 病毒降低,将生物化学(54.00%→84.00%)、病毒应答率(58.00%→92.00%)提升,为肝功能恢复提供有利条件[20]。本研究结果还表明,替诺福韦酯组患者的生物化学应答率、病毒学应答率86.67%(26/30)、93.33%(28/30)均高于恩替卡韦组 56.67%(17/30)、60.00%(18/30)(P<0.05)。替诺福韦酯组患者的有效率93.33%(28/30)高于恩替卡韦组66.67%(20/30)(P<0.05)。替诺福韦酯组患者的满意度96.67%(29/30)高于恩替卡韦组73.33%(22/30)(P<0.05),和上述研究结果一致,原因为替诺福韦酯能够对HBV 复制进行长期阻止,同时没有交叉耐药存在,磷酸化后将替诺福韦二磷酸产生,竞争性结合天然脱氧核糖底物,抑制病毒聚合酶活性,将DNA 链插入终止,使DNA 很难延长,从而对HBV 复制进行抑制。同时,替诺福韦酯能够将抗病毒作用独立发挥出来,不需要激酶、病毒诱导辅助,能够将抑制HBV 复制的作用短时间内发挥出来。此外,替诺福韦酯的耐药屏障较高,耐药性较低。
综上所述,高病毒载量慢性乙型肝炎患者治疗中替诺福韦酯的临床效果较恩替卡韦好,值得推广。
