高锂钾铝电解质的初晶温度
2022-10-09赵天旭吉尚鑫商庭瑞陆泓彬高炳亮
陈 赫, 谭 祺, 赵天旭, 吉尚鑫, 商庭瑞, 陆泓彬, 高炳亮
(东北大学 冶金学院, 沈阳110819)
在电解铝生产过程中,电解质物理化学性质的优劣会直接影响电解槽的运行指标[1].电解质过热度是一个非常重要的工艺控制参数,它是电解质温度与电解质初晶温度之间的差值.电解质过热度直接影响电解质的挥发性和流动性、金属的溶解损失、氧化铝的溶解速率以及电解槽的热平衡等[2].如果能准确测得电解质的组成与温度,采用高可靠性的经验公式计算电解质的初晶温度不失为一种简洁、高效的过热度分析手段.
随着我国电解铝工业的高速发展,许多中低品位铝土矿被用来生产冶金级氧化铝,导致氧化铝中Li,K 等杂质含量较高.随着电解槽槽龄的增长,Li,K 等杂质会以锂盐和钾盐的形式富集于电解质中[3].近年来,国内一些使用国产氧化铝的电解槽的电解质中,锂盐质量分数超过3%,高的已达8%~9%,钾盐质量分数最高可达到4.5%[4].锂盐和钾盐的富集会使电解质物理化学性质(如初晶温度、氧化铝溶解度、氧化铝溶解速率等)发生改变[5-6],电解槽控制难度增大,电解质稳定性变差.因此,掌握高锂钾铝电解质的物理化学性质,尤其是掌握锂盐和钾盐对电解质初晶温度的影响规律,对提高铝电解槽的控制水平至关重要.
许多学者针对LiF 和KF 对初晶温度的影响做了大量的研究工作.有学者指出,在铝电解质中,LiF 质量分数每增加1%,电解质的初晶温度会降低6~8 ℃[7-8];KF 质量分数每增加1%,电解质初晶温度会降低2 ~3 ℃[9-10].Solheim、郭丽莉及Peng 等[11-13]给出了用于预测Na3AlF6-AlF3-Al2O3-CaF2-LiF-KF 体系初晶温度的经验公式,其中Solheim 等发表的初晶温度经验公式影响较大,尤其在预测简单电解质和含锂电解质的初晶温度时准确度较高.但是该公式对于预测同时含有LiF 和KF 的电解质的初晶温度不够准确,尤其是在LiF 质量分数大于2%,KF 质量分数大于6%的情况下,部分误差超过10 ℃[14],因此亟须针对高锂钾铝电解质建立一个更加准确的初晶温度预测模型.
文献中已经报道了大量的铝电解质初晶温度实验数据[11,15-18].本文中将遴选出可靠的实验数据,通过非线性拟合法对得到的数据进行分析,以获得Na3AlF6-AlF3-Al2O3-CaF2-LiF-KF 体系初晶温度的预测模型,并设计含锂无钾、含锂低钾和含锂高钾三种类型的复杂铝电解质,采用差热分析法测试其初晶温度,对该模型的可靠性进行验证;同时,对LiF 和KF 对复杂铝电解质初晶温度的影响进行分析.
1 实 验
1.1 实验试剂
本实验测试所用的铝电解质由分析纯试剂AlF3,NaF,Al2O3,CaF2,LiF 和KF 混合配制而成(详见表2).实验所用的分析纯试剂AlF3,CaF2,LiF 和KF 来自上海阿拉丁生化科技股份有限公司,NaF 和Al2O3来自国药集团试剂有限公司.实验前,将各试剂置于200 ℃干燥箱中干燥48 h,以除去水分.
1.2 初晶温度测试原理
本实验中采用差热分析法(DTA)测定电解质的初晶温度,实验装置如图1 所示.首先,将各试剂按设定量称好,在研钵内充分混匀后放入石墨坩埚中,同时将适量α-Al2O3粉末加入到坩埚壁的小孔内,将坩埚放到电阻炉内加热到设定温度,保温30 min,确保电解质充分融化.其次,将两只K 型热电偶分别插入坩埚内的电解质熔体及坩埚壁的α-Al2O3粉末中,浸没在电解质中的热电偶测量的温度记作电解质温度,插入在α-Al2O3粉末中的热电偶测量的温度为参比温度.最后,控制高温炉以0.5 ℃/min 的速率降温,采用热电偶模块记录两只热电偶的温度随时间的变化,并传输给计算机.以电解质温度为横坐标,以电解质温度与参比温度的差值(Δt)为纵坐标作图,得到用于判断混合熔盐初晶温度点的差热曲线图.熔融电解质在冷却过程中出现固体结晶相时,释放的热量会减缓电解质的降温速率;而α-Al2O3不发生相变,因而参比温度的降温速率不受影响.两者的温度差会在电解质的初晶温度处发生突变,突变点对应的电解质温度即为待测电解质的初晶温度.

图1 熔盐初晶温度测试装置示意图Fig.1 Schematic diagram of measurement setup for liquidus temperature
1.3 实验装置及可靠性
本文中通过测量NaCl 的熔点对初晶温度测试系统进行标定,所得差热曲线如图2 所示.从图中可以看出,NaCl 熔点的测量值为800.6 ℃,与文献值(801 ℃)相差不超过1 ℃,表明该初晶温度测试系统具有较高的精度.同时,文献中有大量不含LiF 和KF 的简单电解质的初晶温度实验数据,这些数据已经被不同研究者重复测量并验证,具有很高的可靠性.采用该系统测量了3 个组分的简单电解质的初晶温度,与文献中的数值相比,绝对误差不超过2 ℃.实验结果表明,本测试系统能够准确获得熔盐的初晶温度.
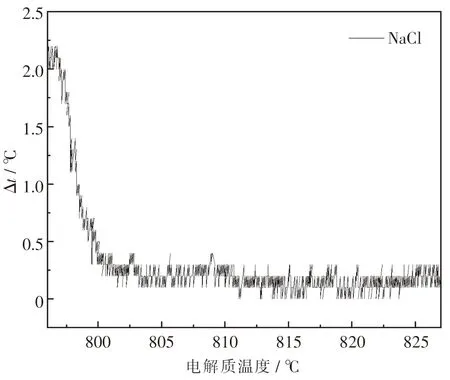
图2 NaCl 冷却过程中的差热曲线图Fig.2 Differential thermal curve of NaCl during cooling
2 结果与讨论
2.1 高锂钾铝电解质初晶温度经验公式的拟合
通过文献中提及的初晶温度数学模型计算、Origin 2018 软件中的“图像数字化工具”读图以及直接采用文献中实验数据的方法,本文中遴选出了130 组铝电解质初晶温度文献数据[11,15-18],采用Origin 2018 软件中非线性拟合功能,得到了用于计算Na3AlF6-AlF3-Al2O3-CaF2-LiF-KF 体系初晶温度的经验公式,如式(1)所示.该公式拟合相关系数R2为0.980 0.式中含有KF 的项与其他组分差别较大,因为“[KF] +[KF]2+[KF] ×[AlF3]”模型(方括号代表成分的质量分数)不能很好地反映出KF 对Na3AlF6-AlF3-Al2O3-CaF2-LiF-KF 体系初晶温度的影响,部分预测结果与实验值的绝对误差超过6 ℃,故采用了更复杂的模型.初晶温度的文献数据来自表1 中所列文献.

表1 铝电解质初晶温度公式拟合所用实验数据来源Table 1 Data sources of experimental liquidus temperatures of aluminum electrolytes

式中:tc代表电解质初晶温度,℃;[AlF3]代表过剩氟化铝的质量分数,%;其余方括号代表各成分的质量分数,%.公式适用范围如下(数值均为质量分数,下同):AlF30 ~13%,Al2O30 ~6%,CaF20~8%,LiF 0~8%,KF 0~8%.
电解质中的过剩氟化铝质量分数[AlF3]与电解质分子比CR 之间的转换关系如下:

式中:∑a 代表试样中除冰晶石和过剩氟化铝外其他各成分的质量分数之和;CR 为铝电解质中NaF 与AlF3的摩尔比,通常称为分子比.
2.2 高锂钾铝电解质初晶温度经验公式的实验验证
为了验证公式(1)的可靠性,本文中设计了含锂无钾、含锂低钾和含锂高钾三种类型总计32种组分的复杂铝电解质测试样品,采用差热分析法测试了样品的初晶温度值.其中样品编号1 ~8为含锂无钾电解质,成分与文献[11]中一致;样品编号9 ~19 为含锂低钾电解质,LiF 含1%~8%,KF 含1%~3%,其余组元成分采用了现行铝电解质成分的典型值;样品编号20 ~32 为含锂高钾电解质,LiF 含2%~8%,KF 含5%~7%,其余组元成分同样为现行铝电解质成分的典型值.32组电解质的成分及初晶温度测量结果和计算结果列于表2 中.

表2 铝电解质初晶温度实验值与计算值的比较Table 2 Experimental and calculated values of liquidus temperature for aluminum electrolytes
图3 显示了含锂无钾、含锂低钾电解质初晶温度的实验值(本文中)与公式(1)计算值、文献[11]中公式计算值之间的误差,图4 显示了含锂高钾电解质初晶温度的实验值与公式(1)计算值之间的误差.如图3 所示,对于含锂无钾电解质初晶温度的预测,公式(1)和文献[11]中公式的计算值与实验值之间的最大绝对误差分别为1.4 和1.7 ℃,说明公式(1)和文献[11]中的公式同样具有很高的可靠性.对于含锂低钾电解质初晶温度的预测,公式(1)和文献[11]中公式的计算值与实验值之间的最大绝对误差分别为2.7 和10.1 ℃,说明公式(1)比文献[11]中的公式具有更高的可靠性.如图4 所示,对于含锂高钾电解质初晶温度的预测,公式(1)的计算值与实验值之间的最大绝对误差为2.7 ℃,说明该公式具有较高的可靠性.由于文献[11]中的公式仅适用于KF质量分数小于5%的电解质,因此未将其计算值在图4 中进行对比分析.文献[11]中的公式不能有效预测同时含有LiF 和KF 的电解质的初晶温度,原因在于文献[11]中在推导KF 对初晶温度的作用系数时所采用的实验数据不超过10 个,而且都是分子比为3.0 的电解质,也没有考察同时含有LiF 和KF 的电解质的初晶温度情况.依据文献[11]中的实验数据和本文中的测试数据,过剩氟化铝和KF 或LiF 对初晶温度存在耦合作用关系,文献[11]中把KF 对含锂电解质初晶温度的影响简单地认定为线性关系,具有一定的局限性.

图3 公式(1)和文献[11]中公式计算值与实验值的误差Fig.3 Error between predicted and experimental values of this work’s calculated and Reference [11]’s formula
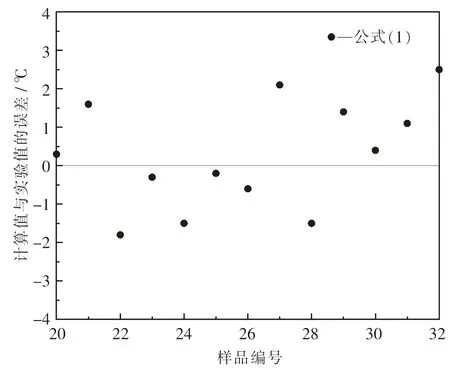
图4 公式(1)计算值与实验值的误差Fig.4 Error between calculated and experimental values of this work’s formula
2.3 KF 对含锂电解质初晶温度的影响
利用初晶温度计算公式(1)考察了电解质分子比和KF 含量对含锂电解质初晶温度的影响,如图5 和图6 所示.图中电解质分子比的变化范围为2.2 ~2.8,KF 质量分数的变化范围为0.5%~7.5%.图5 为低锂含量电解质初晶温度图,LiF 质量分数为2%;图6 为高锂含量电解质初晶温度图,LiF 质量分数为6%.其余组元成分均相同,Al2O3质量分数为2%,CaF2质量分数为4%.
从图5、图6 中可以看出,在分子比为2.2 ~2.8 的范围内,当KF 质量分数从0.5%增加到7.5%时,电解质的初晶温度均呈下降趋势,即KF的加入会使含锂电解质的初晶温度降低.KF 质量分数每增加1%,分子比为2.2,2.4,2.6,2.8 的低锂含量电解质初晶温度平均分别降低0.6 ,1.1 ,1.5 和1.7 ℃,高锂含量电解质的初晶温度平均分别降低1.4,2.3 ,3.0 和3.5 ℃.KF 降低含锂电解质初晶温度的能力随分子比的增大而逐渐增强,而且在高锂含量电解质中,KF 对初晶温度的降低能力更强一些.

图5 不同分子比条件下KF 质量分数对低锂含量([LiF]=2%)电解质初晶温度的影响Fig.5 Effects of KF content and cryolite ratio on liquidus temperatures of aluminum electrolytes with low content of LiF([LiF]=2%)
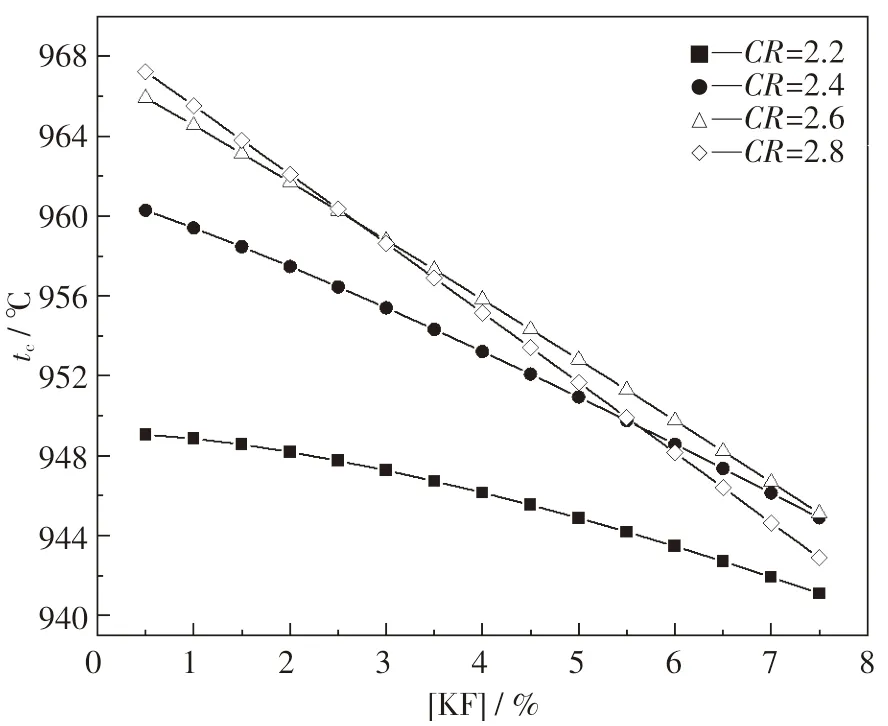
图6 不同分子比条件下KF 质量分数对高锂含量([LiF]=6%)电解质初晶温度的影响Fig.6 Effects of KF content and cryolite ratio on liquidus temperatures of aluminum electrolytes with high content of LiF([LiF]=6%)
如图6 所示,在高锂高钾电解质中,如果KF质量分数超过3%,随着KF 质量分数的增加,高分子比电解质的初晶温度甚至会比低分子比电解质的初晶温度更低.对于高锂高钾电解质而言,通过提高分子比来提高电解质初晶温度的做法往往不起作用,原因就在于此.
2.4 LiF 对含钾电解质初晶温度的影响
利用初晶温度计算公式(1)考察了电解质分子比和LiF 含量对含钾电解质初晶温度的影响,如图7 和图8 所示.图中电解质分子比变化范围为2.2~2.8,LiF 质量分数的变化范围为0.5%~7.5%.图7 为低钾含量电解质初晶温度图,KF 质量分数为2%;图8 为高钾含量电解质初晶温度图,KF 质量分数为6%.其余组元成分均相同,Al2O3质量分数为2%,CaF2质量分数为4%.
从图7、图8 中可以看出,在分子比为2.2 ~2.8 的范围内,当LiF 质量分数从0.5%增加到7.5%时,电解质的初晶温度均呈下降趋势,即LiF的加入会使含锂电解质的初晶温度降低.LiF 质量分数每增加1%,分子比为2.2,2.4,2.6,2.8 的低钾含量电解质初晶温度平均分别降低3.6,3.9,4.1 和4.3 ℃,高钾含量电解质初晶温度平均分别降低3.7,4.0,4.1 和4.3 ℃.可以看出,无论在高钾含量电解质还是低钾含量电解质中,每添加1% 的LiF 对电解质初晶温度的降低能力基本接近,约在4 ℃.此外,在分子比为2.4 ~2.8 的范围内,LiF 降低含钾电解质初晶温度的能力受分子比变化的影响很小.同时对比图5、图6、图7、图8可以看出,LiF 对电解质初晶温度的降低能力要强于KF.
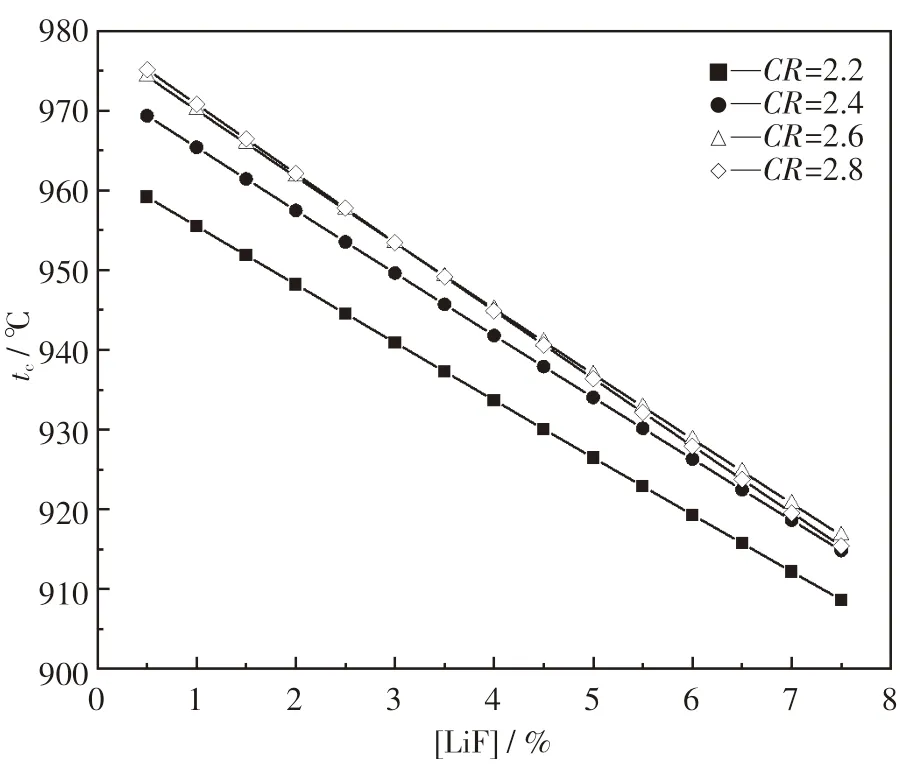
图7 不同分子比条件下LiF 质量分数对低钾含量([KF]=2%)电解质初晶温度的影响Fig.7 Effects of LiF content and cryolite ratio on liquidus temperatures of aluminum electrolytes with low content of KF([KF]=2%)

图8 不同分子比条件下LiF 质量分数对高钾含量([KF]=6%)电解质初晶温度的影响Fig.8 Effects of LiF content and cryolite ratio on liquidus temperatures of aluminum electrolytes with high content of KF([KF]=6%)
3 结 论
(1)通过对Na3AlF6-AlF3-Al2O3-CaF2-LiF-KF体系初晶温度的研究,获得了适用于高锂钾复杂铝电解质体系初晶温度的经验公式,公式计算值与实验值的最大绝对误差为2.7 ℃.该经验公式对同时含有LiF 和KF 的复杂铝电解质体系初晶温度的预测具有很高的可靠性.
(2)在同时含有LiF 和KF 的复杂铝电解质中,增加KF 含量或者LiF 含量,对高分子比电解质初晶温度的降低作用要强于低分子比电解质初晶温度.
(3)KF 对复杂铝电解质初晶温度的降低能力会随着电解质中LiF 含量的增大而略有增强.
