g-C3N4-Bi2O3/Al2O3复合材料光催化还原水中U(Ⅵ)
2022-10-09袁亦雷谢水波刘岳林史艳丹刘迎九
袁亦雷,谢水波,,刘岳林,史艳丹,刘迎九
(1. 南华大学 土木工程学院,湖南 衡阳 421001;2. 南华大学 污染控制与资源化技术湖南省重点实验室,湖南 衡阳 421001)
铀矿冶炼废水中的铀主要以U(Ⅵ)为主,多以铀酰离子(UO)的形式存在。目前,处理含铀废水的方法主要有吸附法、膜分离法、萃取法和生物法。其中,吸附法和膜分离法投资运行费用高、操作复杂且产物不易分离;萃取法需要大量使用萃取剂,不但费用高,而且还存在二次污染的风险;生物法尽管经济、环保,但处理周期过长,尤其不适合处理中高浓度的含铀废水。光催化还原技术是一种新型的废水处理技术,它能将含铀废水中迁移性强、易溶于水的U(Ⅵ)还原为迁移性弱、难溶于水的U(Ⅳ),实现U(Ⅵ)与水的分离,具有处理效果好、操作简单、节能环保等优点。石墨相氮化碳(g-CN)具有独特的电子结构和化学特性,且制备简单、价廉易得,作为非金属催化剂,极具发展前景。但由于电子-空穴复合率高、可见光利用率低和比表面积小等缺陷,大大限值了它的使用范围。为此,g-CN用作光催化剂时,通常需要改性。目前常用的改性方法有形貌调节、元素掺杂、构建复合半导体等。其中构建g-CN复合半导体材料能够有效提高电子-空穴的分离效率,提高光催化性能。氧化铋(BiO)作为禁带宽度可调(=2.34~3.40 eV)的半导体材料,被广泛应用于光催化领域。氧化铝(AlO)具有比表面积大、容易吸附等优点,在催化领域和材料领域常作为载体。
本研究以AlO为载体,BiO为半导体材料,采用热聚合法将BiO、g-CN相互结合形成异质结,制备出g-CN-BiO/AlO复合光催化剂,运用多种手段进行了表征,并考察了该催化剂对模拟含铀废水中U(Ⅵ)的光催化还原性能和重复利用性能,探讨了其光催化还原U(Ⅵ)的机理。
1 实验部分
1.1 材料、试剂和仪器
模拟含铀废水采用UO(基准纯 GBW04201)配制而成。
AlO、BiO、尿素:均为分析纯。实验用水为蒸馏水。
Escalab 250Xi型X射线光电子能谱分析仪:美国Thermo Fisher Scientific公司;T6新世纪型紫外-可见分光光度计:北京普析公司;FLS980型稳态/瞬态荧光光谱仪:英国爱丁堡仪器公司;FEG Quanta 450型场发射扫描电镜:美国FEI公司;D8 Advance型X射线衍射仪:德国布鲁克公司;UV270 型紫外-可见漫反射仪:日本岛津公司。
1.2 实验方法
1.2.1 g-CN-BiO/AlO的制备
将10 g 尿素置于马弗炉中升温至 550 ℃,煅烧 2 h,冷却至室温后研磨,得到淡黄色固体粉末,即g-CN。将AlO、g-CN、BiO以质量比为3∶2∶1的比例混合,加入一定量的蒸馏水,搅拌均匀,超声混合15 min;将悬浮液转移到陶瓷坩埚中,在80 ℃下加热蒸干;再将陶瓷坩埚置于马弗炉中,在500 ℃条件下煅烧2 h,冷却至室温,将其内容物研磨成粉末,得到复合光催化剂g-CN-BiO/AlO。
1.2.2 g-CN-BiO/AlO光催化还原U(Ⅵ)性能研究
光催化反应器中以500 W氙灯作为光源模拟太阳光,配有石英冷阱内冷却循环水系统,用于吸收氙灯散发的热量,反应器底部配有磁力搅拌器,可以使光催化剂悬浮在溶液中,与溶液中的U(Ⅵ)充分接触。
在试管中分别加入20 mL U(Ⅵ)质量浓度为10 mg/L的模拟含铀废水(初始pH为5)和10 mg的催化剂(投加量为0.5 g/L),将其置于黑暗环境中搅拌30 min,然后再置于光催化反应器中光照60 min。间隔一定时间取样,离心,测定上清液在578 nm处的吸光度,计算废水中U(Ⅵ)的质量浓度及去除率。
1.2.3 光催化剂的收集和重复使用
使用过的光催化剂经离心收集后用稀盐酸浸泡2~3 h;用蒸馏水洗涤至pH为中性;将洗涤好的催化剂置于60 ℃的真空干燥箱中烘干至恒重以备重复使用。
1.3 分析与表征
采用分光光度法测定上清液在578 nm处的吸光度,计算废水中U(Ⅵ)的质量浓度及去除率。
采用XRD表征光催化剂的晶相结构;采用SEM观察光催化剂的微观形貌;采用XPS分析光催化剂的表面元素及其化学形态;采用UV-Vis DRS考察光催化剂的光学性能;采用PL分析光催化剂中光生电子-空穴对的分离情况。
2 结果与讨论
2.1 g-C3N4-Bi2O3/Al2O3的晶相结构
图1为g-CN-BiO/AlO的XRD谱图。由图1可见:在衍射角2为27.6°和12.9°处出现的衍射峰分别对应g-CN的(002)和(100)晶面;在2为30.459°,31.959°,32.875°,46.355°,54.400°,55.667°处出现的衍射峰依次对应四方相β-BiO的(211)、(002)、(220)、(222)、(400)、(203)和(421)晶面(JCPDS No.27-0050);在2为28.3°处出现的衍射峰对应AlO(PDF#47-1308) 的(220)晶面。g-CN-BiO/AlO谱图中没有出现新的衍射峰,说明本实验成功制备了g-CN-BiO/AlO复合光催化剂。
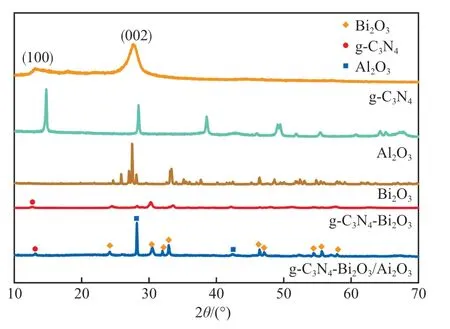
图1 g-C3N4-Bi2O3/Al2O3的XRD谱图
2.2 g-C3N4-Bi2O3/Al2O3的微观形貌
图2为3种光催化材料的SEM 照片。由图2可见:g-CN为无规则块状结构,大小分布不一,内部结构十分松散;g-CN-BiO中,BiO和g-CN相互混合聚集在一起,但没有表现出明显的异质结构;与g-CN和g-CN-BiO相比,g-CN-BiO/AlO的表面出现了许多聚合晶体块状结构,这可能是由于BiO、g-CN和AlO经过高温煅烧后发生相互作用,形成了异质结。

图2 3种光催化材料的SEM照片
2.3 g-C3N4-Bi2O3/Al2O3的XPS分析
图3为g-CN-BiO/AlO的XPS谱图。由图3a可见,单组分的BiO中Bi 4及Bi 4的结合能分别为164.6,159.3 eV,说明样品中的Bi以正三价的形式存在。由图3b可见,531.7 eV和532.0 eV分别为BiO中Bi—O键的结合能和AlO中Al—O键的结合能。由图3c可见,结合能398.8 eV处的峰归属于g-CN结构中分别与两个C相连的2杂化态芳香N(C=N—C),结合能400.4 eV处的N 1峰归属于g-CN结构中的两种N基团(H—N—(C)或N—(C))。由图3d可见,结合能288.3 eV处的峰归属于g-CN结构中三嗪环(N—C=N)上2杂化态的C,结合能284.7 eV处的峰归属于g-CN中以2杂化态存在的C—C键中的C。XPS的结果进一步证明了材料元素的组成。

图3 g-C3N4-Bi2O3/Al2O3的XPS谱图
2.4 g-C3N4-Bi2O3/Al2O3的光学性能分析
图4为不同光催化材料的紫外-可见漫反射谱图。由图4可见,与g-CN和g-CN-BiO相比,g-CN-BiO/AlO在400~800 nm区域具有较强的吸收带。
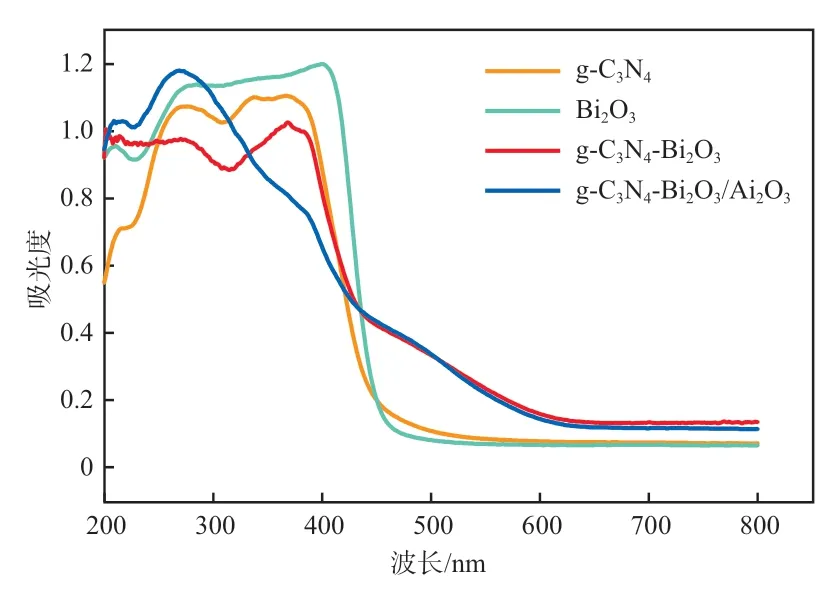
图4 不同光催化材料的紫外-可见漫反射谱图
利用 Tauc-Plot 法计算不同光催化剂的禁带宽度,其计算方法见式(1)。

式中:,,依次为半导体的吸收系数、 普朗克常数和光子频率;为禁带宽度;为常数;由于g-CN和BiO均属于直接型半导体,所以=1/2。以()对作图(见图 5),求得g-CN、BiO、g-CN-BiO和g-CN-BiO/AlO的禁带宽度分别为2.82,2.67,2.79,2.47 eV。由此可见,g-CN-BiO/AlO的带隙能较单体材料和二元材料有所降低,更容易被可见光所激发,且g-CN-BiO/AlO的光谱响应范围变宽,对可见光的吸收性能增强。

图5 (αhv)1/n~ hv的关系
2.5 光生电子-空穴对的分离分析
在325 nm的激发波长条件下,测定g-CN、g-CN-BiO和g-CN-BiO/AlO三者的荧光谱图,结果见图6。由图6可见:在460 nm处,g-CN出现了光谱的最高峰,说明有很多光生电子与空穴结合,大量的能量被释放出来,光催化效果最差;相对于g-CN和g-CN-BiO,g-CN-BiO/AlO在荧光光谱中没有明显波峰,表明光生电子和空穴的复合效率降低,光催化性能增强。
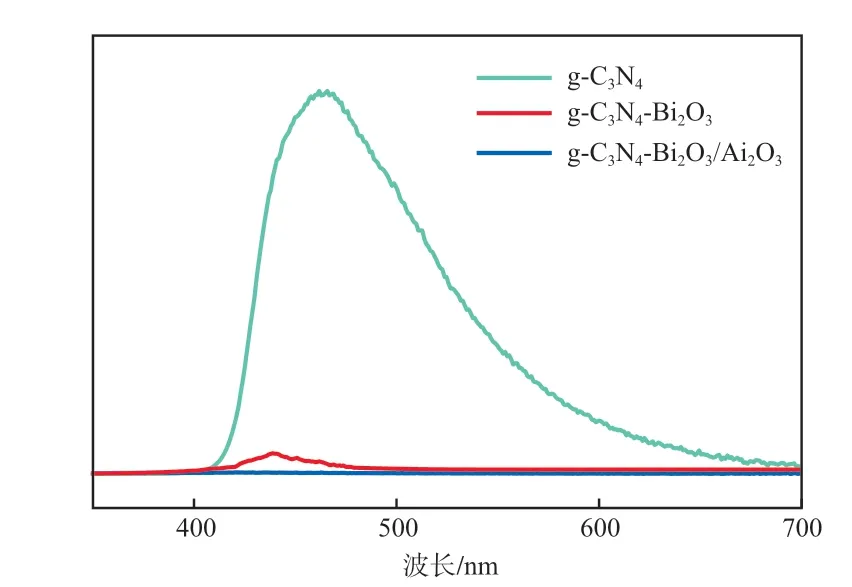
图6 不同光催化材料的荧光谱图
2.6 光催化剂对U(Ⅵ)的还原性能
不同光催化剂对U(Ⅵ)的去除率见图7。由图7可见,反应90 min后,g-CN和BiO对U(Ⅵ)的去除率约为30%;g-CN-BiO对U(Ⅵ)的去除率约为74%;而g-CN-BiO/AlO对U(Ⅵ)的去除率达到了98%,其去除率是一元材料g-CN和BiO(30%)的3.27倍,是二元复合材料g-CN-BiO(74%)的1.32倍。
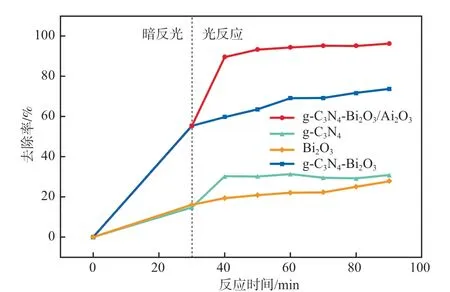
图7 不同光催化剂对U(Ⅵ)的去除率
2.7 光催化剂的稳定性和重复使用性能
g-CN-BiO/AlO光催化剂的重复使用性能见图8。由图8可见,在第5次重复使用时,g-CN-BiO/AlO光催化剂对U(Ⅵ)的去除率仍高达85%,表现出良好的的稳定性和重复使用性能。
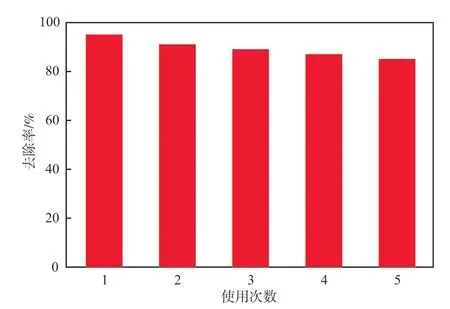
图8 g-C3N4-Bi2O3/Al2O3光催化剂的重复使用性能
2.8 光催化还原U(Ⅵ)的机理分析
暗反应和光反应后g-CN-BiO/AlO的XPS谱图见图9。由图9可见:暗反应后,在381.9 eV和392.9 eV处出现了两个窄而尖锐的峰,分别归属于U 4和U 4,这表明在暗反应阶段没有发生氧化还原反应,此过程中只有吸附作用;光反应后,U 4和U 4峰值分别位于380.7 eV和391.6 eV处,这表明经过光反应以后,g-CN-BiO/AlO将U(Ⅵ)还原为U(Ⅳ),表明光反应阶段发生了氧化还原反应。

图9 暗反应和光反应后g-C3N4-Bi2O3/Al2O3的XPS谱图
在此基础上,分别以对苯醌(BQ)作为超氧自由基(·O)捕获剂、甲醇(AO)作为空穴(h)捕获剂、KSO作为光生电子(e)捕获剂、叔丁醇(TBA)作为羟基(-OH)捕获剂,对g-CN-BiO/AlO光催化U(Ⅵ)过程中的活性物种进行了捕获实验。图10为捕获剂对g-CN-BiO/AlO光催化还原U(Ⅵ) 的影响。由图10可见,BQ和KSO的加入明显降低了光催化还原U(Ⅵ)的效率,可见,在 g-CN-BiO/AlO光催化反应中起主要作用的活性物种为超氧自由基(·O)和光生电子(e)。

图10 捕获剂对g-C3N4-Bi2O3/Al2O3光催化还原U(Ⅵ)的影响
综上所述,g-CN-BiO/AlO光催化还原U(Ⅵ)的机理(见图11)为:AlO将大量U(Ⅵ)吸附到表面上;在光照条件下,g-CN和BiO的价带、导带可以分别产生光生电子和空穴,其中g-CN表面的电子可以通过异质结转移到BiO,而BiO表面上的空穴也可以以类似的方式转移到g-CN上,电荷转移有效地延缓了二者中光生电子-空穴对的复合;BiO表面上一些电子可直接与U(Ⅵ)反应生成U(Ⅳ),另一部分电子与水中的溶解氧反应生成·O,最后也参与到U(Ⅵ)还原为U(Ⅳ)的过程中。
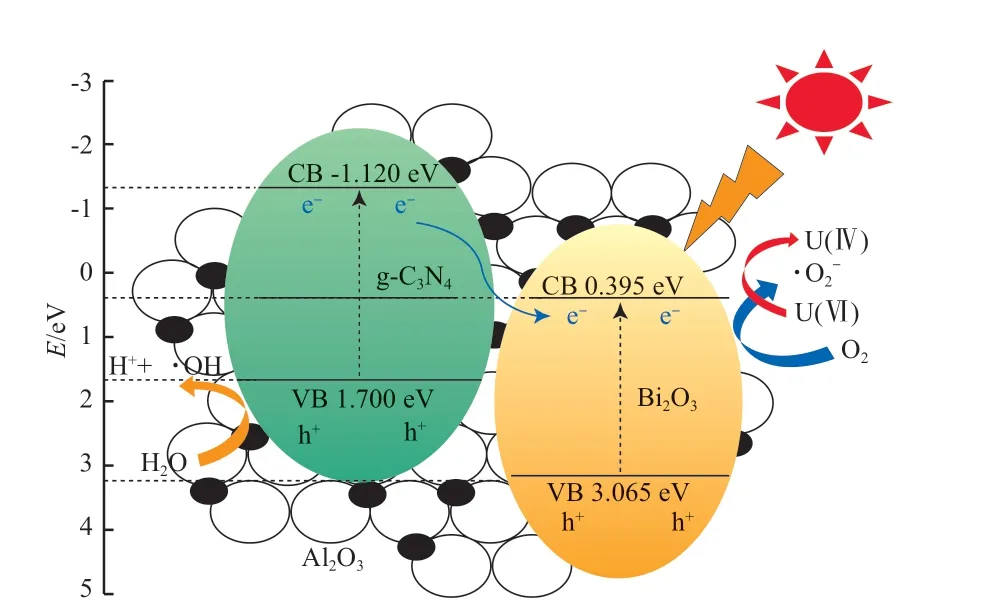
图11 g-C3N4-Bi2O3/Al2O3光催化还原U(Ⅵ)的机理
3 结论
a)在AlO、g-CN、BiO质量比为3∶2∶1的条件下,采用热聚合法制备了g-CN-BiO/AlO复合型光催化剂。表征结果显示,所制备的g-CN-BiO/AlO催化剂具有p-n异质结,能够有效延缓光生电子-空穴对的复合,增强光催化性能。
b)在g-CN-BiO/AlO投加量为0.5 g/L、模拟废水初始pH为5、U(Ⅵ)质量浓度为10 mg/L的条件下,经暗反应30 min、光反应60 min后,模拟废水中U(Ⅵ)去除率达到98%。g-CN-BiO/AlO催化剂重复使用5次后对U(Ⅵ)的去除率仍可达85%,表现出良好的稳定性和重复利用性能。
c)催化还原反应机理分析显示,g-CN-BiO/AlO光催化还原U(Ⅵ)的主要机理是是光生电子(e)和超氧自由基(·O)的作用。
